大环内酯化合物和免疫检查点抑制剂的组合的制作方法
 2021-01-08 11:01:40|
2021-01-08 11:01:40| 501|
501| 起点商标网
起点商标网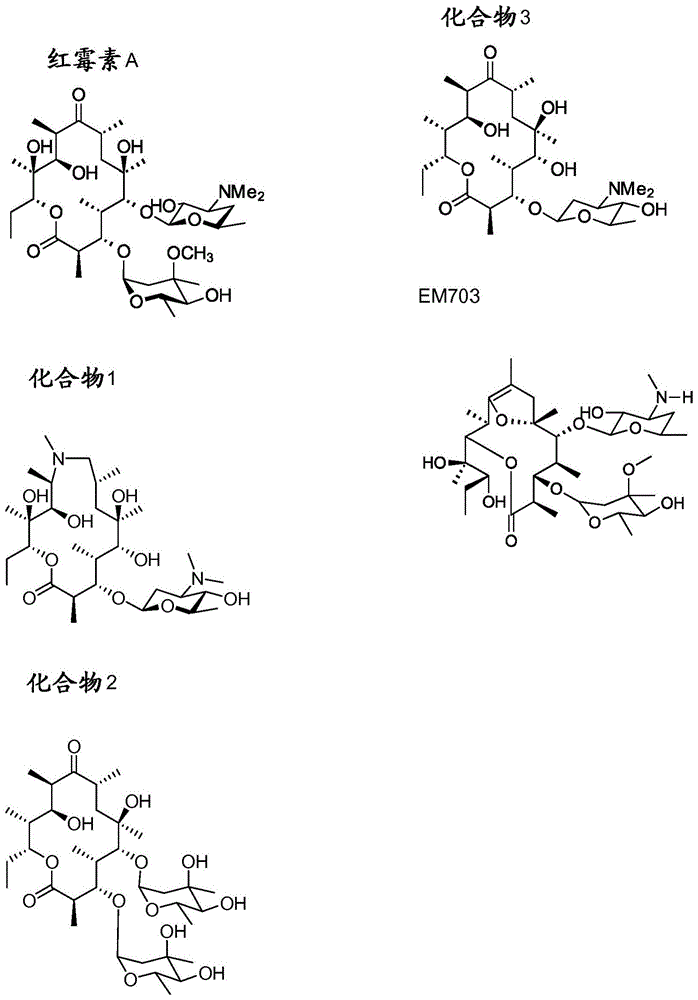
发明领域本发明涉及免疫检查点抑制剂和能够刺激免疫系统的大环内酯的组合,称为免疫肽(immunolide)。本发明涉及所述组合以及所述组合在医药中的用途,特别是在癌症的免疫治疗和病毒性疾病如hiv的治疗中的用途。发明背景癌细胞的特征在于产生大量癌症特异性抗原的大量遗传突变和表观遗传改变。这些抗原被t细胞检测到,t细胞利用抗原将癌前和/或癌细胞与它们的正常对应物区分开,并引发癌症特异性免疫应答。t细胞介导的免疫应答的幅度和特性通常由免疫检查点调节,免疫检查点可定义为分别起增加或减少应答幅度作用的刺激性和抑制性分子和/或分子途径。在正常生理条件下,免疫检查点对于预防自身免疫和保护免受由病原体感染引起的组织损伤是至关重要的。然而,癌细胞可利用免疫检查点蛋白的失调作为获得免疫抗性的方式。一种触发t细胞介导的抗肿瘤免疫应答的方法被称为“检查点阻断”,是指癌细胞所利用的免疫抑制检查点的阻断或抑制。由于许多免疫检查点是由配体-受体相互作用启动的,这些检查点可被抗体阻断或被所讨论的配体和/或受体的重组形式调节。单独或组合的若干免疫检查点在增强t细胞介导的抗肿瘤免疫应答方面是相关的。它们包括但不限于细胞毒性t淋巴细胞相关抗原4(ctla4,也称为cd152)、程序性细胞死亡蛋白1(pd-1,也称为cd279)、pd-1配体1(pd-l1,也称为b7-h1和cd274)、pd-1配体2(pd-l2,也称为b7-dc和cd-273)、t细胞膜蛋白3(tim3,也称为havcr2)、腺苷a2a受体(a2ar)、淋巴细胞活化基因3(lag3,也称为cd223)和b7-h3(也称为cd276)、b7-h4(也称为b7-s1、b7x和vctn1)、2b4(也称为cd244)和b和t淋巴细胞衰减子(btla,也称为cd272)。此外,相关免疫检查点的其他示例可以在科学和专利文献中找到,并且也在本发明的范围内。尽管免疫检查点抑制可用于增强t细胞介导的抗肿瘤免疫,但本发明人预期将免疫检查点抑制与一种或多种补充机制组合以进一步增强t细胞活化将提供甚至更好的抗肿瘤效果。为此,本发明人已经认识到大环内酯具有免疫刺激性抗癌和免疫刺激性抗病毒作用,这已经引导本发明人在本发明利用互补机制实现改进的治疗方案。cd4+t细胞是免疫应答的关键介质,本领域非常需要在癌症患者中提高cd4+t细胞的免疫能力的方法和手段。附图简述图1.大环内酯类红霉素a、化合物1、化合物a、化合物b和em703的结构。图2.t-细胞和b-细胞上的cd69上调。pbmc用化合物1、化合物a和活化对照lps和ifn-γ处理24小时。用流式细胞术在cd4+t细胞群(左)和cd19+b细胞群(右)上测量早期活化标记物cd69的表达。所述值表示一式三份样品中的平均荧光强度,mfi,和误差棒标准偏差。图3.t-细胞和b-细胞上的hla-a,b,c上调。pbmc用化合物1或化合物a以及活化对照lps和ifn-γ处理24小时。用流式细胞术在cd4+t细胞群(左)和cd19+b细胞群(右)上测量hla-a,b,c的表达。所述值表示一式三份样品中的平均荧光强度,mfi,和误差棒标准偏差。图4.血液单核细胞上的cd80和hla-dr上调。pbmc用化合物1或化合物a以及活化对照lps和ifn-γ处理24小时。用流式细胞术在单核细胞细胞群上测量cd80和hla-dr的表达。所述值表示一式三份样品中的平均荧光强度,mfi,和误差棒标准偏差。图5.血液单核细胞上的cd80上调。pbmc用化合物1或化合物a以及活化对照ifn-γ处理24小时。用流式细胞术在单核细胞群上测量cd80的表达。所述值表示一式三份样品中的平均荧光强度,mfi,和误差棒标准偏差。图6.用化合物1刺激pbmc达48小时或1周后从pbmc产生il-10,其用elisa测量。图7.用化合物1刺激6天后的cd4t细胞增殖,其用增殖染料celltraceviolet(invitrogen)和流式细胞术测量。未处理的细胞(unt)或化合物a用作对照。图8.用化合物1温育后的cmv特异性cd8t细胞上il-7受体α(cd127)的上调,其用流式细胞术测量。图9:在存在或不存在化合物1或化合物a的情况下,与cmv肽一起生长的pbmc(来自cmv+供体)的干扰素-γ分泌(通过流式微球分析技术(cytometricbeadassay)测定)5天。图10:用指定化合物刺激48小时的巨噬细胞的干扰素-γ分泌(通过流式微球分析技术测量)。图11:用指定化合物刺激48小时的pbmc或巨噬细胞的趋化因子rantes分泌(通过流式微球分析技术测定)。图12:用指定化合物刺激48小时的pbmc或巨噬细胞的il12p70分泌(通过流式微球分析技术测定)。图13:用指定化合物刺激48小时的pbmc、巨噬细胞或cd4t细胞的il1b分泌(通过流式微球分析技术测量)。图14:先前用指定剂量的化合物1注射24小时的c57bl/6小鼠血液中的%cd25high细胞。通过流式细胞术测量cd25表达。图15:先前24小时注射了所示化合物的3只c57bl/6小鼠的脾脏中的%mhci类高cd11b+细胞。通过流式细胞术测量mhci类和cd11b表达。图16:抗pd-1阻断和isr397之间的协同效应。c57bl/6j小鼠皮下接种b16-f10黑素瘤细胞,然后用抗pd-1(实心圆)、抗pd-1+isr397(实心正方形)处理或不处理(实心三角形)。显示在第3、8、11、15、18天测量的肿瘤体积。图17:抗pd-1阻断和isr397之间的协同效应。c57bl/6j小鼠皮下接种b16-f10黑素瘤细胞,然后或者保持不处理(粉红色),用抗pd-1处理(紫色)或者用抗pd-1+isr397处理(红色)。显示了实验终止时(第18天)测量的肿瘤体积。图18.抗pd-1阻断和isr397之间的协同作用。c57bl/6j小鼠皮下接种b16-f10黑素瘤细胞,然后用抗pd-1(实心圆)、抗pd-1+isr397(实心正方形)处理或不处理(实心三角形)。显示了在第3、8、11、15、18天测量的肿瘤体积。图19.所提出的isr397(化合物1)作用机制的描述。发明介绍大环内酯类例如红霉素和阿奇霉素已经常年用于治疗细菌感染。红霉素是通过放线菌糖多孢红霉菌(saccharopolysporaerythraea)的发酵产生的聚酮天然产物大环内酯。阿奇霉素是红霉素的半合成氮杂内酯衍生物。许多参考文献描述了大环内酯类例如红霉素的抗菌活性。这种抗菌机制是通过分子与细菌50s细菌核糖体上的p位点结合来实现的,从而干扰trna结合。许多参考文献描述了通过半合成和生物合成工程产生红霉素的类似物。特别是,已经描述了用于半合成去除红霉素、去氧糖胺(desosamine)/克拉定糖和碳霉糖(mycarose)上的糖基的方法。已经描述了用于生物转化以向红霉素糖苷配基添加替代糖基的其他方法(例如参见gaisser等人,2000、schell等人,2008和wo2001/079520)。然而,该公开的工作的主要焦点是产生抗菌红霉素类似物。wo2007/004267公开了通过施用包含含有mtor抑制剂和白蛋白的纳米颗粒的组合物与包含第二治疗剂的组合物组合来治疗实体瘤的方法和组合物。wo2016/100882公开了用于治疗癌症的包含免疫调节剂和第二治疗剂的组合,其中所述免疫调节剂是免疫检查点分子的抑制剂。发明描述本发明涉及大环内酯和免疫检查点抑制剂的组合,以改善治疗,尤其是在癌症和刺激免疫系统有益的癌症中的治疗。以前没有报道过缺乏抗菌活性的大环内酯类的免疫刺激活性。令人惊讶的是,现在已经发现本发明的化合物,如化合物1(图8),对免疫系统的若干细胞类型具有有效的免疫刺激作用。在用1μm化合物1体外刺激外周血单核细胞(pbmc)24-48小时后,cd4+t细胞和b细胞上的激活标记物cd69被上调(图1)。我们还观察到t细胞和b细胞上mhci类分子(hla-abc)的上调(图2),表明对病毒抗原的抗原呈递的影响。用化合物1刺激pbmc群体中的单核细胞导致共刺激分子cd80以及抗原呈递分子mhcii类(hla-dr)的上调(图3)。分化成巨噬细胞的单核细胞也响应于化合物1的刺激而显示出cd80上调(图4)。此外,用化合物1刺激的pbmc表达改变的细胞因子谱,其中免疫抑制细胞因子il-10的产生增加,表明在某些条件下具有免疫抑制作用。化合物1的免疫学作用的进一步分析显示,用流式细胞术测量,刺激6天后t细胞的细胞因子驱动的增殖谱的改变(图6)。此外,病毒特异性t细胞增殖受化合物1的影响。在cmv抗原和化合物1存在下培养的巨细胞病毒(cmv)感染的供体的pbmc显示出活化的cmv特异性cd8+t细胞的表型改变,以及il-7受体α(cd127)表达增加(图7)。cd127对于t细胞稳态、分化和功能至关重要,并且表达降低与hiv和其他慢性病毒性疾病中的疾病严重性相关(crawley等人2012)。总之,化合物1具有通过影响抗原呈递、共刺激和t细胞活化和增殖来特异性激活和修饰免疫应答的惊人能力。在许多本文提供的实例中,包括化合物2(图8)(先前在schell等人2008中作为化合物20公开的另一种相关的具有改变的糖基化的大环内酯红霉素类似物)作为阴性对照,因为它在试验中显示很小活性或没有活性。大环内酯与免疫检查点抑制剂组合使用最大化免疫系统的调节作用,同时最小化治疗上不想要的直接抗菌作用。因此,本发明涉及大环内酯和免疫检查点抑制剂的组合。所述组合可用于预防和治疗癌症。预期大环内酯和免疫检查点抑制剂的组合将通过将大环内酯的免疫刺激作用与检查点抑制剂介导的释放对免疫系统的中断这二者组合,而导致增强的抗肿瘤作用。用于这种组合的大环内酯类包括式(i)的大环内酯(参见本文的单独段落),但不限于此。所感兴趣的特异性免疫检查点抑制剂包括选自ctla4抑制剂、pd-1抑制剂、pd-l1抑制剂、pd-l2抑制剂、lag3抑制剂、b7-h3抑制剂和cmtm6抑制剂的活性剂,但不限于此。在本文的单独段落中给出了适合与大环内酯组合使用的免疫检查点抑制剂的实例。大环内酯和免疫检查点抑制剂的特别令人感兴趣的组合包括其中大环内酯选自本文所述化合物的组合。更特别感兴趣的是选自本文给出的具有包括化合物1(isc397)的结构式的化合物的大环内酯类与选自pd-1、pd-l1和ctla-4的抑制剂的免疫检查点抑制剂的组合,如isc397+pd-1、isc397+pd-l1或isc397+ctla-4或isc397+pd-1+ctla-4或isc397+pd-l1+ctla-4。大环内酯和免疫检查点抑制剂的组合可以是包含大环内酯、免疫检查点抑制剂和一种或多种药学上可接受的赋形剂的药物组合物的形式,或者其可以是两种药物组合物的形式,其中一种组合物包含大环内酯和一种或多种药学上可接受的赋形剂,另一种组合物包含免疫检查点抑制剂和一种或多种药学上可接受的赋形剂。在后一种情况下,两种组合物可以设计用于相同或不同的施用途径。或者,大环内酯和免疫检查点抑制剂的组合可以是化妆品组合物的形式,所述化妆品组合物包含大环内酯、免疫检查点抑制剂和一种或多种化妆品可接受的赋形剂。大环内酯和免疫检查点抑制剂的组合还可以是药盒的形式,所述药盒在单个包装中包括:i)第一组合物,其包含大环内酯,ii)第二组合物,其包含免疫检查点抑制剂,和iii)使用说明书。本发明组合的通用用途大环内酯和免疫检查点抑制剂的组合可用于药物和/或化妆品。大环内酯和免疫检查点抑制剂的组合在医药中的用途是特别令人感兴趣的。潜在的应用包括治疗或预防任何相关癌症形式的方法,所述方法包括向有需要的人或动物个体施用治疗有效量的大环内酯和免疫检查点抑制剂的组合。本发明还涉及用于治疗或预防癌症的方法,所述方法包括向有需要的人或动物个体施用治疗有效量的根据本文所述的权利要求和实施方案中任一项的组合。大环内酯和免疫检查点抑制剂的组合,包括包含所述组合的药物组合物和药盒,预期可用于预防和治疗任何形式的癌症,包括但不限于肾上腺癌、肛门癌、胆管癌、膀胱癌、骨癌、脑/cns肿瘤、乳腺癌、castleman病、宫颈癌、结肠/直肠癌、子宫内膜癌、食道癌、眼癌、胆囊癌、胃肠道类癌肿瘤(gastrointestinalcarcinoidtumors)、胃肠道间质瘤(gastrointestinalstromaltumor)(gist)、妊娠滋养细胞疾病、霍奇金病、卡波西肉瘤(kaposisarcoma)、肾癌、喉癌和下咽癌(laryngealandhypopharyngealcancer)、急性髓性白血病(acutemyeloidleukemia)、慢性淋巴细胞白血病(chroniclymphocyticleukemia)、急性淋巴细胞白血病(acutelymphocyticleukemia)、慢性髓性白血病(chronicmyeloidleukemia)、慢性粒单核细胞白血病(chronicmyelomonocyticleukemia)、肝癌(livercancer)、非小细胞肺癌(non-smallcelllungcancer)、小细胞肺癌(smallcelllungcancer)、肺类癌(lungcarcinoidtumor)、淋巴瘤(lymphoma)、恶性间皮细胞瘤(malignantmesothelioma)、多发性骨髓瘤(multiplemyeloma)、骨髓增生异常综合征(myelodysplasticsyndrome)、鼻腔和副鼻窦癌(nasalcavityandparanasalsinuscancer)、鼻咽癌(nasopharyngealcancer)、神经母细胞瘤(neuroblastoma)、非霍奇金淋巴瘤(non-hodgkinlymphoma)、口腔和口咽癌(oralcavityandoropharyngealcancer)、骨肉瘤(osteosarcoma)、卵巢癌(ovariancancer)、胰腺癌(pancreaticcancer)、阴茎癌(penilecancer)、垂体瘤(pituitarytumors)、前列腺癌(prostatecancer)、视网膜母细胞瘤(retinoblastoma)、横纹肌肉瘤(rhabdomyosarcoma)、唾液腺癌(salivaryglandcancer)、基底细胞和鳞状细胞皮肤癌(basalandsquamouscellskincancer)、黑色素瘤(melanoma)、梅克尔细胞皮肤癌(merkelcellskincancer)、小肠癌(smallintestinecancer)、胃癌(stomachcancer)、睾丸癌(testicularcancer)、胸腺癌(thymuscancer)、甲状腺癌(thyroidcancer)、子宫肉瘤(uterinesarcoma)、阴道癌(vaginalcancer)、外阴癌(vulvarcancer)、华氏巨球蛋白血症(waldenstrommacroglobulinemia)和肾母细胞瘤(wilmstumor)。本文公开的本发明组合还可用于治疗其中免疫应答刺激有用的疾病、障碍、病症和征状,如用于治疗感染有病毒物质或患有病毒性疾病的患者,所述病毒和病毒性疾病例如hiv、腺病毒、甲病毒、虫媒病毒、borna病、布尼亚病毒、杯状病毒、尖锐湿疣、冠状病毒、柯萨奇病毒、巨细胞病毒、登革热病毒、传染性脓疱(contageousecthyma)、爱泼斯坦-巴尔病毒、感染性红斑、汉坦病毒、病毒性出血热、病毒性肝炎、单纯疱疹病毒、带状疱疹病毒、感染性单核球增多症、流感、拉沙热病毒、麻疹、腮腺炎、传染性软疣、副粘病毒、白蛉热、多瘤病毒、裂谷热、风疹、慢性病病毒、天花、亚急性硬化性脑炎、肿瘤病毒感染、西尼罗病毒、黄热病毒、狂犬病病毒和呼吸道合胞病毒(respiratorysyncitialvirus)。特别是,在本发明的上下文中hiv是令人感兴趣的。本文所述的大环内酯类可用于医药、医学研究或用于制造用于此用途的组合物。因此,当在下文中术语“大环内酯类”与医药用途或药物组合物结合使用时,该术语还包括式(i)化合物。特别地,本文所述的式(i)大环内酯的医药用途包括这样的化合物,其中当r1是et,r2是式(ii)的糖,r13是oh,r14是h,ra是h,r4是me,r5是h,r6是oh,r7是h,r8是nr11r12,r9是h,r10是h,且x是c=o。设计式(i)的大环内酯类是为了使直接抗菌作用最小化,而关注于免疫激活特性。当将本发明化合物加入到细菌大肠杆菌(e.coli)、唾液链球菌(s.salivarius)、干酪乳杆菌(l.casei)、长双歧杆菌(b.longum)或藤黄微球菌(m.luteus)的培养物中时,没有发现抗菌作用或发现最低限度的抗菌作用。具有影响宿主细胞的单独的免疫刺激性质的化合物的优点是避免了细菌抗性的出现。此外避免了大环内酯类药物公知的影响肠道微生物群的副作用,其具有使导致腹泻和假性结肠炎(pseudomebraneouscolitis)的梭状芽孢杆菌(clostridiumdifficile)过度生长的风险。许多细胞内病原体,例如mtb以及病毒和癌症已经发展出避免免疫识别的机制,即通过下调hla表达,以避免被t细胞检测。化合物的干预机制依赖于感染细胞上hla分子的激活和提高的表达。hla分子加载并呈递源自细胞内感染物质的肽,以呈现t细胞的识别信号,以允许消除受感染的细胞与已知的大环内酯类相比,式(i)化合物的有利性质可以包括以下一种或多种:-降低的直接抗菌活性-改善的mhci类刺激-改善的免疫调节-改善的抗原呈递细胞的活化-改善的t细胞应答-改善的抗肿瘤应答-改善的抗病毒活性-改善的mhcii类抗原呈递包含本发明组合的药物组合物本发明还提供了包含本发明的组合以及一种或多种药学上可接受的稀释剂或载体的药物组合物。大环内酯和免疫检查点抑制剂的组合可以是包含大环内酯、免疫检查点抑制剂和一种或多种药学上可接受的赋形剂的药物组合物的形式,或者其可以是两种药物组合物的形式,其中一种组合物包含大环内酯和一种或多种药学上可接受的赋形剂,另一种组合物包含免疫检查点抑制剂和一种或多种药学上可接受的赋形剂。在后一种情况下,两种组合物可以设计用于相同或不同的施用途径。本发明的组合或其制剂可以通过任何常规途径施用,例如但不限于它们可以肠胃外、口服、局部或经由粘膜(包括颊、舌下、透皮、阴道、直肠、鼻、眼等)、经由医疗装置(例如支架)或通过吸入施用。治疗可以由在一段时间内的单次施用或多次施用组成。每种化合物(即分别为大环内酯和检查点抑制剂)或包含化合物的组合物可以通过单独的施用途径和以不同的制剂类型施用。此外,施用频率可以不同。大环内酯和检查点抑制剂的施用方案可以根据所讨论的化合物或组合物的性质而变化。施用方案可以由该组合的单次施用或分别包含大环内酯或检查点抑制剂的两种组合物组成。施用方案还可以是在一个或多个时间段内的多次施用。根据具体用途、待治疗的疾病和待治疗患者的身体状况和特征(如性别、体重和年龄),可以每日一次、每日两次、每日三次、每日四次、较不频繁或更频繁地进行施用。还可以通过连续施用(例如通过滴剂或通过贮库的静脉内施用或缓释制剂)来进行治疗。虽然本发明的组合可以以这样的形式施用,但是优选以药物制剂的形式与一种或多种可接受的载体一起提供。载体必须是“可接受的”,即与本发明的化合物相容,并且对其接受者无害。合适载体的实例更详细地描述于下文中。药物组合物可以方便地以合适的包括单位剂型在内的剂型存在,并且可以通过药学领域熟知的任何方法制备。这些方法包括使本发明化合物与一种或多种赋形剂结合的步骤。通常,药物组合物通过将本发明化合物与赋形剂均匀且紧密地结合在一起来制备,然后,如果需要,将所得组合物成型为例如片剂。本发明的组合通常通过任何常规施用途径施用,通常通过口服或任何肠胃外途径,以包含活性成分的药物制剂的形式施用,任选地以无毒的有机或无机酸或碱、加成盐的形式,并以药学上可接受的剂型施用。取决于病症和待治疗的患者,以及施用途径,组合物可以不同的剂量和/或频率施用。药物组合物在制造和储存条件下必须是稳定的;因此,如果必要的话,应该防止微生物如细菌和真菌的污染作用。在液体制剂如溶液、分散液,乳液和混悬液的情况下,载体可以为含有例如以下物质的溶剂或分散介质:水、乙醇、多元醇(例如甘油、丙二醇和液体聚乙二醇)、植物油、及其合适的混合物。例如,本发明的组合物可以以片剂、胶囊、薄膜、珠剂、酏剂、溶液、乳液或混悬液的形式口服、含服或舌下施用,其可含有调味剂或着色剂。适合于口服施用的本发明药物组合物可以作为离散单元存在,例如胶囊、扁囊剂或片剂,各自含有预定量的活性成分;作为多个单元存在,例如片剂或胶囊形式;作为粉末或颗粒存在;作为水性液体或非水性液体中的溶液或混悬液存在;或者作为水包油液体乳液或油包水液体乳液存在。活性成分也可以以大丸剂、药糖剂或糊剂形式存在。适于口服施用的本发明的组合的溶液或混悬液还可含有一种或多种溶剂,包括水、醇、多元醇等,以及一种或多种赋形剂,如ph调节剂、稳定剂、表面活性剂、增溶剂、分散剂、防腐剂、香料等。具体实例包括例如n,n-二甲基乙酰胺、分散剂,例如聚山梨醇酯80、表面活性剂和增溶剂,例如,聚乙二醇、phosal50pg(由磷脂酰胆碱、大豆脂肪酸、乙醇、甘油单酯/甘油二酯、丙二醇和抗坏血酸棕榈酸酯组成)。根据本发明的制剂还可以为乳液形式,其中本发明的组合可以存在于乳液中,例如水包油乳液或油包水乳液。油可以为天然或合成油或任何类似油的物质,例如大豆油或红花油或其组合。片剂可含有赋形剂,例如微晶纤维素、乳糖(例如乳糖一水合物或无水乳糖)、柠檬酸钠、碳酸钙、磷酸氢钙和甘氨酸、丁基化羟基甲苯(e321)、交联聚维酮、羟丙甲纤维素、崩解剂,例如淀粉(优选玉米、马铃薯或木薯淀粉)、羟基乙酸淀粉钠、交联羧甲基纤维素钠和某些复合硅酸盐、和造粒粘合剂,例如聚乙烯吡咯烷酮、羟丙基甲基纤维素(hpmc)、羟丙基纤维素(hpc)、聚乙二醇8000、蔗糖、明胶和阿拉伯胶。此外,可以包括润滑剂,例如硬脂酸镁、硬脂酸、山嵛酸甘油酯和滑石。片剂可以通过压制或模塑制得,任选地含有一种或多种辅助成分。压制片剂可以通过在合适的机器中压制自由流动形式(如粉末或颗粒)的活性成分,任选地与粘合剂(例如聚维酮、明胶、羟丙基甲基纤维素)、润滑剂、惰性稀释剂、防腐剂、崩解剂(例如羟基乙酸淀粉钠、交联聚维酮、交联羧甲基纤维素钠)、表面活性剂或分散剂混合来制备。模制片剂可以通过在合适的机器中模塑用惰性液体稀释剂润湿的粉末化合物的混合物来制备。片剂可以任选地被包衣或刻痕,并且可以配制成使其中的活性成分缓慢或受控释放,例如使用不同比例的羟丙基甲基纤维素以提供所需的释放曲线。类似类型的固体组合物也可用作明胶胶囊中的填充剂。就此而言,优选的赋形剂包括乳糖、淀粉、纤维素、乳糖或高分子量聚乙二醇。对于含水混悬液和/或酏剂,本发明的组合可与各种甜味剂或调味剂、着色剂或染料、乳化剂和/或混悬剂以及稀释剂(例如水、乙醇、丙二醇和甘油)、以及它们的组合混合。适于在口腔中局部施用的本发明的药物组合物包括:含有在调味基质(通常为蔗糖和阿拉伯胶或黄蓍胶)中的活性成分的锭剂;软锭剂(pastille),其包含在惰性基质(例如明胶和甘油,或蔗糖和阿拉伯胶)中的活性成分;和漱口水,其包含在适合的液体载体中的活性成分。适于局部施用的本发明的药物组合物可以配制成软膏剂、霜剂、混悬液、洗剂、粉末、溶液、糊剂、凝胶、浸渍敷料剂、喷雾剂、气雾剂或油剂、透皮装置、扑粉(dustingpowder)等。这些组合物可通过含有活性剂的常规方法制备。因此,它们还可以包含相容的常规载体和添加剂,例如防腐剂、有助于药物渗透的溶剂,霜剂或膏剂中的润肤剂和用于洗剂的乙醇或油醇。这些载体可以占组合物的约1%至约98%。更常见的是,它们将占组合物的约80%。仅作为说明,通过将足量的含有约5-10%重量的化合物的亲水性材料和水以足够的量混合,来制备霜剂或膏剂,以产生具有所需稠度的霜剂或膏剂。适于透皮施用的本发明的药物组合物可以作为离散的贴剂存在,其旨在与受体的表皮保持长时间的紧密接触。例如,可通过离子电渗从贴剂递送活性成份。对于施用于外部组织(例如口腔和皮肤),组合物优选作为局部霜剂或膏剂施用。当配制成膏剂时,活性成份可与石蜡或水混溶性软膏基质一起使用。或者,可以将活性成份配制成具有水包油乳膏基质或油包水基质的霜剂。对于肠胃外施用,使用活性成分和无菌载体制备流体单位剂型,无菌载体例如但不限于水、醇、多元醇、甘油和植物油,优选水。取决于使用的载体和浓度,活性成分可以是胶状的、混悬的或溶解在载体中。在制备溶液时,可将活性成分溶解在注射用水中并过滤灭菌,然后装入合适的小瓶或安瓿中并密封。有利地,诸如局部麻醉剂、防腐剂和缓冲剂的试剂可以溶解在载体中。为了增强稳定性,可以在填充到小瓶中之后冷冻组合物并在真空下去除水。然后将干燥的冻干粉末密封在小瓶中,并且可以提供附带的注射用水小瓶,以在使用前重新配制液体。适用于注射用途的本发明药物组合物包括无菌水溶液或分散液。此外,组合物可以是无菌粉末的形式,用于临时制备这种无菌可注射溶液或分散液。在所有情况下,最终的可注射形式必须是无菌的并且必须是有效的流体以便于注射。胃肠外混悬液以与溶液基本相同的方式制备,不同之处在于活性成分混悬在载体中而不是溶解,并且不能通过过滤完成灭菌。活性成分可以在混悬于无菌载体中之前通过暴露于环氧乙烷来灭菌。有利地,组合物中包含表面活性剂或润湿剂以促进活性成分的均匀分布。应当理解,除了上面特别提到的成分之外,本发明的制剂可以包括本领域中常规的与所讨论的制剂类型有关的其他试剂,例如适合口服施用的制剂可包括调味剂。本领域技术人员将知道如何选择合适的制剂以及如何制备它(参见例如remington’spharmaceuticalsciences第十八版或更新版本)。本领域技术人员还将知道如何选择合适的施用途径和剂量。本领域技术人员将认识到,本发明的组合的单个剂量的最佳量和间隔将取决于所治疗病症的性质和程度、施用的形式、途径和部位、以及所治疗的特定个体的年龄和状况。并且医生将最终确定要使用的适当剂量。该剂量可以适当地重复进行。如果产生副作用,则可以根据正常的临床实践改变或减少剂量的量和/或频率。除非上下文另有要求,否则本文提及的所有%值均为%w/w。用于本发明组合的大环内酯类用于本发明组合的免疫刺激性大环内酯是式(i)的大环内酯或其药学上可接受的盐、水合物、溶剂合物、互变异构体、对映异构体或非对映异构体:其中x选自c=o、-nr3ch2-、-ch2nr3-、-nr3(c=o)-、-(c=o)nr3-、c=noh和-ch(oh)-,且r2是式(ii)或式(iii)的糖:其中r1选自烷基、杂烷基、环烷基、芳基和杂芳基结构部分,其中烷基结构部分选自任选支化的c1-c6烷基,其中杂烷基结构部分选自任选支化或被取代的且任选地包含一个或多个杂原子的c1-c6烷基,其中环烷基结构部分选自任选被取代的且任选地包含一个或多个杂原子的c1-c6环烷基,其中芳基结构部分选自任选地被取代的c6芳环,其中杂芳基结构部分选自包含一个或多个杂原子的任选取代的c1-c5芳环,其中杂原子选自o、n、p和s,其中取代基独立地选自烷基、oh、f、cl、nh2、nh-烷基、nh-酰基、s-烷基、s-酰基、o-烷基和o-酰基,其中所述酰基选自选自任选支化的c1-c4酰基,其中r3选自h和me,其中r4选自h和me,其中ra选自h和-cr21r22r23,其中r21、r22、r23和r5、r6、r7、r8、r9和r10独立地选自h、me、nr11r12、no2和or11,其中式(ii)中的r23与r4一起、式(ii)中的r4与r5一起、式(ii)中的r5与r7一起、以及式(ii)中的r7与r9一起各自独立地结合来表示键,从而在各基团连接的碳原子之间形成双键,使得其中如果r23和r4连接形成双键,则式(ii)可以通过以下表示:其中如果r4和r5连接形成双键,则式(ii)可以通过以下表示:其中如果r5和r7连接形成双键,则式(ii)可以通过以下表示:其中如果r7和r9连接形成双键,则式(ii)可以通过以下表示:其中式(iii)中的r4与r5一起,式(iii)中的r4与r7一起,式(iii)中的r7与r9一起各自独立地结合来表示键,从而在各基团连接的碳原子之间形成双键,使得其中如果r4和r5连接形成双键,则式(iii)可以通过以下表示:其中如果r4和r7连接形成双键,则式(iii)可以通过以下表示:其中如果r7和r9连接形成双键,则式(iii)可以通过以下表示:其中r21与r22一起,r5与r6一起,r7与r8一起,或r9与r10一起可被羰基替代,其中r11和r12独立地选自h和烷基,其中r13选自h、oh和och3,其中r14选自h和oh,且其中r5、r6、r7、r8、r9或r10之一选自nr11r12和no2。在一些方面,大环内酯为式(i),条件是当r1是et,r2是式(ii)的糖,r13是h或oh,r14是h或oh,ra是h,r4是me,r5是h,r6是oh,r7是h,r8是nr11r12,r9是h,且r10是h时,x可以不是c=o,条件是当r1是et,r2是式(ii)的糖,r13是h或oh,r14是h或oh,ra是h,r4是me,r5是oh,r6是h,r7是oh,r8是me,r9是h,且r10是h时,x可以不是c=o,条件是当r1是et,r2是式(ii)的糖,r13是h或oh,r14是h或oh,ra是h,r4是me,r5是oh,r6是h,r7是h,r8是nr11r12,r9是h,且r10是oh时,x可以不是c=o。式(i)的免疫刺激性大环内酯类或其药学上可接受的盐、水合物、溶剂合物、互变异构体、对映异构体或非对映异构体可具有以下结构式(i)其中x选自c=o、-nr3ch2-和-ch(oh)-,且r2是式(ii)的糖:式(ii)其中r1选自烷基或环烷基结构部分,其中烷基结构部分选自任选支化的且独立地、任选地被羟基取代的c1-c6烷基,其中环烷基结构部分选自任选取代的c1-c6环烷基、其中取代基选自烷基和oh,其中r3选自h和me,其中r4选自h和me,其中ra选自h和-cr21r22r23,其中r21、r22、r23和r5、r6、r7、r8、r9和r10独立地选自h、me、nr11r12、no2和or11,其中式(ii)中的r23与r4一起、式(ii)中的r4与r5一起、式(ii)中的r5与r7一起、以及式(ii)中的r7与r9一起各自独立地结合来表示键,从而在各基团连接的碳原子之间形成双键,使得其中如果r23和r4连接形成双键,则式(ii)可以通过以下表示:其中如果r4和r5连接形成双键,则式(ii)可以通过以下表示:其中如果r5和r7连接形成双键,则式(ii)可以通过以下表示:其中如果r7和r9连接形成双键,则式(ii)可以通过以下表示:其中r21与r22、r5与r6、r7与r8或r9与r10一起可被羰基替代,其中r11和r12独立地选自h和烷基,其中r13选自h、oh和och3,其中r14选自h和oh,且其中r5、r6、r7、r8、r9或r10之一选自nr11r12和no2。在一个方面,上述提及的大环内酯类为式(i)条件是当r1是et,r2是式(ii)的糖,r13是h或oh,r14是h或oh,ra是h,r4是me,r5是h,r6是oh,r7是h,r8是nr11r12,r9是h,且r10是h时,x可以不是c=o。条件是当r1是et,r2是式(ii)的糖,r13是h或oh,r14是h或oh,ra是h,r4是me,r5是oh,r6是h,r7是oh,r8是me,r9是h,且r10是h时,x可以不是c=o。条件是当r1是et,r2是式(ii)的糖,r13是h或oh,r14是h或oh,ra是h,r4是me,r5是oh,r6是h,r7是h,r8是nr11r12,r9是h,且r10是oh时,x可以不是c=o。所述大环内酯类可通过用于制备式(i)化合物的方法提供,所述方法包括将式iv的糖苷配基添加到在3-羟基位置糖基化的生物转化菌株的培养物中。感兴趣的大环内酯类的选择是其中r2选自以下的化合物:l-六碳氨糖、3-氨基-2,3,6-三脱氧-l-阿拉伯糖-己糖(l-acosamine)、l-利托胺(l-ristosamine)、d-利托胺、4-氧代-l-万古胺(4-oxo-l-vancosamine)、l-万古胺、d-福莫胺(d-forosamine)、l-放线菌胺(l-actinosamine)、3-表-l-万古胺(3-epi-l-vancosamine)、l-维吉尼胺(l-vicenisamine)、l-海藻糖胺(l-mycosamine)、d-海藻糖胺、d-3-n-甲基-4-o-甲基-l-利托胺、d-红霉脱氧糖胺(desosamine)、n,n-二甲基-l-吡咯烷胺、l-megosamine、l-nogalamine、l-紫红霉胺(l-rhodosamine)、d-安哥拉糖胺(d-angolosamine)、l-可达菌胺(l-kedarosamine)、2'-n-甲基-岩藻糖胺(2'-n-methyl-fucosamine)、3-n,n-二甲基-l-eremosamine、d-拉维胺(d-ravidosamine)、3-n,n-二甲基-d-海藻糖胺/d-碳霉糖(3-n,n-dimethyl-d-mycosamine/d-mycaminose)、3-n-乙酰基-d-拉维胺、4-o-乙酰基-d-拉维胺、3-n-乙酰基-4-o-乙酰基-d-拉维胺、d-葡萄糖胺、n-乙酰基-d-葡萄糖胺、l-红霉脱氧糖胺、d-阿毛示糖(d-amosamine)、d-紫霉胺(d-viosamine)、l-avidinosamine、d-古洛糖胺(d-gulosamine)、d-别霉胺(d-allosamine)和l-西伯利亚霉胺(l-sibirosamine)。另一个感兴趣的大环内酯类的选择是其中r2选自d-安哥拉糖胺、n-去甲基d-安哥拉糖胺、n-二去甲基d-安哥拉糖胺、n-去甲基n-乙基d-安哥拉糖胺和n-二去甲基n-二乙基d-安哥拉糖胺的化合物。另一个感兴趣的大环内酯类的选择是其中r2选自n-去甲基d-安哥拉糖胺、n-二去甲基d-安哥拉糖胺、n-去甲基n-乙基d-安哥拉糖胺和n-二去甲基n-二乙基d-安哥拉糖胺的化合物。另一个感兴趣的大环内酯类的选择是其中r2是根据式(ii)的糖的化合物。另一个感兴趣的大环内酯类的选择是其中r2是根据式2的糖的化合物,其中ra是h,r4是me,r5是h,r6是oh,r7是h,r8是nr11r12,r9是h,且r10是h。另一个感兴趣的大环内酯类的选择是化合物,其中r11选自h、me和et,且r12选自h、me和et。另一个感兴趣的大环内酯类的选择是化合物,其中r11是et,且r12是et。另一个感兴趣的大环内酯类的选择是化合物,其中r11是me,且r12是et。另一个感兴趣的大环内酯类的选择是化合物,其中x选自c=o、–nr3ch2-和-ch(oh)-另一个感兴趣的大环内酯类的选择是化合物,其中r1选自me、et和环烷基。另一个感兴趣的大环内酯类的选择是化合物,其中r1选自me和et。另一个感兴趣的大环内酯类的选择是化合物,其中x选自-nr3ch2-或-ch2nr3-。另一个感兴趣的大环内酯类的选择是化合物,其中r5、r6、r7或r8之一是nr11r12。另一个感兴趣的大环内酯类的选择是化合物,其中r21、r22、r23和r5、r6、r7、r8、r9和r10独立地选自h、me、nr11r12和or11。另一个感兴趣的大环内酯类的选择是化合物,其中r13和r14是oh。特别感兴趣的是式(i)的大环内酯类,其中r1是et,r2是式(ii)的糖,r13是oh,r14是h,ra是h,r4是me,r5是h,r6是oh,r7是h,r8是nr11r12,r9是h,r10是h,且x是c=o。具体的大环内酯类包括:如本文实施例所示,一些大环内酯类如本文所定义没有实质的抗菌活性。式(i)的大环内酯类的通用制备方法技术人员将认识到,可以使用已知方法以多种方式制备式(i)的大环内酯类。以下路线仅说明可用于制备式(i)的化合物的一些方法当生物转化需要糖苷配基时,可以通过多种方式获得这些糖苷配基。阿奇霉素和红霉素很容易获得并被认为是合适的起点。通过化学方法(例如糖苷切割)去除碳霉糖/克拉定糖和/或去氧糖胺。简而言之,在一种方法中,可以通过用酸处理来去除糖。为了便于去除氨基糖,首先必须氧化二甲胺以形成n-氧化物,然后通过热解将其去除。然后可以通过酸性降解将所得的5-o/3-o糖去除。lemahieu等人1974和djokic等人1988教导了一种合适的方法。最后,使用添加氨基糖的细菌菌株对该化合物进行生物转化。合适的糖苷配基的另一种途径是通过发酵和从合适的阻断型突变株(blockedmutant)中分离。例如,红霉内酯(erythronolide)b(3a)可以通过糖基化阻断的糖多孢红霉菌(s.erythraea)菌株的发酵来产生,例如在us.3,127,315(例如nrrl2361、nrrl2360、nrrl2359和nrrl2338)和gaisser等人2000(例如糖多孢红霉菌dmδbvδciii)中描述的菌株和方法。简而言之,通过本领域已知的方法进行发酵。通常,制备菌种培养物并将其转移至生产容器中。生产阶段为4-10天,生物体在24℃-30℃之间生长,并进行适当的搅拌和通气。然后可以通过提取和纯化分离糖苷配基。当本发明的糖苷配基或化合物具有氨基糖或任何其它叔胺并且通过发酵制备时,需要提取细菌发酵液并纯化该化合物。通常,将细菌发酵液调节至ph8-10,理想的是9.5。然后可以用合适的有机溶剂提取发酵液。该溶剂不是水溶性的,并且理想的是乙酸乙酯、甲基叔丁基醚(mtbe)或具有类似性质的溶剂。将发酵液和溶剂理想地通过搅拌混合一段时间,例如30分钟或1小时。然后分离各相并除去有机萃取物。发酵液可以这种方式多次提取,理想的是两次或三次。然后可以在真空中浓缩合并的有机萃取物。然后将残余物溶解或混悬在弱酸性水溶剂中。通常,这是氯化铵水溶液。然后用水不混溶的有机溶剂如乙酸乙酯萃取多次,理想的是2或3次。收集所得的水层并将ph调节至ph8-10,理想的是9.0。然后将所得水层用与水不混溶的有机溶剂如乙酸乙酯萃取多次,理想的是2或3次。合并有机萃取物并真空浓缩,以得到目标化合物富集的粗提物,其需要进一步纯化。化合物纯化可以通过色谱法或(重)结晶进行,所需的方法是本领域技术人员公知的。当需要在正相二氧化硅上进行色谱法并且本发明的糖苷配基或化合物具有氨基糖或其他叔胺时,则向流动相中添加碱性改性剂是有利的。例如,在正相二氧化硅上进行的色谱法可以使用加入0-5%的氢氧化铵水溶液的己烷、乙酸乙酯、甲醇系统进行洗脱。理想地,加入2%氢氧化铵水溶液。在生物转化之后,可以使用合适的溶剂系统将未使用的糖苷配基和本发明的化合物与相同的粗提取物分开纯化。如果需要进一步纯化,可任选地通过制备型hplc进行。将伯胺或仲胺烷基化的还原胺化是本领域技术人员公知的。将胺在溶剂中与醛或酮混合,并加入还原剂。然后硼氢化钠可以还原由胺和羰基反应产生的亚胺或半缩醛胺,产生例如烷基化胺。硼氢化钠也可以还原存在的其他羰基,例如酮类。尽管对于本领域技术人员来说显而易见的是,可能需要测试不同的还原剂、溶剂、温度和反应时间以找到最佳条件,但在还存在酮的情况下,优选使用对质子化亚胺更具特异性的还原剂,例如氰基硼氢化钠。用于本发明组合的检查点抑制剂目前已知的检查点抑制剂以及仍未鉴定的检查点抑制剂是本发明感兴趣的。因此,感兴趣的是以下活性剂,其选自ctla4抑制剂,如伊匹木单抗和tremelimumab,或选自pd-1抑制剂,如派姆单抗(mk3475)、纳武单抗(mdx-1106)、pidilizumab(ct-011)、amp-224,或选自pd-l1抑制剂,如阿特朱单抗、阿维鲁单抗、德瓦鲁单抗、mdx-1105、anti-pd-1(来自merck、johnson、roche或astra的克隆rmp1-14),或选自pd-l2抑制剂,或选自lag3抑制剂,如imp321,或选自b7-h3抑制剂,如enoblituzumab和mgd009,或选自cmtm6。特别感兴趣的是选自伊匹木单抗、派姆单抗、纳武单抗、阿特朱单抗、阿维鲁单抗和德瓦鲁单抗的免疫检查点抑制剂。甚至更特别感兴趣的是选自pd-1抑制剂的免疫检查点抑制剂。然而,免疫检查点抑制剂的其它实例可在科学和专利文献中找到,并且也在本发明的范围内明。定义本文使用的单数形式的术语和“该”或“所述”是指一(种)或多于一个(种)(即至少一个(种))所述术语。举例来说,“一种类似物”表示一种类似物或多于一种类似物。如本文所用,术语“直接抗菌作用”是指通过与细菌rrna复合物结合而发生的红霉素和类似物的抗菌活性。该效果不需要任何宿主免疫系统组分的存在,因此在标准抗菌测定中是显而易见的,例如体外最小抑菌浓度(mic)测定和圆纸片抑制测定。如本文所用,术语“没有实质的抗菌活性”意指当与根据本文实施例13测试其对大肠杆菌、唾液链球菌、干酪乳杆菌和长双歧杆菌的抗菌活性时,本发明化合物的mic值>64μg/ml。如本文所用,术语“免疫刺激剂”意指激活免疫系统的化合物。如本文所用,句子“免疫检查点抑制剂靶向免疫检查点”意指其阻断检查点信号传导。如本文所用,术语“烷基”是指仅由sp3-杂化的碳原子组成的任何直链或支链,其用氢原子完全饱和,例如对于直链烷基为–cnh2n+1,其中n可以为1-6,例如甲基、乙基、丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、新戊基、异戊基、己基或异己基。本文使用的烷基可以进一步被取代。本文中的术语“杂烷基”表示单独或组合使用的基团-x-c1-6烷基,其中c1-6烷基如上所定义,x为o、s、nh或n-烷基。直链杂烷基的实例为甲氧基、乙氧基、丙氧基、丁氧基、戊氧基和己氧基。支链杂烷基的实例为异丙氧基、仲丁氧基、叔丁氧基、异戊氧基和异己氧基。环状杂烷基的实例为环丙氧基、环丁氧基、环戊氧基和环己氧基。本文所用的杂烷基可以进一步被取代。如本文所用,术语“环烷基”是指具有通式–cnh2n-1的环状/环状结构的碳链,其中n为3-6,例如环丙基、环丁基、环戊基或环己基等。本文所用的环烷基可以进一步被取代或在环状结构中含有杂原子(o、s、nh或n-烷基)。本文所用的术语“芳基”旨在包括碳环芳环系统。芳基还旨在包括以下列举的碳环系统的部分氢化衍生物。本文所用的术语“杂芳基”包括含有一个或多个选自氮、氧和硫的杂原子的杂环不饱和环系,例如呋喃基、噻吩基、吡咯基,并且还包括以下列举的杂环体系的部分氢化衍生物。本文所用的术语“芳基”和“杂芳基”是指芳基,所述芳基可以是任选地未取代的或单取代的、二取代的或三取代的;或杂芳基,其可以是任选未取代的或单取代的、二取代或三取代。“芳基”和“杂芳基”的实例包括但不限于苯基、联苯基、茚基、萘基(1-萘基、2-萘基)、n-羟基四唑基、n-羟基三唑基、n-羟基咪唑基、蒽基(1-蒽基、2-蒽基、3-蒽基)、菲基、芴基、并环戊二烯基(pentalenyl)、薁基、联苯基(biphenylenyl)、噻吩基(1-噻吩基、2-噻吩基)、呋喃基(furyl)(1-呋喃基、2-呋喃基)、呋喃基(furanyl)、噻吩基(thiophenyl)、异噁唑基、异噻唑基、1,2,3-三唑基、1,2,4-三唑基、吡喃基、哒嗪基、吡嗪基、1,2,3-三嗪基、1,2,4-三嗪基、1,3,5-三嗪基、1,2,3-噁二唑基(oxadiazolyl)、1,2,4-噁二唑基、1,2,5-噁二唑基、1,3,4-噁二唑基、1,2,3-噻二唑基、1,2,4-噻二唑基、1,2,5-噻二唑基、1,3,4-噻二唑基、四唑基、噻二嗪基(thiadiazinyl)、吲哚基、异吲哚基、苯并呋喃基、苯并噻吩基(硫杂茚基)、吲哚基、噁二唑基、异噁唑基、喹唑啉基、芴基、呫吨基(xanthenyl)、异茚满基、二苯甲基、吖啶基、苯并异噁唑基、嘌呤基、喹唑啉基、喹嗪基(quinolizinyl)、喹啉基(quinolinyl)、异喹啉基、喹喔啉基、萘啶基(naphthyridinyl)、喋啶基(phteridinyl)、氮杂基(azepinyl)、二氮杂基(diazepinyl)、吡咯基(2-吡咯基)、吡唑基(3-吡唑基)、5-噻吩-2-基-2h-吡唑-3-基、咪唑基(1-咪唑基、2-咪唑基、4-咪唑基、5-咪唑基)、三唑基(1,2,3-三唑-1-基、1,2,3-三唑-2-基、1,2,3-三唑-4-基、1,2,4-三唑-3-基)、噁唑基(2-噁唑基、4-噁唑基、5-噁唑基)、噻唑基(2-噻唑基、4-噻唑基、5-噻唑基)、吡啶基(2-吡啶基、3-吡啶基、4-吡啶基)、嘧啶基(2-嘧啶基、4-嘧啶基、5-嘧啶基、6-嘧啶基)、吡嗪基、哒嗪基(3-哒嗪基、4-哒嗪基、5-哒嗪基)、异喹啉基(1-异喹啉基)、3-异喹啉基、4-异喹啉基、5-异喹啉基、6-异喹啉基、7-异喹啉基、8-异喹啉基)、喹啉基(2-喹啉基、3-喹啉基、4-喹啉基、5-喹啉基、6-喹啉基、7-喹啉基、8-喹啉基)、苯并[b]呋喃基(2-苯并[b]呋喃基、3-苯并[b]呋喃基、4-苯并[b]呋喃基、5-苯并[b]呋喃基、6-苯并[b]]呋喃基、7-苯并[b]呋喃基)、2,3-二氢-苯并[b]呋喃基(2-(2,3-二氢-苯并[b]呋喃基)、3-(2,3-二氢-苯并[b]呋喃基)、4-(2,3-二氢-苯并[b]呋喃基)、5-(2,3-二氢-苯并[b]呋喃基)、6-(2,3-二氢-苯并[b]呋喃基)、7-(2,3-二氢-苯并[b]呋喃基))、苯并[b]噻吩基(2-苯并[b]噻吩基、3-苯并[b]噻吩基、4-苯并[b]噻吩基、5-苯并[b]噻吩基、6-苯并[b]噻吩基、7-苯并[b]噻吩基)、2,3-二氢-苯并[b]噻吩基(2-(2,3-二氢-苯并[b]噻吩基)、3-(2,3-二氢-苯并[b]噻吩基)、4-(2,3-二氢-苯并[b]噻吩基)、5-(2,3)-二氢-苯并[b]噻吩基)、6-(2,3-二氢-苯并[b]噻吩基)、7-(2,3-二氢-苯并[b]噻吩基))、吲哚基(1-吲哚基、2-吲哚基、3-吲哚基、4-吲哚基、5-吲哚基、6-吲哚基、7-吲哚基)、吲唑基(1-吲唑基、2-吲唑基、3-吲唑基、4-吲唑基、5-吲唑基、6-吲唑基、7-吲唑基)、苯并咪唑基、(1-苯并咪唑基、2-苯并咪唑基、4-苯并咪唑基、5-苯并咪唑基、6-苯并咪唑基、7-苯并咪唑基、8-苯并咪唑基)、苯并噁唑基(1-苯并噁唑基、2-苯并噁唑基)、苯并噻唑基(1-苯并噻唑基、2-苯并噻唑基、4-苯并噻唑基、5-苯并噻唑基、6-苯并噻唑基、7-苯并噻唑基)、咔唑基(1-咔唑基、2-咔唑基、3-咔唑基、4-咔唑基)。部分氢化衍生物的非限制性实例是1,2,3,4-四氢萘基、1,4-二氢萘基、吡咯啉基、吡唑啉基、二氢吲哚基、噁唑烷基、噁唑啉基、氧氮杂环庚三烯基(oxazepinyl)等。本发明化合物的药学上可接受的盐包括由药学上可接受的无机或有机酸或碱形成的常规盐以及季铵的酸加成盐。合适的酸盐的更具体实例包括盐酸、氢溴酸、硫酸、磷酸、硝酸、高氯酸、富马酸、乙酸、丙酸、琥珀酸、乙醇酸、甲酸、乳酸、马来酸、酒石酸、柠檬酸、棕榈酸、丙二酸、羟基马来酸、苯乙酸、谷氨酸、苯甲酸、水杨酸、甲苯磺酸、甲磺酸、萘-2-磺酸、苯磺酸、羟基萘甲酸、氢碘酸、苹果酸、硬脂酸(steroic)、单宁酸等。其它酸(例如草酸)虽然本身不是药学上可接受的,但可用于制备可用作获得本发明化合物及其药学上可接受的盐的中间体的盐。合适的碱性盐的更具体实例包括钠、锂、钾、镁、铝、钙、锌、n,n'-二苄基乙二胺、氯普鲁卡因、胆碱、二乙醇胺、乙二胺、n-甲葡糖胺和普鲁卡因盐。通过以下非限制性实施方案进一步描述本发明:1.大环内酯和免疫检查点抑制剂的组合。2.根据实施方案1的组合,其中大环内酯没有实质的抗菌活性。3.根据实施方案2的组合,其中当根据实施例13中所述的抗菌活性试验进行测试时,大环内酯具有>64μg/ml的mic值。4.根据前述实施方案中任一项的大环内酯和免疫检查点抑制剂的组合,其中大环内酯具有式i其中x选自c=o、-nr3ch2-、-ch2nr3-、-nr3(c=o)-、-(c=o)nr3-、c=noh和-ch(oh)-,且r2是式(ii)或式(iii)的糖:其中r1选自烷基、杂烷基、环烷基、芳基和杂芳基结构部分,其中烷基结构部分选自任选支化的c1-c6烷基,其中杂烷基结构部分选自任选支化或被取代的且任选地包含一个或多个杂原子的c1-c6烷基,其中环烷基结构部分选自任选被取代的且任选地包含一个或多个杂原子的c1-c6环烷基,其中芳基结构部分选自任选地被取代的c6芳环,其中杂芳基结构部分选自包含一个或多个杂原子的任选取代的c1-c5芳环,其中杂原子选自o、n、p和s,其中取代基独立地选自烷基、oh、f、cl、nh2、nh-烷基、nh-酰基、s-烷基、s-酰基、o-烷基和o-酰基,其中所述酰基选自选自任选支化的c1-c4酰基,其中r3选自h和me,其中r4选自h和me,其中ra选自h和cr21r22r23,其中r21、r22、r23和r5、r6、r7、r8、r9和r10独立地选自h、me、nr11r12、no2和or11,其中式(ii)中的r23与r4一起、式(ii)中的r4与r5一起、式(ii)中的r5与r7一起、以及式(ii)中的r7与r9一起各自独立地结合来表示键,从而在各基团连接的碳原子之间形成双键,其中r21与r22一起,r5与r6一起,r7与r8一起,或r9与r10一起可被羰基替代,其中r11和r12独立地选自h和烷基,其中r13选自h、oh和och3,其中r14选自h和oh,且其中r5、r6、r7、r8、r9或r10之一选自nr11r12和no2,或其药学可接受的盐。5.根据前述实施方案中任一项的组合,其中大环内酯选自:或其药学可接受的盐。6.根据前述实施方案中任一项的组合,其中大环内酯是或其药学可接受的盐。7.根据前述实施方案中任一项的组合,其中免疫检查点抑制剂靶向选自细胞毒性t淋巴细胞相关抗原4(ctla4,也称为cd152)、程序性细胞死亡蛋白1(pd-1,也称为cd279)、pd-1配体1(pd-l1,也称为b7-h1和cd274)、pd-1配体2(pd-l2,也称为b7-dc和cd-273)、t细胞膜蛋白3(tim3,也称为havcr2)、腺苷a2a受体(a2ar)、淋巴细胞活化基因3(lag3,也称为cd223)、b7-h3(也称为cd276)、b7-h4(也称为b7-s1、b7x和vctn1)、2b4(也称为cd244)、b和t淋巴细胞衰减子(btla,也称为cd272)和cmtm6的免疫检查点。8.根据前述实施方案中任一项的组合,其中免疫检查点抑制剂选自ctla4抑制剂、pd-1抑制剂、pd-l1抑制剂、pd-l2抑制剂、tim3抑制剂、a2ar抑制剂、lag3抑制剂、b7-h3抑制剂、b7-h4抑制剂、2b4抑制剂、btla抑制剂和cmtm6抑制剂。9.根据实施方案8的组合,其中大环内酯是或其药学可接受的盐,且所述免疫检查点抑制剂是pd-1抑制剂。10.根据前述实施方案中任一项的组合,其中免疫检查点抑制剂选自伊匹木单抗、tremelimumab、派姆单抗、纳武单抗、pidilizumab、amp-224、阿特朱单抗、阿维鲁单抗、德瓦鲁单抗、mdx-1105、imp321、enoblituzumab和mgd009。11.根据实施方案10的组合,其中免疫检查点抑制剂选自伊匹木单抗、派姆单抗、纳武单抗、阿特朱单抗、阿维鲁单抗和德瓦鲁单抗。12.根据前述实施方案中任一项的组合,其为两种药物组合物的形式,其中一种组合物包含大环内酯和一种或多种药学上可接受的赋形剂,另一种组合物包含免疫检查点抑制剂和一种或多种药学上可接受的赋形剂。13.根据实施方案12的组合,其中两种药物组合物被设计用于相同或不同的施用途径。14.如实施方案1至13中任一项所定义的组合,其用于医药中。15.根据实施方案14的的组合,其用作免疫刺激剂。16.实施方案14-15中任一项的组合,其用于治疗癌症。17.根据实施方案16的组合,其中癌症选自肾上腺癌、肛门癌、胆管癌、膀胱癌、骨癌、脑/cns肿瘤、乳腺癌、castleman病、宫颈癌、结肠/直肠癌、子宫内膜癌、食道癌、眼癌、胆囊癌、胃肠道类癌肿瘤(gastrointestinalcarcinoidtumors)、胃肠道间质瘤(gastrointestinalstromaltumor)(gist)、妊娠滋养细胞疾病、霍奇金病、卡波西肉瘤(kaposisarcoma)、肾癌、喉癌和下咽癌(laryngealandhypopharyngealcancer)、急性髓性白血病(acutemyeloidleukemia)、慢性淋巴细胞白血病(chroniclymphocyticleukemia)、急性淋巴细胞白血病(acutelymphocyticleukemia)、慢性髓性白血病(chronicmyeloidleukemia)、慢性粒单核细胞白血病(chronicmyelomonocyticleukemia)、肝癌(livercancer)、非小细胞肺癌(non-smallcelllungcancer)、小细胞肺癌(smallcelllungcancer)、肺类癌(lungcarcinoidtumor)、淋巴瘤(lymphoma)、恶性间皮细胞瘤(malignantmesothelioma)、多发性骨髓瘤(multiplemyeloma)、骨髓增生异常综合征(myelodysplasticsyndrome)、鼻腔和副鼻窦癌(nasalcavityandparanasalsinuscancer)、鼻咽癌(nasopharyngealcancer)、神经母细胞瘤(neuroblastoma)、非霍奇金淋巴瘤(non-hodgkinlymphoma)、口腔和口咽癌(oralcavityandoropharyngealcancer)、骨肉瘤(osteosarcoma)、卵巢癌(ovariancancer)、胰腺癌(pancreaticcancer)、阴茎癌(penilecancer)、垂体瘤(pituitarytumors)、前列腺癌(prostatecancer)、视网膜母细胞瘤(retinoblastoma)、横纹肌肉瘤(rhabdomyosarcoma)、唾液腺癌(salivaryglandcancer)、基底细胞和鳞状细胞皮肤癌(basalandsquamouscellskincancer)、黑色素瘤(melanoma)、梅克尔细胞皮肤癌(merkelcellskincancer)、小肠癌(smallintestinecancer)、胃癌(stomachcancer)、睾丸癌(testicularcancer)、胸腺癌(thymuscancer)、甲状腺癌(thyroidcancer)、子宫肉瘤(uterinesarcoma)、阴道癌(vaginalcancer)、外阴癌(vulvarcancer)、华氏巨球蛋白血症(waldenstrommacroglobulinemia)和肾母细胞瘤(wilmstumor)。18.根据实施方案14-15中任一项的组合,其用于治疗病毒性疾病。19.根据实施方案18的组合,其中病毒性疾病选自hiv、腺病毒、甲病毒、虫媒病毒、borna病、布尼亚病毒、杯状病毒、尖锐湿疣、冠状病毒、柯萨奇病毒、巨细胞病毒、登革热病毒、传染性脓疱(contageousecthyma)、爱泼斯坦-巴尔病毒、感染性红斑、汉坦病毒、病毒性出血热、病毒性肝炎、单纯疱疹病毒、带状疱疹病毒、感染性单核球增多症、流感、拉沙热病毒、麻疹、腮腺炎、传染性软疣、副粘病毒、白蛉热、多瘤病毒、裂谷热、风疹、慢性病病毒、天花、亚急性硬化性脑炎、肿瘤病毒感染、西尼罗病毒、黄热病毒、狂犬病病毒和呼吸道合胞病毒(respiratorysyncitialvirus)。20.药物组合物,其包含根据实施方案1-13中任一项的组合和一种或多种药学上可接受的赋形剂。21.药物组合物,其包含根据实施方案14-19中任一项的组合和一种或多种药学上可接受的赋形剂。22.药盒,其在单个包装中包括:i)第一组合物,其包含大环内酯,ii)第二组合物,其包含免疫检查点抑制剂,和iii)使用说明书,用于治疗或预防癌症。23.根据实施方案22的药盒,其中大环内酯选自:或其药学可接受的盐。24.根据实施方案21的药盒,其中大环内酯是或其药学可接受的盐。25.一种用于治疗或预防癌症的方法,所述方法包括向有需要的人或动物个体施用治疗有效量的根据实施方案1-13中任一项的组合。实验材料除非另有说明,否则以下实施例中使用的所有试剂均来自商业来源。阿奇霉素b的示例性供应商包括santacruzbiotech-nology(德克萨斯,美国)和torontoresearchchemicals(多伦多,加拿大)。抗体抗cd80v450、抗cd69pe、抗hla-drapc-r700、抗cd127-apc和抗-hla-a,b,cfitc购自bdbiosciences。用于t细胞增殖测定的celltraceviolet购自invitrogen。elisa抗体购自bdbiosciences。培养基rpmi-1640(invitrogen)补充有25mmhepes、l-谷氨酰胺、丙酮酸钠、10%胎牛血清(gibco)、100μg/ml青霉素和100μg/ml链霉素通用生物学方法可以使用下述一种或多种方法测试本发明化合物对免疫刺激的作用:通用化合物方法化合物分析-溶液中的溶解度和稳定性发酵液和化合物的分析将如下所述得到的等分试样的发酵液与等体积的乙酸乙酯剧烈摇动30分钟,然后离心分离,或将已经分离的化合物溶于甲醇:水(9:1,0.1mg/ml)中,然后离心分离。通过lcms和lc-ms/ms分析上清液,并使用在40℃加热的lunahplc柱(250×4.6mm;phenomenex(macclesfield,uk)),在碱性去活的lunac18反相二氧化硅(5微米粒径)上实现色谱法。包括四元泵、自动进样器、柱温箱和二极管阵列检测器的agilent1100hplc系统与brukeresquire离子阱ms连接。流动相a=0.1%甲酸水溶液流动相b=0.1%甲酸乙腈溶液梯度:t=0分钟,b=50%;t=4.5分钟,b=50%;t=7分钟,b=100%;t=10.5分钟,b=100%;t=10.75分钟,b=50%;t=13分钟,b=50%。通过lc-ms和lc-ms/ms鉴定化合物,并通过lc-ms/ms对内标物进行定量。通过流式细胞术的标志物表达的分析用ficoll-paque密度离心纯化来自健康供体的人外周血单核细胞(pbmc)。将细胞在37℃、5%co2的条件下在补充有25mmhepes、l-谷氨酰胺、丙酮酸钠(sigma)、10%胎牛血清、100μg/ml青霉素和100μg/ml链霉素(hyclone)的完全rpmi-1640培养基(invitrogen)中培养24-72小时,并用浓度增加的化合物1和化合物2刺激。然后在pbs中洗涤细胞并用对细胞表面标志物(bdpharmingen)特异的单克隆抗体染色,并使用bdfacscantoii流式细胞仪,用流式细胞术进行分析。所有样品一式两份进行测试。巨细胞病毒(cmv)培养物用ficoll-paque密度离心纯化来自健康cmv阳性供体的人外周血单核细胞(pbmc)。pbmc用5μmcelltraceviolet(invitrogen)在pbs中标记15分钟,然后用完全细胞培养基洗涤。标记的pbmc在涵盖(spanning)cmvpp65蛋白(1μg肽/ml,jpt)的肽库的存在下在37℃、5%co2的条件下在补充有l-谷氨酰胺、丙酮酸钠(sigma)、10%胎牛血清、100μg/ml青霉素和100μg/ml链霉素(hyclone)的aim-v培养基(invitro-gen)中培养6-8天。使用bdfacscantoii流式细胞仪,用流式细胞术评估细胞增殖。elisa在37℃、5%co2的条件下在完全rpmi培养基中与2.5μm化合物1和100u/mlil-2(miltenyibiotechnologies)温育48小时和7天后,用标准夹心elisa(所有抗体来自bdbiosciences)测量上清液il-10。tlr2测定在invivogen使用细胞报告试验并使用其标准测定条件,在重组hek-293-tlr细胞系上一式两份测试样品和对照。这些细胞系在功能上过表达人tlr2蛋白以及作为分泌型碱性磷酸酶(seap)的报告基因。该报告基因的产生由nfkb诱导型启动子驱动。tlr报告细胞系活化结果以光密度值(od)给出。使用20μl的每种测试物在200μl最终反应体积中刺激htlr2报告细胞系。使用至少两种测试浓度-20μm和10μm一式两份测试样品。细胞渗透性评估(双向)将10μm测试物添加至caco-2细胞单层的顶端(a)表面(在37℃下的具有0.3%dmso和5μmly的hbss缓冲液中),并在温育90分钟后测量化合物渗透到基底外侧(b)室中。这也是在相反方向(基底到顶端)进行,以研究有效输送。lc-ms/ms用于量化测试化合物和标准对照化合物的水平。通过将b至a的渗透率除以a至b的渗透率来计算流出率。药物渗透性:papp=(va/(面积×时间))×([药物]受体/(([药物]初始,供体)×稀释因子)代谢稳定性评估(微粒体稳定性测定)微粒体中的代谢速率按如下测试:用缓冲液c(0.1m磷酸钾缓冲液,1.0mmedta,ph7.4)稀释人肝微粒体至2.5mg/ml的浓度。通过向孔中加入30μl的1.5μm化合物加标(spiking)溶液(将1.5μl的500μm加标溶液(10μl的10mmdmso原液加入190μlcan以最终产生1μm的最终测试浓度)和18.75μl的20mg/ml肝微粒体加入479.75μl缓冲液c)进行微粒体稳定性研究。将所有样品在37℃预温育约15分钟。此后,通过在温和混合下加入15μlnadph溶液(6mm)引发反应。在0、5、15、30和45分钟取出等分试样(40μl)并用含有内标(135μl)的acn淬灭。通过离心(4000rpm,15分钟)去除蛋白,并通过lc-ms/ms分析样品板的化合物浓度。然后通过标准方法计算半衰期,比较分析物的浓度与初始存在的量。实施例实施例1–化合物1的制备(isc397)阿奇霉素糖苷配基(az-ag)的制备(1a)使用文献(djokic等人1988)中描述的方法产生阿奇霉素糖苷配基(1a)。简而言之,通过酸性去除3-o和5-o糖将阿奇霉素转化为阿奇霉素糖苷配基。首先将5-o氨基糖氧化并热解以促进裂解。能够糖基化红霉素糖苷配基(红霉内酯)的生物转化菌株的生成:糖多孢红霉菌18a1(paes52)的产生按如下产生paes52,其为含有angai、angaii、angcvi、ang-orf14、angmiii、angb、angmi和angmii以及actii-orf4pacti/iii表达系统的表达质粒(rowe等人,1998)。从由美国典型培养物保藏中心(americantypeculturecollection)(马纳萨斯,弗吉尼亚州,美国)中获得的菌株泛温链霉菌(s.eurythermus)atcc23956的粘粒文库扩增安哥拉霉素(angolamycin)糖生物合成基因。生物合成基因簇序列保藏为eu038272、eu220288和eu232693(schell等人2008)。如先前所述(schell等人2008,esi)将生物合成基因盒组装在载体psg144中,连续添加基因直至获得糖生物合成所需的8,产生质粒paes52。将paes52转化到菌株18a1中(wo2005054265)。将paes52转化为糖多孢红霉菌18a1使用标准方法通过原生质体将paes52转化到糖多孢红霉菌18a1中(kieser等人2000和gaisser等人1997)。所得菌株命名为isom-4522,其于2017年1月24日保藏于ncimb,保藏号为:ncimb42718。糖多孢红霉菌sgt2(paes54)的产生按如下产生paes54,其为含有angai、angaii、angcvi、ang-orf14、angmiii、angb、angmi和angmii以及actii-orf4pacti/iii表达系统的表达质粒(rowe等人1998)。从由美国典型培养物保藏中心(manassas,virginia,usa)中获得的菌株泛温链霉菌(s.eurythermus)atcc23956的粘粒文库扩增安哥拉霉素糖生物合成基因。生物合成基因簇序列保藏为eu038272、eu220288和eu232693(schell等人2008)。如先前所述(schell等人2008,esi)将生物合成基因盒组装在载体psg144中,连续添加基因直至获得糖生物合成所需的8,产生质粒paes52。通过连接含有actii-orf4pacti/iii启动子系统的11,541bpspei-nhei片段制备质粒paes54,用来自pgp9的5,087bpxbai-spei片段从paes52切下8个ang基因,其含有安普霉素抗性基因、oric、用于转移链霉菌的orit和具有用于整合转化的attp位点的phibt1整合酶。(在连接期间,兼容的nhei和xbai位点被去除)。然后将paes54转化到糖多孢红霉菌sgt2(gaisser等人2000,wo2005054265)。将paes54转化为糖多孢红霉菌sgt2使用标准方法通过缀合将paes54转化到糖多孢红霉菌sgt2中。简而言之,通过标准程序用paes54转化大肠杆菌et12567puz8002,并与阿泊拉霉素(50μg/ml)、卡那霉素(50μg/ml)和氯霉素(33μg/ml)选择物涂布到2ty上。将该板在37℃下孵育过夜。将来自其的菌落用于建立新鲜液体2ty培养物,将其在37℃孵育直至达到后期对数生长期。收获细胞,洗涤,与糖多孢红霉菌sgt2的孢子混合,涂布在r6板上并在28℃孵育。24小时后,将这些板用1ml含有3mg阿泊拉霉素和2.5mg萘啶酸的无菌水覆盖,并在28℃下再孵育5-7天。将该板上的结合后体(exconjugant)转移到含有阿泊拉霉素(100μg/ml)的新鲜r6板上。备选生物转化菌株或者,biot-2945(schell等人2008)可以用作生物转化菌株,因为该菌株也将安哥拉糖胺加入到红霉内酯中。阿奇霉素糖苷配基的生物转化以制备化合物1将含有sv2培养基(40ml)和8ul硫链丝菌素(25mg/ml)的锥形烧瓶(250ml)用0.2ml菌株isom-4522的孢子原液接种,在30℃下孵育并以2.5cm幅度(throw)以300rpm振荡48小时。sv2培养基:准备含有erypp培养基(7ml)的无菌盖塞离心管(50ml),并接种来自种子烧瓶的不含抗生素的培养物(每个离心管0.5ml)。将离心管在30℃下孵育并以2.5cm幅度以300rpm振荡24小时。erypp培养基:24小时后,将阿奇霉素糖苷配基(在dmso中的0.5mm,50μl)加入至每个离心管中,并以2.5cm幅度在300rpm下继续培养6天。分离化合物1将全培养液调节至ph9.5并用一体积的乙酸乙酯(etoac)萃取两次。离心(3,500rpm,25分钟)后通过抽吸收集有机层。合并有机层并真空浓缩,以得到含有化合物1的棕色胶状物。将该提取物在乙酸乙酯(200ml)和氯化铵水溶液(20ml50%浓缩溶液)之间分配。分离后,用另外体积(200ml)的氯化铵水溶液萃取有机层。然后用氢氧化钠水溶液将合并的水层调节至ph9.0,然后用一体积当量的乙酸乙酯萃取两次。合并有机层,并真空浓缩,得到棕色固体。然后将该提取物加载于二氧化硅柱并用如下物质逐步洗脱(500ml份额):溶剂己烷etoacmeohnh4oh水溶液a0.4990.49900.002b0.2500.74800.002c00.99800.002d00.9880.010.002e00.9780.020.002f00.9680.030.002g00.9580.040.002化合物1主要在f和g中。将这些溶剂合并,并真空蒸发,以得到含有化合物1的棕色固体。然后通过制备型hplc(c18gemininx柱,phenomenex,使用20mm乙酸铵和乙腈作为溶剂)纯化该物质。合并含有目标化合物的馏分并干燥,然后在c18spe柱(cartridge)上脱盐。实施例2–化合物3的制备(已知化合物-对应于schell等人2008中的化合物17)_红霉内酯b(3a)可以通过在糖基化中被阻断的糖多孢红霉菌菌株的发酵产生,例如在us.3,127,315(例如nrrl2361、nrrl2360、nrrl2359和nrrl2338)和gaisser等人2000(例如糖多孢红霉菌dmδbvδciii)中描述的菌株和方法。然后将红霉内酯b(3a)加入到能够将安哥拉糖胺添加到3-羟基的生物转化菌株(例如ncimb42718)中,并使用标准方法从发酵液中分离化合物3。实施例3–化合物4的制备阿奇霉素b糖苷配基(4a)通过与阿奇霉素a相同的方式从阿奇霉素b中水解糖而产生。然后将阿奇霉素b糖苷配基(4a)加入到能够将安哥拉糖胺添加到3-羟基的生物转化菌株(例如ncimb42718)中,并使用标准方法从发酵液中分离。实施例4–化合物5的制备使用wo98/01571中描述的方法产生环丁基红霉内酯b(5a)。简而言之,用pig1转化糖多孢红霉菌dmδbvδciii(gaisser等人2000)(long等人,2002,wo98/01571)。添加环丁烯羧酸,进行所得菌株的发酵从而产生环丁基红霉内酯b(5a)。使用标准方法将其从发酵液中分离出来。然后将环丁基红霉内酯b(5a)加入到能够将安哥拉糖胺添加到3-羟基(例如ncimb42718)的生物转化菌株中,并使用标准方法从发酵液中分离化合物5。实施例5–化合物6的制备通过将化合物3加入到atcc31771的发酵中并使用标准方法从发酵液中分离化合物6,从而将甲基从化合物3的氨基糖(参见实施例2)中去除。实施例6–化合物7的制备在溶剂中用硼氢化钠处理化合物3。在标准的反应后处理后,通过标准方法纯化化合物7。实施例7–化合物8的制备使用wo2000/00618中描述的方法产生14-去甲基红霉内酯b(8a)。简而言之,用ppfl43转化糖多孢红霉菌dmδbvδciii(gaisser等人2000)。使用典型方法发酵所得菌株,并使用色谱法分离化合物8a。然后将14-去甲基红霉内酯b(8a)加入到能够将安哥拉糖胺添加到3-羟基的生物转化菌株(例如ncimb42718)中,并使用标准方法从发酵液中分离。实施例8–化合物9的制备通过将化合物3(参见实施例2)加入到娄彻氏链霉菌(s.rochei)atcc21250(其添加羟基)的发酵中产生14-羟基安哥拉糖胺红霉内酯b(9)。然后使用标准方法从发酵液中分离化合物9。实施例9–化合物10的制备将化合物6(6.0mg,0.01mmol)溶解在二氯甲烷(1ml)中,并加入乙醛(1.0μl,0.02mmol)。在室温下搅拌反应,并加入三乙酰氧基硼氢化钠(2.1mg,0.01mmol)。将反应搅拌30分钟,然后通过加入浓的碳酸氢钠水溶液(25ml)淬灭。用乙酸乙酯(3×25ml)萃取含水萃取物。合并有机萃取物,用浓盐水溶液洗涤,并真空去除溶剂。然后通过制备型hplc纯化目标化合物10。实施例10–化合物12的制备通过将化合物3(参见实施例2)加入到atcc31771的发酵中来生物转化,以从氨基糖中去除两个甲基,并使用标准方法从发酵液中分离化合物11。将化合物11溶解在thf中,并加入乙醛。在室温下搅拌反应,加入氰基硼氢化钠。继续搅拌反应,并通过加入碳酸氢钠水溶液淬灭反应。用etoac(3x体积当量)萃取含水萃取物。合并有机萃取物,用盐水洗涤,并真空去除溶剂。然后使用标准方法纯化目标化合物12。实施例11–化合物14的制备通过将化合物1(参见实施例1)加入到atcc31771的发酵中来生物转化,以从氨基糖中去除甲基,并使用标准方法从发酵液中分离化合物13。将化合物13溶解在thf中,并加入乙醛。在室温下搅拌反应,加入氰基硼氢化钠。继续搅拌反应,并通过加入碳酸氢钠水溶液淬灭反应。用etoac(3×体积当量)萃取含水萃取物。合并有机萃取物,用盐水洗涤,并真空去除溶剂。然后使用标准方法纯化目标化合物14。实施例12–化合物16的制备通过将化合物1(参见实施例1)加入到atcc31771的发酵中来生物转化,以从氨基糖中去除两个甲基,并使用标准方法从发酵液中分离化合物15。将化合物15溶解在thf中,并加入乙醛。在室温下搅拌反应,加入氰基硼氢化钠。继续搅拌反应,并通过加入碳酸氢钠水溶液淬灭反应。用etoac(3×体积当量)萃取含水萃取物。合并有机萃取物,用盐水洗涤,并真空去除溶剂。然后使用标准方法纯化目标化合物16。实施例13–直接抗菌活性的评估使用最小抑菌浓度(mic)测定评估大环内酯类化合物对4种常见肠道细菌(大肠杆菌(escherichiacoli)、唾液链球菌唾液亚种(streptococcussalivariussubsp.salivarius)、干酪乳杆菌(lactobacilluscasei)和长双歧杆菌婴儿亚种(bifidobacteriumlongumsubsp.infantis))和常见的哺乳动物皮肤分离物滕黄微球菌(micrococcusluteus)的生物活性。除了藤黄微球菌(m.luteus)(其由ncimb获得,并在-80℃下储存在20%甘油中)外,细菌菌株购自dsmz(brunswick,德国)。将阳性对照(阿奇霉素和红霉素)和测试化合物1和2的原液(100%dmso)在发酵液中稀释至工作储备浓度为256μg/ml(最终试验测定浓度范围128μg/ml至0.00391μg/ml)。将所有其他化合物的原液在发酵液中稀释至工作储备浓度为128μg/ml(最终试验测定浓度范围为64μg/ml至0.00195μg/ml)。除了在37℃需氧培养的藤黄微球菌外,将细菌菌株在37℃的厌氧室中的适当培养液中培养。将18小时培养物在发酵液中稀释至od595为0.1,然后以1:10进一步稀释。在96孔板中,一式两份地将200μl试验化合物的工作原液转移到孔1中并在发酵液中连续稀释(1:2)。将100μl细菌悬浮液等分到每个孔中并充分混合。包括适当的无菌对照,并将板在厌氧培养室中在37℃下孵育18小时、或在有氧条件下(藤黄微球菌)在37℃下孵育18小时。mic被确定为没有可见生长的第一个孔中测试化合物的浓度。表1:从表1中的数据可以看出,化合物1、3、4、5、6、7、8和9对任何测试的细菌菌株都没有抗菌活性,而红霉素和阿奇霉素对多种细菌显示出强效活性。实施例14–免疫刺激活性的评估用ficoll-paque密度离心纯化来自健康供体人外周血单核细胞(pbmc)。将细胞在补充有25mmhepes、l-谷氨酰胺、丙酮酸钠(sigma)、10%胎牛血清、100μg/ml青霉素和100μg/ml链霉素(hyclone)的完全rpmi-1640培养基(invitrogen)中培养。将细胞在组织培养板中用浓度增加的化合物1和2在37℃、5%co2下刺激24小时(研究1-4)或48小时至1周(研究5)。从板中取出细胞,在pbs中洗涤,并使用来自bdpharmingen的单克隆抗体和facscantoii流式细胞仪,用流式细胞术分析细胞特异性表面标志物和mhci类的表达。在用含有2.5μm化合物1和100u/mlil-2(miltenyibiotechnologies)的完全rpmi培养基,在37℃、5%co2下的孵育48小时和7天后,用标准夹心elisa(所有抗体来自bdbiosciences)测量上清液il-10。研究1:用1μm化合物1(图8)体外刺激外周血单核细胞(pbmc)24小时后,激活标记物cd69在cd4+t细胞和b细胞上被上调(图1)。研究2:我们还观察到分子mhci类(hla-abc)在t细胞和b细胞上的上调(图2),表明对病毒抗原的抗原呈递的影响。研究3:用化合物1刺激pbmc导致共刺激分子cd80以及单核细胞上的抗原呈递分子mhcii类(hla-dr)的上调(图3)。研究4:分化成巨噬细胞的单核细胞也响应于化合物1的刺激而上调cd80(图4)。研究5:用化合物1刺激48小时和7天的pbmc表达改变的细胞因子谱,并且用夹心elisa测得免疫抑制细胞因子il-10的产生增加。这表明在某些条件下的免疫抑制作用(图5)。研究6:用化合物1刺激pbmc,并在il-2(miltenyibiotechnologies)和celltracevioletdye(invitrogen)的存在下在rpmi培养基中培养6天。用流式细胞术测量增殖。对化合物1的免疫学作用的分析揭示了改变的细胞因子驱动的t细胞增殖谱(图6)。研究7:病毒特异性t细胞增殖也受化合物1的影响。在巨细胞病毒(cmv)抗原和化合物1存在下将来自cmv感染的供体的pbmc培养6天,该pbmc显示出活化的cmv特异性cd8+t细胞的改变的表型,其中il-7受体α(cd127)的表达增加,用流式细胞仪测得(图7)。cd127对于t细胞稳态、分化和功能至关重要,并且表达降低与hiv和其他慢性病毒性疾病中的疾病严重程度相关(crawley等人2012)。可以看出,化合物1具有通过影响抗原呈递、共刺激和t细胞活化和增殖来特异性激活和修饰免疫应答的惊人能力。在许多这些研究中,包括了化合物,化合物2是先前在schell等人,2008中作为化合物20公开的另一种相关的具有改变的糖基化的大环内酯红霉素类似物,并且在测定中显示很少或没有活性。研究8:来自cmv感染的供体的pbmc在cmv抗原的存在下培养,其中未处理或暴露于化合物1或化合物2下3天。暴露于化合物1诱导分泌高水平的ifn-γ,而单独的抗原培养物或抗原与化合物a一起培养不诱导ifn-γ分泌(图9)。研究9:来自健康供体的巨噬细胞,其暴露于化合物1或2下48小时。只有暴露于化合物1的巨噬细胞分泌ifn-γ,而未处理的巨噬细胞和暴露于化合物a的巨噬细胞不分泌ifn-γ(图10)。因此,化合物1能够在来自健康供体的巨噬细胞中诱导ifn-γ分泌。研究10:暴露于化合物1或2下2天的pbmc和巨噬细胞(图11)。在pbmc中rantes的基础表达不受化合物2的影响,而化合物1诱导表达的双重上调。rantes的表达在巨噬细胞中微乎其微,而化合物1诱导高表达。研究11:暴露于化合物1和2下2天的pbmc和巨噬细胞。pbmc和巨噬细胞响应于化合物1分泌il-12p70,而化合物2未能诱导超过未处理的细胞的分泌(图12)。研究12:暴露于化合物1和2下2天的pbmc、巨噬细胞和cd4+t细胞。化合物1增加巨噬细胞中的il-1β分泌,轻微增加pbmc中的il-1β分泌,而在cd4+t细胞中没有诱导il-1β(图13)。研究13:化合物1以0.165mg/kg至5mg/kg静脉内施用于c57bl/6小鼠。在接受最高剂量5mg/kg的动物中cd25+细胞丰度增加(图14),同一组中的体重也是如此(未显示)。研究14:化合物1或化合物2静脉内施用于c57bl/6小鼠。24小时后取出脾脏并评估cd11b+脾细胞上的mhci类表达。化合物1诱导具有高mhci表达的脾细胞增加,而注射有化合物a的小鼠的脾细胞未观察到任何效果。实施例15–代谢稳定性的评估在标准人微粒体稳定性测定中评估本发明化合物的代谢稳定性(参见通用方法)。具有较长半衰期的化合物预计在施用后具有较长的半衰期,这对于允许较低频率的施用是有用的。具有较短半衰期的化合物可用作“软药(softdrugs)”,其中活性实体一旦进入患者体系就迅速降解。评估的化合物的半衰期如下表2所示:表2:t1/2(分钟)阿奇霉素245红霉素31化合物1108化合物335化合物4160化合物583化合物6109化合物756化合物833化合物9100化合物1031化合物17151化合物1825化合物1918em70397可以看出,与阿奇霉素、红霉素和em703(例如参见ep1350510)相比,本发明的许多化合物具有增加或降低的代谢稳定性。实施例16–caco-2渗透性的评估在标准caco-2双向渗透性测定中评估本发明化合物的渗透性(参见通用方法)。具有增加的渗透性的化合物预期具有更好的细胞渗透性和潜在的效果,具有改善的渗透性和/或减少的流出物的化合物预期具有增加的口服生物利用度。化合物的渗透性和流出如下表3所示:表3:pappx106/cm.s-1流出比率阿奇霉素<0.14>78化合物10.3263化合物30.27166化合物40.3849化合物50.4781化合物80.4656化合物101.2326化合物170.539化合物189.443.5em703<0.15>108可以看出,与阿奇霉素和em703(例如参见ep1350510)相比,本发明的许多化合物具有改善的细胞渗透性和/或减少的流出物。实施例17–tlr2刺激的评估使用测量tlr2受体刺激的tlr2报告分析(参见通用方法)测试化合物。由于分泌型碱性磷酸酶(seap)的释放,测量到刺激效应,其表现为光密度(od)增加,如表4所示:表4:可以看出,化合物1以低至5um的浓度刺激tlr2,化合物17以低至10um的浓度刺激tlr2,而红霉素a、阿奇霉素和化合物2和3(先前在schell等人2008中作为化合物17和20公开的具有改变的糖基化的相关的大环内酯红霉素类似物)在高达20um的浓度下显示很少或没有刺激。实施例18–化合物17的制备糖苷配基17a由9-脱氧-8a-氮杂-8a-甲基-8a-同型红霉素(wilkening1993)产生,然后水解糖。然后将17a加入到能够将安哥拉糖胺添加到3-羟基(例如ncimb42718)的生物转化菌株中,并使用标准方法从发酵液中分离的化合物17。实施例19–化合物18的制备将6-脱氧红霉内酯b(6-deb,18a)加入到能够将安哥拉糖胺添加到3-羟基(例如ncimb42718)的生物转化菌株中,并使用标准方法从发酵液中分离。实施例20–isc397和检查点抑制剂的组合的效果的研究c57bl/6j小鼠购自德国charlesriverlaboratories。在异氟烷麻醉下,将小鼠皮下注射到右后胁腹,注射1x106b16-f10黑素瘤细胞。治疗组是(每组10只小鼠):1)在第1、3、6、9和12天,抗pd-1(来自merck,johnson,roche或astra的克隆rmp1-14,200微克/剂)。2)抗pd-1(来自merck,johnson,roche或astra的克隆rmp1-14,200微克/剂)在第1、3、6、9和12天+isr397(500微克/剂)每天直至实验终止。3)未处理。静脉内注射所有化合物,每天测量肿瘤体积,并且每天两次测量动物的健康状况。如果肿瘤达到2ml或如果健康状况差,则杀死动物。在第18天终止实验,所有小鼠通过颈椎脱臼处死。结果示于图16-19中。参考kieser等人2000practicalstreptomycesgenetics,由johninnesfoundation出版crawley等人theinfluenceofhivoncd127expressionanditspotentialimplicationsforil-7therapy.seminimmunol.2012年6月;24(3):231-40.gaisser等人analysisofsevengenesfromtheeryai-erykregionoftheerythromycinbiosyntheticgeneclusterinsaccharopolysporaerythraea.mol.gen.genet.,1997oct;256(3):239-51.gaisser等人adefinedsystemforhybridmacrolidebiosynthesisinsaccharopolysporaerythraeamol.micro.,2000;36(2):391–401schell等人engineeredbiosynthesisofhybridmacrolidepolyketidescontainingd-angolosamineandd-mycaminosemoietiesorg.biomol.chem.,2008;6:3315-3327lemahieu等人glycosidiccleavagereactionsonerythromycina.preparationoferythronolidea,j.med.chem.,1974,17(9):953-956djokic等人erythromycinseries.part13.synthesisandstructureelucidationof10-dihydro-10-deoxo-11-methyl-11-azaerythromycinaj.chem.res.(s),1988;5:152-153glansdorp等人usingchemicalprobestoinvestigatethesub-inhibitoryeffectsofazithromycin,org.biolmol.chem.,2008;208(6):4120-4124rowe等人constructionofnewvectorsforhigh-levelexpressioninactinomycetes.gene.1998aug17;216(1):215-23.long等人engineeringspecificityofstarterunitselectionbytheerythromycin-producingpolyketidesynthase.mol.microbiol.2002mar;43(5):1215-25.wilkening等人thesynthesisofnovel8a-aza-8a-homoerythromycinderivativesviathebeckmannrearrangementof(9z)-erythromycinaoxime,bioorg.med.chemlett.1993,3(6),第1287-1292页本申请中提及的所有参考文献,包括专利和专利申请,都通过引用以最大可能的方式并入本文。当前第1页1 2 3
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



