一种血液中还原性谷胱甘肽荧光检测纳米晶材料及其制备方法和检测试剂盒与流程
 2021-02-02 17:02:05|
2021-02-02 17:02:05| 444|
444| 起点商标网
起点商标网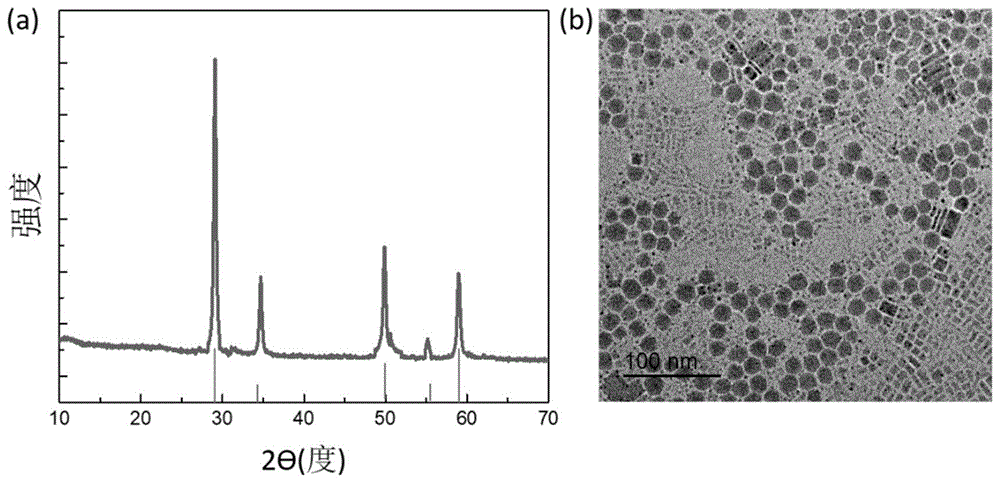
本申请涉及血液中生物小分子检测领域,尤其涉及一种血液中还原性谷胱甘肽荧光检测纳米晶材料及其制备方法和检测试剂盒。
背景技术:
谷胱甘肽(gsh),细胞内含量最丰富的非蛋白巯基化合物,不仅是人体内一种必需的内源性抗氧化剂,而且在清除自由基方面扮演着重要角色,易与某些药物、重金属离子结合,将机体中有害的毒物转化为无害物质,并排出体外。gsh含量在所有组织细胞内为毫克级别,在血液、唾液、脑脊液和尿液等人体体液中的浓度均为微摩尔级别。据报道,gsh的含量与人类各种疾病如癌症、肝损伤、艾滋病和糖尿病有关联。因此,发展有效方法监测gsh浓度变化,对于更好地了解其生理和病理功能具有重要意义。检测gsh的方法包括高效液相色谱法、电化学法、酶联免疫吸附法、表面增强拉曼散射法、比色法和荧光光谱法等。
目前,已有一些关于gsh荧光检测的报道,如利用荧光分子探针、金属纳米簇、碳纳米材料和上转换荧光纳米粒子等检测gsh浓度。然而,这些“单信号”荧光传感器,易受检测体系浓度、激发光强度和检测环境等因素影响。而基于两个荧光发射峰强度比值变化的比率型荧光探针,拥有自校正的内部参考,可减少因样品、设备等外界条件引起的干扰,从而提高测量结果的可靠性。因此,比率型荧光探针受到化学研究者的极大关注。
技术实现要素:
为了解决上述的技术问题,本申请的一个目的是提供一种血液中还原性谷胱甘肽荧光检测纳米晶材料,由于在其表面修饰了羟基氧化钴,实现了该纳米晶对还原性谷胱甘肽的比率型荧光检测,具有非接触式、快响应、高空间分辨率与高准确度的优势。
为了实现上述的目的,本申请采用了以下的技术方案:
一种血液中还原性谷胱甘肽荧光检测纳米晶材料,该纳米晶材料的分子式为nalumo2o8:yb/tm/ce/eu@coooh。
优选,该纳米晶材料为水溶性纳米晶材料,其由油性纳米晶经hcl溶液处理去掉表面的油酸配体,获得水性纳米晶后由羟基氧化钴修饰nalumo2o8:yb/tm/ce/eu纳米晶构成。
优选,nalumo2o8:yb/tm/ce/eu@coooh纳米晶的分子式为nalumo2o8:10yb/0.5tm/20ce/5eu@coooh。
优选,该纳米晶材料在980nm近红外光激发条件下,材料在蓝光区域表现出很强的上转换发光;在254nm波长的紫外光激发条件下,材料在红光区域表现出很强的下转换发光。
进一步,本申请提供了一种血液中还原性谷胱甘肽荧光检测纳米晶材料的制备方法,该方法包括以下的步骤:
1)1毫摩尔硝酸钠nano3,0.645毫摩尔硝酸镥lu(no3)3∙5h2o,0.2毫摩尔硝酸铈ce(no3)3∙5h2o,0.005毫摩尔硝酸铥tm(no3)3∙5h2o以及0.05毫摩尔硝酸铕tb(no3)3∙5h2o溶于8毫升去离子水中,搅拌均匀;
2)搅拌20分钟后,加入2毫摩尔钼酸钠na2moo4和30毫升聚乙二醇,搅拌1小时后,转移到高压水热釜中,于180℃加热6小时,产物用乙醇和去离子水的混合液洗涤3-5次;
3)在2ml离心管中,加入100μl表面亲水处理后的纳米晶水溶液,加入不同量的10mmcocl20-200μl溶液超声1min,依次加入0.8mnaoh100μl和0.2mnaclo100μl溶液,继续超声10min,离心分离,水洗后分散到1.0ml去离子水中。
优选,该方法还包括纳米晶表面处理步骤:将步骤2)制备得到的10-100mg油性纳米晶分散在1-3ml乙醇与浓度为0.2mol/l的hcl0.5-1ml的混合液中,将混合液超声5-10min,然后加入乙醇洗涤、离心以及烘干等处理后即可获得水性纳米晶。
进一步,本申请提供了所述的纳米晶材料用于血液中痕量还原性谷胱甘肽荧光检测。
进一步,本申请提供了一种血液中还原性谷胱甘肽比率型荧光检测试剂盒,该试剂盒包括所述的纳米晶材料。
本申请通过一种溶剂热法制备出四方相nalumo2o8:yb/tm/ce/eu纳米晶,纳米晶由于表面经过hcl处理去掉了油酸配体,能够很好地分散在水溶液中。当在纳米晶分散的水溶液中加入还原性谷胱甘肽后,表面修饰的羟基氧化钴可与gsh作用。在980近红外光和紫外光共同激发条件下,tm3+离子的蓝光与羟基氧化钴的吸收光谱重叠较好而被后者淬灭;相比之下,eu3+离子的红光发射信号变化较小。当有gsh时,gsh可与羟基氧化钴生成co2+,使得蓝光的淬灭效应消除,这样以红光为参比,通过拟合eu3+离子与tm3+离子的荧光强度比与gsh浓度的关系曲线,能够很好地应用于还原性谷胱甘肽的比率型定量检测。
附图说明
图1(a)和(b)分别为产物的xrd图谱和透射电子显微镜图。
图2(a)nalumo2o8:10yb/0.5tm/20ce/5eu纳米晶在980纳米近红外激光器激发条件下的上转换发射谱,(b)nalumo2o8:10yb/0.5tm/20ce/5eu纳米晶在紫外激发条件下的下转换发射谱,(c)产物在紫外与近红外激光器双波长激发条件下的发射谱,(d)产物的发光强度随敏化离子ce3+的变化关系曲线。
图3nalumo2o8:10yb/0.5tm/20ce/5eu纳米晶的水溶液(黑色线)、nalumo2o8:10yb/0.5tm/20ce/5eu纳米晶的水溶液中加入coooh(红色线),以及coooh修饰的nalumo2o8:10yb/0.5tm/20ce/5eu纳米晶水溶液(蓝色线)的ucl光谱。
图4在coooh修饰的nalumo2o8:10yb/0.5tm/20ce/5eu纳米晶的生理缓冲溶液中加入gsh后,蓝色和红色发射荧光的强度比与gsh浓度的关系曲线。
图5(a)在稀释的小牛血清溶液(25%)中,coooh和coooh修饰的纳米晶的ucl光谱,λem=980nm;(b)在coooh修饰的纳米的小牛血清溶液(25%)中加入gsh后,蓝色发射和红色发射的强度比与gsh浓度的线性拟合曲线。
具体实施方式
1.实验部分
1.1主要仪器和试剂:
硝酸钠(99.0%),硝酸镥(99.9%),硝酸铈(99.9%),硝酸镱(99.9%),硝酸铥(99.9%),硝酸铕(99.9%),钼酸钠(98.0%)与乙二醇(99.8%)购买于sigma-aldrich公司,无水乙醇、氯化钴、氢氧化钠、次氯酸钠、还原性谷胱甘肽购买于国药集团化学试剂有限公司,小牛血清购买于gibco公司。
1.2nalumo2o8:yb/tm/ce/eu@coooh纳米晶的制备
以nalumo2o8:10yb/0.5tm/20ce/5eu纳米晶为例,1毫摩尔硝酸钠(nano3),0.645毫摩尔硝酸镥(lu(no3)3∙5h2o),0.2毫摩尔硝酸铈(ce(no3)3∙5h2o),0.005毫摩尔硝酸铥(tm(no3)3∙5h2o),0.05毫摩尔硝酸铕(tb(no3)3∙5h2o)以及3毫摩尔柠檬酸溶于8毫升去离子水中,搅拌20分钟后,加入2毫摩尔钼酸钠(na2moo4)和30毫升聚乙二醇,搅拌1小时后,转移到高压水热釜中,于180℃加热6小时。产物用乙醇和去离子水的混合液洗涤3-5次。
在2ml离心管中,加入100μl表面亲水处理后的纳米晶水溶液,加入不同量的10mmcocl20-200μl溶液超声1min;依次加入0.8mnaoh100μl和0.2mnaclo100μl溶液,继续超声10min,离心分离,水洗后分散到1.0ml去离子水中。
不同浓度或种类的离子掺杂样品,通过改变前驱溶液中相应的离子浓度或种类来实现。
纳米晶表面处理步骤:将制备得到的10-100mg油性纳米晶分散在1-3ml乙醇与浓度为0.2mol/l的hcl0.5-1ml的混合液中,将混合液超声5-10min,然后加入乙醇洗涤、离心以及烘干等处理后即可获得水性纳米晶。
1.3表征仪器
x射线衍射图谱(brukerd8advance,cu-kα(λ=1.5405å)),透射电子显微镜(tem,feitecnaig2f20),光谱仪(flurohub-b,horibajobinyvon),紫外灯功率为50w,980nm近红外激光器功率范围为0-2w。
x射线衍射样品的制备:将烘干的纳米晶铺满样品支架的凹槽;
透射电子显微镜样品的制备:将每次合成的全部纳米晶溶于4毫升乙醇溶液中,超声5分钟后,滴3-6滴液体于超薄碳膜上。
还原性谷胱甘肽的检测方法:将纳米晶溶于水溶液中,分成若干组,将不同浓度的谷胱甘肽等体积的加入到纳米晶水溶液中,在980nm和254nm的激光共同激发下通过荧光光谱仪表征其荧光变化的性能,并拟合出标准曲线。
2.数据分析与讨论
nalumo2o8:10yb/0.5tm/20ce/5eu产物的x射线衍射图谱如图1a所示,所有衍射峰均与标准pdf卡片jcpds54-0896号一一对应,且无多余的衍射峰,表明本申请得到的产物为纯四方相。透射电子显微镜分析结果表明产物为四方块状,分散性很好。单分散纳米颗粒在溶液中分散性好,能够与金属离子大面积接触,有利金属离子的检测。
在980nm近红外光激发条件下,产物在蓝光区域表现出很强的上转换发光(图2a),对应于tm3+离子1g4→3h6的跃迁;在254nm波长的紫外光激发条件下,产物在红光区域表现出很强的下转换发光,对应于eu3+离子的f→f跃迁(图2b)。基于此,本申请将紫外氙灯与近红外激光器同时照射样品,产物能够同时表现出蓝光和红光发射(图2c)。随着敏化离子ce3+离子浓度从10增到20mol%,纳米晶的吸收能力增大,因此发光强度显著增强,当ce3+离子浓度超过20mol%,敏化离子与激活离子之间的无辐射交叉弛豫几率增大,导致发光强度下降(图2d)。
如图3所示,与nalumo2o8:10yb/0.5tm/20ce/5eu纳米晶的光谱以及nalumo2o8:10yb/0.5tm/20ce/5eu纳米晶和coooh的混合溶液相比,将coooh修饰在nalumo2o8:10yb/0.5tm/20ce/5eu纳米晶表面时能量传递效果更大,因而荧光淬灭程度也大。这是因为修饰后纳米晶与coooh的距离更近,更有利于能量传递。
如图4所示,当溶液中加入还原性谷胱甘肽后,在紫外光与近红外双波长激发条件下,tm3+离子的发光强度明显增强。以tm3+离子的发光强度为检测信号,eu3+离子的发光强度为参比信号,他们的荧光强度比随着gsh浓度的增加逐渐增强,能够很好地应用于gsh的定量检测。这种比率型荧光检测方法不受外界环境的影响,比如光源的稳定性,样品的浓度与环境温度等,具有很高的准确度。以上机理解释如下:当nalumo2o8:10yb/0.5tm/20ce/5eu@coooh纳米晶水溶液中加入gsh后,gsh会与coooh作用,从而消除coooh对tm3+离子蓝光的淬灭效应,导致tm3+离子的发光增强,而eu3+离子的红光信号强度几乎不受影响。
在稀释的小牛血清(25%,以下简称血清溶液)中考察纳米探针对gsh的响应能力。如图5a所示,用980nm的近红外激光激发时,血清溶液和coooh的血清溶液在350-700nm的范围内都监测不到发射光谱,而coooh修饰的纳米晶的血清溶液有很强的ucl发射。这也说明用coooh修饰的纳米晶在生物样品中检测gsh时具有很高的信噪比。随后,我们在血清溶液中加入不同浓度的gsh后用980nm的近红外和紫外激光共同激发,如图5b所示,发现在0-50μm的浓度范围内血清溶液的荧光发射强度比与gsh的浓度呈线性关系。而正常人体血液中gsh的浓度在20到40μm的范围内。在血清样品中的实验结果表明,coooh修饰的纳米晶具有临床应用的潜能。
3.结论
本申请通过溶剂热法制备出水溶性nalumo2o8:10yb/0.5tm/20ce/5eu纳米晶,分散性好,然后在其表面修饰了羟基氧化钴,从而能够应用于还原性谷胱甘肽的荧光定量检测。研究结果表明coooh的吸收光谱和tm3+离子蓝光发射光谱有较大的重叠而使其荧光淬灭,但加入还原性谷胱甘肽后,会与coooh作用从而使得tm3+离子的荧光信号强度恢复,另外,由于eu3+离子的红光强度不受影响,因此在紫外光和近红外光双波长激发条件下,eu3+离子与tm3+离子的发光强度比能够很好的应用于血液中gsh的比率型荧光定量检测。这种荧光检测方法具有响应快、空间分辨率高以及准确度高的优势,具有很好的应用前景。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询



 商标分类
商标分类  商标转让
商标转让 



