一种聚集诱导发光纳米颗粒及其制备方法和应用与流程
 2021-01-08 12:01:02|
2021-01-08 12:01:02| 334|
334| 起点商标网
起点商标网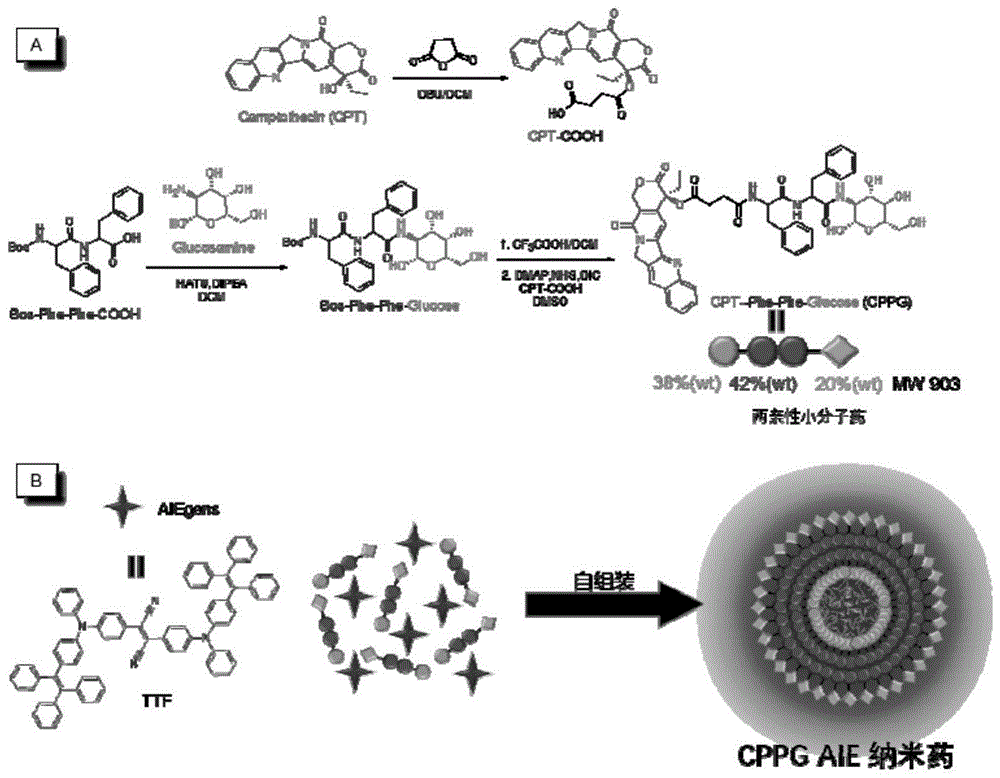
本发明涉及纳米医学领域,特别涉及一种两亲性小分子自组装的聚集诱导发光纳米颗粒及其制备方法和应用。
背景技术:
与常规染料相比,聚集诱导发光(aggregation-inducedemission,aie)生物探针在分子溶解状态下显示弱荧光或无荧光。但是,当它们处于聚集状态以限制分子内自由旋转时,可以观察到强荧光。aie材料的优势主要体现在:低背景、信噪比高、灵敏度好、抗光漂白能力强等方面。这种独特的性能使aie染料成为发光探针和超亮有机纳米颗粒(nanoparticles,nps)设计的理想候选者,这在监测细胞内生物过程和追踪许多疾病中非常重要。此外,通过纳米颗粒表面修饰,aie材料在细胞器染色、病原体识别、细胞长周期示踪、光动力学治疗等领域表现出了显著的优势。
对aie染料荧光探针的研究,主要解决aie的水溶性及生物相容性问题。为了解决上述问题,现有技术中普遍使用以下方案:aie染料和两亲性分子的非共价自组装、aie染料与亲水性分子的共价共轭、aie染料与其他单体的聚合以及aie染料在二氧化硅纳米粒子中的包封等。
喜树碱是一种效果良好的植物性抗肿瘤药物,对消化道癌症、肝癌和头颈部癌有较好的疗效,而且副作用较少。但是其水溶性差,多采用注射的方式给药,如果想采用方便的口服方式给药,就需要提高其水溶性。
到目前为止,基于aie染料的纳米探针的包封基团的生物医学应用主要集中在生物学成像上,并无其他诊疗功能。并且其中不乏缺少良好的稳定性和低细胞毒性的aie染料。在医学成像上使用基于aie染料的纳米探针进行肿瘤细胞成像本身就是一个复杂的操作,如果想针对肿瘤细胞进行治疗还需要额外给药或者化疗,患者要承受加倍的肉体折磨,用药量加大,所以迫切的需要能把上述两个过程结合在一起的技术,而现有技术中没有既能够解决aie的水溶性问题又同时具有靶向和杀伤肿瘤细胞功能的纳米颗粒,抗癌药物的水溶性也亟待提高,所以开发具有生物成像以及诊疗双重作用的aie纳米颗粒并同时具有良好的稳定性是亟待解决的科学问题。
技术实现要素:
针对现有技术中的缺陷,本发明利用一种自组装元件二苯丙氨酸肽(l-苯丙氨酰-苯丙氨酸)将具有肿瘤杀伤效果的药物以及肿瘤靶向性的亲水基团氨基葡萄糖,在水溶液中自组装成纳米颗粒,然后以此结构为基础,形成可以负载聚集诱导发光材料(aie)的纳米颗粒,旨在实现靶向肿瘤细胞成像以及杀伤的双重效果,同时提高抗癌药物的水溶性。
为了实现以上目的,本发明提供了以下技术方案:
一种聚集诱导发光纳米颗粒,外侧为一种两亲性分子通过自组装形成的纳米骨架,内部负载aie,所述两亲性分子为抗癌药-二苯丙氨酸肽-氨基葡萄糖。氨基葡萄糖具有靶向肿瘤的作用。抗癌药可以杀伤肿瘤细胞。
进一步的,所述抗癌药为喜树碱、雷公藤甲素、紫杉醇、阿霉素中的任意一种,所述抗癌药均具有疏水性,都具有水溶性差的问题,都具有末端的羟基,能够与苯丙氨酸二肽形成酯键,在结构和性质上相似。
进一步的,所述纳米骨架为水溶性,从而提高了抗癌药物的水溶性。
本发明还提供一种两亲性分子,所述两亲性分子为抗癌药-二苯丙氨酸肽-氨基葡萄糖。所述抗癌药为喜树碱、雷公藤甲素、紫杉醇、阿霉素中的任意一种。
本发明同时提出了一种聚集诱导发光纳米颗粒的制备方法,包括如下步骤:
(1)制备抗癌药-二苯丙氨酸肽-氨基葡萄糖两亲性分子;
(2)抗癌药-二苯丙氨酸肽-氨基葡萄糖两亲性分子通过自组装作用形成水溶性的纳米骨架;
(3)制备内部负载聚集诱导发光材料的抗癌药-二苯丙氨酸肽-氨基葡萄糖aie纳米颗粒。
进一步的,所述步骤(1)中首先制备羧酸-抗癌药,然后制备叔丁氧羰基-二苯丙氨酸肽-氨基葡萄糖,再制备抗癌药-二苯丙氨酸肽-氨基葡萄糖两亲性分子。
进一步的,所述步骤(2)中的纳米骨架由抗癌药-二苯丙氨酸肽-氨基葡萄糖于水溶液中自组装形成。
进一步的,所述步骤(3)中将2,3-双(4-(苯基(4-(1,2,2-三苯基乙烯基)苯基)氨基)苯基)富马腈在超声环境中加入到步骤(2)形成的水溶液中,透析。
进一步的,所述抗癌药-二苯丙氨酸肽-氨基葡萄糖和2,3-双(4-(苯基(4-(1,2,2-三苯基乙烯基)苯基)氨基)苯基)富马腈体积比为1:1。这个比例对于聚集诱导发光材料的包载非常关键。2,3-双(4-(苯基(4-(1,2,2-三苯基乙烯基)苯基)氨基)苯基)富马腈的量要小于或者等于二苯丙氨酸肽-氨基葡萄糖的量。本发明尝试过其他比例,当2,3-双(4-(苯基(4-(1,2,2-三苯基乙烯基)苯基)氨基)苯基)富马腈的量大于二苯丙氨酸肽-氨基葡萄糖,会导致2,3-双(4-(苯基(4-(1,2,2-三苯基乙烯基)苯基)氨基)苯基)富马腈过量而以沉淀的形式析出,1:1效果最好,不会浪费喜树碱-二苯丙氨酸肽-氨基葡萄糖2,3-双(4-(苯基(4-(1,2,2-三苯基乙烯基)苯基)氨基)苯基)富马腈的量也恰好合适。
本发明同时提出了所述的聚集诱导发光纳米颗粒在制备抗肿瘤药物中的应用。
本发明还提出了所述的聚集诱导发光纳米颗粒在细胞器染色、病原体识别、细胞长周期示踪、肿瘤细胞成像中的应用。
综上,与现有技术相比,本发明达到了以下技术效果:
1、本发明的纳米药物修饰的aie纳米颗粒,具有靶向癌细胞成像并且杀伤癌细胞的双重作用,可为aie的生物医学临床研究提供基础。
2、制备的纳米颗粒水溶性良好。
3、提高了抗癌药物的水溶性。单纯的喜树碱只溶于二甲基亚砜或者四氢呋喃中,本发明中,在水溶液中,通过自组装元件将喜树碱包裹于疏水核心,亲水基团-氨基葡萄糖裸露在外侧,从而形成水溶性的纳米颗粒,在超声的环境下,加入一定比例的aie,从而将aie包裹与疏水核心中。
4、本发明的自组装纳米颗粒具有良好的稳定性。
5、本发明的自组装元件制备方法适用性广,便于操作推广,为后续的研究奠定了基础。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
图1为喜树碱-二苯丙氨酸肽-氨基葡萄糖(cppg)aie纳米颗粒制备示意图。
图2为不同浓度的喜树碱-二苯丙氨酸肽-氨基葡萄糖与2,3-双(4-(苯基(4-(1,2,2-三苯基乙烯基)苯基)氨基)苯基)富马腈的用量下喜树碱-二苯丙氨酸肽-氨基葡萄糖(cppg)aie纳米颗粒的包载浓度和荧光强度。
图3为喜树碱-二苯丙氨酸肽-氨基葡萄糖(cppg)aie纳米颗粒7天内的粒径大小。
图4为为喜树碱-二苯丙氨酸肽-氨基葡萄糖(cppg)aie纳米颗粒的光稳定性结果。
图5为喜树碱-二苯丙氨酸肽-氨基葡萄糖(cppg)aie纳米颗粒性质表征图。
图6为喜树碱-二苯丙氨酸肽-氨基葡萄糖(cppg)aie纳米颗粒对肿瘤细胞的杀伤效果。
图7为喜树碱-二苯丙氨酸肽-氨基葡萄糖(cppg)aie纳米颗粒在细胞内的成像。
具体实施方式
为了使本技术领域的人员更好地理解本发明方案,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分的实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都应当属于本发明保护的范围。
本发明的聚集诱导发光纳米材料能够靶向并杀伤肿瘤细胞的机理:
研究表明,葡萄糖转运蛋白在癌细胞表面过表达,使得氨基葡萄糖可以在肿瘤部位大量富集,本发明的两亲性分子:抗癌药-二苯丙氨酸肽-氨基葡萄糖中含有氨基葡萄糖,从而达到靶向肿瘤的功能。同时本发明的两亲性小分子自组装的aie纳米材料中含有抗癌药,如喜树碱(cpt),能够杀伤肿瘤细胞。本发明的方法还可改善纳米药的水溶性问题,将不溶性的抗癌药包裹于带有亲水基团的纳米颗粒中,从而形成水溶性的纳米颗粒。同时结合aie材料的聚集发光特征,将癌细胞靶向成像和杀伤完美的结合起来。
本发明用纳米药包裹aie形成纳米颗粒的制备方法是:首先通过化学合成的方法得到两亲性的分子:抗癌药-二苯丙氨酸肽-氨基葡萄糖,合成的方法见实施例1,然后在水溶液中进行自组装形成纳米颗粒,以此作为纳米颗粒骨架,将2,3-双(4-(苯基(4-(1,2,2-三苯基乙烯基)苯基)氨基)苯基)富马腈(ttf)溶解在四氢呋喃(thf)中,然后按照1:1的比例,在超声的环境中,将ttf溶液逐滴加入到纳米颗粒的水溶液中,然后将制备的溶液放入透析袋中,去除游离的单分子,最后得到两亲性小分子自组装的aie纳米颗粒,方法流程见图1。
本发明中使用的药品和试剂的公司及货号如下:
dbu:阿拉丁,d106478;
喜树碱:可从商业途径购买得到,不限公司和货号;
hatu:安耐吉化学,a020149;
dipea:梯希爱化成工业,d1599;
dcm:上海凌峰化学,da402;
tfa:阿拉丁,t103291;
dmso:罗恩,r017418;
nhs:阿达玛斯试剂有限公司,6066-82-6;
dic:sigma-aldrich,d125407;
dmap:安耐吉化学,b040170。
以下实施例以喜树碱为例,但是雷公藤甲素、紫杉醇、阿霉素等抗癌药物均具有疏水性,都具有水溶性差的问题,都具有末端的羟基,能够与苯丙氨酸二肽形成酯键,在结构和性质上相似,因此本领域技术人员能够推及雷公藤甲素、紫杉醇、阿霉素均可适用以下的方案。
实施例1两亲性分子喜树碱-二苯丙氨酸肽-氨基葡萄糖(cppg)的制备步骤
具体步骤如下:
(1)在0℃将1,8-二氮杂双环十一碳-7-烯(dbu)缓慢加入喜树碱和丁二酸酐的二氯甲烷溶液中。将反应混合物在室温搅拌数小时,薄层层析硅胶板(tlc)监测直到反应完成。旋干溶剂,粗产物用甲醇重结晶,得到目标产物cpt-cooh为浅黄色粉末。
(2)将叔丁氧羰基-二苯丙氨酸肽-羧基和2-(7-偶氮苯并三氮唑)-n,n,n',n'-四甲基脲六氟磷酸酯(hatu)溶于二氯甲烷中。0℃加入n,n-二异丙基乙胺(dipea),并将混合物在室温下搅拌10分钟。然后将以上反应液加入氨基葡萄糖盐酸盐和dipea的二氯甲烷悬浮液中。室温下搅拌过夜,将反应液倒入饱和盐水中。离心收集二氯甲烷相中的不溶固体。用水洗涤沉淀物,并真空干燥,得到白色固体为目标产物。
(3)将叔丁氧羰基-二苯丙氨酸肽-氨基葡萄糖溶解在二氯甲烷(dcm)中并加入三氟乙酸(tfa)搅拌一小时后旋干溶剂,加入1ml无水二甲基亚砜(dmso)、羧酸喜树碱(cpt-cooh)、n-羟基丁二酰亚胺(nhs),n,n'-二异丙基碳二亚胺(dic)、4-二甲氨基吡啶(dmap),在室温下搅拌2小时。然后加入二氯甲烷和水,离心收集二氯甲烷相中的不溶固体。用水和二氯甲烷洗涤沉淀物,并真空干燥,得到目标产物cppg浅黄色固体。
实施例2纳米药物与aie染料ttf结合形成纳米颗粒的过程和表征
以自组装的两亲性分子喜树碱-二苯丙氨酸肽-氨基葡萄糖(cppg)为纳米颗粒骨架制备纳米药包裹aie的纳米颗粒,具体步骤如下:
(1)将1mgcppg和1mg2,3-双(4-(苯基(4-(1,2,2-三苯基乙烯基)苯基)氨基)苯基)富马腈(ttf-一种常用的aie分子)分别溶解于四氢呋喃(thf)中,然后在超声环境下将cppg逐滴加入到水中,并用移液枪反复吹打以便除去thf,使两亲性分子通过自组装作用从而形成水溶性的纳米骨架。
(2)以(1)中形成的水溶液为模板,在同等条件下,按照1:1的体积,吸取等体积的ttf溶液,逐滴加入其中,并用移液枪反复吹打以便除去thf,使两亲性分子通过自组装作用从而形成水溶性的纳米骨架。随后将烧杯里的液体转移至分子量1000的透析袋内,并用蒸馏水透析48小时,期间每8小时换水一次,以除去没有形成颗粒的游离单分子。
喜树碱-二苯丙氨酸肽-氨基葡萄糖和ttf的比例对于最终聚集诱导发光材料能否成功包载非常关键。ttf的量要小于或者等于二苯丙氨酸肽-氨基葡萄糖的量。本发明尝试过其他比例,如图2所示,喜树碱-二苯丙氨酸肽-氨基葡萄糖和ttf的体积比分别为1:0.3、1:0.5、1:1,ttf的量大于二苯丙氨酸肽-氨基葡萄糖,会导致ttf过量而以沉淀的形式析出,1:1效果最好,不会浪费喜树碱-二苯丙氨酸肽-氨基葡萄糖,ttf的量也恰好合适。由图2a的结果显示,喜树碱-二苯丙氨酸肽-氨基葡萄糖和ttf的体积比为1:1时,纳米药物的荧光强度最高。荧光强度越高,代表负载的aie浓度越高。
将透析后的纳米颗粒水溶液装在测量皿中,用粒度仪测定其粒径,通过测定不同粒径颗粒的数量,最后通过计算所有颗粒的平均值即为其平均粒径,结果如图3所示,得到的纳米颗粒的平均粒径约为57nm,且粒径在7天内基本保持不变,说明本发明的aie纳米自组装颗粒具有良好的结构稳定性。并且检测了纳米颗粒在0-4000s时间长度内的光照下荧光强度的变化情况,结果如图4所示,荧光强度几乎没有任何变化,说明本发明的aie纳米自组装颗粒具有良好的光稳定性。
以下通过透射电子显微镜获得电镜图,通过荧光光谱仪测定荧光强度,通过紫外分光光度计测定组成纳米颗粒的各个组分的吸收强度,从而确定纳米颗粒包装成功。
将cppgaie纳米颗粒水溶液装置于比色皿中,利用荧光光谱仪,488nm波长激发,检测荧光发射峰,如图5a所示,发射峰位于650nm处,进而证明aie与纳米颗粒包装成功。利用紫外分光光度计,测定不同组分的吸收峰,结果如图5b所示,cppgaie纳米颗粒不仅具有cpt的吸收峰,也包含aie的吸收峰,进而证明cppgaie纳米颗粒各组分包装成功。将cppgaie纳米颗粒水溶液滴于载样片的铜网上,利用透射电镜拍摄纳米颗粒的形态,结果如图5c所示,从而证明纳米颗粒包装成功。
实施例3cppgaie纳米颗粒靶向肿瘤细胞成像及杀伤效果
分别将肿瘤细胞mcf7以及正常细胞lo2以5×103个/孔的密度铺在96孔板中,在细胞培养箱中孵育24h后,弃去上清,然后加入200μl含有不同浓度cppgaie纳米颗粒(0、1、2、4、6、8、10mg/ml)的完全培养基到对应的孔中,每一个浓度设置5个复孔,置于37℃、5%co2细胞培养箱中孵育48h。最后弃去上清,每孔加入100μlcck8检测试剂,置于37℃、5%co2细胞培养箱中孵育40min后,检测在450nm处的吸收值,从而计算纳米药物对细胞的杀伤效果。结果显示,如图6所示,左边的柱子代表肿瘤细胞的存活率,右边的柱子代表正常细胞的存活率,随着cppgaie纳米颗粒浓度的增加,肿瘤细胞的存活率显著低于正常细胞,所以相较于正常细胞cppgaie纳米药物对肿瘤细胞的杀伤效果更显著。
将mcf7和lo2细胞分别与cppgaie纳米颗粒在37℃下孵育3小时后,将细胞用pbs洗涤3次。最后使用共聚焦激光扫描显微镜进行细胞成像,使用480nm激光作为光源,并收集了600至700nm的发射光。实验结果如图7所示,在mcf7细胞中可以明显检测到大量aie纳米颗粒的聚集,而lo2中较少。纳米颗粒在肿瘤细胞中大量富集,在正常细胞中较少,说明本发明的纳米颗粒能够有效的靶向和杀伤肿瘤细胞。
综上,与现有技术相比,本发明达到了以下技术效果:
1、本发明的纳米药物修饰的aie纳米颗粒,具有靶向癌细胞成像并且杀伤癌细胞的双重作用,可为aie的生物医学临床研究提供基础。
2、制备的纳米颗粒水溶性良好。
3、提高了抗癌药物的水溶性。单纯的喜树碱只溶于二甲基亚砜或者四氢呋喃中,本发明中,在水溶液中,通过自组装元件将喜树碱包裹于疏水核心,亲水基团-氨基葡萄糖裸露在外侧,从而形成水溶性的纳米颗粒,在超声的环境下,加入一定比例的aie,从而将aie包裹于疏水核心中。
4、本发明的自组装纳米颗粒具有良好的稳定性。
5、本发明的自组装元件制备方法适用性广,便于操作推广,为后续的研究奠定了基础。
本发明的聚集诱导发光纳米颗粒能够用于制备抗肿瘤药物,还可以应用在细胞器染色、病原体识别、细胞长周期示踪、肿瘤细胞成像中。
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询



 商标分类
商标分类  商标转让
商标转让 



