一种拉西地平片的制备方法与流程
 2021-01-08 11:01:50|
2021-01-08 11:01:50| 370|
370| 起点商标网
起点商标网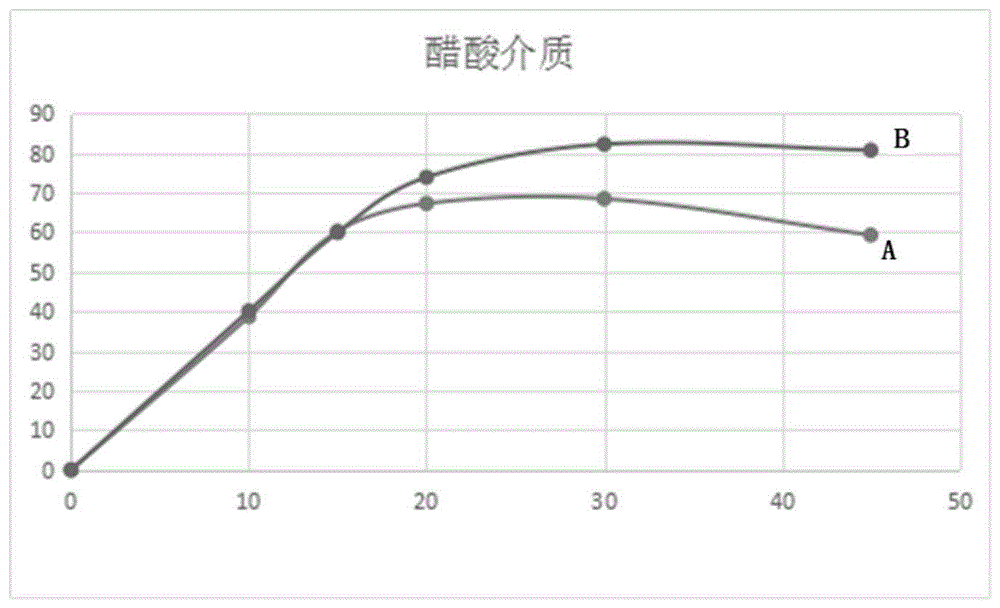
本发明属于医药
技术领域:
;具体涉及是一种拉西地平片的制备方法。
背景技术:
:拉西地平属于第三代长效钙离子拮抗剂,属于二氢吡啶类化合物。拉西地平由英国gsk公司首先研发出来,于1991年获准在意大利首先上市,商品名为lacipil和motens。拉西地平的化学名称为:(e)-4-{2-[3-(羧叔丁基)-3-氧代-1-丙烯基]苯基}-1,4-二氢-2,6-二甲基-3,5-吡啶-二羧酸二乙酯,分子式:c26h33no6,其分子量为455.59。本品为白色或类白色结晶性粉末,无臭无味,遇光不稳定,在乙酸乙酯中易溶,丙酮中溶解,甲醇、乙醇中略溶,在水中几乎不溶。熔点:175-179℃。拉西地平通过选择性地阻滞电压依赖性l-型钙通道,减少跨膜ca离子内流,有效扩张周围动脉血管,从而减小周围血管阻力,降低心脏后负荷,降低血压。由于在分子结构中引入叔丁基,拉西地平的脂溶性大大高于其它钙离子拮抗剂,疗效更为显著,药效更为持久,每日仅需2-6mg即可满足需求。另外,拉西地平有效克服了同类产品的作用时间短、药物速率不均匀和副作用较多的缺点。基于这些独特的药理药效,拉西地平成为抗压治疗的首选药物。此外,拉西地平可以明显降低血浆lpo和巨噬细胞诱导的一氧化氮合酶的活性,避免内皮氧化损伤,从而抑制颈动脉内膜中层厚度增加以及减少斑块数量,从而有效地防止动脉粥样硬化。最新研究也表明,拉西地平还具有抑制肾损伤和影响心脏重构的作用。国内上市情况1995年5月,哈尔滨制药三厂,获得片剂新药证书及生产批件。2006年7月,浙江贝得药业有限公司,获得分散片生产批件。2006年9月,浙江金华康恩贝生物制药有限公司,获得分散片生产批件。2008年3月,万特制药(海南)有限公司,分散片未获批准。2008年5月,广州邦民制药有限公司,片剂未获批准。2010年9月,哈尔滨制药三厂,提交补充申请,更名为哈药集团三精明水药业有限公司。2012年,glaxowellcom生产的拉西地平片,商品名“乐息平”,在中国获批上市。拉西地平溶解性极差,目前国内上市的药物剂型仅有拉西地平片,溶解速度缓慢,生物利用度较低。此外,现有片剂的均匀度也不够理想。为了改善上述缺点,哈药集团三精制药股份有限公司在中国专利申请cn101653423a公开了一种拉西地平片及其制备方法,通过将拉西地平片原料与乳糖按照1:1超微粉碎混合均匀,然后再加入其它辅料制成拉西地平片。然而,超微粉碎耗能较高,同时拉西地平片的溶出速度较慢,同时机械强度不理想,在实际生产中容易出现裂片和碎片等问题。浙江贝得药业有限公司在中国专利申请cn102198107b中公开了一种拉西地平分散片及其制备方法。该分散片通过在制备工艺中引入聚乙二醇作为药物分散介质,将拉西地平预先制成固体分散体再与其它辅料压片。该分散片溶出速率较快,然而平均溶出度不高;同时分散片的机械强度尤其是硬度仍然难以满足需要。因此,针对现有技术的上述缺陷,需要进一步寻找一种新的拉西地平片及其制备方法。技术实现要素:本发明的目的是克服现有制备拉西地平片的方法存在实际生产中容易出现裂片和碎片、溶出速率与累积溶出度不能同时提高以及机械强度尤其是硬度低的问题,提供一种溶出速度较快同时累积溶出度明显提高的拉西地平片的制备方法。为了实现以上目的,本发明采用的技术方案是:本发明的一种拉西地平片的制备方法,是按以下步骤进行:一、过筛:取拉西地平、聚维酮k30、一水乳糖、干燥乳糖或无水乳糖过30目筛,硬脂酸镁过100目筛;二、称量:取各组分,按下述质量份数称量:2~8份的拉西地平、16-96份的聚维酮k30、128.7~225.12份的一水乳糖、干燥乳糖或无水乳糖a、38.6~93.8份的一水乳糖、干燥乳糖或无水乳糖b、45.5-695份的无水乙醇、0.6-3份的硬脂酸镁以及4.5-15份包衣粉;三、配制:将步骤二称取的拉西地平、聚维酮k30与无水乙醇溶解;四、固体分散体制备:将步骤二称取的一水乳糖、干燥乳糖或无水乳糖a放入流化床中,将步骤三溶解物喷涂于一水乳糖、干燥乳糖或无水乳糖a上制粒,干燥后,得固体分散体;五、分散体与辅料混合:将步骤四制得的分散体与步骤二称取一水乳糖或干燥乳糖或无水乳糖b混合20~40min,再加入步骤二称取的硬脂酸镁,混合5~15min,即得分散体与辅料混合粉;六、压片:将步骤四制得分散体与辅料混合粉,采用旋转式压片机在8-11kn压力下进行直接压片,片重为285-315mg/片,即得拉西地平片;七、包衣:将步骤六制得的拉西地平片,采用高效包衣机进行包衣,即得包衣后的拉西地平片。进一步地,步骤二中所述的取步骤一过筛后的各组分,按下述质量份数称量:1~7份的拉西地平、8-84份的聚维酮k30、137.7~232.4份的一水乳糖、干燥乳糖或无水乳糖a、41.3~96.8份的一水乳糖、干燥乳糖或无水乳糖b、45.5-507份的无水乙醇、0.5-2.5份的硬脂酸镁和3-13.5份包衣粉。进一步地,步骤二中所述的取步骤一过筛后的各组分,按下述质量份数称量:2~10份的拉西地平、16-120份的聚维酮k30、111~225.2份的一水乳糖、干燥乳糖或无水乳糖a、33.3~93.8份的一水乳糖、干燥乳糖或无水乳糖b、93.5-695份的无水乙醇、0.5-3.5份的硬脂酸镁和5-16.5份包衣粉。进一步地,步骤二中所述的取步骤一过筛后的各组分,按下述质量份数称量:2~7份的拉西地平、16-84份的聚维酮k30、137.7~225.2份的一水乳糖、干燥乳糖或无水乳糖a、41.3~93.8份的一水乳糖、干燥乳糖或无水乳糖b、80-507份的无水乙醇、0.5-2.5份的硬脂酸镁和5-13.5份包衣粉。进一步地,步骤二中所述的取步骤一过筛后的各组分,按下述质量份数称量:4份的拉西地平、40份的聚维酮k30、203.6份的一水乳糖、干燥乳糖或无水乳糖a、50.9份的一水乳糖、干燥乳糖或无水乳糖b、193份的无水乙醇、1.5份的硬脂酸镁和12份包衣粉。进一步地,步骤三中所述的取步骤二称量后的各组分,按下述方法配制:在30-60度无水乙醇中先溶解拉西地平至澄清透明再溶解聚维酮k30至澄清透明或在30-60度无水乙醇中先溶解聚维酮至澄清透明再溶解拉西地平至澄清透明。进一步地,步骤四中所述的取步骤二称取的203.6份一水乳糖和/或干燥乳糖和/或无水乳糖与步骤二配制的澄清透明溶液,按下述方法制备:将一水乳糖和/或干燥乳糖和/或无水乳糖放入流化床中,制粒在进风温度40~70℃,物料温度25~60℃,雾化压力0.1-0.6mpa,供液量0.25-0.6份/分钟下将步骤二澄清透明溶液喷涂于一水乳糖和/或干燥乳糖和/或无水乳糖上制粒,在25~100℃干燥后,继续处理固体分散体温度120±10℃时间30~90min;进一步地,步骤五中所述的将步骤四制得的分散体与步骤二称取的50.9份一水乳糖和/或干燥乳糖和/或无水乳糖混合20~40min,再加入步骤一称取的硬脂酸镁,混合5~15min,即得分散体与辅料混合粉。与现有技术相比,本发明具有下列有益技术效果:i)本发明的拉西地平片在提供处方简单辅料种类少同时,片剂均匀好,溶出速度较快,同时累积溶出度明显提高。ii)本发明采用固体分散技术,在喷雾干燥的情况下将原料药均匀的喷涂在乳糖上干燥再处理进而制备出拉西地平分散体,提高片剂均匀度和累积溶出度,同时包衣避免拉西地平光敏感,口感好便于口服,辅料常用安全,稳定性;设备成本低且无污染;工业化稳定,可产生巨大的社会效益和经济效益,适合普遍推广使用。附图说明图1为在醋酸介质中累积溶出曲线图,其中,a为分散体1,b为分散体2;图2为在盐酸介质中累积溶出曲线图,其中,a为参照样品,b为样品1,c为样品2,d为样品3;图3为在醋酸介质中累积溶出曲线图,其中,a为参照样品,b为样品1,c为样品2,d为样品3;图4为在磷酸介质中累积溶出曲线图,其中,a为参照样品,b为样品1,c为样品2,d为样品3;图5为在标准介质中累积溶出曲线图,其中,a为参照样品,b为样品1,c为样品2,d为样品3。具体实施方式本领域的普通技术人员可以理解,上述各实施方式是实现本发明的具体实施例,而在实际应用中,可以在形式上和细节上对其作各种改变,而不偏离本发明的精神和范围。为使本发明实施例的目的、技术方案和优点更加清楚明白,下面将详细叙述清楚说明本发明所揭示内容的精神,任何所属
技术领域:
技术人员在了解本
发明内容的实施例后,当可由本
发明内容所教示的技术,加以改变及修饰,其并不脱离本
发明内容的精神与范围。本发明的示意性实施例及其说明用于解释本发明,但并不作为对本发明的限定。通过以下实施例验证本发明的有益效果:本实施例的一种拉西地平片的制备方法是按以下步骤进行:一、过筛:取拉西地平、聚维酮k30、一水乳糖和/或干燥乳糖和/或无水乳糖过30目筛,硬脂酸镁过100目筛;二、称量:取各组分,按下述质量份数称量:4份的拉西地平、40份的聚维酮k30、203.6份的一水乳糖、干燥乳糖或无水乳糖a、50.9份的一水乳糖、干燥乳糖或无水乳糖b、193份的无水乙醇、1.5份的硬脂酸镁以及12份包衣粉;三、配制:将步骤二称取的拉西地平、聚维酮k30与无水乙醇溶解;四、固体分散体制备:将步骤二称取的一水乳糖、干燥乳糖或无水乳糖a放入流化床中,制粒将步骤三溶解物喷涂于一水乳糖、干燥乳糖或无水乳糖a上制粒,干燥后,继续处理固体分散体;五、分散体与辅料混合:将步骤四制得的分散体与步骤二称取一水乳糖或干燥乳糖或无水乳糖b混合20~40min,再加入步骤二称取的硬脂酸镁,混合5~15min,即得分散体与辅料混合粉;六、压片:将步骤四制得分散体与辅料混合粉,采用旋转式压片机在8-11kn压力下进行直接压片,片重为285-315mg/片,即得拉西地平片;七、包衣:将步骤六制得的拉西地平片,采用高效包衣机进行包衣,即得包衣后的拉西地平片。本实施例的拉西地平片,采用固体分散技术,制备溶媒将拉西地平与聚维酮k30结合,再利用流化床将拉西地平均匀喷涂于一水乳糖、干燥乳糖或无水乳糖a上制粒进而保证拉西地平分散性更均匀,干燥,继续处理固体分散体是拉西地平与聚维酮k30和乳糖充分结合保证溶出速度较快,累积溶出度明显提高。同时包衣避免拉西地平光敏感,口感好便于口服,辅料常用安全,稳定性。1.将本实施例在固体分散体制备中干燥和干燥后处理进行效果比较,累积溶出实验结果如下:表1ph4.0醋酸-0.2%吐温-20介质醋酸介质01015203045分散体10.0038.7160.2867.3068.5059.33分散体20.0040.1559.9473.9282.2780.76结果表明:固体分散体制备中,固体分散体干燥得分散体1累积溶出度明显低于固体分散体干燥后处理得分散体2累积溶出度。2.将本实施例制得的拉西地平片,参照中国药典进行累积溶出实验:表2ph1.2盐酸-1%吐温-20介质盐酸介质01015203045f2参照样品0.0041.7866.1780.6088.5589.30——样品10.0039.2661.5476.5187.1990.0176.37样品20.0048.5865.7276.7087.3590.0969.4样品30.0041.2064.0078.7090.4092.8084.9表3ph4.0醋酸缓冲盐-1%吐温-20介质醋酸介质01015203045f2参照样品0.0040.0863.5679.1089.6892.10——样品10.0038.1060.4274.0387.4590.5772.9样品20.0042.7260.8273.2085.8990.0469.3样品30.0044.3064.4080.0091.6096.1079.25表4ph6.8磷酸缓冲盐-1%吐温-20介质磷酸介质01015203045f2参照样品0.0046.4371.5385.8293.5594.25——样品10.0043.1161.4178.3388.7190.6561.29样品20.004567.2279.1689.6992.8870.87样品30.0048.575.4587.7894.6197.3579.34表51%-吐温-20标准介质标准介质01015203045f2参照样品0.0040.6364.6580.4991.4794.07——样品10.0039.8160.7775.988.8393.3473.1样品20.0047.9365.1876.3488.7393.0767.2样品30.004568.784.895.198.969.83预be餐前实验ratio(%)90%ci(%)差值cmax餐前93.77(66.03,133.18)-0.82auc0-t(h*ng/ml)餐前104.56(80.49,135.81)25.63auc0-∞(h*ng/ml)餐前104.89(81.66,134.73)27.9结果表明:由图1至5以及表1至5可知,由于进行拉西地平分散体的制备,导致本发明实施制得的拉西地平片有很好的均匀度进而累积溶出度达到90%以上,另外,对片剂进行包衣避免拉西地平光敏感。当前第1页1 2 3
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



