5-取代-4-硫-2’,3’,5’-O-三叔丁基二甲硅烷基核苷化合物合成方法与流程
 2021-02-02 21:02:20|
2021-02-02 21:02:20| 260|
260| 起点商标网
起点商标网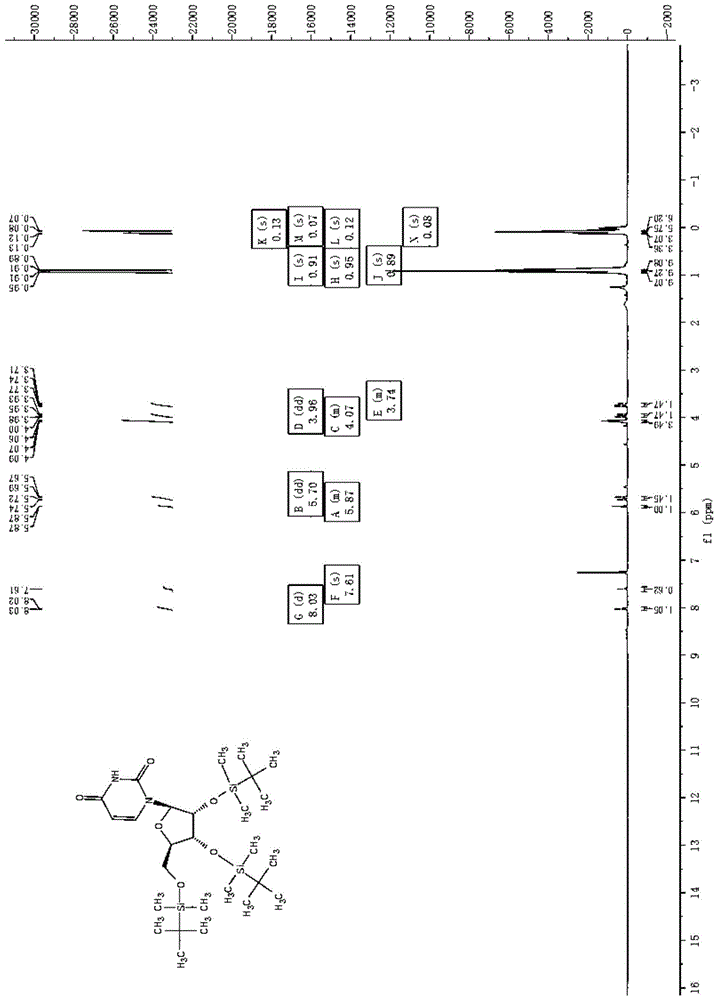
本发明属于化学合成技术领域,本发明涉及一种5-取代-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基核苷化合物的快速合成方法。
背景技术:
1988年,elion和hitchings因“发现了药物治疗的重要原则”获得诺贝尔生理学或医学奖,这些原则促进了一系列新的核酸衍生物的开发(thenobelprizeinphysiologyormedicine1988-pressrelease.nobelmediaab[eb/ol].http://www.nobelprize.org/nobel_prizes/medicine/laureates/1988/press.html.),其中他们开发的6-硫鸟嘌呤(6-thioguanine,6-tgua)、6-巯基嘌呤(6-mercaptopurine,6-mp)和硫唑嘌呤(azathioprine)核酸衍生物在治疗白血病和抑制移植器官排斥等疾病中表现出出色的化疗效果(eliongb.thepurinepathtochemotherapy[j].science,1989,244(4900):41-47.)。硫化后的天然核苷化合物与天然核苷相比,在生物活性方面表现出独特的性质,有研究表明含有硫羰基的核苷类化合物其嘧啶碱基上4-位羰基氧被硫取代后吸光度变大,最大吸收峰红移,对光极其敏感(霍书华,李德鹏,王健,等.分子科学学报,2013,29(5):392-396.),使dna分子对长波紫外线(uva)或近紫外线光敏感。其中4-硫代脱氧核苷类似物对紫外线很敏感,可作为潜在抗肿瘤药物,尤其是与近紫外光(uva)结合后可用于治疗皮肤癌(pridgeonsw,heerr,taylorgabr.j.cancer2011,104,1869.)。硫代核苷这些独特的生物学性质引起了科学家对硫代核苷化合物合成的兴趣。
目前报道的4-硫代核苷化合物的合成主要是通过劳森试剂在1,4-二氧六环溶剂中硫化核苷化合物合成,该反应存在反应温度高(一般在100℃左右反应),反应时间长(3小时反应完成),生成大量黑色副产物,后处理存在目标化合物难分离的困难等缺点。
技术实现要素:
为了克服现有技术的不足,本发明提供一种5-取代-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基核苷化合物的快速合成方法。该合成方法具有缩短反应时间(一般1小时之内完成反应)、产率高、无难分离的副产物且副产物极少等特点。此外,虽然该技术的反应温度高,但后处理仅需要水洗,二氯甲烷萃取,减压蒸发即可得较纯的5-取代-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基核苷化合物,更纯的5-取代-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基核苷化合物可通过柱层析快速分离得到。
本发明的上述目的是通过以下技术方案实现的:
一种5-取代-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基核苷化合物;具有通式(b)结构:
其中,x=ch3、h、f、cl、br、i。
5-取代-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基核苷化合物的具体结构式如下:
其中a为5-甲基-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基尿苷,b为4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基尿苷,c为5-氟-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基尿苷,e为5-溴-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基尿苷,f为5-碘-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基尿苷。
一种5-取代-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基核苷化合物的快速合成方法;以核苷为原料,以p2s5为硫化剂,nahco3为催化剂,在二乙醇二甲醚中发生化学反应,最终得到通式(b)所示化合物;
其中,x=ch3、h、f、cl、br、i。
进一步的,上述5-取代-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基核苷化合物的快速合成方法步骤为:在氮气保护下,将5-取代核苷化合物与叔丁基二甲基氯硅烷(tbscl)反应,反应完成后进行后处理得通式(a)所示的化合物a;化合物a接着与溶解在二乙醇二甲醚溶剂中的p2s5和nahco3反应,得黄色固体b。
进一步的,上述5-取代-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基核苷化合物的快速合成方法的具体步骤为:
s1.化合物a的合成:在氮气保护下,将1当量5-取代核苷化合物和4.5当量咪唑溶解在二氯甲烷中,冰水浴下(0℃)搅拌30分钟;30分钟后,向反应体系中加入3.5当量叔丁基二甲基氯硅烷(tbscl),室温搅拌1小时;tlc检测反应结束后,用水进行猝灭,二氯甲烷萃取;合并有机相,用饱和nacl洗涤,无水naso4干燥,过滤,减压蒸去溶剂,得化合物a,为白色固体,无须纯化直接进行下一步s2;
s2.化合物b的合成:将1当量的化合物a加入到溶有2当量p2s5的二乙醇二甲醚溶液中,待搅拌均匀后将4当量的nahco3固体加入到反应体系中,反应速度取决于co2的析出。将反应液继续搅拌至110℃,直至tlc检测反应结束。反应结束后,将反应液倒入冷水中,有黄色固体析出,过滤分离,用冷水洗涤,收集产物。
本发明与现有技术相比的有益效果是:
本发明为制备此类5-取代-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基核苷化合物提供了一种快速的合成方法。从化合物a-化合物b的合成中,利用p2s5作为硫化剂,在nahco3催化下与p2s5形成nasps2盐的特点,nasps2在反应溶液中形成sps2-,sps2-作为亲核试剂进攻5-取代-2’,3’,5’-o-三叔丁基二甲硅烷基核苷化合物嘧啶环上的4位羰基氧,继而合成目标化合物5-取代-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基核苷化合物。本发明实现了5-取代-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基核苷化合物4位氧原子的快速硫化,区别于常用的硫化手段—直接硫化法,现有技术常使用劳森试剂、五硫化二磷或硫代乙酸等硫化试剂直接硫化嘧啶核苷化合物嘧啶环上的4位氧原子,而本发明则利用sps2-离子作为亲核试剂快速硫化嘧啶核苷化合物嘧啶环上的4位氧原子,该反应具有反应时间短(一般1小时内完成),产物专一,反应产率高,副产物极少,后处理过程中利用二乙醇二甲醚和无机盐易溶于水,而5-取代-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基核苷化合物难溶于水易溶于二氯甲烷的溶解性特点,简化了高沸点二乙醇二甲醚溶剂的后处理过程,本发明在合成过程中避免使用毒性大、有恶臭的吡啶溶剂,避免使用高沸点的1,4-二氧六环溶剂,避免使用容易变质且反应副产物多的劳森试剂,简化了后处理的过柱过程。
附图说明
图1为本发明实施例1的化合物a1的核磁表征图谱。
图2为本发明实施例1的化合物b1的核磁表征图谱。
具体实施方式
下面通过具体实施例详述本发明,但不限制本发明的保护范围。如无特殊说明,本发明所采用的实验方法均为常规方法,所用实验器材、材料、试剂等均可从商业途径获得。
实施例1
4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基尿苷,其结构式为通式(b1)所示,
s1.化合物a1的合成:在氮气保护下,将尿苷(1g)和咪唑(1.67g)溶解在二氯甲烷(10ml)中,冰水浴下(0℃)搅拌30分钟。30分钟后,向反应体系中加入叔丁基二甲基氯硅烷(tbscl)(3.7g),室温搅拌1小时(25℃-30℃)。tlc检测反应结束后,用水进行猝灭,二氯甲烷萃取。合并有机相,用饱和nacl洗涤,无水naso4干燥,过滤,减压蒸去溶剂,得化合物a1,为白色油状固体,2.28g,产率95%,无须纯化直接进行下一步s2。1hnmr(cdcl3,500mhz)δ:8.03(d,j=8.1hz,1h),7.61(s,1h),5.90–5.85(m,1h),5.70(dd,j=24.6,7.8hz,1h),4.10–4.06(m,3h),3.96(dd,j=24.0,11.5hz,1h),3.77–3.70(m,1h),0.95(s,9h),0.91(s,9h),0.89(s,9h),0.13(s,3h),0.12(s,3h),0.08(s,6h),0.07(s,6h).
s2.化合物b1的合成:将0.227gp2s5在1ml的二乙醇二甲醚中充分溶解后,将上述制备的化合物a1(0.3g)投入到该反应液中充分溶解,加入固体nahco3(0.171g),加入nahco3后可看到有气体迅速生成,反应速度取决于co2的析出速度,将反应液继续搅拌至110℃,直至tlc检测不到原料a1为止。反应完成后,将冷水加入到反应液中有黄色固体迅速析出,过滤及得到化合物b1,0.2773g,产率90%,更纯的化合物可通过柱层析快速分离得到(tlc:石油醚:乙酸乙酯(v:v)=5:1)。1hnmr(cdcl3,500mhz)δ:9.29(s,1h),7.94(d,j=7.6hz,1h),6.37(d,j=6.5hz,1h),5.81(d,j=3.1hz,1h),4.10–4.04(m,3h),4.01(d,j=11.9hz,1h),3.76(d,j=11.6hz,1h),0.94(s,9h),0.93(s,9h),0.90(s,9h),0.13(s,3h),0.12(s,3h),0.10(s,3h),0.09(s,3h),0.08(s,3h),0.07(s,3h).
实施例2
5-甲基-4-硫-2’,3’,5’-o-三叔丁基二甲硅烷基尿苷,其结构式为通式(b2)所示,
s1.化合物a2的合成:在氮气保护下,将5-甲基尿苷(1g)和咪唑(1.18g)溶解在二氯甲烷(9.35ml)中,冰水浴下(0℃)搅拌30分钟。30分钟后,向反应体系中加入叔丁基二甲基氯硅烷(tbscl)(2g),室温搅拌1小时(25℃-30℃)。tlc检测反应结束后,用水进行猝灭,二氯甲烷萃取。合并有机相,用饱和nacl洗涤,无水naso4干燥,过滤,减压蒸去溶剂,得化合物a2,为白色油状固体,2g,产率90%,无须纯化直接进行下一步s2。
s2.化合物b2的合成:将0.22gp2s5在1ml的二乙醇二甲醚中充分溶解后,将上述制备的化合物a2(0.3g)投入到该反应液中充分溶解,然后加入固体nahco3(0.17g),加入nahco3后可看到有气体迅速生成,反应速度取决于co2的析出速度,将反应液继续搅拌至110℃,直至tlc检测不到原料a2为止。反应完成后,将冷水加入到反应液中有黄色固体析出,过滤及得到化合物b2,0.277g,产率90%,更纯的化合物可通过柱层析快速分离得到(tlc:石油醚:乙酸乙酯(v:v)=5:1)。
以上所述实施方式仅为本发明的优选实施例,而并非本发明可行实施的全部实施例。对于本领域一般技术人员而言,在不背离本发明原理和精神的前提下对其所作出的任何显而易见的改动,都应当被认为包含在本发明的权利要求保护范围之内。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询



 商标分类
商标分类  商标转让
商标转让 



