一株大肠杆菌工程菌及其全细胞催化产淫羊藿苷元的方法与流程
 2021-02-02 18:02:35|
2021-02-02 18:02:35| 481|
481| 起点商标网
起点商标网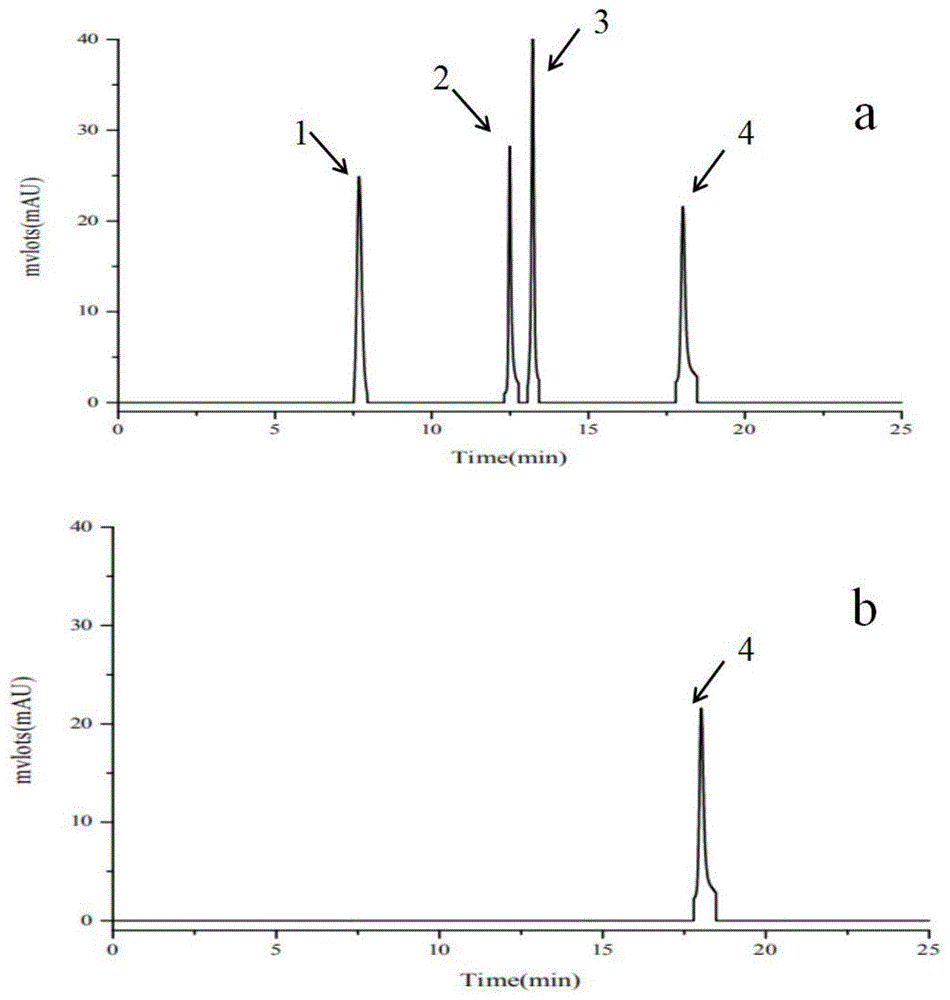
本发明涉及生物工程及天然化合物的生物合成领域,具体涉及一株大肠杆菌工程菌及其全细胞催化淫羊藿苷生产淫羊藿苷元的方法。
背景技术:
:淫羊藿苷元(脱水淫羊藿素,淫羊藿素)是小檗科淫羊藿属植物淫羊藿中一种多羟基黄酮类单体成分,具有抗肿瘤(刘松,刘超明,赖丽娟等《淫羊藿素的药理作用研究进展[j]》.赣南医学院学报,2017,37(04):631-635.)、抗氧化、抗肝纤维化、促分化、矿化、抗骨质疏松(zhengzg,zhangx,zhouyp,etal.anhydroicaritin,asrebpsinhibitor,inhibitsrankl-inducedosteoclasticdifferentiationandimprovesdiabeticosteoporosisinstz-inducedmice[j].europeanjournalofpharmacology,2017,809:156-162.)、抗炎、促进血管内皮细胞增生及血管形成(赵曙炎,马泽云《淫羊藿苷及其代谢产物脱水淫羊藿素促血管内皮细胞增殖的初步机制研究[j]》.黑龙江医学,2015,39(03):313-315.)、改善前列腺和免疫抑制等多重功效。淫羊藿苷元主要提取自淫羊藿属植物,但是自然状态下淫羊藿素植物中淫羊藿苷元的含量极低。因此,随着国内外对淫羊藿苷元药效的进一步发掘,如何绿色高效地制备淫羊藿苷元成为重点。淫羊藿是一味传统中药材,在我国具有悠久的药用历史,其主要有效成分是淫羊藿总黄酮(张嘉丽,丁辉,宋新波《淫羊藿总黄酮抗衰老研究进展[j]》天然产物研究与开发,2018.),其中黄酮类化合物是以3-苯并吡喃酮为母核的化合物,主要有淫羊藿苷、淫羊藿次苷i、宝藿苷i、朝藿定a、朝藿定b、朝藿定c等物质。几种常见的淫羊藿类物质在化学结构上具有相似性,它们的共同苷元都是脱水淫羊藿素(anhydroicaritin),差异性则在于在这一基本分子骨架的c-3位和c-7位连接上了不同种类和数量的糖基(葡萄糖基、鼠李糖基、木糖基)。自然环境中提取的淫羊藿中的黄酮存在形式主要是结合型糖苷,约占淫羊藿中黄酮含量的95%以上,其中含量最多的是淫羊藿苷,游离型的淫羊藿苷元一般不足5%,但在活性作用上游离型苷元要明显高于结合型的糖苷。目前淫羊藿苷元主要通过水解淫羊藿苷获得,方法主要包括酸水解、酶水解和酸酶结合的方法(路宇仁,陈昳冰,崔元璐等《淫羊藿苷药理作用研究进展[j]》中国实验方剂学杂志,2018(17))。酸水解是通过低浓度的盐酸硫酸等稀酸溶液水解掉淫羊藿苷c-3及c-7位点的糖苷键制备脱水淫羊藿素,如cn201110427160.0在高温状态下利用稀盐酸溶液水解淫羊藿粗提物制备出了纯度在95%以上的脱水淫羊藿素,但这种方法使用到了对环境有危害的酸,且反应温度过高(90-100℃);酸酶结合法也是较常用的方法,如zl201310280568.9主要通过酸水解掉淫羊藿苷c-3位上的鼠李糖基,再用β-葡聚糖或纤维素酶水解掉c-7位上的葡萄糖基,其酸水解过程副产物多且可调控性差,甚至可能造成产物淫羊藿苷元的母核结构的改变;cn109988137a通过smith降解,大孔树脂吸附纯化,醇洗等步骤得到高纯度淫羊藿苷元,虽然成功解决了酸水解造成的结构改变的问题,但是smith降解过程时间长且过程繁琐,有的反应过程甚至长达150小时;酶水解常通过混合酶去断裂淫羊藿苷不同c位的糖基生成淫羊藿苷元,如cn201410274823.3利用α-l-鼠李糖苷酶和β-葡萄糖苷酶组成的复合酶系-柚苷酶(商品化纯酶)来转化淫羊藿苷生成淫羊藿苷元,鼠李糖苷酶可以断裂淫羊藿苷c-3鼠李糖基的糖苷键生成淫羊藿次苷i,β-葡萄糖苷酶可以催化淫羊藿苷c-7位葡萄糖基的糖苷键生成宝霍苷i,鼠李糖苷酶和β-葡萄糖苷酶共同作用于淫羊藿苷时则生成脱水淫羊藿素,但是其反应时间长达30小时,且效率低至只能证明产生了淫羊藿苷元;zl200910184282.4利用含有纤维素酶、果胶酶、淀粉酶、蛋白酶等20多种酶的混合酶系-蜗牛酶(商品化纯酶)来制备淫羊藿苷元,其反应时间长达72小时,且产物得率较低;zl200710099025.1利用一种商品化的β-葡萄糖苷酶就可以水解淫羊藿苷生成淫羊藿苷元,但是其催化反应过程长达24小时,且产物得率最高仅为55%。因此,进一步改进淫羊藿苷元的制备方法尤为重要。以淫羊藿苷元为发明名称查找国家知识产权局专利检索数据库,共出现55条检索结果,涉及到淫羊藿苷元的专利有55项。其中,关于淫羊藿苷元制备方法的专利有8项(其中有双酶组合催化法2项,smith降解法1项,复合酶催化法4项),关于水合淫羊藿素(将淫羊藿苷的c-3,c-7上的糖取代基水解掉,且在淫羊藿苷的8-异戊烯基上加合一分子水)制备方法的专利有2项(均为酸酶结合法),关于环淫羊藿苷元(3,5-二羟基-4′-甲氧基-6″,6″-二甲基二氢吡喃并<2″,3″:7,8>黄酮)制备方法的专利有2项(均为化学法),关于淫羊藿苷元应用的专利有17项,关于环淫羊藿苷元应用的专利有1项,而其他检索结果都是与含有淫羊藿苷元的制剂制备或淫羊藿苷元衍生物的制备及它们的应用相关。以淫羊藿素为发明名称查找国家知识产权局专利检索数据库,共出现138条检索结果,涉及到淫羊藿素(脱水淫羊藿素,淫羊藿苷元)的专利有138项。其中,关于淫羊藿素制备方法的专利有22项(其中有化学合成法11项,有机酸解法3项,酶解后重结晶法4项,混合酶解法2项,酸酶结合法2项),关于水合淫羊藿素制备方法的专利有2项(都是酸酶结合法),关于环淫羊藿素制备方法的专利有4项(都是酸解法),关于淫羊藿素应用的专利有30项,关于水合淫羊藿素应用的专利有2项,关于环淫羊藿素应用的专利有3项,而其他检索结果都是与含有淫羊藿素的制剂制备或材料制备或淫羊藿苷元衍生物的制备及它们的应用相关。经文献检索,目前尚未见有全细胞催化制备淫羊藿苷元(脱水淫羊藿素,淫羊藿素)方法的报道。公开于该
背景技术:
部分的信息仅仅旨在增加对本发明的总体背景的理解,而不应当被视为承认或以任何形式暗示该信息构成已为本领域一般技术人员所公知的现有技术。技术实现要素:本发明针对现有技术中淫羊藿苷转化率不高、淫羊藿苷元产量不高的问题,发明一株大肠杆菌工程菌,以及利用该工程菌进行全细胞催化淫羊藿苷生产淫羊藿苷元的方法,直接实现淫羊藿苷到淫羊藿苷元的转化,并且具有较高的转化率。为实现上述目的,本发明提供的技术方案如下:一株大肠杆菌工程菌,以多顺反子形式共表达一个编码α-l-鼠李糖苷酶sprha2的基因和一个编码β-葡萄糖苷酶pbgl的基因;其中,所述的编码α-l-鼠李糖苷酶sprha2的基因来自鞘氨醇杆菌novosphingobiumsp.gx9,碱基序列如seqidno.1所示,所述的编码β-葡萄糖苷酶pbgl的基因来自克氏类芽孢杆菌paenibacilluscookiigx-4。利用共表达大肠杆菌工程菌pqe-sprha2-pbgl催化淫羊藿苷生产淫羊藿苷元的方法,包含以下操作步骤:(1)构建共表达大肠杆菌工程菌pqe-sprha2-pbgl,诱导培养共表达大肠杆菌工程菌pqe-sprha2-pbgl,30℃诱导8h,诱导培养结束后,收集菌体,称量菌体湿重;(2)清洗菌体3次,再用缓冲液重悬菌体,获得共表达大肠杆菌工程菌pqe-sprha2-pbgl全细胞催化液;(3)向步骤(4)所得共表达大肠杆菌工程菌pqe-sprha2-pbgl全细胞催化液中加入适当浓度的淫羊藿植物提取物,反应10h;(4)沸水浴后终止反应,获得产物,即淫羊藿苷元。作为优选,步骤(1)中所述的大肠杆菌工程菌pqe-sprha2-pbgl为多顺反子形式,目的基因pbgl位于目的基因sprha2的下游。作为优选,步骤(1)中所述的诱导培养为30℃、0.5mm的iptg诱导培养8h。作为优选,步骤(2)中所述的清洗菌体为用0.9%的nacl溶液重悬菌体。作为优选,步骤(2)中所述的缓冲液为硼酸硼砂缓冲液。作为优选,所述的硼酸硼砂缓冲液中含有0.2m的硼酸和0.05m的硼砂,ph值为8.0。作为优选,步骤(2)中清洗前菌体的浓度为16.7g/l。作为优选,步骤(3)中所述的反应条件为55℃,220rpm。作为优选,步骤(3)中所述的淫羊藿植物提取物为含有70%淫羊藿苷的淫羊藿苷粗提物。作为优选,步骤(3)中所述的适当浓度的淫羊藿植物提取物为62.5g/l浓度的淫羊藿苷粗提物。作为优选,步骤(4)中所述100℃沸水浴5min后终止反应。与现有技术相比,本发明具有如下有益效果:(1)本发明首次提供一种采用两种糖苷酶(α-l-鼠李糖苷酶sprha2和β-葡萄糖苷酶pbgl)共表达全细胞催化淫羊藿苷生产淫羊藿苷元的新方法,构建了一个含多顺反子的重组大肠杆菌菌株,采用全细胞催化的方法,直接实现淫羊藿苷到淫羊藿苷元的转化,淫羊藿苷的水解率在98%以上;(2)本发明的方法中所涉及的两种酶理化性质明确,能够通过共表达协同作用于淫羊藿苷;全细胞催化的方法,省去纯化酶的繁琐步骤,操作简单,在催化淫羊藿苷水解生产淫羊藿苷元的过程中具有转化效率高、经济、工业化潜力高等优点。附图说明图1为本发明大肠杆菌工程菌pqe-sprha2-pbgl全细胞催化淫羊藿苷生成淫羊藿苷元的hplc图;其中,a-1保留时间7.686min为淫羊藿苷,a-2保留时间12.49min为淫羊藿次苷i,a-3保留时间13.222min为宝藿苷i,a-4保留时间18.02min为淫羊藿苷元;a为含有淫羊藿苷,淫羊藿次苷i,宝藿苷i和淫羊藿苷元的标准品,b为工程菌pqe-sprha2-pbgl全细胞催化淫羊藿苷生成淫羊藿苷元的hplc图。图2为sprha2与pbgl加酶比例为4:1时水解淫羊藿苷的hplc分析;其中,a为标样,1为淫羊藿苷,2为淫羊藿次苷ⅰ,3为宝霍苷ⅰ,4为脱水淫羊藿素;b为反应5min所得结果,c为反应5h所得结果。具体实施方式下面结合附图具体实施方式进行详细描述,但应当理解本发明的保护范围并不受具体实施方式的限制。实施例中采用的原料、实际若无特殊说明,皆为市售所得。实施例11.1纯化的双酶催化淫羊藿苷的加酶量配比摸索20℃、0.5mm的iptg、180rpm诱导培养pqe-sprha2达20h,30℃、0.5mm、200rpm的iptg诱导培养pse-pbgl8h;对诱导后的pqe30-sprha2,pse-pbgl菌体进行破胞纯化后得到纯酶,对纯化后的纯酶进行蛋白定量,得出sprha2为2.2μg/μl,pbgl为1.2μg/μl,已知sprha2在加酶量为50μg/ml时反应0.3%(w/v)的淫羊藿苷6h转化率在95%以上,固定sprha2的加酶量为50μg/ml取两种纯酶稀释适当倍数后按不同加酶量比例(1:1、2:1、3:1、4:1、5:1)去反应0.3%(w/v)的淫羊藿苷;为了观察反应过程中两种酶的反应速度,分别在反应5分钟和5小时进行取样,热终止5min后hplc检测水解产物;检测结果表明,当sprha2与pbgl加酶比例为4:1,反应5h时可反应完全0.3%(w/v)的淫羊藿苷,sprha2与pbgl加酶比例为4:1时的液相检测结果如图2所示。从图2的实验结果表明:双酶作用5min时中间产物淫羊藿次苷ⅰ和宝霍苷ⅰ有剩余,且宝霍苷的剩余量较多,见图2b;随着反应时间延长,作用5h则淫羊藿苷全部水解为脱水淫羊藿素,见图2c。双酶协同完全转化淫羊藿苷所需时间比sprha2单酶水解底物时短,推测是单酶作用时生成的中间产物被很快转化为终产物淫羊藿苷元,中间产物对单酶的产物抑制作用减轻。反应生成脱水淫羊藿素需要α-l-鼠李糖苷酶sprha2的加酶量比β-葡萄糖苷酶pbgl多,sprha2是双酶催化体系的限速酶。故后续在大肠杆菌体系构建多顺反子共表达菌株时选择将sprha2放在pbgl前,距离启动子较近以确保构建的多顺反子水解淫羊藿苷效果较好。1.2大肠杆菌多顺反子共表达菌株的构建一株大肠杆菌工程菌,其构建方法操作步骤如下:(a)以本实验室自行构建的pqe-sprha2重组质粒设计引物,克隆得到线性化的pqe-sprha2:pqe30-sprha2-f:5′-aattagctgagcttggactcctgttgatagatcca-3′如seqidno.2;pqe30-sprha2-f:5′-aagctttcagcgggtcgtgcccagcgtgaccgggc-3′如seqidno.3;(b)以本实验室自行构建的pse-pbgl重组质粒为模板设计引物,克隆得到基因序列前带有pqe30载体核糖体结合位点(rbs)的pbgl基因序列:pbgl-f:5′-ggcacgacccgctgaaagcttaggagaaattaactatgagaaaccatacttcagacacg-3′如seqidno.4;pbgl-r:5′-aacaggagtccaagctcagctaatttcagcttctacggtatttcttggtt-3′如seqidno.5;(c)使用in-fusion酶(购自takara公司)连接线性化的pqe-sprha2和基因序列前带有pqe30载体核糖体结合位点(rbs)的pbgl基因序列,获得重组质粒pqe-sprha2-pbgl,转化至大肠杆菌jm109中,获得重组共表达大肠杆菌工程菌pqe-sprha2-pbgl,所得大肠杆菌工程菌pqe-sprha2-pbgl为多顺反子形式,目的基因pbgl位于目的基因sprha2的下游。实施例2利用实施例1构建所得共表达大肠杆菌工程菌pqe-sprha2-pbgl催化淫羊藿苷生成淫羊藿苷元的方法,操作步骤如下:(1)30℃、0.5mm的iptg诱导培养实施例1所得共表达大肠杆菌工程菌pqe-sprha2-pbgl8h,发酵结束后,收集菌体,称量菌体湿重;(2)用0.9%的nacl溶液清洗23.8mg湿重的菌体3次,用含有0.2m的硼酸和0.05m的硼砂、ph值为8的硼酸硼砂缓冲液重悬菌体,获得4.76mg/ml共表达大肠杆菌工程菌pqe-sprha2-pbgl全细胞催化液;(3)向步骤(2)所得共表达大肠杆菌工程菌pqe-sprha2-pbgl全细胞催化液中加入47.62g/l浓度的淫羊藿植物提取物,55℃、220rpm反应10h;淫羊藿植物提取物为含有70%淫羊藿苷的淫羊藿苷粗提物;(4)100℃沸水浴5min后终止反应,获得产物,即淫羊藿苷元,对获得的产物淫羊藿苷元进行高效液相色谱hplc分析。实施例3利用实施例1构建所得共表达大肠杆菌工程菌pqe-sprha2-pbgl催化淫羊藿苷生成淫羊藿苷元的方法,操作步骤如下:(1)30℃、0.5mm的iptg诱导培养实施例1所得共表达大肠杆菌工程菌pqe-sprha2-pbgl8h,发酵结束后,收集菌体,称量菌体湿重;(2)用0.9%的nacl溶液清洗55.5mg湿重的菌体3次,用含有0.2m的硼酸和0.05m的硼砂、ph值为8的硼酸硼砂缓冲液重悬菌体,获得11.1mg/ml共表达大肠杆菌工程菌pqe-sprha2-pbgl全细胞催化液;(3)向步骤(2)所得共表达大肠杆菌工程菌pqe-sprha2-pbgl全细胞催化液中加入44.4g/l浓度的淫羊藿植物提取物,55℃、220rpm反应10h;淫羊藿植物提取物为含有70%淫羊藿苷的淫羊藿苷粗提物;(4)100℃沸水浴5min后终止反应,获得产物,即淫羊藿苷元,对获得的产物淫羊藿苷元进行高效液相色谱hplc分析。实施例4利用实施例1构建所得共表达大肠杆菌工程菌pqe-sprha2-pbgl催化淫羊藿苷生成淫羊藿苷元的方法,操作步骤如下:(1)30℃、0.5mm的iptg诱导培养实施例1所得共表达大肠杆菌工程菌pqe-sprha2-pbgl8h,发酵结束后,收集菌体,称量菌体湿重;(2)用0.9%的nacl溶液清洗83.5mg湿重的菌体3次,用含有0.2m的硼酸和0.05m的硼砂、ph值为8的硼酸硼砂缓冲液重悬菌体,获得16.7mg/ml共表达大肠杆菌工程菌pqe-sprha2-pbgl全细胞催化液;(3)向步骤(2)所得共表达大肠杆菌工程菌pqe-sprha2-pbgl全细胞催化液中加入62.5g/l浓度的淫羊藿植物提取物,55℃、220rpm反应10h;淫羊藿植物提取物为含有70%淫羊藿苷的淫羊藿苷粗提物;(4)100℃沸水浴5min后终止反应,获得产物,即淫羊藿苷元,对获得的产物淫羊藿苷元进行高效液相色谱hplc分析。实施例5利用实施例1构建所得共表达大肠杆菌工程菌pqe-sprha2-pbgl催化淫羊藿苷纯物质(纯度≥98%)生成淫羊藿苷元的方法,操作步骤如下:(1)30℃、0.5mm的iptg诱导培养实施例1所得共表达大肠杆菌工程菌pqe-sprha2-pbgl8h,发酵结束后,收集菌体,称量菌体湿重;(2)用0.9%的nacl溶液清洗15mg湿重的菌体3次,用含有0.2m的硼酸和0.05m的硼砂、ph值为8的硼酸硼砂缓冲液重悬菌体,获得5mg/ml共表达大肠杆菌工程菌pqe-sprha2-pbgl全细胞催化液;(3)向步骤(2)所得共表达大肠杆菌工程菌pqe-sprha2-pbgl全细胞催化液中加入2g/l的淫羊藿苷标准品,55℃、220rpm反应1h;淫羊藿苷标准品中含有纯度≥98%的淫羊藿苷;(4)100℃沸水浴5min后终止反应,获得产物,即淫羊藿苷元,对产物淫羊藿苷元进行核磁共振nmr分析。检测分析:一、利用实施例1构建所得共表达大肠杆菌工程菌pqe-sprha2-pbgl催化淫羊藿苷生成淫羊藿苷元的高效液相色谱hplc分析条件:仪器设备:agilentg1311c1260quatpumpvl四元泵、agilentg1329b1260als自动进样器、co-1000columnoven柱温箱、agilentg1314f1260vwd紫外检测器。色谱柱:c18柱(alltima,250×4.6mm,5μm)检测条件:检测波长270nm,柱温30℃,流速1ml/min。流动相a:100%乙腈;流动相b:超纯水,梯度洗脱程序如下:32%a0-5min32-80%a5-12min80%a12-17min80-32%a17-20min32%a20-25min利用实施例1构建所得共表达大肠杆菌工程菌pqe-sprha2-pbgl催化淫羊藿苷纯物质生成淫羊藿苷元的hplc纯化条件:仪器设备:awatersacquityuplctm(waters,milford,ma,usa),waters2535四元梯度模块,2707自动进样器,2489uv/visible检测器,反向c18柱(sunfiretm,250×10mm,5μm)和馏分收集器iii(waterscorporation,milford,usa)。生成淫羊藿苷元的核磁共振分析条件:仪器设备brukeravance600nmr光谱仪(swissavance),氘代试剂:二甲基亚砜(dmso-d6),25℃下600mhz分析1h,150mhz分析13c。转化率和保留率的计算:淫羊藿苷的转化率%=(淫羊藿苷的初始量-淫羊藿苷的剩余量)/淫羊藿苷的初始量×100%;宝藿苷i的生成量=宝藿苷i的终产量-宝藿苷i的初始量;淫羊藿次苷i的生成量=淫羊藿次苷i的终产量-淫羊藿次苷i的初始量;淫羊藿苷元的生成量=淫羊藿苷元的终产量-淫羊藿苷元的初始量。二、结果使用高效液相色谱hplc对上述实施例得到的水解产物进行分析,大肠杆菌工程菌pqe-sprha2-pbgl通过全细胞催化,将淫羊藿苷转化为淫羊藿次苷或宝藿苷i,再由淫羊藿次苷或宝藿苷i转化为淫羊藿苷元。对实施例2-4中淫羊藿苷的转化率进行分析、统计,见表1:表1.大肠杆菌工程菌全细胞催化淫羊藿植物提取物实施例细胞浓度(mg/ml)底物浓度(mg/ml)淫羊藿苷水解率(%)24.7647.6272.4311.144.498.2416.762.599.4由表1可知,在底物浓度为细胞浓度的四倍左右时,本发明所述的实施例中3、4共表达大肠杆菌工程菌pqe-sprha2-pbgl制备淫羊藿苷元的方法,对淫羊藿苷的水解率均在98%以上。图1为实施例4中淫羊藿苷的转化产物的高效液相色谱hplc分析图,其中,a为含有淫羊藿苷,淫羊藿次苷i,宝藿苷i和淫羊藿苷元的标准品,a-1为淫羊藿苷,a-2为淫羊藿次苷i,a-3为宝藿苷i,a-4为淫羊藿苷元;b为工程菌pqe-sprha2-pbgl全细胞催化淫羊藿苷的反应产物分析图。对实施例5中淫羊藿苷的转化产物淫羊藿苷元的核磁共振nmr分析结果见表2:表2大肠杆菌工程菌pqe-sprha2-pbgl全细胞催化淫羊藿苷水解产物的nmr分析表表2中a为淫羊藿苷元标准品,b为工程菌全细胞催化淫羊藿苷水解产物,对实施例5中水解产物转化率在95%以上的结果进行制备型液相纯化,对纯度达标的产物进行nmr分析,从表2中的1h-nmr、13c-nmr和dept135的核磁共振波谱数据可以得出该大肠杆菌工程菌pqe-sprha2-pbgl催化淫羊藿苷生成的物质为淫羊藿苷元。综上,本发明首次提供一株大肠杆菌共表达工程菌,以多顺反子共表达一个编码α-l-鼠李糖苷酶的基因和一个编码β-葡萄糖苷酶的基因协同作用淫羊藿苷制备淫羊藿苷元,具有效率高、转化率高,经济、工业化潜力高等优点。前述对本发明的具体示例性实施方案的描述是为了说明和例证的目的。这些描述并非想将本发明限定为所公开的精确形式,并且很显然,根据上述教导,可以进行很多改变和变化。对示例性实施例进行选择和描述的目的在于解释本发明的特定原理及其实际应用,从而使得本领域的技术人员能够实现并利用本发明的各种不同的示例性实施方案以及各种不同的选择和改变。本发明的范围意在由权利要求书及其等同形式所限定。sequencelisting<110>广西大学<120>一株大肠杆菌工程菌及其全细胞催化产淫羊藿苷元的方法<130>jc<160>5<170>patentinversion3.3<210>1<211>3498<212>dna<213>novosphingobiumsp.<400>1atgatcgagccggcattccgccgcattcgcaccgccctgctgctggccagcgcgcttgcc60ggaatgggcgccctgccggaccgggcgacggccgagccggcacccgatgcggccgccagc120ccggtccccggcgccggggcggtgcatgccggcatggccgttccgctcgatctgcaattc180cgcgatccgcccgcttcggcccggccgcgcgtatggtggcactggatgaacggcaatgtc240acacaggatggcatcgccaaggacatcgactggatgagccgcatggggatcggcggcttg300caggcgtttgacgccgggctgatgacgccgcaagtggtcgatcaccgcctggtgttcatg360tcgcccgaatggaaggatgccttccgctttgccgcgcagagcgccgatgcgcgcgggctg420gaactggcaattgcctcttcgcccggctggtctgaaaccggcggcccctgggtgcaaccg480gccgacgcgctcaagaaagtggtgtggagcgagaccgtggtgcccggcggcaagccgctg540tccgctccgctggccgcgccgccccatgtcaccggcacgttccaggacatggaactgaac600gatccgctggcggcgctgaccaaggaaggccccgatcagcaccacgaattctatgccgac660atcgccgtgctggccgtgccggtggacgcggccggggccacgctgccgctgccggtgatc720accggcccggatggcaaggcgttggatgccgcactgctgaccggtgacagctttgccaag780gggcagatggtgccgcacggcaccgagcagcaaccttcggtggtgctggcgcggttcgac840cggccgcagaccgtgcgcggggtcacgctgttcctggccggagccaagggcatgttctcg900ggcgccgttgtcgcgcccaggctggaagcgagcagcgacggcacgacctggagcaaagtg960gccgatgtgccggtcacctcggccccgaccagcgtgagcttcgcgccggtcaccgccagc1020cagttccgcgtcgtgctggcgcccttgccgttcaagggctccaacctgggcgatccggca1080ccgggcgcggccaccgatgtcggtttcatgaagatgatggcggccggggccaccgcgccg1140ttcgacttgcgccacttccgcctgcacggggagccgcgcatcgaccggttcgaggccaag1200gccggtttctccatcgagcaggactattacgccctgggcatgcccgatgccggcgcggcc1260gggccggatgccgtcaaggtggtgaacctgacaggcaagctgcgccccgacggcacgctg1320gactggacaccgccggcgggcagcgcctggcgcatcctgcgctttggcaccagcctgctg1380ggcactaccaaccaccccgcagccccggaagcgaccgggctggaagtggacaagttcgat1440ggcgcggcggtgcggcgctacctgacgcactacttggggatgtatcgcgacgcgaccggg1500ccggaactgatgggccagcatggcgtgaaagccctgctgacggattcgatcgaagtgggc1560gcggccaactggacgcccaagatgatcgaccagttcaagcgcttgcgcggctatgatccc1620accccctggctgccgacgctggccggcgtgctgatcggcagccgcgccgatgccgaccgt1680ttcctctatgactggcgccgcacgctcgccgatctgctcgcctcggagcattatggcatg1740gtggcgcaagtggcgcacgagaacggcctcaaggtctacggcgaggcgctggaggacaac1800cgcccgatgctgggcgatgacatggccatgcgcatgcgcgccgatgtgccgatggcggcg1860ctgtggacctttggccgcgagacggggccgaaccccagctatctcgccgacatgaaaggc1920gccgcctcggtcgcgcacgtctatgggcagaacctggttgcggctgagtccatgacgtct1980gccctggcgccctgggcctacacgcccaaggacttgcgccggatcatcgacctggaattc2040gtcagcgggatcaaccgcccggtggtgcacacctcggtccaccagccggtggacgacaag2100gtgccgggcctgtcgctgatgatctttggccagttcttcaaccgccacgaaagctgggcc2160gagatggcgcggccctgggtggattacatggcgcgcaattcgctgctgttgcagcaaggg2220cgcaacgtggccgatgtcgcttatttctatggcgaggaagccccactgaccgggctttac2280ggcaaggcaccggtggccgatgcgcccaaggccaacgcctatgacttcgtcaatgccgac2340gcgctgggtggcgtgctgctcaaccaaggcaacgaactcgtcagccagggcggggcacgc2400tatcgcgcggtctacctcggcggttcgtcgcggatgatgacgctcaagaccctgcgccgc2460ctcgccgaactggtggatggtggcgccacggtaattggcctggcgccgcagggttcgccc2520gcgctcgacgatgcgcaagcggccaaggcggcggagtggcagcaactggtggcgcggctc2580tggccaggcagcggcgacgccacggtgggcaagggccgcgtgattgcgttggccgatgtc2640gacgccgggctggcgcggctgggcgtggcgcccgatttccggctggtgggcgcaagcgat2700gcgcaagtgccgttcgtgcaccgccaactcgccgatggcgacgcctggttcctggtcaac2760cgccgcaaccgcgatgaaacgttcgaggcgcatttccgcgtcaccggcaagcagcccgag2820ctgtggcacgccgacagcggcagggtggagccggtatcgtggcgcagcgagaacggcgaa2880accatcgtgccgctcagcctgccggcggaaagttcggtcttcgtggtgttccgcaagccg2940gccacgaccacccatggcgaagtgcgggcggtgcatgacatgccgctcggcactctcggc3000gcggcgaccggatcgacccgcagcaagtcgcgcgatgccggctggatggtcgcgttccag3060gccggccggggtgcgcccgcttcgctggccatgcctaccttggcgcggctggaccagaat3120gccgcgcccggcgtgcgctatttctccggcatcgcgacctatgcccgcagcttccgcctg3180cccaagggctggaagaaaggccagccgctgtggctcgacctgggtgaagtgcacgatatt3240gcgcaagtcactgtcaacggccaggatctgggcacgcagtggcacgcgccctatcgcttc3300gatgtcggcagcgcggtgcacaatggcaccaacgcgatccaggtgcgcgtggccaatagc3360tgggtcaaccgcctgatcggcgatgcgcagcccggcgccaccaaggtgacctggaccgcg3420attcccacctacaatgccgatgccccgctgcgaccttcgggcctggttggcccggtcacg3480ctgggcacgacccgctga3498<210>2<211>35<212>dna<213>artificialsequence<400>2aattagctgagcttggactcctgttgatagatcca35<210>3<211>35<212>dna<213>artificialsequence<400>3aagctttcagcgggtcgtgcccagcgtgaccgggc35<210>4<211>59<212>dna<213>artificialsequence<400>4ggcacgacccgctgaaagcttaggagaaattaactatgagaaaccatacttcagacacg59<210>5<211>50<212>dna<213>artificialsequence<400>5aacaggagtccaagctcagctaatttcagcttctacggtatttcttggtt50当前第1页1 2 3
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



