长链非编码RNA作为生物标志物在造影剂致急性肾损伤诊断中的应用的制作方法
 2021-02-02 18:02:06|
2021-02-02 18:02:06| 398|
398| 起点商标网
起点商标网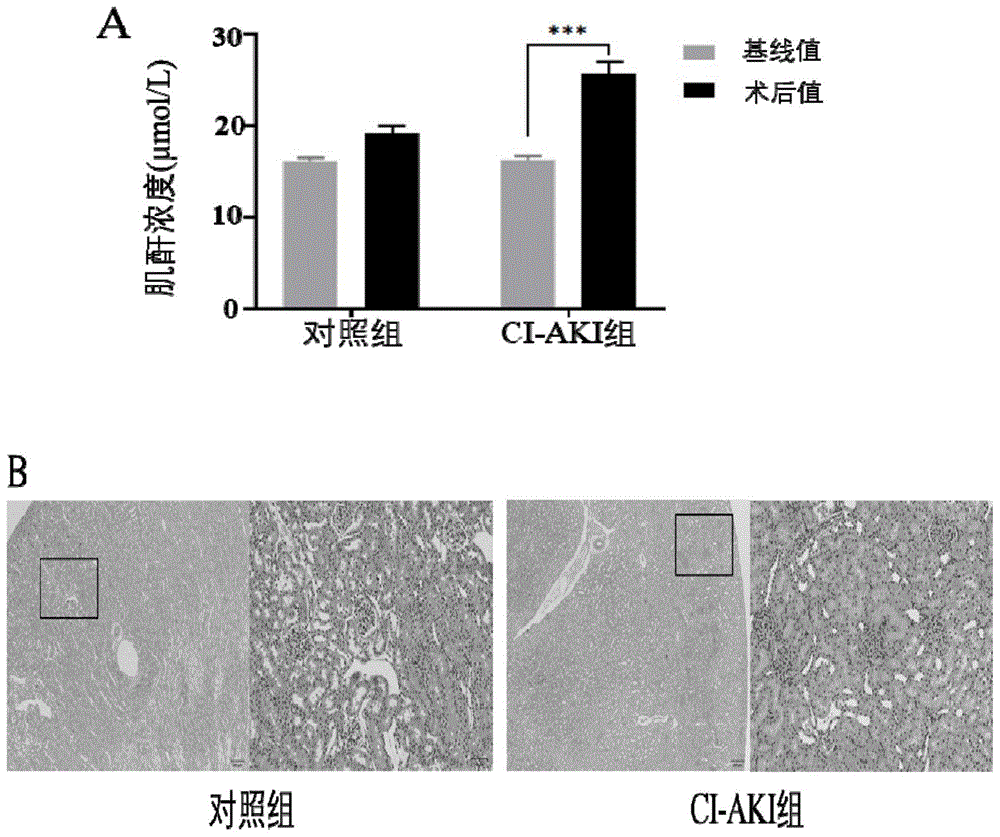
本发明属于生物医学领域,涉及两种作为长链非编码rna生物标志物在造影剂致急性肾损伤中诊断治疗的运用,所述两种lncrna分别为lnc-hilpda和lnc-prnd。
背景技术:
造影剂所致急性肾损伤(contrast-inducedacutekidneyinjury,ci-aki)是指血管内给予碘化造影剂后几天内的肾功能的下降,是心导管插入术常见的并发症。到目前为止,因造影剂而造成肾脏损害的患者预计达到数百万人,增加了巨大的疾病负担。因此,ci-aki的早期诊断十分重要。目前研究者广泛使用血清肌酐作为急性肾损伤的检测指标,kdigo工作组提出了“造影剂所致急性肾损伤”这一术语,并建议以使用造影剂后7日内出现的血清肌酐1.5倍的增加或者超出基线水平作为定义的依据;或以在使用造影剂后48小时内血清肌酐水平增加超出基线值至少0.3mg/dl(26.5μmol/l)为定义的依据;或以在使用造影剂后每小时尿量少于0.5ml/kg并持续6小时以上作为定义的依据。此定义里的血清肌酐的特异性较差,因为血清肌酐受体液转移和药物效应的影响而产生波动。另外血清肌酐的不敏感性和迟发性以及准确的新型生物标志物的缺失也给ci-aki的早期检测带来了很大的挑战。此外,由于ci-aki的关键分子机制和调控网络仍不清楚,应用生理盐水水化等经典预防策略的有效性存在争议和局限性,缺乏特定的靶向药物。因此,筛选潜在的生物标志物并揭示关键的分子发病机制可能是ci-aki的基石。
长链非编码rna(longnon-codingrnas,lncrnas)是一种含有200多个核苷酸,主要存在于真核生物中,不编码蛋白质的rna。它具有广泛的生物学过程,参与调控机体生长、发育和疾病发生等许多生命活动。由于其高度的特异性、体液的稳定性和可检测性,lncrnas可以作为预测各种疾病的新型生物标志物。目前在ci-aki领域中,lncrnas作为新型生物标志物的研究为数不多,亟需进一步地去研究和探讨。
技术实现要素:
本发明的目的在于克服上述现有技术的不足之处而提供长链非编码rna作为生物标志物在制备诊断造影剂致急性肾损伤试剂中的应用以及包含能检测本发明所述长链非编码rna的检测引物。
一方面本发明提供了长链非编码rna作为生物标志物在制备诊断造影剂致急性肾损伤试剂中的应用。
优选地,所述长链非编码rna包括lnc-hilpda或/和lnc-prnd。
另一方面发明提供了一种检测造影剂致急性肾损伤的产品,所述产品包括用于检测长链非编码rnalnc-hilpda或/和lnc-prnd的引物。
优选地,所述产品为诊断试剂或试剂盒。
优选地,所述诊断试剂或试剂盒包括对lnc-hilpda或/和lnc-prnd具有检测特异性的探针、基因芯片或pcr引物。
优选地,所述引物的核苷酸序列如seqidno:1~4所示,其中用于检测lnc-hilpda的引物为如seqidno:1~2所示的核苷酸序列,用于检测lnc-prnd的引物为如seqidno:3~4所示的核苷酸序列。
优选地,所述试剂盒还包括内参基团、cdna模板、taqmandna聚合酶、阳性对照液、阴性对照液、荧光染料、dntp。
优选地,所述阳性对照液是lnc-hilpda或/和lnc-prnd的标准溶液,阴性对照液为不含任何标准品的空白对照液。
本发明主要是通过四步筛选过程,包括:大鼠肾组织进行illumina二代测序和逆转录定量实时聚合酶链反应(reversetranscriptionquantitativereal-timepolymerasechainreaction,rt-qpcr)筛选、大鼠全血样本rt-qpcr筛选、鼠源-人源lncrna比对转换和临床ci-aki患者全血rt-qpcr验证。本发明人首次发现lnc-hilpda和lnc-prnd在ci-aki中表达差异显著(fc>2,p<0.01),相对于正常组显示高表达(图4),并且绘制受试者工作特征曲线来评估lnc-hilpda和lnc-prnd对ci-aki的预测效能,结果表明lnc-hilpda和lnc-prnd的auc分别为0.917和0.903,预测效能高。而且,lnc-hilpda的约登指数为0.74(敏感性74.36%,特异性100%),lnc-prndy的约登指数为0.67(敏感性79.49%,特异性87.18%)。当将两者结合预测,其约登指数为0.79(敏感性92.31%,特异性87.18%),表明筛选的lnc-hilpda和lnc-prnd可以作为ci-aki敏感、精准的新型生物标志物。基于发现的这两个lncrnas新型生物标志物,本专利旨在发明一种检测lnc-hilpda和lnc-prnd表达量的试剂盒,为ci-aki的诊断提供新的方向。
本发明的有益效果:
1.本发明筛选的lncrnas生物标志物具有体液稳定性:lncrnas在体内具有广泛的调节功能,适用于广泛的生物学过程和人类疾病,具有高特异性、体液稳定性和可检测性的特点。且相较于肌酐,其体液稳定性更高。
2.本发明首次发现lnc-hilpda和lnc-prnd在ci-aki患者全血中表达水平显著升高,且lnc-hilpda和lnc-prnd生物标志物预测效能高,构建检测lnc-hilpda和lnc-prnd的试剂盒应用于临床,可以快速、简便和准确地指导临床医师诊断ci-aki疾病。
3.本发明区别于以前利用高渗性造影剂建立的ci-aki大大鼠模型,主要是通过使用低渗性造影剂碘普罗胺建立新型低渗ci-aki大鼠模型,这可以更好模拟临床实践。
4.本发明在筛选lncrnas创新性使用了人鼠lncrnas同源转换技术,保证了筛选的lncrnas标志物在人鼠中具有高的序列同源性。
附图说明
图1:大鼠肾组织血样中的血清肌酐(scr)浓度(a图);ci-aki大鼠的肾组织病理学切片(b图)。
图2:ci-aki大鼠肾脏组织差异表达的lncrnas的热图(a图)和火山图(b图)。
图3:在ci-aki大鼠肾组织和全血中的5种候选lnc-rna的表达水平。
图4:在ci-aki患者全血中的5种lncrnas的表达水平。
图5:lnc-hilpda和lnc-prnd的受试者工作特征曲线及相应临界值,auc表示曲线下面积。
图6:具体步骤流程图。
具体实施方式
为了更加简洁明了的展示本发明的技术方案、目的和优点,下面结合具体实施例及其附图对本发明做进一步的详细描述。
实施例1、建立新型ci-aki大鼠模型
(1)20只大鼠随机分为ci-aki组和对照组,并脱水处理24小时,造影剂暴露前6小时,两组大鼠腹腔注射速尿15ml/kg;ci-aki组尾静脉给药低渗性造影剂碘普罗胺15ml/kg,对照组接受等量的生理盐水;
(2)所有大鼠暴露于造影剂后24小时处死,采集肾脏组织,在基线和给药24小时后分别从眼眶静脉采集血样;检测血样中的血清肌酐(scr)浓度。(结果如图1a)。图1a结果表明实验组大鼠的scr浓度平均相对升高了56.81%,表明实验组大鼠的scr浓度升高远超过基础值的1.5倍,而对照组的大鼠scr浓度相对只升高了17.99%。实验组大鼠符合ci-aki诊断标准。
(3)苏木精-伊红染色检测ci-aki的组织病理学改变:选取对照组3例,实验模型组3例,用10%中性福尔马林固定24小时,石蜡包埋,然后用切片机切取4mm厚的组织切片进行观察(结果如图1b)。结果示对照组肾组织基本正常,实验组肾组织表现为典型的急性肾损伤病理特征,包括严重的肾小管阻塞、广泛的肾小管细胞脱离和大量炎性细胞浸润等。表明ci-aki大鼠模型构建成功。
实施例2、二代测序技术检测ci-aki大鼠肾脏组织lncrnas谱
(1)提取和纯化rna:使用trizol试剂(invitrogen,carlsbad,ca)按照常规方法提取ci-aki大鼠肾脏组织中的总rna。用ribo-zerorrnaremoval试剂盒(epicentre)按照说明书去除核糖rna以纯化总rna。
(2)rna纯度和质量的分析:用nanodrop2000分光光度计(thermofisherscientific,wilmington,de)测定总rna的浓度和纯度,当od260/od280为1.8-2.2时,认为总rna的浓度是符合rna测序标准的。并用agilent2100生物分析仪和rna6000纳米试剂盒(agilent,santaclara,ca,usa))检查rna样品的质量。rna完整性为8或更高的样品被认为是合格的,合格的rna在-80℃下保存。
(3)采用illuminageneexpressionsamplepreparation试剂盒构建文库;
(4)测序:在illuminahiseqtm2000(中国科学院北京基因组研究所)平台中对构建的文库进行测序,检测lncrnas的表达情况。
(5)对测序结果进行分析,得到表达差异的lncrnas谱,差异表达lncrna的热图及火山图详见图2a-b。
根据图2的结果,ci-aki组中共有91个lncrnas表达量有差异性显著(标准为lncrnas在ci-aki组和对照组的表达量相差2倍以上,且p<0.05)。
实施例3、逆转录定量实时聚合酶链反应(reversetranscriptionquantitativereal-timepolymerasechainreaction,rt-qpcr)验证ci-aki大鼠肾脏组织和全血中14个lncrnas的表达情况。步骤如下:
(1)参照上述rna提取方法,提取大鼠肾组织rna,用primescripttmrtreagentkit(rr037)随机选择6mers和oligo-dt引物(takara,japan),将rna反向转录为cdna;
(2)针对上述14个lncrnas分别设计检测引物,以gapdh为内参,lncrnas和gapdh的引物序列如下表1。
(3)在tb
(4)根据监测的荧光信号绘制成曲线,并通过标准曲线对未知模板进行定量分析;
(5)其中发现在ci-aki大鼠肾组织有3个lncrna的差异表达值fc<2倍,未达到差异显著表达标准,因此排除这3个lncrna。
(6)在大鼠的全血样本中进一步采用rt-qpcr检测剩下的11个lncrnas表达情况。
根据图3结果发现,只有5个lncrnas表达水平达到fc>2倍和p<0.01的显著差异表达标准,即lnc-hilpda、lnc-prnd、lnc-cdk6、lnc-cdc42se1、neat1。
表1大鼠中相关的lncrna与gapdh的引物信息(转接下一页)
实施例4、鼠源-人源lncrna转换
(1)通过数据库找到鼠源lncrnas所在染色体位置及序列;
(2)进行鼠源lncrnas-人源dna比对,记录人源dna所在染色体位置及序列;
(3)通过人类lncrna收录网站找到人源dna对应的lncrna序列信息;
(4)将鼠源-人源lncrna进行对比并评分,符合标准即转换成功。
经过鼠源-人源lncrna转换后,发现在前面筛选出的具有表达差异的91个lncrnas中,有77个lncrnas无法在人类中找到同源性的lncrnas。因此大鼠肾组织中只有14个lncrnas是符合鼠源-人源lncrna转换,表明这14个lncrnas在人类中存在同源性的lncrnas,符合筛选的标准。
实施例5、在ci-aki患者全血中验证lncrnas表达情况。
(1)患者样本的选择:对2016年4月至2017年5月期间在广东省心血管病研究所心内科接受冠状动脉造影(cag,coronaryarteriography)或经皮冠状动脉介入治疗(pci,percutaneouscoronaryintervention)的398名患者进行筛选,在患者入院时和干预后72小时内测量scr。ci-aki的定义是72小时内scr的绝对增加≥0.5mg/dl(44.2μmol/l)或scr的相对增加≥25%。筛选入组的患者cag/pci术后ci-aki发生率为12.06%,即有48例ci-aki患者。其中只有39例全血样本符合要求。本研究最终采用39例ci-aki患者和39例对照组全血样本进行病例对照研究。
(2)参照上述的rna提取方法和rt-qpcr方法(相关引物序列信息如表2),进一步验证39例ci-aki患者的全血样本中的5个lncrnas表达情况。
表2人类中相关的lncrnas和gapdh的引物信息
根据图4结果表明,在暴露于cm后24-30小时,ci-aki患者的lnc-hilpad和lnc-prnd的表达水平明显高于对照组,具有显著性差异(lnc-hilpda的平均变化差异为:lnc-hilpda,4.475[2.753-6.198],p<0.001;lnc-prnd,5.794[3.744-7.845],p<0.001)。但是,lnc-cdk6、lnc-cdc42se1和neat1的表达水平均未达到fc>2倍和p<0.01的显著差异表达标准,因此在ci-aki患者全血中确定了表达差异显著的2个候选lncrnas:lnc-hilpda和lnc-prnd。
(3)对候选的lnc-hilpda和lnc-prnd进行鼠源-人源转换,lnc-hilpda和lnc-prnd在人类、家属和褐鼠中的序列信息结果如下:
通过对比它们在lnc-hilpda和lnc-prnd在人类、家属和褐鼠中的序列信息,发现这2个序候选lncrna在人鼠中有高同源性。
实施例6、绘制受试者工作特征曲线(receiveroperatingcharacteristiccurve,roccurve),验证候选lncrnas对ci-aki的预测效能。
结果如图6发现,lnc-hilpda和lnc-prnd其曲线下面积分别为0.917和0.903,预测效能高。而且,lnc-hilpda的约登指数为0.74(敏感性74.36%,特异性100%),lnc-prndy的约登指数为0.67(敏感性79.49%,特异性87.18%)。当将两者结合预测,其约登指数为0.79(敏感性92.31%,特异性87.18%)。因此,lnc-hilpda和lnc-prnd可以作为检测cag/pci患者ci-aki的新型有效生物标记物。
实施例7、结合上述筛选的lnc-hilpda和lnc-prnd生物标志物进一步制成lncrna诊断试剂盒,用于ci-aki的诊断
lncrna诊断试剂盒的制作主要基于rt-qpcr等技术。所述试剂盒包括可以用于标记rna样品的标记物,以及与所述标记物相对应的底物。此外,所述检测试剂盒还包括可扩增lnc-hilpdacdna和lnc-prndcdna的正向引物和反向引物,内参基团扩增正向引物和反向引物(lnc-hilpda的引物、lnc-prnd的引物和内参基团引物序列如表2),以及cdna模板、taqmandna聚合酶、阳性对照液、阴性对照液、荧光染料、dntp、以及其他盐离子等。其中阳性对照液是指lnc-hilpda和lnc-prnd的标准溶液,阴性对照液为不含任何标准品的空白对照液(如生理盐水)。所述试剂盒可用于检测全血中的lnc-hilpda和lnc-prnd的表达水平,从而更快速、简便、准确地诊断ci-aki疾病。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询



 商标分类
商标分类  商标转让
商标转让 



