抗细菌粘附的表面的制作方法
 2021-02-02 17:02:24|
2021-02-02 17:02:24| 266|
266| 起点商标网
起点商标网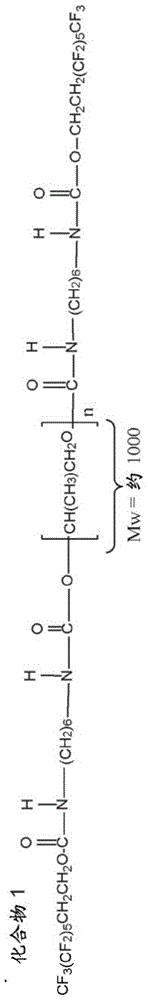
相关申请
这是基于2018年5月18日提交的美国临时申请no.62/673,490的优先权要求35u.s.c.§119的权益的专利合作条约申请,该临时申请全文经此引用并入本文。
本发明提出抗细菌粘附的表面。
背景技术:
细菌通常存在于两种类型的种群之一中:浮游型,其自由存在于散装溶液中,和固着型,其作为附着于表面或在生物膜的界限内的单元。生物膜附着于基底并由借助菌体附器(physicalappendage)和细胞外聚合物质共附着的许多细菌组成。细菌生物膜是大多数生物医学和工业系统中的生物污损的根本原因。
可植入或可插入医疗器材经常由于微生物定殖和粘附而阻塞。对于适于相对长期(即大约30天至大约12个月或更久)保持植入的医疗器材,这一问题特别普遍。微生物,如细菌,经常定殖在医疗器材上和其周围,并在附着于器材表面后,在由细胞外聚合物质,通常多糖组成的复合基质内增殖并形成聚集体。附着的微生物和相关联的细胞外聚合物质的集合体(mass)通常被称为生物膜或粘液(slime)。抗微生物剂难以渗透生物膜和杀死和/或抑制生物膜内的微生物的增殖。微生物在器材上和周围的定殖和生物膜屏障的合成最终导致该器材的结壳、阻塞、失效以及局部或全身感染。
增强系统的生物污损管理的一种方式是抑制或阻碍细菌粘附于所述系统内的表面。本发明提供可用于显著抑制细菌粘附于表面和控制系统的生物污损的方法和特定的组合物。
技术实现要素:
发明概述
本发明提出减少细菌粘附于表面的方法。
在一个方面中,本发明提出一种减少细菌粘附于聚合物表面的方法。该方法包括将基础聚合物与任何式(i)-(xxi)的化合物混合以形成聚合物表面,其中与由不存在所述化合物的情况下基础聚合物形成的表面相比将细菌粘附减少了至少50%(例如55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。
在另一个方面中,本发明提出一种减少细菌粘附于在流动条件下的聚合物表面的方法。该方法包括(i)提供由包含与任何式(i)-(xxi)的化合物混合的基础聚合物的混合物形成的聚合物表面,和(ii)使所述聚合物表面经受流动条件,其中与由不存在所述化合物的情况下基础聚合物形成的表面相比在流动条件下将细菌粘附减少了至少50%(例如55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。在特定实施方案中,流动条件包括具有1s-1至3500s-1(例如1s-1至15s-1、5s-1至100s-1、50s-1至500s-1、500s-1至1000s-1、或950s-1至3500s-1)的剪切速率的水溶液。
在一个方面中,本发明提出一种减少细菌粘附于在静态水性条件下的聚合物表面的方法。该方法包括(i)提供由包含与任何式(i)-(xxi)的化合物混合的基础聚合物的混合物形成的聚合物表面,和(ii)使所述聚合物表面经受静态水性条件,其中与由不存在所述化合物的情况下基础聚合物形成的表面相比在静态水性条件下将细菌粘附减少了至少50%(例如至少55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。
在上述方法的特定实施方案中,该方法包括在使聚合物表面与含蛋白质的水性混合物接触的同时减少细菌粘附。
在另一个方面中,本发明提出一种减少细菌粘附于暴露于环境空气的聚合物表面的方法。该方法包括(i)提供由包含与任何式(i)-(xxi)的化合物混合的基础聚合物的混合物形成的聚合物表面,和(ii)使所述聚合物表面经受环境空气条件,其中与由不存在所述化合物的情况下基础聚合物形成的表面相比在环境空气条件下将细菌粘附减少了至少50%(例如至少55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。
在一个方面中,本发明提出一种减少细菌粘附于血液驻留的聚合物表面的方法。该方法包括(i)提供由包含与任何式(i)-(xxi)的化合物混合的基础聚合物的混合物形成的聚合物表面,和(ii)使所述聚合物表面与血液接触,其中与由不存在所述化合物的情况下基础聚合物形成的表面相比在血液驻留条件下将细菌粘附减少了至少50%(例如至少55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。
在另一个方面中,本发明提出一种减少细菌粘附于尿液驻留的聚合物表面的方法。该方法包括(i)提供由包含与任何式(i)-(xxi)的化合物混合的基础聚合物的混合物形成的聚合物表面,和(ii)使所述聚合物表面与尿液接触,其中与由不存在所述化合物的情况下基础聚合物形成的表面相比在尿液驻留条件下将细菌粘附减少了至少50%(例如至少55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。
在一个方面中,本发明提出一种减少尿液驻留器材的聚合物表面上的细菌介导成盐的方法。该方法包括(i)提供由包含与任何式(i)-(xxi)的化合物混合的基础聚合物的混合物形成的聚合物表面,和(ii)使所述聚合物表面与尿液接触,其中与由不存在所述化合物的情况下基础聚合物形成的表面相比在尿液驻留条件下将盐沉积减少了至少20%(例如至少25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。
在另一个方面中,本发明提出一种减少聚合物表面上的细菌生物膜形成的方法。该方法包括提供由包含与任何式(i)-(xxi)的化合物混合的基础聚合物的混合物形成的聚合物表面,其中与由不存在所述化合物的情况下基础聚合物形成的表面相比将细菌生物膜形成减少了至少20%(例如至少25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。
在一个方面中,本发明提出一种减少聚合物表面上的细菌生物负荷的方法。该方法包括将基础聚合物与任何式(i)-(xxi)的化合物混合以形成聚合物表面,其中与由不存在所述化合物的情况下基础聚合物形成的表面相比将细菌生物负荷减少了至少20%(例如至少25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。
在另一个方面中,本发明提出一种降低表面上的细菌生长速率的方法,该方法包括(i)提供包括与任何式(i)-(xxi)的化合物混合的基础聚合物的表面,和(ii)使所述表面与抗微生物剂、防腐剂或消毒剂接触,其中与由不存在所述化合物的情况下基础聚合物形成的表面相比将细菌生长速率降低至少50%(例如至少55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。在特定实施方案中,在步骤(ii)之后至少6小时、12小时或24小时,与由不存在所述化合物的情况下基础聚合物形成的表面相比将细菌生长速率降低至少50%(例如至少55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。
在一个方面中,本发明提出一种减少表面上的细菌粘附的方法,该方法包括(i)提供包括与任何式(i)-(xxi)的化合物混合的基础聚合物的表面,和(ii)使所述表面与抗微生物剂、防腐剂或消毒剂接触,其中与由不存在所述化合物的情况下基础聚合物形成的表面相比将细菌粘附减少了至少50%(例如至少55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。在特定实施方案中,在步骤(ii)之后至少6小时、12小时或24小时,与由不存在所述化合物的情况下基础聚合物形成的表面相比将细菌粘附减少了至少50%(例如至少55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。
在另一个方面中,本发明提出一种降低聚合物表面上的生物膜形成速率的方法,该方法包括(i)提供包括与任何式(i)-(xxi)的化合物混合的基础聚合物的表面;和(ii)使所述表面与抗微生物剂、防腐剂或消毒剂接触,其中与由不存在所述化合物的情况下基础聚合物形成的表面相比将生物膜形成速率降低至少20%(例如至少25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。在特定实施方案中,在步骤(ii)之后至少6小时、12小时或24小时,与由不存在所述化合物的情况下基础聚合物形成的表面相比将生物膜形成速率降低至少20%(例如至少25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。
在任何上述方法的一个实施方案中,聚合物表面可在离体环境中。例如,聚合物表面可以是冷却塔、泵、热交换器、管道、供暖系统、燃料箱、制药设备、废水处理系统、水净化系统、冷却系统、生物反应器、食品加工系统、洗涤系统、金属加工液、造纸设备、船体或纺织品制造设备上的表面。
在上述方法中,聚合物表面可在体内环境中。
在上述方法中,聚合物表面可以是医疗器材的表面。
在上述方法中,医疗器材的聚合物表面可进一步包括填料、不透射线材料(例如硫酸钡)、着色剂或抗微生物剂。例如,医疗器材的聚合物表面可包括1%至45%(w/w)(例如1%至10%(w/w)、10%至30%(w/w)、20%至40%(w/w)、25%至45%(w/w)、20%至35%(w/w)、25%至40%(w/w)、30%至45%(w/w)、或35%至45%(w/w))的硫酸钡填料。在另一些实施方案中,医疗器材的聚合物表面不包括硫酸钡填料。当医疗器材包括抗微生物剂时,抗微生物剂可以是本文所述的任何抗微生物剂。
在一个方面中,本发明提出一种减少植入医疗器材的聚合物表面上的细菌粘附量的方法,该方法包括将医疗器材植入对象,其中所述医疗器材包括表面,所述表面包括(i)抗微生物剂和(ii)与任何式(i)-(xxi)的化合物混合的基础聚合物,其中在步骤(ii)之后至少24小时,与由不存在所述化合物的情况下基础聚合物形成的表面相比将细菌粘附量减少了至少50%。
在另一个方面中,本发明提出一种减少植入医疗器材的聚合物表面上的细菌粘附量的方法,该方法包括(i)向对象施用抗微生物剂;和(ii)将医疗器材植入对象,其中所述医疗器材包括表面,所述表面包括与任何式(i)-(xxi)的化合物混合的基础聚合物,其中在步骤(ii)之后至少6小时、12小时或24小时(例如36小时、48小时或72小时),与由不存在所述化合物的情况下基础聚合物形成的表面相比将细菌粘附量减少了至少50%(例如至少55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。
在另一个方面中,本发明提出一种减少植入医疗器材的聚合物表面上的细菌粘附量的方法,该方法包括(i)提供正在用抗微生物剂处理的对象;和(ii)将医疗器材植入所述对象,其中所述医疗器材包括表面,所述表面包括与任何式(i)-(xxi)的化合物混合的基础聚合物,其中在步骤(ii)之后至少6小时、12小时或24小时(例如36小时、48小时或72小时)小时,与由不存在所述化合物的情况下基础聚合物形成的表面相比将细菌粘附量减少了至少50%(例如至少55%、60%、65%、70%、75%、80%、85%、90%、95%或99%)。
在任何上述方法的一个实施方案中,聚合物表面是在基底上的涂层。在特定实施方案中,基底是医疗器材。医疗器材可部分或完全植入,或与对象身体接触有限时间(例如少于48小时、24小时、12小时或4小时)。
在任何上述方法的一个实施方案中,聚合物表面是医疗或生物技术产品上的表面,所述产品如创伤敷料、绷带、纱布、胶带、衬垫、海绵、血液氧合器、呼吸机、泵、管材、线材、电极、避孕器具、女性卫生用品、内窥镜、透析膜、导丝、流体收集袋、药物输送袋和管材、饲管、血袋和组织再生或细胞培养装置。
在上述方法中,聚合物表面可以是血液驻留的、尿液驻留的,和/或聚合物表面可与蛋白质环境接触。当聚合物表面是医疗器材的表面时,医疗器材可选自医疗仪器、牙科设备、牙植入物、药物输送装置、移植物、支架、起搏器、可植入复律器-除颤器、心脏再同步治疗装置、心血管装置引线、心室辅助装置和传动系统、心脏瓣膜、腔静脉滤器、血管内线圈、导管、导管接头、导管阀、静脉输送管线、静脉输送歧管、分流器、伤口引流器、引流导管、输液口、人工耳蜗、气管内导管、气管造口管、呼吸机呼吸管和线路、可植入传感器、眼科装置、矫形外科装置、牙植入物、牙周植入物、乳房植入物、阴茎植入物、颌面部植入物、整形植入物、瓣膜、矫正器(appliances)、脚手架(scaffolding)、缝合材料、针、疝气修补网、无张力阴道吊带和阴道悬带(sling)、假体神经装置(prostheticneurologicaldevices)和耳管。
在特定实施方案中,(i)聚合物表面在正在用低于标准方案的抗微生物剂进行治疗的对象体内,和(ii)聚合物表面和抗微生物剂各自的存在量一起足以与在不含所述化合物的聚合物表面存在下接受抗微生物处理的对象相比减少聚合物表面上的细菌粘附。在特定实施方案中,该对象正接受抗微生物治疗作为与医疗程序(例如医疗器材的植入)结合的抗感染预防措施,并通过在聚合物表面中包括所述化合物来降低感染的风险。
在某些实施方案中,(i)聚合物表面在正在用低于标准方案的抗微生物剂进行处理的对象体内,和(ii)聚合物表面和抗微生物剂各自的存在量一起足以与在不含所述化合物的聚合物表面存在下接受抗微生物处理的对象相比降低对象的感染风险。在特定实施方案中,该对象正接受抗微生物治疗作为与医疗程序(例如医疗器材的植入)结合的抗感染预防措施,并通过在聚合物表面中包括所述化合物来降低感染的风险。
在任何上述方法的特定实施方案中,聚合物表面是医用或非医用的制品、材料或装置的表面,其需要在一段时间内保持人类或动物健康安全的清洁无污染状态。该制品、材料或装置可以是本文所述的任何制品、材料或装置。
在一些实施方案中,抗微生物剂是银、青霉素g、青霉素v、甲氧西林、苯唑西林、氯唑西林、双氯西林、萘夫西林、氨苄青霉素、阿莫西林、羧苄青霉素、替卡西林、美洛西林、哌拉西林、阿洛西林、替莫西林、先锋霉素(cepalothin)、头孢匹林、头孢拉定、头孢噻啶、头孢唑啉、头孢孟多、头孢呋辛、头孢氨苄、头孢丙烯、头孢克洛、氯碳头孢、头孢西丁、头孢美唑(cefmatozole)、头孢噻肟、头孢唑肟、头孢曲松、头孢哌酮、头孢他啶、头孢克肟、头孢泊肟、头孢布烯、头孢地尼、头孢匹罗、头孢吡肟、bal5788、bal9141、亚胺培南、厄他培南、美罗培南、卡巴里路(astreonam)、克拉维酸、舒巴坦、他唑巴坦、链霉素、新霉素、卡那霉素、巴龙霉素、庆大霉素、妥布霉素、阿米卡星、奈替米星、壮观霉素、西索米星、地贝卡星(dibekalin)、异帕米星、四环素、金霉素、地美环素、米诺环素、土霉素、美他环素、多西环素、红霉素、阿奇霉素、克拉霉素、泰利霉素、abt-773、林可霉素、克林霉素、万古霉素、奥利万星、达巴万星、替考拉宁、奎奴普丁和达福普丁、对氨基苯磺酰胺(sulphanilamide)、对氨基苯甲酸、磺胺嘧啶、磺胺异恶唑、磺胺甲恶唑、磺胺杀利定、利奈唑胺、萘啶酸、奥索利酸、诺氟沙星、培氟沙星、依诺沙星、氧氟沙星、环丙沙星、替马沙星、洛美沙星、氟罗沙星、格帕沙星、司帕沙星、曲伐沙星、克林沙星、加替沙星、莫西沙星、吉米沙星、西他沙星、甲硝唑、达托霉素、加雷沙星、雷莫拉宁、法罗培南、多粘菌素、三氯生、利福平、米诺环素、替加环素、azd2563、甲氧苄氨嘧啶或其组合。
在一些实施方案中,消毒剂或防腐剂是甲醛、戊二醛、邻苯二甲醛、过氧化氢、过乙酸、过氧化氢/过乙酸组合、次氯酸钠、碘伏(例如聚维酮碘)、洗必泰、异丙醇、酚、季铵化合物或其组合。
在上述方法的任何实施方案中,所述化合物是(如附图中描绘的)化合物1-57的任一种,或所述化合物具有(如表1中所述的)smm1–smm16的任一种化学式。聚合物表面可包括0.05%(w/w)至15%(w/w)(例如0.1%(w/w)至15%(w/w)、0.5%(w/w)至15%(w/w)、1%(w/w)至15%(w/w)、0.1%(w/w)至5%(w/w)、0.5%(w/w)至5%(w/w)、或1%(w/w)至5%(w/w))的任何式(i)-(xxi)的化合物,例如化合物1-57的任一种和/或具有smm1–smm16的任一种化学式的化合物。
在上述方法的任何实施方案中,基础聚合物选自有机硅、聚烯烃、聚酯、聚碳酸酯、聚砜、聚酰胺、聚醚、聚脲、聚氨酯(pu)、聚醚酰亚胺、聚苯乙烯、纤维素聚合物、聚丙烯(pp)、聚乙烯(pe)、聚氯乙烯(pvc)、聚乙烯醇(pva)、聚乙烯基吡咯烷酮(pvp)、聚丙烯酰胺(paam)、聚环氧乙烷(peo)、聚(环氧乙烷)-嵌段-聚(环氧丙烷)-嵌段-聚(环氧乙烷)、聚(甲基丙烯酸羟乙酯)(polyhema)、聚对苯二甲酸乙二醇酯(pet)、聚对苯二甲酸丁二醇酯(pbt)、聚甲基丙烯酸甲酯(pmma)、聚醚醚酮(peek)、聚醚-嵌段-聚酰胺、环烯烃聚合物(cop)、环烯烃共聚物(coc)、甲基丙烯酸甲酯-丙烯腈-丁二烯-苯乙烯(mabs)、苯乙烯-丙烯腈(san)、苯乙烯-甲基丙烯酸甲酯(smma)、甲基丙烯酸酯-丁二烯-苯乙烯(mbs)、苯乙烯-丁二烯(sb)、聚(苯乙烯-嵌段-异丁烯-嵌段-苯乙烯)(sibs)和乙烯-乙酸乙烯酯(eva)。
在上述方法的任何实施方案中,基础聚合物是聚氨酯(pu)。pu基础聚合物可以是本文所述的任何pu基础聚合物。在上述方法的特定实施方案中,基础聚合物是有机硅(si)。有机硅基础聚合物可以是本文所述的任何有机硅基础聚合物。
在一个相关方面中,本发明提出一种医疗器材,其包括表面,所述表面包括(i)抗微生物剂和(ii)与任何式(i)-(xxi)的化合物混合的基础聚合物。在上述医疗器材的任何实施方案中,所述化合物是化合物1-57的任一种。在上述医疗器材的任何实施方案中,所述化合物具有smm1–smm16的任一种化学式。该表面可包括0.05%(w/w)至15%(w/w)(例如0.1%(w/w)至15%(w/w)、0.5%(w/w)至15%(w/w)、1%(w/w)至15%(w/w)、0.1%(w/w)至5%(w/w)、0.5%(w/w)至5%(w/w)、或1%(w/w)至5%(w/w))的任何式(i)-(xxi)的化合物,例如化合物1-57的任一种和/或具有smm1–smm16的任一种化学式的化合物。在上述医疗器材的一个实施方案中,基础聚合物选自上述方法中描述的或本文中描述的任何基础聚合物。在上述医疗器材的另一实施方案中,抗微生物剂选自上述方法中描述的或本文中描述的任何抗微生物剂。在特定实施方案中,医疗器材是可植入医疗器材(例如导管)或创伤敷料。医疗器材可含有进一步包括银、三氯生、利福平、米诺环素或其组合的本发明的聚合物表面。
在任何前述方面的一些实施方案中,任何式(i)-(xxi)的化合物具有smm1的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物40、45或54)。在另一些实施方案中,任何式(i)-(xxi)的化合物具有smm2的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物56)。在另一些实施方案中,任何式(i)-(xxi)的化合物具有smm3的化学式且基础聚合物是pu或si(其中所述化合物是化合物57)。在进一步实施方案中,任何式(i)-(xxi)的化合物具有smm4的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物2)。
在任何前述方面的另一些实施方案中,任何式(i)-(xxi)的化合物具有smm5的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物37或38)。在再一些实施方案中,任何式(i)-(xxi)的化合物具有smm6的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物11)。在进一步实施方案中,任何式(i)-(xxi)的化合物具有smm7的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物1)。在再进一步实施方案中,任何式(i)-(xxi)的化合物具有smm8的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物44)。在又一些实施方案中,任何式(i)-(xxi)的化合物具有smm9的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物21)。
任何前述方面的再进一步实施方案中,任何式(i)-(xxi)的化合物具有smm10的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物22或39)。在一些实施方案中,任何式(i)-(xxi)的化合物具有smm11的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物24)。在一些实施方案中,任何式(i)-(xxi)的化合物具有smm12的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物18)。在进一步实施方案中,任何式(i)-(xxi)的化合物具有smm13的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物20)。在另一些实施方案中,任何式(i)-(xxi)的化合物具有smm14的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物13)。
在任何前述方面的再进一步实施方案中,任何式(i)-(xxi)的化合物具有smm15的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物55)。在一些实施方案中,任何式(i)-(xxi)的化合物具有smm16的化学式且基础聚合物是pu或si(例如其中所述化合物是化合物43)。
对于任何式(i)-(xxi)的化合物的任一种,例如具有smm1–smm16的任一种化学式的化合物,ft可以是具有100da至1,500da的理论分子量的多氟有机基团。例如,ft是cf3(cf2)r(ch2ch2)p–,其中p是0或1,r是2-20,和cf3(cf2)s(ch2ch2o)χ,其中χ是0至10且s是1至20。ft也可以是chmf(3-m)(cf2)rch2ch2-或chmf(3-m)(cf2)s(ch2ch2o)χ-,其中m是0、1、2或3;χ是0至10的整数;r是2至20的整数;且s是1至20的整数。在另一些实施方案中,ft是1h,1h,2h,2h-全氟-1-癸醇;1h,1h,2h,2h-全氟-1-辛醇;1h,1h,5h-全氟-1-戊醇;或1h,1h-全氟-1-丁醇或其混合物。
在一些实施方案中,聚合物表面包括0.05%(w/w)至15%(w/w)(例如0.1%(w/w)至15%(w/w)、0.5%(w/w)至15%(w/w)、1%(w/w)至15%(w/w)、0.1%(w/w)至5%(w/w)、0.5%(w/w)至5%(w/w)、或1%(w/w)至5%(w/w))的任何式(i)-(xxi)的化合物,例如化合物1-57的任一种和/或具有smm1–smm16的任一种化学式的化合物。
在另一个方面中,本发明提出一种组合物,其包括与式(i)-(xxi)中的任一种的化合物混合的基础聚合物,其中所述组合物可用于本发明的方法(例如用于减少细菌粘附)。在特定实施方案中,该组合物包括0.05%(w/w)至15%(w/w)(例如0.1%(w/w)至15%(w/w)、0.5%(w/w)至15%(w/w)、1%(w/w)至15%(w/w)、0.1%(w/w)至5%(w/w)、0.5%(w/w)至5%(w/w)、或1%(w/w)至5%(w/w))的任何式(i)-(xxi)的化合物,例如化合物1-57的任一种和/或具有smm1–smm16的任一种化学式的化合物。
在本文中进一步描述了包括本发明的组合物的制品。在一些实施方案中,该制品是:(a)医疗器材,其选自医疗仪器、牙科设备、牙植入物、药物输送装置、移植物、支架、起搏器、可植入复律器-除颤器、心脏再同步治疗装置、心血管装置引线、心室辅助装置和传动系统、心脏瓣膜、腔静脉滤器、血管内线圈、导管、导管接头、导管阀、静脉输送管线、静脉输送歧管、分流器、伤口引流器、引流导管、输液口、人工耳蜗、气管内导管、气管造口管、呼吸机呼吸管和线路、可植入传感器、眼科装置、矫形外科装置、牙植入物、牙周植入物、乳房植入物、阴茎植入物、颌面部植入物、整形植入物、瓣膜、矫正器、脚手架、缝合材料、针、疝气修补网、无张力阴道吊带和阴道悬带、假体神经装置和耳管,或(b)创伤敷料、绷带、纱布、胶带、衬垫、海绵、血液氧合器、呼吸机、泵、管材、线材、电极、避孕器具、女性卫生用品、内窥镜、透析膜、导丝、流体收集袋、药物输送袋和管材、饲管、血袋、或组织再生或细胞培养装置。例如,该制品可以是导管、引流导管、支架、分流器、输液口、静脉输送管线、牙科设备、血袋、乳房植入物、阴茎植入物、伤口引流器、饲管、气管内导管、呼吸管、耳管、内窥镜或女性卫生用品。在特定实施方案中,本发明的制品是包含基础聚合物pu、si或聚氯乙烯的导管,其中基础聚合物与本发明的化合物混合。在某些实施方案中,本发明的制品是包含基础聚合物pu或si的输液口,其中基础聚合物与本发明的化合物混合。在另一些实施方案中,本发明的制品是包含基础聚合物pu、si或聚乙烯的支架,其中基础聚合物与本发明的化合物混合。在某些实施方案中,本发明的制品是包含基础聚合物pu或si的分流器,其中基础聚合物与本发明的化合物混合。在一些实施方案中,本发明的制品是包含基础聚合物pu、si、聚乙烯或聚氯乙烯的管(例如耳管、气管内导管、呼吸管或饲管),其中基础聚合物与本发明的化合物混合。在某些实施方案中,本发明的制品是包含基础聚合物pu的静脉输送管线,其中基础聚合物与本发明的化合物混合。在特定实施方案中,本发明的制品是包含基础聚合物聚氯乙烯、聚乙烯或聚丙烯的血袋,其中基础聚合物与本发明的化合物混合。在某些实施方案中,本发明的制品是包含基础聚合物si的假体植入物(例如乳房植入物或阴茎植入物),其中基础聚合物与本发明的化合物混合。在一些实施方案中,本发明的制品是包含基础聚合物pu或聚丙烯酸酯的正畸校准器或正畸矫正器,其中基础聚合物与本发明的化合物混合。在某些实施方案中,本发明的制品是包含基础聚合物pu、si或聚氯乙烯的伤口引流器,其中基础聚合物与本发明的化合物混合。在特定实施方案中,本发明的制品是包含基础聚合物pu或聚乙烯的内窥镜,其中基础聚合物与本发明的化合物混合。在某些实施方案中,本发明的制品是包含基础聚合物pu或si的女性卫生用品,其中基础聚合物与本发明的化合物混合。在一些实施方案中,本发明的制品是被基础聚合物(例如基础聚合物pu、si或聚乙烯)涂布的金属支架,其中基础聚合物在金属支架(例如冠状动脉、输尿管、肾、胆道、结肠直肠、食管、肺、尿道或血管支架)上的涂层中与本发明的化合物混合。在任何上述实施方案中,基础聚合物可与式(i)-(xxi)中的任一种的化合物混合,其中该组合物包括0.05%(w/w)至15%(w/w)(例如0.1%(w/w)至15%(w/w)、0.5%(w/w)至15%(w/w)、1%(w/w)至15%(w/w)、0.1%(w/w)至5%(w/w)、0.5%(w/w)至5%(w/w)、或1%(w/w)至5%(w/w))的任何式(i)-(xxi)的化合物,例如化合物1-57的任一种和/或具有smm1–smm16的任一种化学式的化合物。
在一个相关方面中、本发明提出一种形成本发明的制品的方法,其中该方法包括(i)制备包括与式(i)-(xxi)中的任一种的化合物混合的基础聚合物的组合物,和(ii)加工(例如挤出、注射成型、压延、混合、喷涂、浸涂、溶液纤维纺丝、静电纺丝或浇铸)所述组合物以形成或涂布所述制品。
定义
本文所用的术语“大约”是指所列数值的±20%的值。
本文所用的术语“添加剂”是指式(i)、(ii)、(iii)、(iv)、(v)、(vi)、(vii)、(viii)、(ix)、(x)、(xi)、(xii)、(xiii)、(xiv)、(xv)、(xvi)、(xvii)、(xviii)、(xix)、(xx)和(xxi)中任一种的多嵌段化合物(segmentedcompound)。某些添加剂可具有小于或等于20kda(例如小于或等于10kda)的理论分子量。某些添加剂可具有大于或等于200da(例如大于或等于300da)的理论分子量。添加剂的非限制性实例包括具有500至10,000道尔顿、500至9,000道尔顿、500至5,000道尔顿、1,000至10,000道尔顿、1,000至6,000道尔顿、或1,500至8,000道尔顿的理论分子量的那些。本领域技术人员会认识到,这些结构式代表理想化的理论结构。具体而言,链段以特定化学计量比反应而作为具有变化的链段比的分子分布提供添加剂。相应地,式(i)-(xxi)中的变量n是指链段的理论化学计量比。
术语“环境空气”是指未被空气传播的病原体污染的其自然状态的大气空气。
术语“细菌粘附”是指使细菌附着或粘附于其它细胞和表面的过程。粘附是定殖新的宿主或环境的重要步骤并对细菌致病机理作出贡献。本发明的方法可将聚合物表面上的细菌粘附减少至少50%,例如至少55%、60%、65%、70%、75%、80%、85%、90%、95%或99%。
本文所用的术语“基础聚合物”是指具有大于或等于20kda(例如大于或等于50kda、大于或等于75kda、大于或等于100kda、大于或等于150kda、或大于200kda)的理论分子量的聚合物。基础聚合物的非限制性实例包括:有机硅、聚烯烃、聚酯、聚碳酸酯、聚砜、聚酰胺、聚醚、聚脲、聚氨酯、聚醚酰亚胺、纤维素聚合物、和它们的共聚物和它们的共混物。基础聚合物的进一步非限制性实例包括聚丙烯(pp)、聚乙烯(pe)、聚氯乙烯(pvc)、聚乙烯醇(pva)、聚乙烯基吡咯烷酮(pvp)、聚丙烯酰胺(paam)、聚环氧乙烷(peo)、聚(环氧乙烷)-嵌段-聚(环氧丙烷)-嵌段-聚(环氧乙烷)、聚(甲基丙烯酸羟乙酯)(polyhema)、聚对苯二甲酸乙二醇酯(pet)、聚对苯二甲酸丁二醇酯(pbt)、聚甲基丙烯酸甲酯(pmma)、聚醚醚酮(peek)、聚醚-嵌段-聚酰胺(例如pebax)、环烯烃聚合物(cop)、环烯烃共聚物(coc)、甲基丙烯酸甲酯-丙烯腈-丁二烯-苯乙烯(mabs)、苯乙烯-丙烯腈(san)、苯乙烯-甲基丙烯酸甲酯(smma)、甲基丙烯酸酯-丁二烯-苯乙烯(mbs)、苯乙烯-丁二烯(sb)、聚(苯乙烯-嵌段-异丁烯-嵌段-苯乙烯)(sibs)、乙烯-乙酸乙烯酯(eva)、和它们的共聚物和它们的共混物。
术语“生物负荷”是指表面上的微生物污染或微生物负荷的程度或量。本发明的方法可将聚合物表面上的细菌生物负荷减少至少20%,例如至少25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或99%。
术语“生物膜”是指附着于表面,如医疗器材表面的微生物和由一种或多种附着的微生物产生的相关联的细胞外物质的集合体。细胞外物质通常是聚合物质并普遍包括复合多糖、蛋白质物质和糖肽的基质。本发明的方法可将聚合物表面上的细菌生物膜形成减少至少20%,例如至少25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或99%。
术语“血液驻留的聚合物表面”是指与血液接触的聚合物表面,例如,手术、医疗、诊断或牙科仪器、牙科设备或植入物、管材、线材、女性卫生用品、移植物(包括小直径<6mm)、支架(包括冠状动脉、输尿管、肾、胆道、结肠直肠、食管、肺、尿道和血管)、支架移植物(包括腹部血管、胸部血管和外周血管)、起搏器、可植入复律器-除颤器、心脏再同步治疗装置、心血管装置引线、心室辅助装置和传动系统、心脏瓣膜、腔静脉滤器、血管内线圈、导管、静脉输送管线和岐管、分流器(内部或外部,包括心室、房室、脑室腹膜和腰腹膜)、伤口引流器、引流导管、透析膜、输液口、人工耳蜗、气管内导管、气管造口管、呼吸机呼吸管和线路、导丝、流体收集袋、药物输送袋和管材、可植入传感器(例如血管内、经皮、颅内)、眼科装置(包括隐形眼镜)、矫形外科装置(包括髋关节植入物、膝盖植入物、肩部植入物、脊柱植入物(包括颈椎板系统、椎弓根螺钉系统、椎体间融合器、人工椎间盘和其它运动保留装置)。
本文所用的“c”是指链终止基团。示例性的链终止基团包括含有胺、醇或羧酸官能团的单官能基团。
本文所用的术语“碳酸酯键”是指碳酸的酯。
术语“流动条件”是指聚合物表面经受速率为至少0.1ml/min(例如0.2ml/min、0.3ml/min、0.4ml/min、0.5ml/min、0.6ml/min、0.7ml/min、0.8ml/min、0.9ml/min或1.0ml/min)的液体(例如尿液或血液)流动的条件。可如实施例12中所述在流动条件下进行测试和评估。
本文所用的术语“linkb”是指连接两个低聚物链段和表面活性基团的偶联链段。通常,linkb具有40至700的分子量。优选地,linkb可选自官能化二胺、二异氰酸酯、二磺酸、二羧酸、二酰氯和二醛,其中官能化组分具有仲官能团,经其连接表面活性基团。这样的仲官能团可以是酯、羧酸盐、磺酸盐、膦酸盐、硫醇、乙烯基类和伯胺或仲胺。低聚物链段中间体的末端羟基、胺或羧酸可与二胺反应以形成低聚酰胺;与二异氰酸酯反应以形成低聚氨酯、低聚脲或低聚酰胺;与二磺酸反应以形成低聚磺酸酯或低聚磺酰胺;与二羧酸反应以形成低聚酯或低聚酰胺;与二酰二氯反应以形成低聚酯或低聚酰胺;或与二甲醛(dicarboxaldehyde)反应以形成低聚缩醛或低聚亚胺。
本文所用的术语“具有两个末端羰基的连接基”是指具有56da至1,000da的分子量的二价基团,其中第一个化合价属于第一羰基,第二个化合价属于第二羰基。在这种连接基内,第一羰基键合至第一碳原子,第二羰基键合至第二碳原子。具有两个末端羰基的连接基可以是小分子二羰基(例如降冰片烯-二羰基、苯-二羰基、联苯-二羰基、亚烷基-二羰基(例如琥珀酰基、戊二酰基、己二酰基、庚二酰基、辛二酰基等))。
本文所用的术语“分子量”是指阿伏伽德罗数的组成相同的分子的理论重量。由于添加剂的制备可涉及生成一定的化合物分布,术语“分子量”是指由反应性成分的化学计量比决定的理想化结构的摩尔质量。因此,本文所用的术语“分子量”是指理论分子量。
本文所用的术语“低聚物连接基”是指含有2至50个互相键合的相同化学结构部分的二价基团。该化学结构部分可以是氧化亚烷基(例如氧化亚乙基)。
本文所用的术语“低聚物链段”是指相对较短长度的重复单元,通常小于大约50个单体单元和小于10,000道尔顿,但优选<7,000道尔顿和在一些实例中,<5,000道尔顿的理论分子量。在某些实施方案中,oligo选自聚氨酯、聚脲、聚酰胺、聚环氧烷、聚碳酸酯、聚酯、聚内酯、聚有机硅、聚醚砜、聚烯烃、聚乙烯基化合物、多肽、多糖,和醚和胺连接的它们的链段。
本文所用的术语“氧羰基键”是指将氧原子与羰基相连的键。在酯和氨酯中可找到示例性的氧羰基键。优选地,氧羰基键是在酯中的键。
本文所用的术语“聚砜”是指包括结构部分–芳基-so2-芳基-作为重复子单元的一类聚合物。聚砜包括但不限于聚醚砜和聚(氧基-1,4-亚苯基磺酰基-1,4-亚苯基氧基-1,4-亚苯基异丙叉基-1,4-亚苯基)。
术语“聚烯(polyalkylene)”当在本文中关于基础聚合物使用时,是指由具有2至4个碳原子的直链或支链亚烷基重复单元和/或任选的3至10个碳原子的环烯烃(例如降冰片烯或四环十二烯)组成的基础聚合物。各亚烷基重复单元任选被选自氯、甲氧基羰基、乙氧基羰基、羟乙氧基羰基、吡咯烷酮、羟基、乙酰氧基、氰基和苯基的一个取代基取代。聚烯基础聚合物的非限制性实例包括聚苯乙烯、环烯烃聚合物(cop)、环烯烃共聚物(coc)、甲基丙烯酸甲酯丙烯腈丁二烯苯乙烯(mabs)、苯乙烯丙烯腈(san)、苯乙烯甲基丙烯酸甲酯(smma)、甲基丙烯酸酯丁二烯苯乙烯(mbs)、苯乙烯丁二烯(sb),和聚丙烯酸酯(例如pmma)。
本文所用的术语“多氟有机基团”是指可任选被一个、两个或三个非连续氧原子插入的烃基团,其中2至59个氢原子被氟原子替代。多氟有机基团含有1至30个碳原子。多氟有机基团可含有直链烷基、支链烷基或芳基,或它们的任何组合。多氟有机基团(例如多氟烷基)可以是“多氟酰基”,其中多氟有机基团(例如多氟烷基)经其连接到分子其余部分上的碳原子被氧代取代。多氟有机基团(例如多氟烷基)内的烷基链可被最多9个氧原子插入,条件是多氟有机基团内的两个最靠近的氧原子被至少两个碳原子隔开。当多氟有机基团由任选被氧代取代和/或任选被氧原子插入的直链或支链烷基组成时,如本文中定义,这样的基团可被称为多氟烷基。一些多氟有机基团(例如多氟烷基)可具有100da至1,500da的理论分子量。多氟烷基可以是cf3(cf2)r(ch2ch2)p–,其中p是0或1,r是2至20,或cf3(cf2)s(ch2ch2o)χ–,其中χ是0至10,且s是1至20。或者,多氟烷基可以是chmf(3-m)(cf2)rch2ch2-或chmf(3-m)(cf2)s(ch2ch2o)χ-,其中m是0、1、2或3;χ是0至10;r是2至20的整数;且s是1至20的整数。在特定实施方案中,χ是0。在某些实施方案中,多氟烷基由1h,1h,2h,2h-全氟-1-癸醇;1h,1h,2h,2h-全氟-1-辛醇;1h,1h,5h-全氟-1-戊醇;或1h,1h,全氟-1-丁醇及其混合物形成。在另一些实施方案中,多氟烷基是全氟庚酰基。在再一些实施方案中,多氟烷基是(cf3)(cf2)5ch2ch2o-、(cf3)(cf2)7ch2ch2o-、(cf3)(cf2)5ch2ch2o-、chf2(cf2)3ch2o-、(cf3)(cf2)2ch2o-或(cf3)(cf2)5-。在再一些实施方案中,多氟烷基是(cf3)(cf2)5-,例如其中多氟烷基键合到酯基团的羰基上。在某些实施方案中,多氟有机基团是–(o)q-[c(=o)]r-(ch2)o(cf2)pcf3,其中q是0且r是1,或q是1且r是0;o是0至2;且p是0至10。
术语“生物膜形成速率”是指附着于表面的微生物质量(mass)的生长速率。与由不存在所述化合物的情况下基础聚合物形成的表面相比可将生物膜形成速率降低至少20%,例如至少25%、至少30%、至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%。
术语“成盐”是指在与尿液接触的表面上的盐形成和沉积,例如氯化钠、磷酸钙、磷酸镁铵等。
本文所用的术语“低于标准方案”是指在正接受抗微生物治疗的对象中使用本发明的表面和方法,其中给予该对象的抗微生物剂的量为包装说明书中原本指示的该抗微生物剂在治疗和/或预防感染中的用量的小于80%、70%、60%、50%、40%或30%(例如通过减少给药量、减少给药频率和/或减少对象经受抗微生物治疗的时间)。
术语“静态水性条件”是指聚合物表面经受水性环境,例如尿液或血液时的条件,其中不存在流动。
本文所用的术语“表面活性基团”是指键合到添加剂的链段上的疏水基团。例如,可安置表面活性基团以封闭添加剂的中心多嵌段聚合物部分的两个、三个或四个末端和/或可连接到表面改性剂的中心聚合物部分中存在的一个或多个侧链上。表面活性基团的实例包括但不限于聚二甲基硅氧烷、烃、多氟烷基、氟化聚醚及其组合。
术语“尿液驻留的聚合物表面”是指与尿液接触的聚合物表面,例如,导管(包括透析接入、导尿、诊断、药物输送等)和导管接头和阀(包括无针接头)。
本发明的其它特征和优点将从附图、详述和权利要求书中显而易见。
附图说明
图1a-1g显示以下的结构:图1a化合物1;图1b化合物2;图1c化合物3;图1d化合物4;图1e化合物5;图1f化合物6;和图1g化合物7。
图2a-2e显示以下的结构:图2a化合物8;图2b化合物9;图2c化合物10;图2d化合物11;和图2e化合物12。
图3a-3c显示以下的结构:图3a化合物13;图3b化合物14;和图3c化合物15。
图4a-4c显示以下的结构:图4a化合物16;图4b化合物17;和图4c化合物18。
图5a-5c显示以下的结构:图5a化合物19;图5b化合物20;和图5c化合物21。
图6a-6c显示以下的结构:图6a化合物22;图6b化合物23;和图6c化合物24。
图7a-7c显示以下的结构:图7a化合物25;图7b化合物26;和图7c化合物27。
图8a-8d显示以下的结构:图8a化合物28;图8b化合物29;图8c化合物30;和图8d化合物31。
图9a-9d显示以下的结构:图9a化合物32;图9b化合物33;图9c化合物34;和图9d化合物35。
图10a-10d显示以下的结构:图10a化合物36;图10b化合物37;图10c化合物38;和图10d化合物39。
图11a-11d显示以下的结构:图11a化合物40;图11b化合物42;图11c化合物43;和图11d化合物44。
图12a-12e显示以下的结构:图12a化合物45;图12b化合物46;图12c化合物47;图12d化合物48;和图12e化合物49。
图13a-13h显示以下的结构:图13a化合物50;图13b化合物51;图13c化合物52;图13d化合物53;图13e化合物54;图13f化合物55;图13g化合物56;和图13h化合物57。
图14a-14d是一系列图表,其显示在pbs中培养2小时后在聚氨酯(pu)棒上的细菌粘附。
图15a-15d是一系列图表,其显示在pbs中培养2小时后在pu棒上的细菌和真菌粘附。
图16是显示在pbs中培养2小时后在pu棒上的微生物粘附的概况的图表。
图17是显示在pbs中培养2小时后在pu棒上的微生物粘附的概况的图表。
图18是一系列sem图像,其显示在pbs中培养2小时后在含化合物41的pu棒上的金黄色葡萄球菌粘附。
图19a-19e是一系列图表,其显示在pbs中培养2小时后在pu棒上的细菌粘附。
图20是显示在pbs中培养2小时后在含化合物22的pu棒上的细菌粘附的概要图。
图21a-21b是一系列图表,其显示在人工尿液或人类汇集尿液中培养2小时后在具有化合物22的pu棒上的细菌粘附。
图22是显示在人类汇集尿液中培养12小时后在pu棒上的大肠杆菌粘附的图表。
图23是显示在人类汇集尿液中在含化合物22的pu棒上的长时间大肠杆菌粘附(最多7天)的图表。
图24是显示在人类汇集尿液和muellerhinton肉汤中在含化合物22的pu棒上的长时间大肠杆菌粘附(8天)的图表。
图25是一系列sem图像,其显示在人类汇集尿液中培养24小时后在含化合物22的pu棒上的大肠杆菌粘附。
图26是显示在临床尿液中培养24小时后在含化合物22的pu导管上的细菌粘附的图表。
图27是显示在人工尿液和人类汇集尿液中培养24小时后在含化合物22的pu导管上的细菌粘附的图表。
图28是描绘用于研究在流动条件下的细菌粘附的再循环流动系统的图。
图29是显示在人工尿液中在静态和流动条件下24小时后在含化合物22的pu导管上的细菌粘附的图表。
图30是描绘在体内兔子研究中测试的输尿管支架原型的图像。
图31是显示在24小时环丙沙星抗生素暴露后在muellerhinton肉汤中培养7天后在含化合物22的pu棒上的大肠杆菌粘附的图表。
图32a-32b是一系列图表,其显示在pbs中培养2小时后在si棒上的表皮葡萄球菌和金黄色葡萄球菌粘附。
图33a-33b是一系列图表,其显示在人类汇集尿液中培养2小时后在si棒上的尿路病原体粘附。
图34a-34b是一系列图表,其显示在人类汇集尿液中培养最多至24小时后在si棒上的铜绿假单胞菌和粪肠球菌粘附。
图35是显示在人类汇集尿液中培养最多至3天后在si棒上的大肠杆菌粘附的图表。
图36是显示在含化合物43的si棒上的细菌粘附的概要图。
图37是显示在稀释血浆或血清中在pu棒上的金黄色葡萄球菌粘附的图表。
图38是显示在不同流动/剪切速率下在含化合物22的pu导管上的大肠杆菌粘附的图表。
图39是描绘用于研究在流动条件下的细菌粘附的非循环流动系统的图。
图40是显示经au流动7天在含化合物22的pu导管上的大肠杆菌粘附的图表。
图41是显示如目视和通过结晶紫染色可见,经au流动7天在pu导管上的生物污损和大肠杆菌生物膜形成的照片。
图42是一系列sem图像,其显示经au流动7天在pu导管上的大肠杆菌生物膜。
图43是显示在流动24小时后在含化合物22的pu导管上的各种细菌物类的粘附的图表。
图44是一系列图表,其显示在人类汇集尿液或人工尿液中培养24小时后与商业输尿管支架管相比在pu管上的尿路病原体粘附。
图45是显示与商业输尿管支架管相比在流动条件下在pu管上的大肠杆菌粘附的图表。
图46是显示在含奇异变形杆菌(p.mirabilis)细菌的人工尿液中培养2周后在含化合物22的pu管上的结壳沉积物的质量的图表。
图47是一系列图表,其显示在pbs中培养2小时后在pu棒上的金黄色葡萄球菌和表皮葡萄球菌粘附。
图48是显示在人类汇集尿液中培养24小时后在pu棒上的大肠杆菌粘附的图表。
图49是一系列图表,其显示在含和不含不透射线的baso4填料的pu棒上的细菌粘附。
图50是一系列图表,其显示在pbs或人类汇集尿液中培养2小时后在含化合物54和55的pu棒上的细菌粘附。
发明详述
本发明提出由与本发明的添加剂混合的基础聚合物形成的表面。该表面可抗细菌粘附。本发明的表面可施加到:(a)体内或体外、永久或短时间植入或紧靠人类或动物组织或体液的任何医疗器材或材料,和(b)需要在一段时间内保持人类或动物健康安全的清洁无污染状态的任何有用的制品、材料或装置,医用或非医用的。在这些医疗和非医疗应用中,已知的是,可能发生不希望的污损现象,这可能危害在易污染的制品、设备或环境中加工、运输或储存的受波及器材、设备或材料的患者、使用者或消费者。这样的污损现象包括生物膜发展和细菌菌落发展。这样的污损可造成刺激和溶胀、过敏反应、毒性反应、中毒或感染,以及制品的功能变差或破坏。
本发明的制品可至少部分由基础聚合物使用需要高温加工、熔体加工或溶液加工的方法(例如挤出、注射成型、压延、混合、喷涂、浸涂、溶液纤维纺丝、静电纺丝或浇铸)制备。溶液纺丝可以例如在100℃下进行。在一些实施方案中,pu和pvc在180℃下加工。在另一实例中,coc和cop通常需要大于200℃(例如大于或等于250℃或大于或等于300℃)的加工温度。本文所述的添加剂可以是热稳定的(例如可具有大于或等于200℃(例如大于或等于250℃或大于或等于300℃)的热降解温度。相应地,本发明的制品可由基础聚合物和添加剂的混合物在大于200℃(例如大于或等于250℃或大于或等于300℃)的温度下形成。
本发明的制品可由基础聚合物和添加剂的混合物制成(例如通过高温加工、熔体加工或溶液加工)。可在基础聚合物的熔体加工前加入所述添加剂以制造本发明的制品。为了通过熔体加工形成混合物,可将添加剂例如与粒化或粉化的聚合物混合,然后通过已知方法熔体加工,例如模塑或熔体挤出。添加剂可在熔融条件下直接与聚合物混合或可首先在brabender混合机中以添加剂/聚合物混合物的浓缩物形式与聚合物预混。如果需要,可将添加剂的有机溶液与粉化或粒化的基础聚合物混合,然后蒸发溶剂,然后熔体加工。或者,可刚好在挤出成所需形状之前将添加剂注入熔融聚合物料流中以形成混合物。
在熔体加工后,可进行退火步骤以增强基础聚合物中的本文所述的有利性质的展现。除退火步骤外或代替退火步骤,经熔体加工的组合也可在两个加热辊之间压花,其中一个辊或两个辊都可图案化。退火步骤通常在该聚合物的熔融温度以下(例如在大约50℃至大约220℃)进行。
也可通过溶液加工形成混合物,如涂布、微印刷、乳液加工、点印刷、微图案化、纤维纺丝、溶剂吹塑、电喷雾和静电纺丝。电喷涂可以例如通过将该混合物溶解在溶剂中并电喷雾以形成微珠和纳米珠,或将该溶液装载到注射器中并注射到固定的收集板上进行。在针与收集表面之间,可保持电势差。静电纺丝可以例如通过将该混合物溶解在溶剂中并将该溶液以特定速率从注射器注射到以特定旋转速度旋转的圆柱形心轴上以获得对齐的纤维,或注射到固定收集表面上以获得未对齐的纤维而进行。在针与对齐和无规纤维的收集表面之间可保持电势差。
添加剂以足以实现特定应用所需的表面性质的量添加到基础聚合物中。通常,所用添加剂的量在混合物的0.05-15%(w/w)的范围内。可凭经验确定该量并可视必要或需要调节该量以实现所需表面性质而不损害基础聚合物的其它物理性质。
基础聚合物
本发明的方法和制品中所用的基础聚合物可以是有机硅、聚烯烃、聚酯、聚碳酸酯、聚砜、聚酰胺、聚醚、聚脲、聚氨酯(pu,例如carbothane85a(cb))、聚醚酰亚胺或纤维素聚合物、或它们的共聚物或它们的共混物(例如聚丙烯(pp)、聚乙烯(pe)、聚氯乙烯(pvc)、聚乙烯醇(pva)、聚乙烯基吡咯烷酮(pvp)、聚丙烯酰胺(paam)、聚环氧乙烷(peo)、聚(环氧乙烷)-嵌段-聚(环氧丙烷)-嵌段-聚(环氧乙烷)、聚(甲基丙烯酸羟乙酯)(polyhema)、聚对苯二甲酸乙二醇酯(pet)、聚对苯二甲酸丁二醇酯(pbt)、聚甲基丙烯酸甲酯(pmma)、聚醚醚酮(peek)、环烯烃聚合物(cop)、环烯烃共聚物(coc)、甲基丙烯酸甲酯丙烯腈丁二烯苯乙烯(mabs)、苯乙烯丙烯腈(san)、苯乙烯甲基丙烯酸甲酯(smma)、甲基丙烯酸酯丁二烯苯乙烯(mbs)、苯乙烯丁二烯(sb)、聚(苯乙烯-嵌段-异丁烯-嵌段-苯乙烯)(sibs)、乙烯-乙酸乙烯酯(eva)、或它们的共聚物或它们的共混物)。本发明的器材和涂层中所用的基础聚合物可以是热塑性聚合物(例如热塑性聚氨酯)。本发明的器材和涂层的基础聚合物也可是经交联的。
例如,本发明的方法和制品中所用的基础聚合物可以是热塑性聚氨酯。热塑性聚氨酯包含许多不同类型的材料,以及不同硬度的材料。聚氨酯的初始选择可基于该材料的性能。可得到具有60a至85d的肖氏硬度的热塑性聚氨酯。热塑性聚氨酯以各种不同的化学结构存在,根据基础聚合物如何使用和使用多久来进行选择。
可用于本发明的方法和制品的聚氨酯包括,但不限于,聚醚基聚氨酯(例如
可包括在本发明的混合物中的另外的示例性聚(碳酸酯氨酯)包括但不限于
可用于本发明的混合物的其它基础聚合物包括有机硅,如医疗等级有机硅弹性体。可用的有机硅聚合物的一些实例是来自nusiltm的med-4780、med-4765、med3-6320、med-6340、med-6345、med-6350。另一实例是
在另一实例中,本发明的混合物可与聚乙烯基础聚合物一起使用,例如用于胆道或输尿管支架。本发明的混合物也可与pvc基础聚合物一起使用,例如用于导尿管或医用管材。在进一步实例中,本发明的混合物可与聚(苯乙烯-嵌段-异丁烯-嵌段-苯乙烯)(sibs)基础聚合物一起使用,例如用于输尿管支架。聚酰胺基础聚合物(例如尼龙6、尼龙6-6、尼龙11、尼龙12、聚醚嵌段酰胺(peba)、
添加剂
本发明的制品、器材和表面中所用的添加剂可通过下示式(i)、(ii)、(iii)、(iv)、(v)、(vi)、(vii)、(viii)、(ix)、(x)、(xi)、(xii)、(xiii)、(xiv)、(xv)、(xvi)、(xvii)、(xviii)、(xix)、(xx)和(xxi)任一种的结构描述。
(1)式(i):
ft–[b–a]n–b–ft
(i)
其中
(i)a包括氢化聚丁二烯、聚(碳酸(2,2-二甲基)-1,3-亚丙酯)、聚丁二烯、聚(二乙二醇)己二酸酯、聚(碳酸六亚甲基酯)、聚(乙烯-共聚-丁烯)、(新戊二醇-邻苯二甲酸酐)聚酯、(二乙二醇-邻苯二甲酸酐)聚酯、(1,6-己二醇-邻苯二甲酸酐)聚酯或双酚a乙氧基化物;
(ii)b是包括氨酯的链段;且
(iii)ft是多氟有机基团,且
(iv)n是1至10的整数。
(2)式(ii):
ft–[b–a]n–b–ft
(ii)
其中
(i)b包括氨酯;
(ii)a包括聚环氧丙烷、聚环氧乙烷或聚氧化四亚甲基;
(iii)ft是多氟有机基团;且
(iv)n是1至10的整数。
(3)式(iii)或式(iv):
其中
(i)a是含有醚键、酯键、碳酸酯键或聚烯并具有500至3,500道尔顿(例如500至2,000道尔顿、1,000至2,000道尔顿、或1,000至3,000道尔顿)的理论分子量的低聚物链段;
(ii)b是包括异氰脲酸酯三聚物或缩二脲三聚物的链段;b’,当存在时,是包括氨酯的链段;
(iii)各ft是多氟有机基团;且
(iv)n是0至10的整数。
(4)式(v):
ft–[b–a]n–b–ft
(v)
其中
(i)a是包括聚环氧丙烷、聚环氧乙烷或聚氧化四亚甲基并具有500至3,000道尔顿(例如500至2,000道尔顿、1,000至2,000道尔顿、或1,000至3,000道尔顿)的理论分子量的低聚物链段;
(ii)b是由二异氰酸酯形成的链段;
(iii)ft是多氟有机基团;且
(iv)n是1至10的整数。
(5)式(vi):
其中
(i)a是包括聚环氧乙烷、聚环氧丙烷、聚氧化四亚甲基或其混合物并具有500至3,000道尔顿(例如500至2,000道尔顿、1,000至2,000道尔顿、或1,000至3,000道尔顿)的理论分子量的低聚物链段;
(ii)b是包括异氰脲酸酯三聚物或缩二脲三聚物的链段;
(iii)ft是多氟有机基团;且
(iv)n是0至10的整数。
(6)式(vii):
ft–[b–a]n–b–ft
(vii)
其中
(i)a是具有500至3,000道尔顿(例如500至2,000道尔顿、1,000至2,000道尔顿、或1,000至3,000道尔顿)的理论分子量的聚碳酸酯多元醇;
(ii)b是由二异氰酸酯形成的链段;
(iii)ft是多氟有机基团;且
(iv)n是1至10的整数。
(7)式(viii):
其中
(i)a是包括具有500至3,000道尔顿(例如500至2,000道尔顿、1,000至2,000道尔顿、或1,000至3,000道尔顿)的理论分子量的聚碳酸酯多元醇的低聚物链段;
(ii)b是包括异氰脲酸酯三聚物或缩二脲三聚物的链段;
(iii)ft是多氟有机基团;且
(iv)n是0至10的整数。
(8)式(ix):
其中
(i)a包括选自聚环氧丙烷、聚环氧乙烷、聚氧化四亚甲基或其混合物的第一嵌段链段和包括聚硅氧烷或聚二甲基硅氧烷的第二嵌段链段,其中a具有1,000至5,000道尔顿(例如1,000至3,000道尔顿、2,000至5,000道尔顿、或2,500至5,000道尔顿)的理论分子量;
(ii)b是包括异氰脲酸酯三聚物或缩二脲三聚物的链段;
(iii)ft是多氟有机基团;且
(iv)n是0至10的整数。
(9)式(x):
ft–[b–a]n–b–ft
(x)
其中
(i)a是选自氢化聚丁二烯(例如hlbh)、聚丁二烯(例如lbhp)、氢化聚异戊二烯(例如hhtpi)、聚硅氧烷-聚乙二醇嵌段共聚物和聚苯乙烯的链段并具有750至3,500道尔顿(例如750至2,000道尔顿、1,000至2,500道尔顿、或1,000至3,500道尔顿)的理论分子量;
(ii)b是由二异氰酸酯形成的链段;
(iii)ft是多氟有机基团;且
(iv)n是1至10的整数。
(10)式(xi):
其中
(i)a是氢化聚丁二烯(例如hlbh)、聚丁二烯(例如lbhp)、氢化聚异戊二烯(例如hhtpi)或聚苯乙烯并具有750至3,500道尔顿(例如750至2,000道尔顿、1,000至2,500道尔顿、或1,000至3,500道尔顿)的理论分子量;
(ii)b是包括异氰脲酸酯三聚物或缩二脲三聚物的链段;
(iii)ft是多氟有机基团;且
(iv)n是0至10的整数。
(11)式(xii):
其中
(i)a是具有500至3,500道尔顿(例如500至2,000道尔顿、1,000至2,000道尔顿、或1,000至3,000道尔顿)的理论分子量的聚酯;
(ii)b是包括异氰脲酸酯三聚物或缩二脲三聚物的链段;
(iii)ft是多氟有机基团;且
(iv)n是0至10的整数。
(12)式(xiii):
ft–a–ft
(xiii)
其中ft是多氟有机基团和a是低聚物链段。
(13)式(xiv):
其中
(i)ft是共价连接到linkb上的多氟有机基团;
(ii)c是链终止基团;
(iii)a是低聚物链段;
(iv)linkb是偶联链段;且
(v)a是大于0的整数。
(14)式(xv):
其中
(i)各ft独立地为选自聚二甲基硅氧烷、烃和多氟有机基团及其组合的表面活性基团(例如各ft独立地为多氟有机基团);
(ii)x1是h、ch3或ch2ch3;
(iii)x2和x3各自独立地为h、ch3、ch2ch3或ft;
(iv)l1和l2各自独立地为键、低聚物连接基或具有两个末端羰基的连接基;且
(v)n是5至50的整数。
(15)式(xvi):
其中
(i)各ft独立地为表面活性基团(例如多氟有机基团);
(ii)x1、x2和x3各自独立地为h、ch3、ch2ch3或ft;
(iii)l1和l2各自独立地为键、低聚物连接基、具有两个末端羰基的连接基,或由二异氰酸酯形成;且
(iv)n1和n2各自独立地为5至50的整数。
(16)式(xvii):
g–am–[b–a]n–b–g
(xvii)
其中
(i)各a包含氢化聚丁二烯、聚(碳酸(2,2-二甲基)-1,3-亚丙酯)、聚丁二烯、聚(二乙二醇)己二酸酯、聚(碳酸六亚甲基酯)、聚(乙烯-共聚-丁烯)、(二乙二醇-邻苯二甲酸酐)聚酯、(1,6-己二醇-邻苯二甲酸酐)聚酯、(新戊二醇-邻苯二甲酸酐)聚酯、聚硅氧烷或双酚a乙氧基化物;
(ii)各b独立地为键、低聚物连接基或具有两个末端羰基的连接基;
(iii)各g是h或多氟有机基团,条件是至少一个g是多氟有机基团;
(iv)n是1至10的整数;且
(v)m是0或1。
(17)式(xviii):
ft–oc(o)o–b–oc(o)o–[a–oc(o)o–b]n–oc(o)o–ft
(xviii)
其中
a包含软链段并经碳酸酯键共价键合到b上;
(ii)b包含聚环氧烷或由下式描述的结构部分:
并经碳酸酯键共价键合到a上;且
(iii)ft是包含多氟有机基团的表面活性基团,其中ft经碳酸酯键共价键合到b上;且
(iv)n是1至10的整数。
(18)式(xix):
ft–oc(o)o–(ch2ch2o)m–oc(o)o–[a–oc(o)o–(ch2ch2o)m]n–oc(o)o–ft
(xix)
其中
(i)a包含软链段;
(ii)ft是包含多氟有机基团的表面活性基团;
(iii)m是2至4的整数;且
(iv)n是1至10的整数。
(19)式(xx):
其中
(i)ft是多氟有机基团;
(ii)x1和x2各自独立地为h、ch3或ch2ch3;
(iii)b包含聚环氧烷;且
(v)n是5至100的整数。
(20)式(xxi):
其中
(i)各ft是多氟有机基团;
(ii)x1和x2各自独立地为h、ch3或ch2ch3;
(iii)b包含聚环氧烷;且
(iv)n1和n2各自独立地为5至50的整数。
式(i)的添加剂可包括由二异氰酸酯(例如3-异氰酸根合甲基-3,5,5-三甲基-环己基异氰酸酯;4,4’-亚甲基双(环己基异氰酸酯);4,4’-亚甲基双(苯基异氰酸酯);甲苯-2,4-二异氰酸酯;间-四甲基苯二甲基二异氰酸酯;或己二异氰酸酯)形成的b。变量n可以是1或2。本发明的制品、器材和表面可包括含有基础聚合物和式(i)的添加剂的表面。
式(iii)和(iv)的添加剂可包括含有氢化聚丁二烯(hlbh)、聚(碳酸(2,2-二甲基)-1,3-亚丙酯)(pcn)、聚丁二烯(lbhp)、聚氧化四亚甲基(ptmo)、聚环氧丙烷(ppo)、(二乙二醇-邻苯二甲酸酐)聚酯(pdp)、氢化聚异戊二烯(hhtpi)、聚(碳酸六亚甲基酯)、聚(碳酸(2-丁基-2-乙基)-1,3-亚丙酯)或羟基封端的聚二甲基硅氧烷(c22)的低聚物链段作为a。在式(iii)和(iv)的添加剂中,b通过使三异氰酸酯(例如己二异氰酸酯(hdi)缩二脲三聚物、异佛尔酮二异氰酸酯(ipdi)三聚物或己二异氰酸酯(hdi)三聚物)与包括低聚物链段a的二醇反应形成。本发明的制品、器材和表面可包括含有基础聚合物和式(iii)的添加剂的表面。本发明的制品、器材和表面可包括含有基础聚合物和式(iv)的添加剂的表面。
在式(v)的添加剂中,b可以是由3-异氰酸根合甲基-3,5,5-三甲基-环己基异氰酸酯;4,4’-亚甲基双(环己基异氰酸酯);4,4’-亚甲基双(苯基异氰酸酯);甲苯-2,4-二异氰酸酯;间-四甲基苯二甲基二异氰酸酯;和己二异氰酸酯形成的链段。在式(v)的添加剂中,链段a可以是聚(环氧乙烷)-嵌段-聚(环氧丙烷)-嵌段-聚(环氧乙烷)。变量n可以是1至3的整数。本发明的制品、器材和表面可包括含有基础聚合物和式(v)的添加剂的表面。
在式(vi)的添加剂中,b是通过使三异氰酸酯与a的二醇反应形成的链段。该三异氰酸酯可以是己二异氰酸酯(hdi)缩二脲三聚物、异佛尔酮二异氰酸酯(ipdi)三聚物或己二异氰酸酯(hdi)三聚物。在式(vi)的添加剂中,链段a可以是聚(环氧乙烷)-嵌段-聚(环氧丙烷)-嵌段-聚(环氧乙烷)。变量n可以是0、1、2或3。本发明的制品、器材和表面可包括含有基础聚合物和式(vi)的添加剂的表面。
在式(vii)的添加剂中,a可包括聚(碳酸(2,2-二甲基)-1,3-亚丙酯)(pcn)。b可以是由3-异氰酸根合甲基-3,5,5-三甲基-环己基异氰酸酯;4,4’-亚甲基双(环己基异氰酸酯);4,4’-亚甲基双(苯基异氰酸酯);甲苯-2,4-二异氰酸酯;间-四甲基苯二甲基二异氰酸酯;和己二异氰酸酯形成的链段。变量n可以是1、2或3。本发明的制品、器材和表面可包括含有基础聚合物和式(vii)的添加剂的表面。
在式(viii)的添加剂中,b是通过使三异氰酸酯与a(例如低聚物链段)的二醇反应形成的链段。该三异氰酸酯可以是己二异氰酸酯(hdi)缩二脲三聚物、异佛尔酮二异氰酸酯(ipdi)三聚物或己二异氰酸酯(hdi)三聚物。链段a可包括聚(碳酸(2,2-二甲基)-1,3-亚丙酯)(pcn)或聚(碳酸六亚甲基酯)(phcn)。变量n可以是0、1、2或3。本发明的制品、器材和表面可包括含有基础聚合物和式(viii)的添加剂的表面。
在式(ix)的添加剂中,b是通过使三异氰酸酯与a的二醇反应形成的链段。在链段a中,第一嵌段链段和第二嵌段链段的数目可为任何整数或非整数以提供该链段的近似理论分子量。链段a可包括聚环氧丙烷和聚二甲基硅氧烷。该三异氰酸酯可以是己二异氰酸酯(hdi)缩二脲三聚物、异佛尔酮二异氰酸酯(ipdi)三聚物或己二异氰酸酯(hdi)三聚物。变量n可以是0、1、2或3。本发明的制品、器材和表面可包括含有基础聚合物和式(ix)的添加剂的表面。
在式(x)的添加剂中,b是由二异氰酸酯形成的链段。链段a可包括氢化聚丁二烯。或者,链段a可包括聚硅氧烷-聚乙二醇嵌段共聚物(例如peg-pdms-peg)。链段b可由3-异氰酸根合甲基-3,5,5-三甲基-环己基异氰酸酯;4,4’-亚甲基双(环己基异氰酸酯);4,4’-亚甲基双(苯基异氰酸酯);甲苯-2,4-二异氰酸酯;间-四甲基苯二甲基二异氰酸酯;和己二异氰酸酯形成。变量n可以是1、2或3。本发明的制品、器材和表面可包括含有基础聚合物和式(x)的添加剂的表面。
在式(xi)的添加剂中,b是通过使三异氰酸酯与a的二醇反应形成的链段。链段a可以是氢化聚丁二烯(hlbh)或氢化聚异戊二烯(hhtpi)。该三异氰酸酯可以是己二异氰酸酯(hdi)缩二脲三聚物、异佛尔酮二异氰酸酯(ipdi)三聚物或己二异氰酸酯(hdi)三聚物。变量n可以是0、1、2或3。本发明的制品、器材和表面可包括含有基础聚合物和式(xi)的添加剂的表面。
在式(xii)的添加剂中,b是通过使三异氰酸酯与a(例如聚酯)的二醇反应形成的链段。链段a可以是聚(二乙二醇)己二酸酯、(新戊二醇-邻苯二甲酸酐)聚酯、(二乙二醇-邻苯二甲酸酐)聚酯或(1,6-己二醇-邻苯二甲酸酐)聚酯。该三异氰酸酯可以是己二异氰酸酯(hdi)缩二脲三聚物、异佛尔酮二异氰酸酯(ipdi)三聚物和己二异氰酸酯(hdi)三聚物。变量n可以是0、1、2或3。本发明的制品、器材和表面可包括含有基础聚合物和式(xii)的添加剂的表面。
式(xiii)的添加剂可包括少于20个重复单元的支化或非支化低聚物链段(例如2至15个单元、2至10个单元、3至15个单元和3至10个单元)作为链段a。在某些实施方案中,式(xiii)的添加剂包括选自聚氨酯、聚脲、聚酰胺、聚环氧烷、聚碳酸酯、聚酯、聚内酯、聚有机硅、聚醚砜、聚烯烃、聚乙烯基衍生物、多肽、多糖、聚硅氧烷、聚二甲基硅氧烷、聚乙烯-丁烯、聚异丁烯、聚丁二烯、聚环氧丙烷、聚环氧乙烷、聚氧化四亚甲基或聚乙烯丁烯链段的低聚物链段。本发明的制品、器材和表面可包括含有基础聚合物和式(xiii)的添加剂的表面。
式(xiv)的添加剂可包括少于20个重复单元的支化或非支化低聚物链段(例如2至15个单元、2至10个单元、3至15个单元和3至10个单元)作为链段a。在某些实施方案中,式(xiv)的添加剂包括选自聚氨酯、聚脲、聚酰胺、聚环氧烷、聚碳酸酯、聚酯、聚内酯、聚有机硅、聚醚砜、聚烯烃、聚乙烯基衍生物、多肽、多糖、聚硅氧烷、聚二甲基硅氧烷、聚乙烯-丁烯、聚异丁烯、聚丁二烯、聚环氧丙烷、聚环氧乙烷或聚氧化四亚甲基的低聚物链段。本发明的制品、器材和表面可包括含有基础聚合物和式(xiv)的添加剂的表面。
式(xv)的添加剂可包括低聚物连接基(例如少于50个重复单元(例如2至40个单元、2至30个单元、3至20个单元、或3至10个单元))作为链段l1。在式(xv)的一些实施方案中,l2是低聚物连接基(例如少于50个重复单元(例如2至40个单元、2至30个单元、3至20个单元、或3至10个单元))。在式(xv)的特定实施方案中,l1和l2各自是键。在式(xv)的某些实施方案中,该添加剂包括选自聚氨酯、聚脲、聚酰胺、聚环氧烷(例如聚环氧丙烷、聚环氧乙烷或聚氧化四亚甲基)、聚酯、聚内酯、聚有机硅、聚醚砜、聚烯烃、聚乙烯基衍生物、多肽、多糖、聚硅氧烷、聚二甲基硅氧烷、聚(乙烯-共聚-丁烯)、聚异丁烯和聚丁二烯的低聚物链段(例如在l1和l2的任一个中)。在式(xv)的一些实施方案中,该添加剂是式(xv-a)的化合物:
其中m1和m2各自独立地为0至50的整数。在式(xv-a)的特定实施方案中,m1是5、6、7、8、9或10(例如m1是6)。在式(xv-a)的一些实施方案中,m2是5、6、7、8、9或10(例如m2是6)。
在式(xv)或(xv-a)的某些实施方案中,x2是ft。在另一些实施方案中,x2是ch3或ch2ch3。在式(xv)或(xv-a)的特定实施方案中,x3是ft。在另一些实施方案中,各ft独立地为多氟有机基团(例如多氟酰基,如–(o)q-[c(=o)]r-(ch2)o(cf2)pcf3,其中q是0,r是1;o是0至2;且p是0至10)。在式(xv)或(xv-a)的某些实施方案中,n是5至40的整数(例如5至20,如5、6、7、8、9或10)。在式(xv)或(xv-a)的一些实施方案中,各ft包括(cf2)5cf3。本发明的制品、器材和表面可包括含有基础聚合物和式(xv)的添加剂的表面。本发明的制品、器材和表面可包括含有基础聚合物和式(xv-a)的添加剂的表面。
式(xvi)的添加剂可包括低聚物连接基(例如少于50个重复单元(例如2至40个单元、2至30个单元、3至20个单元、或3至10个单元))作为链段l1。在式(xvi)的一些实施方案中,l2是低聚物连接基(例如少于50个重复单元(例如2至40个单元、2至30个单元、3至20个单元、或3至10个单元))。在式(xvi)的特定实施方案中,l1和l2各自是键。在式(xvi)的某些实施方案中,该添加剂包括选自聚氨酯、聚脲、聚酰胺、聚环氧烷(例如聚环氧丙烷、聚环氧乙烷或聚氧化四亚甲基)、聚酯、聚内酯、聚有机硅、聚醚砜、聚烯烃、聚乙烯基衍生物、多肽、多糖、聚硅氧烷、聚二甲基硅氧烷、聚(乙烯-共聚-丁烯)、聚异丁烯或聚丁二烯的低聚物链段(例如在l1和l2的任一个中)。在式(xvi)的一些实施方案中,该添加剂是式(xvi-a)的化合物:
其中m1和m2各自独立地为0至50的整数。在式(xv-a)的特定实施方案中,m1是5、6、7、8、9或10(例如m1是6)。在式(xv-a)的一些实施方案中,m2是5、6、7、8、9或10(例如m2是6)。
在式(xvi)或(xvi-a)的某些实施方案中,x2是ft。在式(xvi)或(xvi-a)的另一些实施方案中,x2是ch3或ch2ch3。在式(xvi)或(xvi-a)的特定实施方案中,x3是ft。在式(xvi)或(xvi-a)的另一些实施方案中,各ft独立地为多氟有机基团(例如多氟酰基,如–(o)q-[c(=o)]r-(ch2)o(cf2)pcf3,其中q是0,r是1;o是0至2;且p是0至10)。在式(xvi)或(xvi-a)的一些实施方案中,各ft包括(cf2)5cf3。本发明的制品、器材和表面可包括含有基础聚合物和式(xvi)的添加剂的表面。本发明的制品、器材和表面可包括含有基础聚合物和式(xvi-a)的添加剂的表面。
在式(xvii)的一些实施方案中,m是1。式(xvii)的添加剂可以是式(xvii-a)的化合物:
g–a–[b–a]n–g
(xvii-a).
在式(xvii)的另一些实施方案中,m是0。式(xvii)的添加剂可以是式(xvii-b)的化合物:
g–[b–a]n–b–g
(xvii-b).
在式(xvii)、(xvii-a)或(xvii-b)的特定实施方案中,每个b是具有两个末端羰基的连接基。在式(xvii)、(xvii-a)或(xvii-b)的某些实施方案中,每个b是键。在式(xvii)、(xvii-a)或(xvii-b)的一些实施方案中。连接g和b的键是氧羰基键(例如酯中的氧羰基键)。在式(xvii)、(xvii-a)或(xvii-b)的另一些实施方案中,n是1或2。
式(xvii)的添加剂可以是式(xvii-c)的化合物:
g–a–g
(xvii-c).
在式(xvii)、(xvii-a)、(xvii-b)或(xvii-c)中,g可以是多氟有机基团(例如多氟烷基)。在式(xvii)、(xvii-a)、(xvii-b)或(xvii-c)的一些实施方案中,g是ft(例如各ft独立地为多氟有机基团(例如多氟酰基,如–(o)q-[c(=o)]r-(ch2)o(cf2)pcf3,其中q是0,r是1;o是0至2;且p是0至10)。在式(xvii)、(xvii-a)、(xvii-b)或(xvii-c)的一些实施方案中,各ft包括(cf2)5cf3。本发明的制品、器材和表面可包括含有基础聚合物和式(xvii)的添加剂的表面。本发明的制品、器材和表面可包括含有基础聚合物和式(xvii-a)的添加剂的表面。本发明的制品、器材和表面可包括含有基础聚合物和式(xvii-b)的添加剂的表面。本发明的制品、器材和表面可包括含有基础聚合物和式(xvii-c)的添加剂的表面。
在式(xviii)中,b可含有聚环氧丙烷、聚环氧乙烷或聚氧化四亚甲基。在式(xviii)中,b可由三乙二醇、四乙二醇或双酚a形成。
在式(xviii)或(xix)中,a可含有氢化聚丁二烯(hlbh)、氢化聚异戊二烯(hhtpi)、聚(碳酸(2,2-二甲基)-1,3-亚丙酯)、聚丁二烯、聚(二乙二醇)己二酸酯(pega)、聚(碳酸六亚甲基酯)(phcn)、聚(乙烯-共聚-丁烯)、(二乙二醇-邻苯二甲酸酐)聚酯、(1,6-己二醇-邻苯二甲酸酐)聚酯、(新戊二醇-邻苯二甲酸酐)聚酯(pdp)、聚硅氧烷、双酚a乙氧基化物、聚(环氧乙烷)-嵌段-聚(环氧丙烷)-嵌段-聚(环氧乙烷)(pln)、聚环氧乙烷(peo)、聚环氧丙烷(ppo)或聚氧化四亚甲基(ptmo)。
在式(xviii)或(xix)的一些实施方案中,a不包括酯键。例如,a包括氢化聚丁二烯(hlbh)、氢化聚异戊二烯(hhtpi)、聚(碳酸(2,2-二甲基)-1,3-亚丙酯)、聚丁二烯、聚(乙烯-共聚-丁烯)、聚硅氧烷、双酚a乙氧基化物、聚(环氧乙烷)-嵌段-聚(环氧丙烷)-嵌段-聚(环氧乙烷)(pln)、聚环氧乙烷(peo)、聚环氧丙烷(ppo)或聚氧化四亚甲基(ptmo)。
在式(xix)中,a可含有三嵌段共聚物ppo-嵌段-peo-嵌段-(聚硅氧烷)-嵌段-peo-嵌段-ppo(plnsi)。在式(xix)中,a可含有氢化聚异戊二烯(hhtpi)或氢化聚丁二烯(hlbh)。在式(xix)中,a可含有聚环氧丙烷(ppo)或聚氧化四亚甲基(ptmo)。在式(xix)中,a可含有聚环氧乙烷-聚二甲基硅氧烷-聚环氧乙烷(c10mwpeo=2,500da)、聚环氧乙烷-聚二甲基硅氧烷-聚环氧乙烷(c15mwpeo=1,000da)或聚环氧乙烷-聚二甲基硅氧烷-聚环氧乙烷(c22mwpeo=2,500da)。在式(xix)中,a可含有环氧丙烷-聚二甲基硅氧烷-环氧丙烷嵌段共聚物(c22mwppo=2,500da)。在式(xix)中,a可含有聚环氧乙烷(peo)。在式(xix)中,a可含有二乙二醇-邻苯二甲酸酐。在式(xix)中,a可含有聚(环氧乙烷)-嵌段-聚(环氧丙烷)-嵌段-聚(环氧乙烷)(pln)。
在式(xx)或(xxi)中,b可含有聚环氧丙烷、聚环氧乙烷或聚氧化四亚甲基。在式(xx)或(xxi)中,b可由三乙二醇或四乙二醇形成。在式(xx)中,b可以是聚环氧乙烷,x1是乙基,且x2是h(ymeroh-1226-pct-pc)。在式(xx)中,b可以是聚环氧乙烷,x1是乙基,且x2是甲基(ymer-1226-pct-pc)。在式(xxi)中,b可以是聚环氧乙烷,x1是h,且x2是h(xmer-1226-pct-pc)。
在式(xviii)、(xix)、(xx)或(xxi)中,该化合物可具有小于10,000da的理论分子量。
对于由二异氰酸酯形成的本发明的任何添加剂,二异氰酸酯可以是3-异氰酸根合甲基-3,5,5-三甲基-环己基异氰酸酯;4,4’-亚甲基双(环己基异氰酸酯)(hmdi);2,2’-、2,4’-和4,4’-亚甲基双(苯基异氰酸酯)(mdi);甲苯-2,4-二异氰酸酯;芳族脂族异氰酸酯,如1,2-、1,3-和1,4-苯二甲基二异氰酸酯;间-四甲基苯二甲基二异氰酸酯(m-tmxdi);对-四甲基苯二甲基二异氰酸酯(p-tmxdi);己二异氰酸酯(hdi);乙二异氰酸酯;丙-1,2-二异氰酸酯;四亚甲基二异氰酸酯;四亚甲基-1,4-二异氰酸酯;八亚甲基二异氰酸酯;十亚甲基二异氰酸酯;2,2,4-三甲基己二异氰酸酯;2,4,4-三甲基己二异氰酸酯;十二烷-1,12-二异氰酸酯;二环己基甲烷二异氰酸酯;环丁烷-1,3-二异氰酸酯;环己烷-1,2-二异氰酸酯;环己烷-1,3-二异氰酸酯;环己烷-1,4-二异氰酸酯;甲基-亚环己基二异氰酸酯(htdi);2,4-二甲基环己烷二异氰酸酯;2,6-二甲基环己烷二异氰酸酯;4,4’-二环己基二异氰酸酯;2,4’-二环己基二异氰酸酯;1,3,5-环己烷三异氰酸酯;异氰酸根合甲基环己烷异氰酸酯;1-异氰酸根合-3,3,5-三甲基-5-异氰酸根合甲基环己烷;异氰酸根合乙基环己烷异氰酸酯;双(异氰酸根合甲基)-环己烷;4,4’-双(异氰酸根合甲基)二环己烷;2,4’-双(异氰酸根合甲基)二环己烷;异佛尔酮二异氰酸酯(ipdi);2,4-六氢甲苯二异氰酸酯;2,6-六氢甲苯二异氰酸酯;3,3’-二甲基-4,4’-联苯二异氰酸酯(todi);聚合mdi;碳二亚胺改性的液体4,4’-二苯甲烷二异氰酸酯;对苯二异氰酸酯(ppdi);间苯二异氰酸酯(mpdi);萘-1,5-二异氰酸酯;2,4’-、4,4’-或2,2’-联苯二异氰酸酯;多苯基多亚甲基多异氰酸酯(pmdi);mdi和pmdi的混合物;pmdi和tdi的混合物;本文所述的任何异氰酸酯的二聚的脲二酮,如甲苯二异氰酸酯的脲二酮、己二异氰酸酯的脲二酮或其混合物;或它们的经取代的或异构体混合物。
对于由异氰酸酯三聚物形成的本发明的任何添加剂,异氰酸酯三聚物可以是己二异氰酸酯(hdi)缩二脲或三聚物、异佛尔酮二异氰酸酯(ipdi)三聚物、己二异氰酸酯(hdi)三聚物;2,2,4-三甲基-1,6-己烷二异氰酸酯(tmdi)三聚物;本文中描述的任何异氰酸酯的三聚的异氰脲酸酯,如甲苯二异氰酸酯的异氰脲酸酯、二苯甲烷二异氰酸酯的三聚物、四甲基苯二甲基二异氰酸酯的三聚物或其混合物;本文中描述的任何异氰酸酯的三聚的缩二脲;衍生自上述二异氰酸酯的改性异氰酸酯;或它们的经取代的或异构体混合物。
该添加剂可包括具有100da至1,500da的理论分子量的多氟有机基团作为基团ft。例如,ft可以是cf3(cf2)r(ch2ch2)p–,其中p是0或1,r是2-20,和cf3(cf2)s(ch2ch2o)χ,其中χ是0至10且s是1至20。或者,ft可以是chmf(3-m)(cf2)rch2ch2-或chmf(3-m)(cf2)s(ch2ch2o)χ-,其中m是0、1、2或3;χ是0至10的整数;r是2至20的整数;且s是1至20的整数。在某些实施方案中,ft是1h,1h,2h,2h-全氟-1-癸醇;1h,1h,2h,2h-全氟-1-辛醇;1h,1h,5h-全氟-1-戊醇;或1h,1h-全氟-1-丁醇或其混合物。在特定实施方案中,ft是(cf3)(cf2)5ch2ch2o-、(cf3)(cf2)7ch2ch2o-、(cf3)(cf2)5ch2ch2o-、chf2(cf2)3ch2o-、(cf3)(cf2)2ch2o-或(cf3)(cf2)5-。在再一些实施方案中,多氟烷基是(cf3)(cf2)5-,例如其中多氟烷基键合到酯基团的羰基上。在某些实施方案中,多氟有机基团是–(o)q-[c(=o)]r-(ch2)o(cf2)pcf3,其中q是0且r是1,或q是1且r是0;o是0至2;且p是0至10。
在一些实施方案中,该添加剂是通过式(i)-(xxi)中的任一种描述的结构。在某些实施方案中,该添加剂是化合物1-57的任一种。化合物1-57的理论结构例示在图1-13中。
在一些实施方案中,式(i)-(xxi)中的任一种的添加剂是式(a)的线性表面改性分子(smm)或式(b1或b2)的支化smm:
ft–[b–a]n–b–ft(a)
其中b是硬链段;a是软链段;ft是多氟有机基团;且n是1至10的整数,或
其中a是软链段;b是支化硬链段;b’,当存在时,是线性硬链段;各ft是多氟有机基团;且n是0至10的整数,并包括下表1中提供的任一示例性添加剂的软和硬链段,其中在实施例中定义了硬和软链段;
或其中该添加剂是式(c1或c2)的smm:
其中ft是多氟有机基团,x1、x2和x3各自独立地为h、ch3、ch2ch3或ft,y是h、ch3或ch2ch3,l1和l2各自独立地为键、低聚物连接基、具有两个末端羰基的连接基,或由二异氰酸酯形成,且n1和n2各自独立地为5至50的整数。
表1
在制剂smm1–smm16的特定实施方案中,pln具有大约1,000da–15,000da(例如大约1,900da、大约3,000da)的理论分子量;pega具有大约1,000da–10,000da(例如大约2,500da)的理论分子量;pdp具有大约1,000da–10,000da(例如大约2,000da)的理论分子量;hlbh具有大约1,000da–10,000da(例如大约2,000da)的理论分子量;c10(二醇)具有大约1,000da–10,000da的理论分子量;ppo具有大约1,000da–10,000da(例如大约1,000da)的理论分子量;且聚(乙二醇)具有大约1,000da–10,000da(例如大约2,000da)的理论分子量。
在制剂smm1–smm16的特定实施方案中,ft是具有100da至1,500da的理论分子量的多氟有机基团。例如,ft可以是cf3(cf2)r(ch2ch2)p–,其中p是0或1,r是2-20,和cf3(cf2)s(ch2ch2o)χ,其中χ是0至10且s是1至20。或者,ft可以是chmf(3-m)(cf2)rch2ch2-或chmf(3-m)(cf2)s(ch2ch2o)χ-,其中m是0、1、2或3;χ是0至10的整数;r是2至20的整数;且s是1至20的整数。在某些实施方案中,ft是1h,1h,2h,2h-全氟-1-癸醇;1h,1h,2h,2h-全氟-1-辛醇;1h,1h,5h-全氟-1-戊醇;或1h,1h-全氟-1-丁醇或其混合物。在特定实施方案中,ft是(cf3)(cf2)5ch2ch2o-、(cf3)(cf2)7ch2ch2o-、(cf3)(cf2)5ch2ch2o-、chf2(cf2)3ch2o-、(cf3)(cf2)2ch2o-或(cf3)(cf2)5-。在另一些实施方案中,多氟烷基是(cf3)(cf2)5-,例如其中多氟烷基键合到酯基团的羰基上。在某些实施方案中,多氟有机基团是–(o)q-[c(=o)]r-(ch2)o(cf2)pcf3,其中q是0且r是1,或q是1且r是0;o是0至2;且p是0至10。ft结构部分可由c6-foh、c8-foh、c6-c8foh、c10-foh、c8-c10foh、c5-foh、c4-foh和/或c3-foh形成(如实施例中定义)。
在某些实施方案中,将任一制剂smm1–smm16与基础聚合物混合以制造抗细菌粘附的表面。在特定实施方案中,基础聚合物选自有机硅、聚烯烃、聚酯、聚碳酸酯、聚砜、聚酰胺、聚醚、聚脲、聚氨酯(pu)、聚醚酰亚胺、聚苯乙烯、纤维素聚合物、聚丙烯(pp)、聚乙烯(pe)、聚氯乙烯(pvc)、聚乙烯醇(pva)、聚乙烯基吡咯烷酮(pvp)、聚丙烯酰胺(paam)、聚环氧乙烷(peo)、聚(环氧乙烷)-嵌段-聚(环氧丙烷)-嵌段-聚(环氧乙烷)、聚(甲基丙烯酸羟乙酯)(polyhema)、聚对苯二甲酸乙二醇酯(pet)、聚对苯二甲酸丁二醇酯(pbt)、聚甲基丙烯酸甲酯(pmma)、聚醚醚酮(peek)、聚醚-嵌段-聚酰胺、环烯烃聚合物(cop)、环烯烃共聚物(coc)、甲基丙烯酸甲酯丙烯腈丁二烯苯乙烯(mabs)、苯乙烯丙烯腈(san)、苯乙烯甲基丙烯酸甲酯(smma)、甲基丙烯酸酯丁二烯苯乙烯(mbs)、苯乙烯丁二烯(sb)、聚(苯乙烯-嵌段-异丁烯-嵌段-苯乙烯)(sibs)和乙烯-乙酸乙烯酯(eva)。在某些实施方案中,将smm1–smm16的任一种与聚氨酯(pu)基础聚合物混合。pu基础聚合物可以是本文中描述的任何pu基础聚合物,例如聚醚基聚氨酯(例如
与抗微生物剂结合的用途
本发明提出可提高聚合物表面上存在的细菌对周围环境中可能存在的抗微生物剂的敏感性的方法和制品、器材和表面。在本发明的方法和制品、器材和表面中可适用的抗微生物剂包括但不限于银、青霉素g、青霉素v、甲氧西林、苯唑西林、氯唑西林、双氯西林、萘夫西林、氨苄青霉素、阿莫西林、羧苄青霉素、替卡西林、美洛西林、哌拉西林、阿洛西林、替莫西林、先锋霉素、头孢匹林、头孢拉定、头孢噻啶、头孢唑啉、头孢孟多、头孢呋辛、头孢氨苄、头孢丙烯、头孢克洛、氯碳头孢、头孢西丁、头孢美唑、头孢噻肟、头孢唑肟、头孢曲松、头孢哌酮、头孢他啶、头孢克肟、头孢泊肟、头孢布烯、头孢地尼、头孢匹罗、头孢吡肟、bal5788、bal9141、亚胺培南、厄他培南、美罗培南、卡巴里路、克拉维酸、舒巴坦、他唑巴坦、链霉素、新霉素、卡那霉素、巴龙霉素、庆大霉素、妥布霉素、阿米卡星、奈替米星、壮观霉素、西索米星、地贝卡星、异帕米星、四环素、金霉素、地美环素、米诺环素、土霉素、美他环素、多西环素、红霉素、阿奇霉素、克拉霉素、泰利霉素、abt-773、林可霉素、克林霉素、万古霉素、奥利万星、达巴万星、替考拉宁、奎奴普丁和达福普丁、对氨基苯磺酰胺、对氨基苯甲酸、磺胺嘧啶、磺胺异恶唑、磺胺甲恶唑、磺胺杀利定、利奈唑胺、萘啶酸、奥索利酸、诺氟沙星、培氟沙星、依诺沙星、氧氟沙星、环丙沙星、替马沙星、洛美沙星、氟罗沙星、格帕沙星、司帕沙星、曲伐沙星、克林沙星、加替沙星、莫西沙星、吉米沙星、西他沙星、甲硝唑、达托霉素、加雷沙星、雷莫拉宁、法罗培南、多粘菌素、三氯生、利福平、米诺环素、替加环素、azd2563和甲氧苄氨嘧啶。在一些实施方案中,抗微生物剂为消毒剂形式。消毒剂的非限制性实例是醛(例如甲醛或戊二醛、邻苯二甲醛)、过氧化氢、过乙酸、过氧化氢/过乙酸组合、基于氯的试剂(例如次氯酸钠)、碘伏(例如碘或聚维酮碘)、洗必泰、醇(例如异丙醇或酚)或季铵化合物。
与不透射线材料组合的用途
本发明的聚合物表面可包括其它材料,如不透射线材料(例如作为粉末或其它粒状物)。合适的不透射线添加剂包括碱式碳酸铋、氯氧化铋、三氧化二铋、钨,优选硫酸钡(例如1%至45%(w/w)(例如1%至10%(w/w)、10%至30%(w/w)、20%至40%(w/w)、25%至45%(w/w)、20%至35%(w/w)、25%至40%(w/w)、30%至45%(w/w)、或35%至45%(w/w))不透射线材料)。本发明中使用的其它添加剂包括着色剂,如颜料、染料或其它合适的着色剂材料。
应用
可由本发明的混合物形成或用本发明的混合物涂布的制品包括薄膜、包装材料、粒子、纤维(创伤敷料、绷带、纱布、胶带、衬垫、海绵,包括织造和非织造海绵和专为牙科或眼科手术设计的那些)、手术、医疗或牙科仪器、牙科设备或植入物、血液氧合器、呼吸机、泵、药物输送装置、管材、线材、电极、避孕器具、女性卫生用品、内窥镜、移植物(包括小直径<6mm)、支架(包括冠状动脉、输尿管、肾、胆道、结肠直肠、食管、肺、尿道和血管)、支架移植物(包括腹部血管、胸部血管和外周血管)、起搏器、可植入复律器-除颤器、心脏再同步治疗装置、心血管装置引线、心室辅助装置和传动系统、心脏瓣膜、腔静脉滤器、血管内线圈、导管(包括中心静脉、外周中心、中线、外周、隧道、透析接入、导尿管、神经、腹膜、主动脉内气囊泵、血管成形术球囊、诊断、介入、药物输送等)、导管接头和阀(包括无针接头)、静脉输送管线和岐管、分流器(内部或外部的,包括心室、房室、脑室腹膜和腰腹膜)、伤口引流器、引流导管、透析膜、输液口、人工耳蜗、气管内导管、气管造口管、呼吸机呼吸管和线路、导丝、流体收集袋、药物输送袋和管材、可植入传感器(例如血管内、经皮、颅内)、眼科装置(包括隐形眼镜、泪点塞、眼内装置或植入物)、矫形外科装置(包括髋关节植入物、膝盖植入物、肩部植入物、脊柱植入物(包括颈椎板系统、椎弓根螺钉系统、椎体间融合器、人工椎间盘和其它运动保留装置)、螺钉、板、铆钉、棒、髓内钉、骨水泥、人工腱和其它假体或骨折修复装置)、牙植入物、牙周植入物、乳房植入物、阴茎植入物、颌面部植入物、整形植入物、瓣膜、矫正器、脚手架、缝合材料、针、疝气修补网、无张力阴道吊带和阴道悬带、假体神经装置、耳管、饲管、血袋、组织再生或细胞培养装置、或在体内或与身体接触使用的其它医疗器材或这些中的任一种的任何部分。
在一个实施方案中,该制品是血管置入装置,如外周置入中心静脉导管(picc)、中心静脉导管(cvc)、血液透析导管或静脉瓣。在另一实施方案中,该基底是由医疗等级有机硅或聚氨酯,如
本发明的混合物也可添加到涂料和过滤器中以防止霉菌、细菌污染,和在希望防止细菌介导的污损的其它应用中,如海上应用(例如海洋船只,包括船舶和相关污水舱、灰水舱和水入口/出口管的外表面)、航空工业、家具工业(例如儿童床、健身器材上的把手、或健身器材)、运输工业(例如救护车、公共汽车或公共交通系统)、游泳池、燃料箱、输油管道、工业管道、制药设备、药物输送装置如吸入器、隐形眼镜、牙植入物、体内传感器的涂层、纺织品如医院布帘、服装或床上用品、通风管道、门把手、废水处理装置、水净化、生物反应器和食品加工。
可由本发明的混合物形成或用本发明的混合物涂布的制品还可包括消费品和/或易耗品,例如服装/个人防护服、个人护理产品容器、食品容器、食物和准备表面、通用储存容器、避孕器具、女性卫生用品、电子器件、成人玩具(例如有机硅成人玩具)和办公用品(例如纸、笔、文件夹、便签、笔记本和墨粉或墨盒)。
提出如下文阐述的下列实施例以向本领域普通技术人员提供如何进行、制造和评估本文中要求保护的方法和化合物的完整公开和描述,并且意在仅举例说明本发明而无意限制本发明人视为其发明的范围。
具体实施方式
实施例
实施例1:添加剂的制备
本发明的制品中所用的添加剂可使用本领域中已知的方法由适当选择的试剂,如二异氰酸酯、三异氰酸酯、二羧酸、二醇、全氟化酰氯、双氯甲酸酯和氟化醇制备以形成范围广泛的添加剂。该试剂包括但不限于下面提到的组分试剂。
二异氰酸酯
hmdi=4,4’-亚甲基双(环己基异氰酸酯)
ipdi=异佛尔酮二异氰酸酯
tmxdi=间-四亚甲基苯二甲基二异氰酸酯
hdi=己二异氰酸酯
三异氰酸酯
desmodurn3200或desmodurn-3200=己二异氰酸酯(hdi)缩二脲三聚物
desmodurz4470a或desmodurz-4470a=异佛尔酮二异氰酸酯(ipdi)三聚物
desmodurn3300=己二异氰酸酯(hdi)三聚物
二醇/多元醇
hlbh=氢化的羟基封端聚丁二烯
pcn=聚(碳酸2,2-二甲基-1-3-亚丙酯)二醇
phcn=聚(碳酸六亚甲基酯)二醇
peb=聚(乙烯-共聚-丁烯)二醇
lbhp=羟基封端聚丁二烯多元醇
pega=聚(二乙二醇)己二酸酯
ptmo=聚(氧化四亚甲基)二醇
pdp=二乙二醇-邻苯二甲酸酐聚酯多元醇
hhtpi=氢化的羟基封端聚异戊二烯
c22=羟基封端聚二甲基硅氧烷嵌段共聚物
c25(二醇)=羟基封端聚二甲基硅氧烷(环氧乙烷-pdms-环氧乙烷)嵌段共聚物
c10(二醇)=羟基封端聚二甲基硅氧烷(环氧乙烷-pdms-环氧乙烷)嵌段共聚物
pln=聚(乙二醇)-嵌段-聚(丙二醇))-嵌段-聚(乙二醇)聚合物(peo-ppo-peopluronic聚合物)
pln-si=羟基封端的(ppo-peo-pdms-peo-ppo)pluronic-硅氧烷共聚物
pln3k=聚(乙二醇)-嵌段-聚(丙二醇))-嵌段-聚(乙二醇)聚合物(peo-ppo-peopluronic聚合物)(mw≈3000da)
pln8k=聚(乙二醇)-嵌段-聚(丙二醇))-嵌段-聚(乙二醇)聚合物(peo-ppo-peopluronic聚合物)(mw≈8000da)
peg2k(二醇)=聚(乙二醇)二醇(mw≈2000da)
ddd=1,12-十二烷二醇
sph=1,6-己二醇-邻苯二甲酸酐聚酯多元醇
spn=新戊二醇-邻苯二甲酸酐聚酯多元醇
bpae=双酚a乙氧基化物二醇
ymer(二醇)=羟基封端聚乙二醇单甲基醚
ymeroh(三醇)=三羟甲基丙烷乙氧基化物
xmer(四醇)=季戊四醇乙氧基化物
氟化封端基团
c6-foh=(cf3)(cf2)5ch2ch2oh(1h,1h,2h,2h-全氟己醇)
c8-foh=1h,1h,2h,2h-全氟辛醇
c6-c8foh=(cf3)(cf2)7ch2ch2oh和(cf3)(cf2)5ch2ch2oh(c6-foh和c8-foh的混合物;也称为bal-d)
c10-foh=1h,1h,2h,2h-全氟癸醇
c8-c10foh=c8-foh和c10-foh的混合物
c5-foh=1h,1h,5h-全氟-1-戊醇
c4-foh=1h,1h-全氟丁醇
c3-foh=(cf3)(cf2)2ch2oh(1h,1h-全氟丁醇)
非锡基催化剂
bi348=羧酸铋类型1
bi221=羧酸铋类型2
bi601=羧酸铋类型3
上列铋催化剂可购自kingindustries(norwalkct)。可使用本领域中已知的任何铋催化剂合成本文所述的添加剂。可用于合成聚氨酯的锡基催化剂也可代替铋基催化剂用于合成本文所述的添加剂。
化合物1
用分子量为1000da的ppo二醇、1,6-己二异氰酸酯(hdi)和氟代醇的低沸点馏分(ba-l)合成化合物1。合成条件如下:使10克ppo与3.36克hdi反应2小时,然后将5克ba-l(低沸点馏分)添加到该反应中。使该混合物与42.5毫克催化剂二月桂酸二丁基锡在130毫升二甲基乙酰胺中反应,并使预聚物步骤的反应温度保持在60-70℃内。聚苯乙烯当量重均分子量(equivalentweightaveragemolecularweight)为1.6+/-0.2×104并且其总氟含量为18.87+/-2.38重量%。化合物1的热转变可通过差示扫描量热法检测。观察到在大约14℃和85℃的两个高阶热转变。化合物1的理论化学结构显示在图1a中。
化合物2
用于该合成的所有玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒的三颈1000毫升烘干烧瓶中加入175克(72毫摩尔)氢化的羟基封端聚丁二烯(hlbh多元醇,mw=2000da)。将带有多元醇的烧瓶脱气过夜,然后用干燥n2吹扫。向1000毫升量筒中装入525毫升无水甲苯,用橡胶隔片密封并用干燥n2吹扫。借助双刃针(double-edgedneedle)将甲苯转移到三颈烧瓶中并剧烈搅拌多元醇以溶解在溶剂中。将该烧瓶置于65-70℃的油浴中。将39.70克(151毫摩尔)4,4’-亚甲基双(环己基异氰酸酯)(hmdi)添加到配有搅拌棒的脱气250毫升烧瓶中。也使用双刃针向这一烧瓶中加入来自脱气的n2吹扫的250毫升隔片密封量筒的150毫升无水甲苯并搅拌该混合物以将hmdi溶解在溶剂中。向脱气的50毫升圆底烧瓶中加入8.75克(基于二醇计5.00%w/w)羧酸铋催化剂,接着26毫升甲苯以溶解催化剂。将hmdi溶液转移到含有多元醇的1000毫升烧瓶中。在加入hmdi后立即加入铋催化剂溶液(20毫升)。将反应混合物在70℃下搅拌5小时以制造hmdi-hlbh预聚物。
在另一50毫升圆底烧瓶中加入74.95克(180毫摩尔)c8-c10foh(c8-foh和c10-foh的混合物),用隔片加盖,脱气,然后用n2吹扫。将这添加到含有预聚物的1000毫升烧瓶中。所有添加和转移小心地在干燥n2气氛中进行以避免与空气的任何接触。将所得混合物加热到45℃18小时以制造具有封端c8-c10foh的smm。允许smm溶液冷却到环境温度并形成乳状溶液。该乳状溶液在meoh(甲醇)中沉淀,所得沉淀物用meoh反复洗涤以形成具有类似面团的稠度的白色粘稠材料。这种粘稠半固体材料在thf/edta(乙二胺四乙酸)中洗涤两次以除去残留催化剂,然后在thf/meoh中再接连洗涤两次以除去未反应的单体、低分子量副产物和催化剂残留物。smm首先在流动烘箱(flowoven)中在逐渐提高温度的10小时期间在40-120℃下干燥10小时,最后在真空下在120℃下干燥(24小时)并作为无色橡胶状半固体储存在干燥器中。化合物2的理论化学结构显示在图1b中。
化合物3
使用180克(74毫摩尔)氢化的羟基封端聚丁二烯(hlbh多元醇,mw=2000da)和30.14克(115毫摩尔)4,4’-亚甲基-双(环己基异氰酸酯)(hmdi)如对化合物2所述进行反应以形成预聚物。该预聚物用40.48克(111.18毫摩尔)1h,1h,2h,2h-全氟-1-辛醇(c8-foh)封端以形成作为无色橡胶状半固体的化合物3。如上所述,在羧酸铋催化剂存在下进行偶联,且化合物3在使用前类似于化合物2洗涤和干燥。化合物3的理论化学结构显示在图1c中。
化合物4
使用10克(4毫摩尔)聚(乙烯-共聚-丁烯)(peb多元醇,mw=2500da)和2.20克(8.4毫摩尔)4,4’-亚甲基-双(环己基异氰酸酯)(hmdi)如对化合物3所述进行反应以形成预聚物。该预聚物用3.64克(10毫摩尔)1h,1h,2h,2h-全氟-1-辛醇(c8-foh)封端以形成化合物4。如上所述,在羧酸铋催化剂存在下进行偶联,且化合物4在使用前类似于化合物2洗涤和干燥。化合物4的理论化学结构显示在图1d中。
化合物5
如对化合物4所述进行反应,只是将溶剂从甲苯换成dmac。在此,100克(100毫摩尔)聚(碳酸2,2-二甲基-1,3-亚丙酯)二醇(pcn,mw=1000da)和40.7克(155毫摩尔)4,4’-亚甲基-双(环己基异氰酸酯)(hmdi)以形成预聚物。该预聚物用45.5克(125毫摩尔)1h,1h,2h,2h-全氟-1-辛醇(c8-foh)封端以形成化合物5。与化合物4合成相比如下修改反应后的后处理和后续洗涤程序。来自在dmac中的反应混合物的化合物5在蒸馏水中沉淀并接连在ipa/edta(异丙醇/乙二胺四乙酸)溶液中洗涤,接着在ipa/己烷中再洗涤一次以除去未反应的单体、低分子量副产物和催化剂残留物以产生作为白色非晶粉末的化合物5。如上所述,在羧酸铋催化剂存在下进行偶联并在使用前在真空下干燥。化合物5的理论化学结构显示在图1e中。
化合物6
使用6.0克(6.0毫摩尔)聚(碳酸2,2-二甲基-1,3-亚丙酯)二醇(mw=1000da)和1.90克(8.5毫摩尔)异佛尔酮二异氰酸酯(ipdi)如对化合物5所述进行反应以形成预聚物。该预聚物用1.4克(6.0毫摩尔)1h,1h,5h-全氟-1-戊醇(c5-foh)封端以形成作为白色非晶固体的化合物6。如上所述,在羧酸铋催化剂存在下进行偶联,且化合物6在使用前类似于化合物5洗涤和干燥。化合物6的理论化学结构显示在图1f中。
化合物7
使用10.0克(10.0毫摩尔)聚(碳酸2,2-二甲基-1,3-亚丙酯)二醇(mw=1000da)和4.07克(15.5毫摩尔)4,4’-亚甲基-双(环己基异氰酸酯)(hmdi)如对化合物5所述进行反应以形成预聚物。该预聚物用2.5克(12.5毫摩尔)1h,1h-全氟-1-丁醇(c4-foh)封端以形成作为白色非晶固体的化合物8。如上所述,在羧酸铋催化剂存在下进行偶联,且化合物7在使用前类似于化合物5洗涤和干燥。化合物7的理论化学结构显示在图1g中。
化合物8
使用180克(84.8毫摩尔)羟基封端聚丁二烯(lbhp多元醇,mw=2000da)和29.21克(131.42毫摩尔)异佛尔酮二异氰酸酯(ipdi)如对化合物5所述进行反应以形成预聚物。该预聚物用46.31克(127.18毫摩尔)1h,1h,2h,2h-全氟-1-辛醇(c8-foh)封端以形成作为灰白色不透明粘稠液体的化合物8。如上所述,在羧酸铋催化剂存在下进行偶联,且化合物8在使用前类似于化合物5洗涤和干燥。化合物8的理论化学结构显示在图2a中。
化合物9
使用10克(3.92毫摩尔)聚(二乙二醇己二酸酯)(pega多元醇,mw=2500da)和1.59克(6.08毫摩尔)4,4’-亚甲基-双(环己基异氰酸酯)(hmdi)如对化合物5所述进行反应以形成预聚物。该预聚物用2.14克(5.88毫摩尔)1h,1h,2h,2h-全氟-1-辛醇(c8-foh)封端以形成作为灰白色不透明粘稠液体的化合物9。如上所述,在羧酸铋催化剂存在下进行偶联,且化合物9在使用前类似于化合物5洗涤和干燥。化合物9的理论化学结构显示在图2b中。
化合物10
使用10克(5.06毫摩尔)基于邻苯二甲酸酯-二乙二醇的聚酯多元醇(pdp多元醇,mw=2000da)和1.92克(7.85毫摩尔)间-四亚甲基苯二甲基二异氰酸酯(tmxdi)如对化合物5所述进行反应以形成预聚物。该预聚物用2.76克(7.59毫摩尔)1h,1h,2h,2h-全氟-1-辛醇(c8-foh)封端以形成作为无色固体的化合物10。如上所述,在羧酸铋催化剂存在下进行偶联,且化合物10在使用前类似于化合物5洗涤和干燥。化合物10的理论化学结构显示在图2c中。
化合物11
用ptmo二醇(mw=1000da)、1,6-己二异氰酸酯(hdi)和氟代醇的低沸点馏分(ba-l)合成化合物11。合成条件如下:使10克ptmo与3.36克hdi反应2小时,然后将9克ba-l(低沸点馏分)添加到该反应中。使该混合物与60毫升催化剂二月桂酸二丁基锡在70毫升二甲基乙酰胺(dmac)中反应,并使预聚物步骤的反应温度保持在60-70℃内。聚苯乙烯当量重均分子量为3.0×104并且其总氟含量为7.98重量%。化合物11的理论化学结构显示在图2d中。
化合物12-26
本发明的表面改性剂,如化合物15和化合物17,可通过根据方案1和2中描绘的方案的两步会聚(convergent)法合成。简言之,使多异氰酸酯如desmodurn3200或desmodur4470逐滴与表面活性基团(例如氟代醇)在有机溶剂(例如无水thf或二甲基乙酰胺(dmac))中在催化剂存在下在25℃下反应2小时。在加入氟代醇之后,在50℃下继续搅拌1小时和在70℃下另外搅拌1小时。这些步骤导致形成部分氟化的中间体,其随后与多元醇(例如氢化的羟基封端聚丁二烯,或聚(碳酸2,2-二甲基-1,3-亚丙酯)二醇)在70℃下偶联14小时以提供smm。由于这些反应是湿度敏感的,它们在惰性n2气氛和无水条件下进行。也小心地保持温度分布,尤其是在部分氟化过程中,以避免不想要的副反应。反应产物在meoh中沉淀并用另外的meoh洗涤几次。通过首先将该添加剂溶解在热thf或热ipa中,接着使添加剂与edta溶液反应、接着在meoh中沉淀,清除催化剂残留物。最后,该添加剂在使用前在旋转蒸发器中在120-140℃下干燥。化合物12至26的理论化学结构显示在图2e至7b中。
方案1
方案2
所有玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒和回流冷凝器的三颈5000毫升反应器中加入300克(583毫摩尔)desmodurn3300。该混合物在环境温度下脱气过夜。将氢化的羟基封端聚丁二烯(hlbh多元醇mw=2000da)量入2000毫升烧瓶并在60℃下脱气过夜。将铋催化剂k-kat348(羧酸铋;可获自kingindustries)称出到250毫升烧瓶中并在环境温度下脱气过夜。将全氟化醇量出到1000毫升烧瓶中并在环境温度下脱气30分钟。在脱气后,所有容器用n2吹扫。
然后将300毫升thf(或dmac)添加到含desmodurn3300的容器中,并搅拌该混合物以溶解多异氰酸酯。类似地,将622毫升thf添加到hlbh多元醇中,并搅拌该混合物以溶解多元醇。同样地,将428毫升thf(或dmac)添加到全氟化醇中并搅拌该混合物以溶解。类似地,对于k-kat348,将其溶解在77毫升thf或dmac中。继续搅拌以确保所有试剂在它们各自的容器中溶解。
将一半k-kat溶液转移到全氟化溶液中,将其搅拌5分钟。这种溶液在n2正压下经由套管(双头针)在环境(25℃)温度下经2小时逐滴添加到含desmodurn3300a溶液的反应容器中。在添加后,将温度提高到50℃1小时和70℃另外1小时。全程保持适当搅拌。将剩余k-kat348催化剂转移到hlbh-2000烧瓶中;在搅拌以溶解后,将这添加到含n3300的反应器中。允许反应混合物在70℃下反应过夜14小时以制造具有四个氟化端基的化合物16。化合物16的理论化学结构显示在图4a中。
酯基添加剂的一般合成描述
二醇如ymer二醇、羟基封端聚二甲基硅氧烷或多元醇,如三羟甲基丙烷乙氧基化物或季戊四醇乙氧基化物在一步反应中与表面活性基团前体(例如全氟庚酰氯)在40℃下在氯化有机溶剂,例如氯仿或二氯甲烷中在酸清除剂,如吡啶或三乙胺存在下反应24小时。这种反应用多氟有机基团将羟基封端。由于这些反应对湿敏感,这些反应使用无水溶剂在n2气氛下进行。在反应后,旋转蒸发溶剂并将产物溶解在四氢呋喃(thf)中,其溶解产物并使吡啶盐沉淀,将其滤出,并将滤液进一步旋转蒸发至干。然后通过溶解在最少thf中并在己烷中沉淀来提纯产物。这进行三次,此后最终产物再旋转蒸发并最终在真空烘箱中在60℃下干燥过夜。
化合物27
用于该合成的玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒的2颈1000毫升烘干圆底烧瓶中加入85克(24毫摩尔)c25-二醇(mw=3500da)。带有二醇的烧瓶在温和搅拌下在60℃下脱气过夜,然后用干燥n2吹扫接下来的一天。停止加热。向1000毫升量筒中装载320毫升无水chcl3,用橡胶隔片密封并用干燥n2吹扫。将chcl3经套管转移到2颈烧瓶中并剧烈搅拌二醇以溶解在溶剂中。使用塑料注射器将无水吡啶(11.53克,146毫摩尔)添加到c25-二醇溶液中,并搅拌所得混合物以溶解所有材料。向另一烘干的2颈1000毫升烧瓶中装载32.51克(85毫摩尔)全氟庚酰氯。用橡胶隔片密封烧瓶并脱气5分钟,然后用n2吹扫。这时将235毫升无水chcl3经套管添加到含全氟庚酰氯的1000毫升2颈烧瓶中,并在室温下搅拌以溶解酰氯。这一烧瓶配有加料漏斗并将在chcl3中的c25-二醇-吡啶溶液经套管转移到加料漏斗中。将经过反应器的n2流调节到缓慢和稳定流量。在室温下开始将c25-二醇-吡啶溶液连续逐滴添加到酰氯溶液中,并继续~4小时。保持在足够速度下搅拌以实现试剂的良好混合。在完成c25-二醇-吡啶溶液的添加后,将加料漏斗换成空气冷凝器,并将2颈烧瓶浸在置于配有热电偶单元的加热器上的油浴中。将温度提高到40℃,并在n2下在此温度下继续反应24小时。
通过在旋转蒸发器中蒸发chcl3并通过在加入thf后过滤吡啶盐来提纯产物。粗产物然后在异丙醇/己烷混合物中沉淀两次。如下用热己烷对从ipa/己烷中沉淀的油施以进一步洗涤。在带有搅拌棒的1升烧杯中将大约500毫升己烷添加到该油中。在将己烷加热到沸腾的同时搅拌该混合物。停止加热,并允许该混合物冷却5分钟。油沉降在底部,此时滗析己烷顶层。将分离的油进一步溶解在thf中,转移到圆底烧瓶中,然后旋转蒸发溶剂。该油在真空烘箱中在40℃下最终干燥24小时。纯化产物(二-和单-取代产物的混合物)通过gpc(基于聚苯乙烯标样的分子量)、对氟的元素分析、19fnmr、1hnmr和ftir表征。外观:粘稠油。重均分子量(聚苯乙烯当量)=5791g/mol。pd:2.85。元素分析:f:7.15%。19fnmr(cdcl3,400mhz,ppm):δ-80.78(m,cf3),-118.43(m,cf2),-121.85(m,cf2),-122.62(m,cf2),-126.14(m,cf2)。1hnmr(cdcl3,400mhz):δppm=0.0(m,ch3si),0.3(brm,ch2si),1.4(brm,ch2),3.30(m,ch2’s),4.30(m,ch2coo-).ftir,纯(cm-1):3392(oh),2868(ch2),1781(o-c=o,酯),1241,1212,1141,1087(cf3,cf2)。化合物27的理论化学结构显示在图7c中。
化合物28
向干燥的5升反应器中加入394.4克(1.5摩尔)hmdi,接着350.6克thf,将反应器置于20℃的水浴中并通过鼓入氩气脱气1小时。向2升烧瓶中加入900克(0.75摩尔)聚硅氧烷二醇dms-15,接着800.1克thf,通过鼓入氩气30分钟,在室温下将该溶液脱气。向250毫升量筒中加入4.5克铋min.。将一半催化剂溶液经套管转移到dms-15溶液中并充分搅拌混合物。将dsm-15溶液经1小时恒速缓慢添加到含hmdi的主反应器中。该溶液在搅拌下保持在20℃。在添加后,将温度提高到45℃,保持1小时,然后提高到65℃1小时。向干燥的2升加料烧瓶中加入684.2克(1.88摩尔)capstone62-al,接着608.2克thf,并将其附加到反应器上。通过将氩气鼓过其15分钟,在室温下将其脱气。将剩余羧酸铋催化剂转移到capstone62-al溶液中,并充分搅拌整个混合物。将capstone62-al氟代醇添加到主反应器中,将温度提高到70℃,并使反应在氩气下在搅拌下进行过夜。在反应完成后,使该溶液冷却到室温并在旋转蒸发器上除去50%的thf溶剂。将剩余溶液添加到在配有机械搅拌器的22升烧瓶中的10升去离子水中以形成沉淀物。保持搅拌10分钟,然后停止以允许沉淀物沉降。滗析出上清液,并在64℃下将聚合物溶解在1500克异丙醇中。粗制聚合物在搅拌下在65℃下用100毫升edta溶液(ph~9)处理30分钟,此后加入另外100克edta,并在室温下继续搅拌30分钟。停止搅拌并使该溶液在具有机械搅拌器的22升烧瓶中在10升去离子水中沉淀。在5分钟后,停止搅拌并使聚合物沉降,滗析出水。该聚合物用10升水洗涤两次,然后在旋转蒸发器上干燥至115℃的最大温度以产生黄色蜡状固体(79%)。在真空烘箱中在60℃下进行最终干燥24小时。纯化产物通过gpc(基于聚苯乙烯标样的分子量)和对氟的元素分析表征。平均分子量(聚苯乙烯当量)为9060g/mol。多分散性=1.47。元素分析显示%f=19%。热分解温度(tga,在n2下),第一次起始时:266℃(在5重量%损失下)。化合物28的化学结构显示在图8a中。
化合物29
用于该合成的玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒的2颈100毫升烘干圆底烧瓶中加入10克(5毫摩尔)pdmsc22-二醇(c22二醇,mw=3000da)。带有二醇的烧瓶在温和搅拌下在60℃下脱气过夜,然后用干燥n2吹扫接下来的一天。停止加热。向100毫升量筒中装入50毫升无水chcl3,用橡胶隔片密封并用干燥n2吹扫。将chcl3经套管转移到2颈烧瓶中,并剧烈搅拌二醇以溶解在溶剂中。然后使用塑料注射器将无水吡啶(0.53克,7毫摩尔)添加到c22-二醇溶液中,并搅拌所得混合物以溶解所有材料。向另一烘干的2颈250毫升烧瓶中装载3.19克(8毫摩尔)全氟庚酰氯。该烧瓶然后用橡胶隔片密封,将烧瓶中的混合物脱气5分钟,并用n2吹扫。然后,使用量筒和套管加入22毫升无水chcl3以将溶剂转移到含有全氟庚酰氯的250毫升2颈烧瓶中。所得混合物在室温下搅拌以溶解酰氯。该烧瓶然后配备加料漏斗,并使用套管将在chcl3中的c22-二醇-吡啶溶液转移到加料漏斗中。将经过反应器的n2流调节到缓慢和稳定流量。然后在室温下经~4小时将c22-二醇-吡啶溶液连续逐滴添加到酰氯溶液中。保持在足够速度下搅拌以实现试剂的良好混合。在完成c22-二醇的添加后,将加料漏斗换成空气冷凝器,并将2颈烧瓶浸在置于配有热电偶单元的加热器上的油浴中。将温度提高到50℃,并使反应混合物在n2下在此温度下保持24小时。
然后,停止加热和搅拌。取出烧瓶并将其内容物倒入圆底烧瓶。通过旋转蒸发除去挥发物。在浓缩后,形成致密沉淀物(吡啶盐)。加入thf以溶解产物,并通过使用粗whatman滤纸(no4)过滤除去沉淀的吡啶盐,因为吡啶盐不溶于thf。通过旋转蒸发除去挥发物。然后将粗产物溶解在100毫升chcl3中并倒入分液漏斗。加入150毫升水和5毫升5nhcl以中和任何剩余吡啶。摇动漏斗,并将产物萃取到chcl3中。含产物的chcl3底层然后在分液漏斗中接连用水、5毫升5%(w/v)nahco3溶液洗涤以中和任何剩余hcl,和用蒸馏水洗涤。分离chcl3层并通过旋转蒸发浓缩以获得粗产物,然后将其溶解在10毫升异丙醇中。将所得溶液在连续搅拌下逐滴添加到含有200毫升含1%(v/v)meoh的去离子水的1升烧杯中。作为油分离出产物,此时将该溶液保持在冰浴中20分钟,并滗析顶部水层。将该油溶解在thf中并转移到200毫升圆底烧瓶中。在最多80℃和4毫巴下通过旋转蒸发除去挥发物以除去残留溶剂。所得产物在真空烘箱中在60℃下干燥24小时以产生作为浅黄色清澈油的纯化产物(~64%收率)。该纯化产物通过gpc(基于聚苯乙烯标样的分子量)和元素分析(对于氟)表征。外观:浅黄色清澈油。重均分子量(聚苯乙烯当量)mw=5589da。pd=1.15。元素分析f:12.86%。化合物29的理论化学结构显示在图8b中。
化合物30
用于该合成的玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒的2颈250毫升烘干圆底烧瓶中加入20克(8.0毫摩尔)氢化的羟基封端聚丁二烯(hlbh二醇,mw=2000da)。带有二醇的烧瓶在温和搅拌下在60℃下脱气过夜,然后用干燥n2吹扫接下来的一天。此时,停止加热。向200毫升量筒中装载104毫升无水chcl3,用橡胶隔片密封,并用干燥n2吹扫。将chcl3经套管转移到2颈烧瓶中,并剧烈搅拌二醇以溶解在溶剂中。此时,使用塑料注射器将无水吡啶(3.82克,48毫摩尔)添加到hlbh二醇溶液中,并搅拌所得混合物以溶解所有材料。向另一烘干的2颈100毫升烧瓶中装载反式-5-降冰片烯-2,3-二羰基氯(“nci;”3.70克,17毫摩尔),用橡胶隔片密封,脱气5分钟,然后用n2吹扫。此时,使用量筒和套管加入52毫升无水chcl3以将溶剂转移到含nci的100毫升2颈烧瓶中。搅拌所得混合物以溶解nci。250毫升2颈烧瓶然后配备加料漏斗,并使用套管将nci在chcl3中的溶液转移到加料漏斗中。将经过反应器的n2流调节到缓慢和稳定流量。在室温下经~1小时将nci溶液连续逐滴添加到hlbh-吡啶溶液以形成预聚物。保持在足够速度下搅拌以实现试剂的良好混合。
并行地,向另一烘干的50毫升烧瓶中装载capstonetmal-62全氟化试剂(5.45克,15毫摩尔)。该烧瓶用橡胶隔片密封,脱气15分钟,并用n2吹扫。加入无水chcl3(17毫升)和无水吡啶(1.9克,24毫摩尔)。搅拌该混合物以溶解所有试剂。在nci溶液添加到250毫升2颈烧瓶中完成后,使用套管在搅拌下将capstonetmal-62全氟化试剂溶液添加到这一烧瓶中。将加料漏斗换成空气冷凝器,并将250毫升2颈烧瓶浸在置于配有热电偶单元的加热器上的油浴中。将温度提高到50℃,并在n2下在此温度下继续反应24小时。
在该反应后,停止加热和搅拌。取出反应烧瓶并将其内容物倒入圆底烧瓶。通过旋转蒸发除去chcl3。在浓缩后,形成致密沉淀物(吡啶盐)。加入thf以溶解产物,并通过使用粗whatman滤纸(no4)过滤除去沉淀的吡啶盐。吡啶盐不溶于thf。通过旋转蒸发除去thf。将粗产物溶解在100毫升chcl3中并倒入分液漏斗。加入100毫升水,接着加入5毫升5nhcl以中和任何剩余吡啶。摇动漏斗,并将产物萃取到chcl3中。分离出含产物的chcl3底层并在分液漏斗中用水(加入5毫升5%nahco3溶液以中和任何剩余hcl)洗涤。有机层然后再次用纯蒸馏水洗涤。分离的chcl3层通过旋转蒸发浓缩以获得粗产物。将粗产物溶解在10毫升异丙醇(ipa)中,然后在连续搅拌下逐滴添加到含有200毫升含1%(v/v)meoh的去离子水的烧杯中。作为油分离出产物。该混合物在冰浴中保持20分钟,并滗析顶部水层。将该油溶解在thf中并转移到200毫升圆底烧瓶中。在80℃的最大温度和4毫巴下通过旋转蒸发除去thf以除去所有残留溶剂。所得产物在真空烘箱中在60℃下干燥24小时以产生作为粘稠油的纯化产物(~55%收率)。该纯化产物(二和单取代产物的混合物)通过gpc和对氟的元素分析表征。外观:浅黄色粘稠液体。重均分子量(聚苯乙烯当量)=12389g/mol。pd:1.43。元素分析:f:10.6%。化合物30的理论化学结构显示在图8c中。
化合物31
根据类似于化合物30的程序制备化合物31。用于该合成的玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒的2颈250毫升烘干圆底烧瓶中加入15克(6.0毫摩尔)氢化的羟基封端聚丁二烯(hlbh二醇,mw=2000da)。带有二醇的烧瓶在温和搅拌下在60℃下脱气过夜,然后用干燥n2吹扫接下来的一天。此时,停止加热。向100毫升量筒中装载12毫升无水chcl3,用橡胶隔片密封并用干燥n2吹扫。将chcl3经套管转移到2颈烧瓶中,并剧烈搅拌二醇以溶解在溶剂中。此时,使用塑料注射器将无水吡啶(0.95克,12毫摩尔)添加到hlbh二醇溶液中,并搅拌所得混合物以溶解所有材料。向另一烘干的2颈100毫升烧瓶中装载对苯二甲酰氯(2.57克,13毫摩尔),用橡胶隔片密封,脱气5分钟,然后用n2吹扫。此时,使用量筒和套管加入85毫升无水chcl3以将溶剂转移到100毫升2颈烧瓶中。搅拌所得混合物以溶解对苯二甲酰氯。250毫升2颈烧瓶然后配备加料漏斗,并使用套管将对苯二甲酰氯在chcl3中的溶液转移到加料漏斗中。将经过反应器的n2流调节到缓慢和稳定流量。在室温下经~1小时将对苯二甲酰氯溶液连续逐滴添加到hlbh-吡啶溶液中以形成预聚物。保持在足够速度下搅拌以实现试剂的良好混合。
并行地,向另一烘干的50毫升烧瓶中装载capstonetmal-62全氟化试剂(5.45克,15毫摩尔)。该烧瓶用橡胶隔片密封,脱气15分钟,并用n2吹扫。加入无水chcl3(12毫升)和无水吡啶(0.95克,12毫摩尔)。搅拌该混合物以溶解所有试剂。在对苯二甲酰氯溶液添加到250毫升2颈烧瓶中完成后,在搅拌下将capstonetmal-62全氟化试剂溶液添加到这一烧瓶中。将加料漏斗换成空气冷凝器,并将250毫升2颈烧瓶浸在置于配有热电偶单元的加热器上的油浴中。将温度提高到50℃,并在n2下在此温度下继续反应24小时。
在该反应后,停止加热和搅拌。取出反应烧瓶并将其内容物倒入圆底烧瓶。通过旋转蒸发除去chcl3。在浓缩后,形成致密沉淀物(吡啶盐)。加入thf以溶解产物,并通过使用粗whatman滤纸(no4)过滤除去沉淀的吡啶盐。吡啶盐不溶于thf。通过旋转蒸发除去thf。将粗产物溶解在100毫升chcl3中并倒入分液漏斗。加入100毫升水,接着加入5毫升5nhcl以中和任何剩余吡啶。摇动漏斗,并将产物萃取到chcl3中。分离出含产物的chcl3底层并在分液漏斗中用水(加入5毫升5%nahco3溶液以中和任何剩余hcl)洗涤。有机层然后再次用纯蒸馏水洗涤。分离的chcl3层通过旋转蒸发浓缩以获得粗产物。将粗产物溶解在10毫升异丙醇(ipa)中,然后在连续搅拌下逐滴添加到含有200毫升含1%(v/v)meoh的去离子水的烧杯中。作为油分离出产物。该混合物在冰浴中保持20分钟,并滗析顶部水层。将该油溶解在thf中并转移到200毫升圆底烧瓶中。在80℃的最大温度和4毫巴下通过旋转蒸发除去thf以除去所有残留溶剂。所得产物在真空烘箱中在60℃下干燥24小时以产生作为粘稠油的纯化产物(~87%收率)。该纯化产物(二和单取代产物的混合物)通过gpc和对氟的元素分析表征。外观:灰白色粘稠液体。重均分子量(聚苯乙烯当量)=10757g/mol。pd:1.33。元素分析:f:11.29%。化合物31的理论化学结构显示在图8d中。
化合物32
用于该合成的玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒的2颈100毫升烘干圆底烧瓶中加入10克(5毫摩尔)氢化的羟基封端聚异戊二烯(hhtpi二醇,mw=2000da)。带有二醇的烧瓶在温和搅拌下在60℃下脱气过夜,然后用干燥n2吹扫接下来的一天。此时,停止加热。向100毫升量筒中装载50毫升无水chcl3,用橡胶隔片密封并用干燥n2吹扫。将chcl3经套管转移到2颈烧瓶中,并剧烈搅拌二醇以溶解在溶剂中。此时,使用塑料注射器将过量无水吡啶(0.75克,9毫摩尔)添加到hhtpi二醇溶液中,并搅拌所得混合物以溶解所有材料。向另一烘干的2颈250毫升烧瓶中装载全氟庚酰氯(4.51克,12毫摩尔),用橡胶隔片密封,脱气5分钟,然后用n2吹扫。此时,使用量筒和套管加入22毫升无水chcl3以将溶剂转移到含有全氟庚酰氯的250毫升2颈烧瓶中。所得混合物在室温下搅拌以溶解酰氯。将加料漏斗安装到这一烧瓶上,并将在chcl3中的hhtpi-吡啶溶液添加到加料漏斗中。将经过反应器的n2流调节到缓慢和稳定流量。在室温下经~4小时将hhtpi-吡啶溶液连续逐滴添加到酰氯溶液中。保持在足够速度下搅拌以实现试剂的良好混合。在完成hhtpi二醇的添加后,将加料漏斗换成空气冷凝器,并将2颈烧瓶浸在配有热电偶单元的加热器上的油浴中。将温度提高到50℃,并在n2下在此温度下继续反应24小时。
在该反应后,停止加热和搅拌。取出反应烧瓶并将其内容物倒入圆底烧瓶。通过旋转蒸发除去chcl3。在浓缩后,形成致密沉淀物(吡啶盐)。加入thf以溶解产物,并通过使用粗whatman滤纸(no4)过滤除去沉淀的吡啶盐。吡啶盐不溶于thf。通过旋转蒸发除去thf。将粗产物溶解在100毫升chcl3中并倒入分液漏斗。加入150毫升水,接着加入5毫升5nhcl以中和任何剩余吡啶。摇动漏斗,并将产物萃取到chcl3中。分离出含产物的chcl3底层并在分液漏斗中用水(加入5毫升5%nahco3溶液以中和任何剩余hcl)洗涤。有机层然后再次用纯蒸馏水洗涤。分离的chcl3层通过旋转蒸发浓缩以获得粗产物。将粗产物溶解在10毫升异丙醇(ipa)中并在连续搅拌下逐滴添加到含有200毫升含1%(v/v)meoh的去离子水的1升烧杯中。作为油分离出产物。该混合物在冰浴中保持20分钟,并滗析顶部水层。将该油溶解在thf中并转移到200毫升圆底烧瓶中。在80℃的最大温度和4毫巴下通过旋转蒸发除去thf以除去所有残留溶剂。所得产物在真空烘箱中在60℃下干燥24小时以产生作为无色粘稠油的纯化产物(~99.9%收率)。该纯化产物(二和单取代产物的混合物)通过gpc和对氟的元素分析表征。外观:无色粘稠液体。重均分子量(聚苯乙烯当量)=12622g/mol。pd:1.53。元素分析:f:13.50%。化合物32的理论化学结构显示在图9a中。
化合物33
用于该合成的玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒的2颈1000毫升烘干圆底烧瓶中加入100克(40毫摩尔)氢化的羟基封端聚丁二烯(hlbh二醇,mw=2000da)。带有二醇的烧瓶在温和搅拌下在60℃下脱气过夜,然后用干燥n2吹扫接下来的一天。此时,停止加热。向1000毫升量筒中装载415毫升无水chcl3,用橡胶隔片密封并用干燥n2吹扫。将chcl3经套管转移到2颈烧瓶中,并剧烈搅拌二醇以溶解在溶剂中。使用塑料注射器将过量无水吡啶(19.08克,241毫摩尔)添加到hlbh二醇溶液中,并搅拌所得混合物以溶解所有材料。向另一烘干的2颈1000毫升烧瓶中装载38.45克(101毫摩尔)全氟庚酰氯,用橡胶隔片密封,脱气5分钟,然后用n2吹扫。此时,使用量筒和套管加入277毫升无水chcl3以将溶剂转移到含有全氟庚酰氯的1000毫升2颈烧瓶中。所得混合物在室温下搅拌以溶解酰氯。将加料漏斗安装到这一烧瓶上,并使用套管将在chcl3中的hlbh-吡啶溶液添加到加料漏斗中。将经过反应器的n2流调节到缓慢和稳定流量。在室温下经~4小时开始将hlbh-吡啶溶液连续逐滴添加到酰氯溶液中。保持在足够速度下搅拌以实现试剂的良好混合。在完成hlbh的添加后,将加料漏斗换成空气冷凝器,并将2颈烧瓶浸在配有热电偶单元的加热器上的油浴中。将温度提高到50℃,并在n2下在此温度下继续反应24小时。
在该反应后,停止加热和搅拌。取出反应烧瓶并将其内容物倒入圆底烧瓶。通过旋转蒸发除去chcl3。在浓缩后,形成致密沉淀物(吡啶盐)。加入thf以溶解产物,并通过使用粗whatman滤纸(no4)过滤除去沉淀的吡啶盐。吡啶盐不溶于thf。通过旋转蒸发除去thf。将粗产物溶解在400毫升chcl3中并倒入分液漏斗。加入500毫升水,接着加入20毫升5nhcl以中和任何剩余吡啶。摇动漏斗,并将产物萃取到chcl3中。分离出含产物的chcl3底层并在分液漏斗中用水(加入20毫升5%nahco3溶液以中和任何剩余hcl)洗涤。有机层然后再次用纯蒸馏水洗涤。分离的chcl3层通过旋转蒸发浓缩以获得粗产物。将粗产物溶解在20毫升thf中,然后在连续搅拌下逐滴添加到含有1200毫升含1%(v/v)meoh的去离子水的4升烧杯中。作为油分离出产物。该混合物在冰浴中保持20分钟,并滗析顶部己烷层。将该油溶解在thf中并转移到500毫升圆底烧瓶中。在80℃的最大温度和4毫巴下通过旋转蒸发除去thf以除去所有残留溶剂。所得产物在真空烘箱中在60℃下干燥24小时以产生作为黄色粘稠油的纯化产物(~80%收率)。该纯化产物(二和单取代产物的混合物)通过gpc和对氟的元素分析表征。外观:浅黄色粘稠液体。重均分子量(聚苯乙烯当量)=6099g/mol。pd:1.08。元素分析:f:12.84%。化合物33的理论化学结构显示在图9b中。
化合物34
用于该合成的玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒的2颈1000毫升烘干圆底烧瓶中加入65克(63毫摩尔)ymer-二醇(mw=1000da)。带有二醇的烧瓶在温和搅拌下在60℃下脱气过夜,然后用干燥n2吹扫接下来的一天。此时,停止加热。向1000毫升量筒中装载374毫升无水chcl3,用橡胶隔片密封并用干燥n2吹扫。将chcl3经套管转移到2颈烧瓶中,并剧烈搅拌二醇以溶解在溶剂中。使用塑料注射器将过量无水吡啶(30克,375毫摩尔)添加到ymer-二醇溶液中,搅拌所得物以溶解所有材料。向另一烘干的2颈1000毫升烧瓶中装载59.82克(156毫摩尔)全氟庚酰氯,用橡胶隔片密封,脱气5分钟,然后用n2吹扫。此时使用量筒和套管加入250毫升无水chcl3以将溶剂转移到含有全氟庚酰氯的1000毫升2颈烧瓶中。所得混合物在室温下搅拌以溶解酰氯。将加料漏斗安装到这一烧瓶上,并使用套管将在chcl3中的ymer-二醇-吡啶溶液转移到加料漏斗中。将经过反应器的n2流调节到缓慢和稳定流量。在室温下经~4小时将ymer-二醇-吡啶溶液逐滴连续添加到酰氯溶液中。保持在足够速度下搅拌以实现试剂的良好混合。在完成ymer-二醇-吡啶溶液的添加后,将加料漏斗换成空气冷凝器,并将2颈烧瓶浸在置于配有热电偶单元的加热器上的油浴中。将温度提高到40℃,并在n2下在此温度下继续反应24小时。
在该反应后,停止加热和搅拌。取出反应烧瓶并将内容物倒入圆底烧瓶。通过旋转蒸发除去chcl3。在浓缩后,形成致密沉淀物(吡啶盐)。加入thf以溶解产物。该烧瓶在冰浴中冷却20分钟,此时通过使用粗whatman滤纸(no4)的重力过滤除去沉淀的吡啶盐。吡啶盐不溶于thf。通过旋转蒸发除去thf。将所得粗产物溶解在最少量的异丙醇(ipa)中,并将这一溶液添加到在带有搅拌棒的烧杯中的700毫升己烷中。分离出油。滗析顶层并用200毫升己烷洗涤一次。然后将残留物溶解在200毫升thf中并转移到500毫升圆底烧瓶中。在75℃的最大温度和4毫巴真空下旋转蒸发溶剂以提供油,然后将其转移到广口瓶中。其在真空下在60℃下进一步干燥24小时以产生纯产物,其在室温下冷却时凝固成灰白色蜡状半固体(82%收率)。该纯化产物通过gpc(基于聚苯乙烯标样的分子量)、对氟的元素分析、19fnmr、1hnmr和ftir表征。外观:蜡状半固体。重均分子量(聚苯乙烯当量)=2498g/mol。pd:1.04。元素分析:f:27.79%。19fnmr(cdcl3,400mhz):δppm-81.3(m,cf3),-118.88(m,cf2),-122.37(m,cf2),-123.28(m,cf2),-126(m,cf2)。1hnmr(cdcl3,400mhz):δppm0.83(t,ch3ch2),1.44(q,ch2ch3),3.34(m,ch2),3.51(m,ch2),3.54(m,ch2),4.30(m,ch2coo-)。ftir,纯净(cm-1):2882(ch2),1783(o-c=o,酯),1235,1203,1143,1104(cf3,cf2)。化合物34的理论化学结构显示在图9c中。
化合物35
根据与用于制备化合物34的程序类似的程序制备化合物35。
用于该合成的玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒的2颈1000毫升烘干圆底烧瓶中加入60克(59毫摩尔)ymeroh-三醇(mw=1014da)。带有三醇的烧瓶在温和搅拌下在60℃下脱气过夜,然后用干燥n2吹扫接下来的一天。停止加热。向1000毫升量筒中装载435毫升无水chcl3,用橡胶隔片密封并用干燥n2吹扫。将chcl3液体经套管转移到2颈烧瓶中,并剧烈搅拌三醇以溶解在溶剂中。使用塑料注射器将过量无水吡啶(37克,473毫摩尔)添加到ymeroh-三醇溶液中,搅拌所得混合物以溶解所有材料。向另一烘干的2颈1000毫升烧瓶中装载84.88克(222毫摩尔)全氟庚酰氯,用橡胶隔片密封,脱气5分钟,然后用n2吹扫。使用量筒和套管加入290毫升无水chcl3以将溶剂转移到含有全氟庚酰氯的1000毫升2颈烧瓶中。该混合物在室温下搅拌以溶解酰氯。将加料漏斗安装到这一烧瓶上,并使用套管将在chcl3中的ymeroh-三醇-吡啶溶液转移到加料漏斗中。将经过反应器的n2流调节到缓慢和稳定流量。在室温下经~4小时将ymeroh-三醇-吡啶溶液连续逐滴添加到酰氯溶液中。保持在足够速度下搅拌以实现试剂的良好混合。在完成ymeroh-三醇-吡啶溶液的添加后,将加料漏斗换成空气冷凝器,并将2颈烧瓶浸在置于配有热电偶单元的加热器上的油浴中。将温度提高到40℃,并在n2下在此温度下继续反应24小时。
所得产物以类似于上述化合物7的方式提纯。该提纯涉及旋转蒸发chcl3、加入thf和通过过滤分离吡啶盐。然后在异丙醇(ipa)/己烷中沉淀产物,如上文对化合物7所述洗涤,并在75℃和4毫巴下干燥。也在真空下在60℃下进行最终干燥24小时以产生油(78.2%收率)。该纯化产物通过gpc(基于聚苯乙烯标样的分子量)、对氟的元素分析、19fnmr、1hnmr和ftir表征。外观:浅黄色粘稠油。重均分子量(聚苯乙烯当量)=2321g/mol。pd:1.06。元素分析:f:35.13%。19fnmr(cdcl3,400mhz,ppm):δppm–81.30(m,cf3),-118.90(m,cf2),-122.27(m,cf2),-123.07(m,cf2),-126.62(m,cf2)。1hnmr(cdcl3,400mhz):δppm0.83(t,ch3ch2),1.44(q,ch2ch3),3.34(m,ch2o),3.41(m,ch2’s),3.74(m,ch2),4.30(m,ch2coo-)。ftir,纯净(cm-1):2870(ch2),1780(o-c=o,酯),1235,1202,1141,1103(cf3,cf2)。化合物35的理论化学结构显示在图9d中。
化合物36
根据与用于制备化合物34的程序类似的程序制备化合物36。
用于该合成的玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒的2颈1000毫升烘干圆底烧瓶中加入50克(65毫摩尔)xmer-四醇(mw=771da)。带有四醇的烧瓶在温和搅拌下在60℃下脱气过夜,然后用干燥n2吹扫接下来的一天。停止加热。向1000毫升量筒中装载400毫升无水chcl3,用橡胶隔片密封并用干燥n2吹扫。将chcl3经套管转移到2颈烧瓶中,并剧烈搅拌四醇以溶解在溶剂中。使用塑料注射器将过量无水吡啶(51.30克,649毫摩尔)添加到xmer-四醇溶液中,并搅拌所得混合物以溶解所有材料。向另一烘干的2颈1000毫升烧瓶中装载111.63克(292毫摩尔)全氟庚酰氯,用橡胶隔片密封,脱气5分钟,然后用n2吹扫。使用量筒和套管加入300毫升无水chcl3以将溶剂转移到含有全氟庚酰氯的1000毫升2颈烧瓶中。所得混合物在室温下搅拌以溶解酰氯。将加料漏斗附加到这一烧瓶上,并经套管将在chcl3中的xmer-四醇-吡啶溶液转移到加料漏斗中。将经过反应器的n2流调节到缓慢和稳定流量。在室温下经~4小时将xmer-四醇-吡啶溶液连续逐滴添加到酰氯溶液中。保持在足够速度下搅拌以实现试剂的良好混合。在完成xmer-四醇-吡啶溶液的添加后,将加料漏斗换成空气冷凝器,并将2颈烧瓶浸在置于配有热电偶单元的加热器上的油浴中。将温度提高到40℃,并在n2下在此温度下继续反应24小时。
所得产物以类似于上述化合物7的方式提纯,其中通过旋转蒸发除去chcl3、加入thf和在加入thf后通过过滤分离吡啶盐。然后在异丙醇(ipa)/己烷中沉淀产物,如对化合物7所述洗涤,并在75℃和4毫巴下干燥。也在真空下在60℃下进行最终干燥24小时以产生油(80.9%收率)。该纯化产物通过gpc(基于聚苯乙烯标样的分子量)、对氟的元素分析、19fnmr、1hnmr、ftir和tga表征。外观:浅黄色粘稠油。重均分子量(聚苯乙烯当量)=2410g/mol。pd:1.04。元素分析:f:44.07%。19fnmr(cdcl3,400mhz,ppm):δppm-81.37(m,cf3),-118.89(m,cf2),-122.27(m,cf2),-123.06(m,cf2),-26.64(m,cf2)。1hnmr(cdcl3,400mhz):δppm3.36(m,ch2’s),3.75(m,ch2o),4.39(m,ch2o),4.49(m,ch2coo-)。ftir,纯净(cm-1):2870(ch2),1780(o-c=o,酯),1235,1202,1141,1103(cf3,cf2)。热分解温度(tga),n2,在大约10%(w/w)损失下=327℃。化合物36的理论化学结构显示在图10a中。
化合物37
用于该合成的玻璃器皿在烘箱中在110℃下干燥过夜。将25.04克(9.7毫摩尔)聚乙二醇化聚二甲基硅氧烷二醇(c10-二醇)称入250毫升2颈烧瓶,加热到50℃,并在搅拌下脱气过夜。该二醇然后用n2吹扫并溶解在25毫升无水thf中。向所得混合物中加入在thf中的36毫克羧酸铋催化剂(浓度0.02g/ml),接着加入预先脱气30分钟然后n2吹扫的hmdi二异氰酸酯在thf中的溶液(5.34克,20.4毫摩尔)。使用注射器进行该添加。将反应容器配备空气冷凝器,并使混合物在搅拌下在60℃下反应4小时。在预聚物反应进行的同时,在单独烧瓶中将capstonec6-foh(氟代醇)(8.82克,24.2毫摩尔)脱气15分钟,然后用n2吹扫。将该氟代醇溶解在thf中,并加入另外24毫克在thf中的羧酸铋催化剂。然后经注射器将这一混合物添加到预聚物反应容器中。在添加完成后,允许反应混合物在n2气氛下在45℃下反应过夜。在该反应后,在旋转蒸发器上除去thf溶剂,并将粗制残留物溶解在异丙醇(ipa)中。使用edta溶液(ph~9)萃取铋催化剂残留物。含edta的溶液在1%甲醇溶液-蒸馏水混合物中沉淀以形成粘稠油。滗析水层,残留物在旋转蒸发器中干燥以产生作为琥珀色粘稠液体的产物。在真空下在60℃下进行最终干燥24小时以产生粘稠油(74%收率)。该纯化产物通过gpc(基于聚苯乙烯标样的分子量)、对氟的元素分析和tga表征。外观:琥珀色粘稠油。重均分子量(聚苯乙烯当量)=13583g/mol。pd:1.73。元素分析:f:12.20%。热分解温度(tga),n2,在大约<5%(w/w)损失下=231℃。化合物37的理论化学结构显示在图10b中。
化合物38
根据与用于制备化合物37的程序类似的程序合成化合物38,在提纯工艺中作出一些修改。使25.01克(10.2毫摩尔)c10-二醇与4.29克(16.3毫摩尔)hmdi在thf中在羧酸铋催化剂存在下反应以形成预聚物。该预聚物然后用6.50克(17.9毫摩尔)capstonec6-foh(氟代醇)封端以产生作为粘稠油的产物。在85℃下将这种油溶解在异丙醇中,并用2x15毫升edta(乙二胺四乙酸溶液,ph~9)处理。该聚合物的edta溶液然后在蒸馏水中的1%甲醇溶液中沉淀以形成油,其用沸腾的己烷洗涤一次,然后用室温下的己烷进一步洗涤2x以获得油(66%收率)。该纯化产物通过gpc(基于聚苯乙烯标样的分子量)、对氟的元素分析和tga表征。外观:琥珀色粘稠油。重均分子量(聚苯乙烯当量)=16,278g/mol。pd:1.82。元素分析:f:8.8%。热分解温度(tga),n2,在大约<5%(w/w)损失下=299℃。化合物38的理论化学结构显示在图10c中。
化合物39
通过根据方案2的两步会聚法合成化合物39。简言之,使多异氰酸酯desmodur4470(11.45克,11毫摩尔)与capstonec6-foh(7.65克,21毫摩尔)在无水thf中在羧酸铋催化剂存在下在25℃下反应10分钟。在将氟代醇逐滴添加到多异氰酸酯中后,在40℃下继续搅拌4小时。这些步骤导致形成部分氟化的中间体,其随后与pln8k二醇(40克,5毫摩尔)在70℃下偶联14小时以提供化合物39。由于这些反应对湿敏感,它们在惰性气氛(n2)和无水条件下进行。也小心地保持温度分布,尤其是在部分氟化过程中,以避免不想要的副反应。在反应过程中,反应混合物变得非常粘稠,并且必须保持连续搅拌以防止局部加热。
在该反应后,在旋转蒸发器上蒸发thf溶剂以产生粗产物。该产物通过溶解在氯仿中并加入edta溶液(ph~9.0)来提纯。然后将该混合物转移到分液漏斗,并随水层分离催化剂残留物。将有机层浓缩,将产物溶解在异丙醇中并在己烷中沉淀以产生白色块状固体,其在真空下干燥(66%收率)。该纯化产物通过gpc(基于聚苯乙烯标样的分子量)、对氟的元素分析和tga表征。外观:白色块状固体。重均分子量(聚苯乙烯当量)=31806g/mol。pd:1.32。元素分析:f:3.6%。热分解温度(tga),n2,在大约<5%(w/w)损失下=295℃。化合物39的理论化学结构显示在图10d中。
化合物40
根据与用于制备化合物37的程序类似的程序合成化合物40。因此,使50.0克(5.7毫摩尔)pln8k二醇与4.5克(17.1毫摩尔)hmdi在thf中在羧酸铋催化剂存在下反应以形成预聚物。该预聚物然后用7.28克(20毫摩尔)capstonec6-foh(氟代醇)封端以产生粗产物。edta洗涤以清除催化剂残留物是类似的。通过溶解在异丙醇中并用己烷沉淀来进行最终提纯以产生白色固体(86%收率)。该纯化产物通过gpc(基于聚苯乙烯标样的分子量)、对氟的元素分析和tga表征。外观:白色固体。重均分子量(聚苯乙烯当量)=9253g/mol。pd:1.28。元素分析:f:3.14%。热分解温度(tga),n2,在大约<5%(w/w)损失下=303℃。化合物40的理论化学结构显示在图11a中。
化合物41
根据与用于制备化合物27的程序类似的程序合成化合物41。化合物41的理论化学结构显示在图7c中,只是由c10-二醇形成中间的三嵌段共聚物。
该纯化产物通过gpc(基于聚苯乙烯标样的分子量)、对氟的元素分析和tga表征。外观:无色粘稠液体。重均分子量(聚苯乙烯当量)=5858g/mol。pd:1.21。元素分析:f:18.39%。热分解温度(tga),n2,在大约<10%(w/w)损失下=310℃。
化合物42
用于该合成的所有玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒的2颈1000毫升烘干圆底烧瓶中加入60克(59毫摩尔)ymeroh-二醇(mw=1014da)。该烧瓶在温和搅拌下在60℃下脱气过夜,然后用干燥n2吹扫接下来的一天。停止加热。向1000毫升量筒中装入435毫升无水chcl3,用橡胶隔片密封并用干燥n2吹扫。将chcl3经套管转移到2颈烧瓶中并剧烈搅拌二醇以溶解在溶剂中。使用注射器将过量无水吡啶(37克,473毫摩尔)添加到该溶液中,搅拌以溶解所有材料。向烘干的2颈1000毫升烧瓶中加入84.88克(222毫摩尔)全氟庚酰氯,用橡胶隔片密封,脱气5分钟,然后用n2吹扫。使用量筒和套管加入290毫升无水chcl3,并转移到含有全氟庚酰氯的1000毫升2颈烧瓶中。反应混合物在室温下搅拌以溶解酰氯。使用套管将chcl3转移到加料漏斗中。在室温下经~4小时连续逐滴添加到酰氯溶液中。在完成吡啶溶液的添加后,将反应混合物加热到40℃24小时。
产物以类似于化合物33的方式提纯。产物在ipa/己烷中沉淀,然后在75℃和4毫巴下干燥(78.2%收率)。mw(聚苯乙烯当量)g/mol=2321。pd=1.06。元素分析(原子%f)=35.13。19fnmrcdcl3400mhz(ppm):δ–81.30(m,cf3),-118.90(m,cf2),-122.27(m,cf2),-123.07(m,cf2),-126.62(m,cf2)。1hnmr,cdcl3,400mhz(ppm):δ0.83(t,ch3ch2),1.44(q,ch2ch3),3.34(m,ch2o),3.41(m,ch2’s),3.74(m,ch2),4.30(m,ch2coo-)。ft-ir纯净(cm-1):2870(ch2),1780(o-c=o,酯),1235,1202,1141,1103(cf3,cf2)。化合物42的理论化学结构显示在图11b中。
化合物43
用于该合成的所有玻璃器皿在烘箱中在110℃下干燥过夜。将20克(0.020摩尔)ymeroh三醇(mw=1000da)添加到200毫升2颈烧瓶中,将其脱气过夜,然后用n2吹扫。向配有搅拌棒的500毫升2颈烘干烧瓶中加入21.70克(0.079摩尔)三乙二醇(teg)双氯甲酸酯。将烧瓶脱气15分钟,然后用干燥n2吹扫。在吹扫后,借助套管将62毫升无水甲苯转移到烧瓶中。搅拌teg双氯甲酸酯以溶解在溶剂中。其随后在冰浴下冷却15分钟。向50毫升加料漏斗中加入28.73克(0.079摩尔)capstone62-al氟代醇(1h,1h,2h,2h-全氟-1-辛醇),然后脱气15分钟并用干燥n2吹扫。向这一加料漏斗中加入21毫升无水甲苯,接着7克无水吡啶,并摇动漏斗以溶解所有试剂。将加料漏斗附加到反应烧瓶上并开始将capstone62-al逐滴添加到teg双氯甲酸酯的冷却溶液中直至在~2小时内完成。在添加过程中,使搅拌保持在最低限度。在添加过程中,沉淀出吡啶盐。在冰浴条件下保持温度,并使反应在n2下进行另外10分钟以形成部分氟化的teg双氯甲酸酯-capstone62-al中间体。在部分氟化进行的同时,经套管将无水甲苯(125毫升)添加到含ymeroh三醇的烧瓶中,接着加入6克无水吡啶,并搅拌该混合物以溶解ymeroh三醇。将250毫升加料漏斗附加到含有部分氟化的teg双氯甲酸酯-capstone62-al中间体的500毫升2颈烧瓶上,并将ymeroh-三醇溶液经套管转移到漏斗中。将ymeroh-三醇溶液在冰浴条件下在缓慢连续料流中添加到500毫升容器中,直至加入所有ymeroh-三醇。允许该混合物在n2下在室温下搅拌1小时,然后将温度提高到50℃,并允许反应在搅拌下进行24小时。该反应生成大量白色吡啶盐,其在反应过程中沉淀。所有的添加和转移在干燥n2气氛下进行以避免与空气的任何接触。
该提纯涉及使用whatman滤纸(no4)真空过滤吡啶盐,接着旋转蒸发甲苯。产物用1nhcl处理,并在二氯甲烷-水混合物中萃取以除去过量吡啶,然后用5%nahco3溶液中和。收集底部有机层,用蒸馏水洗涤两次,然后旋转蒸发。粗产物(粘稠油)在250毫升圆底烧瓶中在轻轻摇动下在37℃下用20毫升蒸馏水培养48小时以除去未反应的ymeroh-三醇。该油在二氯甲烷-水混合物中萃取,并在分离后,通过溶解在乙酸乙酯中并在己烷中沉淀而进一步提纯以产生清澈的粘稠油。该纯化产物在75℃和4毫巴下干燥以产生粘稠清澈油(42%收率)。该纯化产物通过gpc和元素分析表征。平均分子量(聚苯乙烯当量)=5083g/mol。多分散性=1.44。元素分析显示%f=11.24%。热分解温度:在5%(w/w)损失下308℃。化合物43的化学结构显示在图11c中。
化合物44
用于该合成的玻璃器皿在烘箱中在110℃下干燥过夜。将84.72克(44.6毫摩尔)聚(乙二醇)-嵌段-聚(丙二醇)-嵌段-聚(乙二醇)(pln二醇)称入250毫升3颈圆底烧瓶,并在真空下在搅拌下脱气过夜。该二醇然后用n2吹扫并溶解在85毫升无水thf中。将10克(59.5毫摩尔)hdi在室温下脱气1小时,并用n2吹扫。将hdi溶解在10毫升thf中,然后添加到pln二醇溶液中。将反应容器配备空气冷凝器,并将混合物加热到50℃。将20毫克dbtdl溶解在1毫升thf中,并在温度达到50℃时将一半的溶液转移到反应混合物中。让反应混合物在65℃下继续4小时。将foh(氟代醇)(11.91克,32.7毫摩尔)脱气30分钟并用n2吹扫。在4小时后,将反应温度冷却到45℃。将foh溶解在12毫升thf中,并添加到反应混合物中。也将另外一半dbtdl溶液添加到反应混合物中。让该反应在45℃下反应过夜。在反应后,在旋转蒸发器上除去溶剂,并将粗产物溶解在120毫升热异丙醇中。然后使用2.5升己烷沉淀聚合物。滗析上清液,该聚合物用100毫升己烷冲洗两次。将该聚合物溶解在thf中,并转移到圆底烧瓶中以便旋转蒸发。该聚合物在真空烘箱中在室温下干燥过夜。聚合物收率为82%。该纯化产物通过gpc和元素分析表征。外观:粘性固体。重均分子量(聚苯乙烯当量)=35,848g/mol。pdi=1.66。元素分析:f:2.3%。第一次起始时的热分解温度=在5%(w/w)损失下289℃。化合物44的理论化学结构显示在图11d中。
化合物45
用于该合成的玻璃器皿在烘箱中在110℃下干燥过夜。将36.21克(19.1毫摩尔)聚(乙二醇)-嵌段-聚(丙二醇)-嵌段-聚(乙二醇)(pln二醇)称入250毫升3颈圆底烧瓶,并在真空下在搅拌下脱气过夜。该二醇然后用n2吹扫并溶解在36毫升无水thf中。将10克(38.1毫摩尔)hmdi在室温下脱气1小时,并用n2吹扫。将hmdi溶解在10毫升thf中,然后添加到pln二醇溶液中。将反应容器配备空气冷凝器,并将混合物加热到50℃。将20毫克dbtdl溶解在1毫升thf中,并在温度达到50℃时将一半的溶液转移到反应混合物中。让反应混合物在65℃下继续4小时。将foh(氟代醇)(15.27克,41.9毫摩尔)脱气30分钟并用n2吹扫。在4小时后,将反应温度冷却到45℃。将foh溶解在thf中,并添加到反应混合物中。也将另外一半dbtdl溶液添加到反应混合物中。允许该反应在45℃下反应过夜。在反应后,在旋转蒸发器上除去溶剂,并将粗产物溶解在100毫升热异丙醇中。然后使用1.5升己烷沉淀聚合物。滗析上清液,该聚合物用80毫升己烷冲洗两次。将该聚合物溶解在thf中,并转移到圆底烧瓶中以便旋转蒸发。该聚合物在真空烘箱中在室温下最终干燥过夜。聚合物收率为73%。该纯化产物通过gpc和元素分析表征。外观:粘稠液体。重均分子量(聚苯乙烯当量)=12,793g/mol。pdi=1.36。元素分析:f:8.1%。热分解温度=在5%(w/w)损失下282℃。化合物45的理论化学结构显示在图12a中。
化合物46
用于该合成的所有玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒的200毫升2颈烘干烧瓶中加入50克(0.048摩尔)ymer二醇(mw=1000da),并在温和搅拌下在60℃下脱气过夜。然后,该ymer二醇用干燥n2吹扫,使用套管将53毫升无水氯仿(chcl3)添加到烧瓶中,接着加入15克无水吡啶。搅拌反应混合物以溶解试剂和获得均匀溶液。向配有搅拌棒的1升2颈烘干烧瓶中加入60.9克(0.221摩尔)三乙二醇(teg)双氯甲酸酯。将烧瓶脱气15分钟,然后用干燥n2吹扫。在吹扫后,借助套管将157毫升无水chcl3转移到烧瓶中。搅拌teg双氯甲酸酯以溶解在溶剂中。向500毫升2颈烧瓶中加入73.59克(0.202摩尔)capstone62-al氟代醇(1h,1h,2h,2h-全氟-1-辛醇),然后脱气15分钟并用干燥n2吹扫。向其中加入314毫升无水chcl3,接着加入28克吡啶。搅拌烧瓶以溶解所有试剂。使用套管将capstone62-al氟代醇溶液转移到预先脱气并用n2吹扫的500毫升加料漏斗中。将加料漏斗附加到在冰浴中冷却的含有teg双氯甲酸酯溶液的1升反应容器中。在n2下逐滴进行氟代醇的添加1小时。在反应过程中使搅拌保持在最低限度,以形成部分氟化的teg双氯甲酸酯-capstone62-al氟代醇中间体。接着,使用20口径(gauge)套管在缓慢连续料流中将ymer二醇溶液转移到1升反应容器中,同时在冰浴下冷却反应容器直至已加入所有ymer二醇溶液。移除冰浴并允许该反应在室温下继续进行另外10分钟。然后将温度提高到50℃并允许该反应运行过夜。所有的添加和转移在干燥n2气氛下进行以避免与空气的任何接触。
通过首先在旋转蒸发器上除去chcl3溶剂,将粗产物溶解在最少thf中并用冰浴冷却20分钟以沉淀吡啶盐,提纯粗产物。真空过滤该溶液并使用旋转蒸发器蒸发thf。产物用1nhcl处理并在二氯甲烷-水混合物中萃取以除去过量吡啶,然后用1nnaoh溶液中和。收集底部有机层,用蒸馏水洗涤两次,然后旋转蒸发。最后,将产物溶解在最少异丙醇(ipa)中,在己烷中沉淀出,用己烷洗涤2x,并在真空下干燥。该产物在真空烘箱中在60℃下干燥过夜以产生作为粘稠液体的产物(59%收率)。该纯化产物通过gpc(基于聚苯乙烯标样的分子量)和对氟的元素分析表征。平均分子量(聚苯乙烯当量)为3422g/mol。多分散性=1.15。元素分析:f=19%。热分解温度(tga,在n2下,第一次起始时:203℃(在5重量%损失下)。化合物46的化学结构显示在图12b中。
化合物47
用于该合成的所有玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒的200毫升2颈烧瓶中加入12克(0.016摩尔)xmer四醇(mw=771da),在温和搅拌下在60℃下脱气过夜,然后用n2吹扫。向配有搅拌棒的500毫升2颈烘干烧瓶中加入9克(0.033摩尔)三乙二醇(teg)双氯甲酸酯。将烧瓶脱气15分钟,然后用干燥n2吹扫。在吹扫后,借助注射器将65毫升无水chcl3转移到烧瓶中。搅拌teg双氯甲酸酯以溶解在溶剂中。向50毫升加料漏斗中加入15克(0.033摩尔)capstone62-al氟代醇(1h,1h,2h,2h-全氟-1-辛醇),脱气15分钟并用干燥n2吹扫。向这一加料漏斗中加入20毫升无水chcl3,接着加入3克无水吡啶,并摇动烧瓶以溶解所有试剂。将加料漏斗附加到在冰中冷却的500毫升反应烧瓶中并将capstone62-al氟代醇逐滴添加到teg双氯甲酸酯中。该添加花费1小时完成,并允许该反应在n2气氛下在室温(25℃)下继续进行另外10分钟以形成部分氟化的teg双氯甲酸酯-capstone62-al中间体。在部分氟化进行的同时,将无水chcl3(122毫升)经套管添加到含xmer四醇的烧瓶中,接着加入2.5克无水吡啶,并搅拌该混合物以溶解试剂。接着,使用20口径套管在缓慢连续料流中将xmer四醇溶液转移到500毫升反应容器中,同时在冰浴中冷却反应容器直至已加入所有xmer四醇溶液。移除冰浴并允许该反应在室温下继续进行另外10分钟。然后将温度提高到50℃并允许该反应运行过夜。所有的添加和转移在干燥n2气氛下进行以避免与空气的任何接触。
该提纯涉及从反应混合物中旋转蒸发chcl3、加入thf和通过真空过滤分离吡啶盐。产物用1nhcl处理并在二氯甲烷-水混合物中萃取以除去过量吡啶,然后用1nnaoh溶液中和。收集底部有机层,进一步用蒸馏水洗涤两次,然后旋转蒸发。最后,将产物溶解在最少异丙醇(ipa)中,在己烷中沉淀出,用己烷洗涤2x,并在真空下干燥。该产物在真空烘箱中在60℃下干燥过夜以产生作为粘稠液体的产物(59%收率)。
该纯化产物通过gpc(基于聚苯乙烯标样的分子量)和对氟的元素分析表征。平均分子量(聚苯乙烯当量)为2322g/mol。多分散性=1.12。元素分析显示f=25.8%。热分解温度(tga,在n2下),第一次起始时:221℃(在10重量%损失下)。化合物47的化学结构显示在图13c中。
化合物48
用于该合成的所有玻璃器皿在烘箱中在110℃下干燥过夜。向配有搅拌棒的100毫升2颈烘干烧瓶中加入15克(0.008摩尔)pdp二醇(mw=2000da),并在温和搅拌下在60℃下脱气过夜。然后该pdp二醇用干燥n2吹扫,使用套管将90毫升无水chcl3转移到烧瓶中,接着2克无水吡啶。搅拌反应混合物以溶解并获得均匀溶液。向50毫升烘干的加料漏斗中加入5.63克(0.016摩尔)双酚a氯甲酸酯,将漏斗脱气15分钟,然后用干燥n2吹扫。在吹扫后,借助套管将45毫升无水chcl3转移到漏斗中。摇动漏斗以溶解氯甲酸酯。将加料漏斗附加到含有pdp二醇的烧瓶中并在室温下经1小时逐滴加入双酚a氯甲酸酯。允许该反应进行3小时,以形成pdp-双酚a预聚物中间体。在预聚物中间体反应运行的同时,将7克(0.019摩尔)capstone62-al氟代醇添加到50毫升2颈烧瓶中。将烧瓶脱气15分钟,然后在干燥n2下吹扫。在用n2吹扫后,将15毫升无水chcl3添加到烧瓶中,接着加入2克吡啶。摇动烧瓶以溶解氟代醇,然后使用套管在缓慢连续料流中将其添加到含有预聚物中间体的200毫升烧瓶中。将温度提高到60℃并允许最终封端反应进行过夜。通过将chcl3反应混合物倒入含有去离子水的分液漏斗中而提纯产物,水层用5nhcl酸化以中和任何残留吡啶。
将产物萃取到用1nnaoh溶液中和的有机层中并用去离子水洗涤2x。有机层经无水na2so4干燥。在旋转蒸发器上除去溶剂,将固体残留物溶解在thf中并在3:1水/甲醇混合物中沉淀。产物在真空烘箱(30毫巴)中干燥2天以产生固体。该纯化产物通过gpc(基于聚苯乙烯标样的分子量)表征。平均分子量(聚苯乙烯当量)为20704g/mol。多分散性=1.52。元素分析显示4.20重量%f,热分解温度(tga,在n2下),第一次起始时:314℃(在5重量%损失下)。化合物48的化学结构显示在图12d中。
化合物49-57
化合物49-57可使用与对化合物1-48描述的方法类似的方法合成。
实施例2:在pbs中培养2小时后在聚氨酯(pu)棒上的细菌粘附
使用实验室微型混料机制备用于细菌粘附分析的含有1-2重量%本发明的化合物的聚氨酯棒。具体地,来自lubrizol的carbothane3585a(cb85a)聚氨酯树脂在真空烘箱中在60℃下干燥4小时。使用15mldsm双螺杆微型混料机以分批模式在3-5分钟的周期时间(在树脂加载后)和215-225℃的熔体温度下将该树脂与本发明的不同化合物共混。通过打开混合室阀以释放熔融聚合物,将该共混物挤出成直径大约3.5mm的棒。所得棒在水浴中淬火并晾干。
将棒样品切割成1.5cm段,环氧乙烷灭菌并置于无菌微量离心管中。菌株在brainheartinfusion(bhi)肉汤中在37℃下在摇动下生长过夜。为了制备细菌接种液,将细菌培养物在4,000rpm下离心10分钟,用pbs洗涤并以108集落形成单位/ml(cfu/ml)的浓度再悬浮在pbs中。下列菌株用于测试:表皮葡萄球菌3399、金黄色葡萄球菌newman、粪肠球菌33186、大肠杆菌gr-12、肺炎杆菌280、铜绿假单胞菌ak-1和奇异变形杆菌296。也用真菌菌株白色念珠菌atcc28367进行测试,其在bhi中在30℃下在摇动下生长过夜并如上所述洗涤/再悬浮在pbs中。所有微生物菌株获自lawsonhealthresearchinstitute(伦敦,ontario),并且除表皮葡萄球菌和粪肠球菌外的所有菌株是来自人类感染的临床分离菌(血液、尿道或其它)。
将1毫升(1ml)接种液吸移到含有样品的微量离心管中并在最低限度的搅动下在37℃下培养2小时。在2小时后,样品用500μlpbs洗涤3x以除去松散附着的细菌并用1毫升pbs转移到新的微量离心管。将样品声处理30分钟,接着涡流处理30秒,以分离附着的细菌。将声处理过的溶液连续稀释并滴板在琼脂平板上。将平板在37℃下培养过夜,此后计数细菌菌落并以cfu/cm2计算细菌粘附。
对各微生物进行至少两次重复实验,其中n=3个棒样品,且数据显示在图14-15中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。图16是显示来自图14和15的累积数据的概要图。图17是显示来自图14和15的累积数据的概要图,但将添加剂改性样品上的平均粘附归一化为对照物上的平均粘附。这一图表能够容易地查看添加剂改性样品上的粘附减少百分比。
与未改性对照物相比添加剂改性样品上的细菌粘附减少为0至大约3log(99.9%),取决于添加剂配方和受试细菌物种。
实施例3:在pbs中培养2小时后在含化合物41的pu棒上的金黄色葡萄球菌粘附
如实施例2中所述制备棒并用金黄色葡萄球菌newman接种液在37℃下培养2小时。在2小时后,样品用500μlpbs洗涤3x以除去松散附着的细菌。然后将样品转移到含有2%戊二醛/二甲胂酸盐缓冲液的微量离心管中并在4℃下固定过夜。在固定后,样品在分级乙醇溶液(例如50%、70%、90%和100%)中脱水10分钟,通过浸泡在六甲基二硅氮烷中10分钟干燥,接着晾干过夜。
使用双面胶碳标签将干燥样品一式三份安装在铝sem支脚上,溅射涂布金,并在具有二次电子检测器的hitachisu3500sem上成像。使用10kv的加速电压、30的点密度和15mm的工作距离。未改性pu对照物和用1%化合物41改性的pu的三个复制棒在500x放大率下的代表性图像显示在图18中。在未改性pu对照样品上可见高浓度的粘附金黄色葡萄球菌(浅灰色球形结构),作为独立细菌或聚集体存在。相反,在添加剂改性表面上观察到很少的金黄色葡萄球菌。
实施例4:在pbs中培养2小时后在pu棒上的细菌粘附
使用实施例2中描述的方法制备具有除实施例2中给出的那些外的另外化合物的聚氨酯棒。
将棒样品切割成1.5cm段,环氧乙烷灭菌并置于无菌微量离心管中。菌株在trypticsoybroth(tsb)中在37℃下在摇动下生长过夜。为了制备细菌接种液,将细菌培养物在4,500rpm下离心10分钟,用pbs洗涤并以108cfu/ml的浓度再悬浮在pbs中。下列菌株用于测试:表皮葡萄球菌3399、金黄色葡萄球菌newman、大肠杆菌67、铜绿假单胞菌ak-1和奇异变形杆菌296。所有微生物菌株获自lawsonhealthresearchinstitute(伦敦,ontario),并且除表皮葡萄球菌外的所有菌株是来自人类感染的临床分离菌(血液、尿道或其它)。
将1毫升(1ml)接种液吸移到含有样品的微量离心管中并在最低限度的搅动下在37℃下培养2小时。在2小时后,样品用750μlpbs洗涤3x以除去松散附着的细菌并用1毫升pbs转移到新的微量离心管。将样品声处理30分钟,接着涡流处理30秒,以分离附着的细菌。将声处理过的溶液连续稀释并一式四份滴板在trypticsoybroth(tsb)琼脂平板上。将平板在37℃下培养过夜,此后计数细菌菌落并以cfu/cm2计算细菌粘附。
对各菌株进行两个重复实验,n=3个棒样品,且数据显示在图19中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。与未改性对照物相比添加剂改性样品上的细菌粘附减少为0至大约3.5log(>99.9%),取决于添加剂配方和受试细菌物种。
来自图14、15和19的含化合物22的pu棒的粘附数据汇集在图20中的概要图中,其中误差条代表标准误差。这一图表显示添加剂化合物22在减少革兰氏阳性和革兰氏阴性细菌物种以及真菌微生物的粘附方面的广谱效力。
实施例5:在人工尿液和人类汇集尿液中培养2小时后在含化合物22的pu棒上的细菌粘附
如实施例2中所述制备含2重量%添加剂化合物22的聚氨酯棒。
根据文献中描述的配方制备人工尿液(au)(mcleanrj等人,aninvitroultrastructuralstudyofinfectiouskidneystonegenesis,infectionandimmunity,1985,第49卷(3):第805-811页)。从三位健康志愿者中收集并汇集人类尿液(hu)。au和hu都过滤灭菌,储存在4℃,并在制备或收集的一周内使用。使用实施例4中描述的方法进行细菌粘附测试,在au或hu中以108cfu/ml制备细菌接种液。尿路感染中盛行的病原体的代表性菌株(大肠杆菌67、粪肠球菌33186和奇异变形杆菌296)用于测试。
对各菌株进行两次重复实验,n=3个棒样品,且数据显示在图21中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。在au和hu中都在添加剂改性样品上观察到与未改性对照物相比最多大约2log(99%)的尿路病原体粘附减少。
实施例6:在人类汇集尿液中培养12小时后在pu棒上的大肠杆菌粘附
如实施例2中所述制备含2重量%添加剂化合物22、38和39的聚氨酯棒。
从三位健康志愿者中收集并汇集用于细菌粘附实验的人类尿液(hu)。将hu过滤灭菌,储存在4℃,并在收集的一周内使用。使用实施例4中描述的方法进行测试,使用临床尿路病原体大肠杆菌菌株(大肠杆菌67)在hu中以106cfu/ml制备细菌接种液。
进行两个重复实验,n=3个棒样品,且数据显示在图22中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。与未改性对照物相比在添加剂改性表面上观察到大约1-2log(90-99%)的大肠杆菌粘附减少。
实施例7:在人类汇集尿液中在含化合物22的pu棒上的长时间大肠杆菌粘附研究(最多7天)
如实施例2中所述制备含2重量%添加剂化合物22的聚氨酯棒。将用于测试的棒样品切割成1.5cm段,环氧乙烷灭菌并置于无菌微量离心管中。
从三位健康志愿者中收集并汇集用于细菌粘附实验的人类尿液(hu)。将hu过滤灭菌,储存在4℃,并在收集的一周内使用。使用实施例4中描述的方法在hu中以106cfu/ml制备临床尿路病原体大肠杆菌菌株(大肠杆菌67)的接种液。将1毫升(1ml)接种液添加到含有样品的微量离心管中并将样品在最低限度的搅动下在37℃下培养24小时。在24小时后,样品用750μlpbs洗涤3x并用1毫升无菌hu转移到新的微量离心管。继续培养最多7天,每天洗涤样品和更换hu。在1、3和7天后使用实施例4中描述的方法测定样品上的细菌粘附。
进行两个重复实验,n=4个棒样品,在实验#1中在1、3和7天和在实验#2中仅在7天分析。数据显示在图23中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。在1和3天与未改性对照物相比在添加剂改性表面上观察到大约2log(99%)的大肠杆菌粘附减少,但到第7天该减少减弱。减弱的效力可能是由于体外实验条件,如有限的培养基更换和流动,并且可能不反映体内或临床性能。
实施例8:在人类汇集尿液相对于meullerhinton肉汤中在含化合物22的pu棒上的长时间大肠杆菌粘附研究(8天)
如实施例2中所述制备含2重量%添加剂化合物22的聚氨酯棒。将用于测试的棒样品切割成1.5cm段,环氧乙烷灭菌并置于无菌微量离心管中。
从三位健康志愿者中收集并汇集用于细菌粘附实验的人类尿液(hu)。将hu过滤灭菌,储存在4℃,并在收集的一周内使用。使用实施例4中描述的方法在hu或meullerhintonbroth(mhb)细菌生长培养基中以106cfu/ml制备临床尿路病原体大肠杆菌菌株(大肠杆菌67)的接种液。将1毫升(1ml)接种液添加到含有样品的微量离心管中并将样品在最低限度的搅动下在37℃下培养24小时。在24小时后,样品用750μlpbs洗涤3x并用1毫升无菌hu或mhb转移到新的微量离心管。继续培养最多7天,每天洗涤样品和更换hu或培养基。在7天后使用实施例4中描述的方法测定样品上的细菌粘附。
进行两次重复实验,n=4个棒样品,且数据显示在图24中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。在mhb中培养8天后与未改性对照物相比在添加剂改性样品上观察到大肠杆菌粘附的大约3log(99.9%)减少,而在这一实验的条件下在人类汇集尿液中培养8天后没有观察到减少。这证实实验条件对体外细菌-表面相互作用的不同影响。
实施例9:在人类汇集尿液中培养24小时后在含化合物22的pu棒上的大肠杆菌粘附的sem成像
如实施例2中所述制备含2重量%添加剂化合物22的聚氨酯棒。将用于测试的棒样品切割成1.5cm段,环氧乙烷灭菌并置于无菌微量离心管中。
从三位健康志愿者中收集并汇集用于细菌粘附实验的人类尿液(hu)。将hu过滤灭菌,储存在4℃,并在收集的一周内使用。使用实施例4中描述的方法在hu中以106cfu/ml制备临床尿路病原体大肠杆菌菌株(大肠杆菌67)的接种液。将1毫升(1ml)接种液添加到含有样品的微量离心管中并将样品在最低限度的搅动下在37℃下培养12小时。在12小时后,样品用750μlpbs洗涤3x并用1毫升无菌hu转移到新的微量离心管。样品37℃下进一步培养另外12小时。此后,样品用750μlpbs洗涤3x并转移到含有2%戊二醛/二甲胂酸盐缓冲液的微量离心管中以在4℃下固定过夜。在固定后,样品在分级乙醇溶液(例如50%、70%、90%和100%)中脱水10分钟,然后通过浸泡在六甲基二硅氮烷中10分钟干燥,接着晾干过夜。
使用双面胶碳标签将干燥样品一式三份安装在铝sem支脚上,溅射涂布金,并在具有二次电子检测器的hitachisu3500sem上成像。使用10kv的加速电压和5mm的工作距离。未改性pu对照物和用2%化合物22改性的pu的三个复制棒在500x放大率下的代表性图像显示在图25中。在未改性pu对照样品上可见高浓度的粘附大肠杆菌(浅灰色杆形结构),作为独立细菌或聚集体存在。相反,在添加剂改性表面上观察到很少的大肠杆菌。
实施例10:在临床尿液中培养24小时后在含化合物22的pu导管上的细菌粘附
通过首先使用商业方法将添加剂化合物22以2%载量配混到carbothane3595a(cb95a)聚氨酯树脂中,制备用于测试的聚氨酯导管。然后使用商业方法将原始cb95a树脂和与化合物22配混的cb95a树脂都挤出成7f管材(外径=2.4mm;内径=1.5mm)。
从具有留置输尿管支架的患者中收集临床尿液样品并储存在4℃直至使用。五百(500μl)各样品在摇动下在37℃下培养24小时,然后接种至培养板以计数总浮游细菌。表现出细菌生长的尿液样品(>2.0x103cfu/ml)用于聚氨酯管材样品的细菌粘附测试。如从培养板上观察到,几个尿液样品含有多个菌株。
将管样品切割成1.0cm段,环氧乙烷灭菌并置于无菌微量离心管中。将五百(500μl)临床尿液添加到含有样品的微量离心管中并将样品在最低限度的搅动下在37℃下培养24小时。在24小时后,使用实施例4中描述的方法量化样品上的细菌粘附。
对各临床尿液样品进行2或3个重复实验,n=3个棒样品,且数据显示在图26中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。在各临床尿液样品中观察到的大菌落类型的数量用(+)符号标示。在受试的8/9尿液临床尿液样品中在添加剂改性样品上观察到统计显著的细菌粘附减少。
实施例11:在人工尿液和人类汇集尿液中培养24小时后在含化合物22的pu导管上的大肠杆菌粘附
通过首先使用商业方法将添加剂化合物22以2%载量配混到carbothane3595a(cb95a)聚氨酯树脂中,制备用于测试的聚氨酯导管。然后使用商业方法将原始cb95a树脂和与化合物22配混的cb95a树脂都挤出成7f管材(外径=2.4mm;内径=1.5mm)。
根据文献中描述的配方制备人工尿液(au)(mcleanrj等人,aninvitroultrastructuralstudyofinfectiouskidneystonegenesis,infectionandimmunity,1985,第49卷(3):第805-811页)。从三位健康志愿者中收集并汇集人类尿液(hu)。au和hu都过滤灭菌,储存在4℃,并在制备或收集的一周内使用。使用实施例4中描述的方法进行细菌粘附测试,使用长度1.5cm的管材样品和在au或hu中以106cfu/ml制备的细菌接种液。
在hu中进行n=3个管材样品的一个实验并在au中进行n=3个样品的两次重复实验。结果显示在图27中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。在au和hu中都在24小时培养后在添加剂改性导管上观察到与未改性对照管材相比大约2-3log(99-99.9%)的大肠杆菌粘附减少。
实施例12:在流动条件下在含化合物22的pu导管上的大肠杆菌粘附
通过首先使用商业方法将添加剂化合物22以2%载量配混到carbothane3595a(cb95a)聚氨酯树脂中,制备用于测试的聚氨酯导管。然后使用商业方法将原始cb95a树脂和与化合物22配混的cb95a树脂都挤出成7f管材(外径=2.4mm;内径=1.5mm)。
如图28中描绘布置用于在流动条件下的细菌粘附测试的再循环系统。该系统由含接种液的储器组成,使用蠕动泵使接种液循环经过试验回路。各试验回路由经有机硅泵管件(长度=18“,内径=1.65mm)连接的两个长20”的试验管件组成。将各回路的入口管头浸没在接种液中,同时出口端头悬挂在接种液上方。将储器保存在37℃水浴中并保持对环境密封。每个实验测试一个未改性对照管回路和一个添加剂改性的管回路并且两个回路都由相同的接种液储器供料。
再循环流动系统的所有组件通过高压釜或环氧乙烷灭菌。根据文献中描述的配方制备人工尿液(au)(mcleanrj等人,aninvitroultrastructuralstudyofinfectiouskidneystonegenesis,infectionandimmunity,1985,第49卷(3):第805-811页)。将au过滤灭菌并保存在4℃直至使用。临床尿路病原体大肠杆菌菌株(大肠杆菌67)在trypticsoybroth(tsb)中在37℃下在摇动下生长过夜。为了制备细菌接种液,将细菌培养物在4,500rpm下离心10分钟,洗涤并以106cfu/ml的浓度再悬浮在au中。
在实验开始时,将含无菌au的储器连接到流动系统并使无菌au以0.5ml/min循环经过试验回路10分钟以预调节管件和确认流量。在10分钟后,将干净的au储器换成含有使用磁搅拌棒连续搅拌的300毫升大肠杆菌接种液的储器。接种液以0.5ml/min循环经过试验回路24小时。
在24小时后,停止泵并从回路中排出接种液。从各试验回路的远端部分(在泵管下游)切割长度为1.5厘米的四个试验管材样品。使用实施例4中描述的方法测定样品上的细菌粘附。进行重复实验且在流动下的细菌粘附数据与相同类型样品和相同培养基/时间框架在静态条件下的粘附一起(数据取自实施例11)呈现在图29中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。
在流动存在下,观察到添加剂改性样品相对于未改性对照物上的细菌粘附减少与静态条件相比进一步放大。具体而言,在流动条件下在添加剂改性管材上观察到大约4log(99.99%)的减少。通过sem成像进一步证实细菌粘附的数量减少。
实施例13:在含化合物22的pu输尿管支架原型上的体内兔子研究
进行初步体内研究以评估用本发明的实施例添加剂进行医疗器材表面改性对防止在细菌暴露后建立感染的潜力。使用兔尿路感染模型进行使用输尿管支架(置入输尿管中的管材以预防或治疗来自肾的尿流的阻塞)作为模型器材的研究。结果测量包括在研究全程的尿细菌计数和在移出后在器材表面上的细菌粘附。
为了制备原型,首先使用商业方法将添加剂化合物22以2%载量配混到carbothane3595a(cb95a)聚氨酯树脂中。然后使用商业方法将原始cb95a树脂和与化合物22配混的cb95a树脂都挤出成7f管材(外径=2.4mm;内径=1.5mm)。将挤出的管材切成大约12厘米长的段并将每段的一端热成型成直径1.0厘米的猪尾形卷以产生输尿管支架原型。在该研究中使用图30中所示的由大约5厘米长的管材组成的原型的支架卷曲部分。
将用于测试的所有器件eto灭菌。使用兔尿路病原体大肠杆菌菌株(we6933)引发兔子的感染。为了制备细菌接种物,菌株在trypticsoybroth(tsb)中在37℃下在摇动下生长过夜。然后将细菌培养物在4,500rpm下离心10分钟,洗涤并以107cfu/ml的浓度再悬浮在盐水中。
将支架卷曲经尿道置入全身麻醉下的newzealandwhite兔的膀胱中。具体而言,借助超声将6fr导管导入膀胱,柔性尖端导丝隧穿其中。取出导管,且支架弯曲段置于导丝上并使用导管作为推杆置入膀胱中。移除导丝,排空膀胱,并经导管在膀胱中注入1.5毫升细菌接种物,接着用0.5毫升无菌盐水冲洗。取出导管并使用超声确认支架弯曲在膀胱中的位置。兔子从麻醉中苏醒并在该研究的持续期间(7天)在独立笼子中用标准饮食和随意提供的水饲养。
在临安置器件前,和此后在1、3、5和7天时在镇静作用下,通过膀胱穿刺术从各兔子的膀胱中收集尿液。将兔尿的样品滴加和铺板在lb琼脂平板上并在37℃下培养24小时,此后计数菌落以测定以cfus/ml计的尿液大肠杆菌浓度。在第7天,将兔子安乐死并收回支架卷曲以进行细菌粘附分析。发现从膀胱中取出的支架卷曲被覆盖在结壳沉积物中,这在兔子模型中常见,因为兔尿已知容易形成沉淀物。为了将附着于器材表面的细菌与截留在表面沉积物中的细菌分离,将样品加工成2部分:(1)将各支架卷曲切成1厘米段并从各段轻轻剥落/刮下结壳沉积物到微量离心管中;和(2)将剩下的管段置于单独的微量离心管中。将1毫升pbs添加到各微量离心管中并声处理样品以打碎结壳沉积物并分离附着/聚集的细菌。使用实施例4中描述的方法进行加工该溶液以便进行cfu计数。
与植入未改性对照物的兔子相比,在植入添加剂改性的支架卷曲的兔子中观察到大肠杆菌尿浓度降低的趋势(在第5和7天~2log或99%减少)。总体而言,粘附于支架卷曲表面的大肠杆菌,包括截留在结壳沉积物中的细菌,在添加剂改性的支架卷曲上与未改性对照物相比减少~1log(90%)。仅就粘附于支架卷曲表面的大肠杆菌而言,不包括截留在结壳沉积物中的细菌,在添加剂改性的支架卷曲上与未改性对照物相比减少~3.5log(99.9%)。由于分析的器材数量少,无法对数据进行统计分析。
实施例14:在外部抗生素暴露后在含化合物22的pu棒上的细菌粘附(抗生素敏感性的体外测试)
植入的医疗器材在临床实践中通常与局部或全身给药的抗生素结合使用以防止细菌感染的发作或持续。有意义的是评估添加剂改性表面是否可影响控制细菌和生物膜的生长和粘附所需的外部施加抗生素的量,并因此有助于限制临床感染率。
使用实施例2中描述的方法制备含2%添加剂制剂22的聚氨酯棒。将棒样品切割成1.5cm段,环氧乙烷灭菌并置于无菌微量离心管中。
临床尿路病原体大肠杆菌菌株(大肠杆菌67)在meullerhintonbroth(mhb)中在37℃下在摇动下生长过夜。为了制备细菌接种液,将细菌培养物在4,500rpm下离心10分钟,洗涤并以106cfu/ml的浓度再悬浮在新鲜mhb中。将1毫升接种液添加到含样品的微量离心管中并将样品在最低限度的搅动下在37℃下培养24小时。在24小时后,样品用750μlpbs洗涤3x并用1毫升无菌mhb转移到新的微量离心管。继续培养7天,每天洗涤样品和更换mhb。在7天后,将棒样品洗涤并转移到具有1毫升以各种浓度(0-0.5μg/ml)在mhb中的环丙沙星抗生素溶液的微量离心管中。棒在环丙沙星溶液中培养24小时,此后将它们洗涤并根据实施例4中描述的方法量化棒上的细菌粘附。
在各环丙沙星浓度下进行2个实验,n=2测试2个棒,且结果显示在图31中。与未改性对照物相比,在添加剂改性样品上实现完全细菌杀灭所需的环丙沙星抗生素的浓度较低,表明改性表面可影响在器材上定殖的细菌对外部施加抗生素的敏感性。但是,不清楚这一效应是该表面直接影响细菌的毒力因子的结果还是只是该表面限制细菌粘附(因此只需较少抗生素就可生效)的能力的结果。
实施例15:有机硅棒上的细菌粘附
在实验室中使用模拟商业有机硅挤出或模制法的方法制备用于细菌粘附测试的有机硅棒表型。医疗等级双组分固化有机硅弹性体med-4780和med-4765获自nusil。等量供应的组分a和组分b化合物单独使用在玻璃表面上的teflon涂布滚动棍或双辊磨软化。然后使用相同设备通过反复捏合运动将添加剂化合物共混到组分a中。然后将组分a共混物进一步与等质量的组分b共混直至制成含有2或4重量%添加剂载量(取决于所用制剂)的充分混合的树脂。
将该共混物填充到塑料注射器中并使用注射器泵以0.2-0.3ml/min的速度模拟挤出成圆柱棒结构。挤出的棒在空气流烘箱中在116℃下固化20分钟。
将棒样品切割成1.5厘米段并使用实施例4中描述的方法在pbs或人类汇集尿液(hu)中测试细菌粘附。从三位健康志愿者中收集并汇集用于实验的hu,过滤灭菌,储存在4℃,并在收集的一周内使用。下列菌株用于测试:表皮葡萄球菌atcc35984、金黄色葡萄球菌newman、粪肠球菌33186、大肠杆菌67、铜绿假单胞菌ak-1、肺炎杆菌280和奇异变形杆菌296。所有微生物菌株获自lawsonhealthresearchinstitute(伦敦,ontario),并且除粪肠球菌外的所有菌株是来自人类感染的临床分离菌(血液、尿道或其它)。在108cfu/ml(2h实验)或106cfu/ml(>24h实验)下制备接种液。对于延长到超过24小时的实验,如实施例7中所述每24小时进行样品洗涤和培养基更换。
对各菌株进行两个重复实验,n=3个棒样品,且评估条件和数据显示在图32-36中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。在pbs和hu中在2小时与未改性对照物相比在添加剂改性样品上观察到最多3log(99.9%)的细菌粘附减少,取决于受试制剂和细菌。对于三种受试细菌(大肠杆菌、铜绿假单胞菌、粪肠球菌)在hu中在24小时保持最多2log(99%)减少。仅用大肠杆菌进行长时间研究并在体外实验的条件下在第3天减少减弱。
图36描绘了显示化合物43在2小时的细菌粘附的累计图。这一图表证实添加剂化合物43在减少有机硅表面上的革兰氏阳性和革兰氏阴性细菌物种粘附方面的广谱效力。
实施例16:在稀释血浆或血清中培养24小时后在含化合物22的pu棒上的金黄色葡萄球菌粘附
某些医疗器材与含有各种量的蛋白质的生物流体接触(例如与血液接触的血管内导管),蛋白质可附着于器材表面并影响细菌粘附。因此,有意义的是评估添加剂改性表面是否可在含蛋白质的流体存在下抗细菌粘附。对于体外测试,使用在pbs中稀释并补充了tsb生长培养基的血浆或血清以代表血液,因为其含有相同蛋白质。
使用实施例2中描述的方法制备含2%添加剂化合物22的聚氨酯棒。将棒样品切割成1.5cm段,环氧乙烷灭菌并使用实施例4中描述的方法在24h细菌粘附测定中测试。金黄色葡萄球菌newman菌株获自lawsonhealthresearchinstitute(伦敦,ontario)。新鲜人类血浆(汇集自至少3位供体并用acd或柠檬酸钠抗凝血)和新鲜汇集的血清获自biochemedservices(winchester,va)。制备接种液以在50%pbs、25%tsb生长培养基和25%血浆或血清的混合物中含有106cfu/ml细菌。通过在100%血浆中培养2小时以允许蛋白质粘附而预调节棒样品,然后转移到接种液中以培养24小时。
用n=3个棒样品进行的实验的结果显示在图37中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。在稀释血浆或血清中培养24小时后与未改性对照物相比在添加剂改性样品上观察到~2log(99%)的金黄色葡萄球菌粘附的减少。这些实验证实改性表面在含蛋白质的溶液存在下抗细菌粘附的能力。
实施例17:在不同流动/剪切速率下的流动条件下在含化合物22的pu导管上的大肠杆菌粘附
医疗器材经受各种流动/剪切速率并且生物膜形成已知受剪切力影响,较高的剪切速率在一些情况下促进生物膜发展,因为细菌群落响应侵略性条件上调生长。有意义的是评估添加剂改性表面是否可在不同流量下抗细菌粘附。
使用实施例12中描述的方法评估经24小时人工尿液流在含2%化合物22的未改性和添加剂改性的7f聚氨酯导管上的大肠杆菌67粘附,但使用4.5ml/min的较高流量(对应于226s-1的腔壁剪切速率)。进行一个实验,并分析来自流动回路的四个1.5cm长的样品的细菌粘附。数据与来自实施例12的使用0.5ml/min流量(对应于25s-1的腔壁剪切速率)的类似数据一起呈现在图38中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。
在这一实验布置中,较高剪切速率在所有试验样品上引发较高的总体大肠杆菌粘附和可能引发生物膜形成,但与未改性的对照管材相比在用2%化合物22改性的管材上仍观察到~3log(99.9%)的减少。这一数据表明改性表面甚至在侵略性条件下也具有抗细菌粘附和生物膜形成的能力。
实施例18:在流动条件下经过延长的时间(7天)在含化合物22的pu导管上的大肠杆菌粘附和生物膜形成
为了评估经过延长的时间在聚氨酯管材样品上的细菌粘附和生物膜形成,设计非循环流动系统以便供应新鲜培养基和除去细菌废物,由此实现连续生物膜生长和更近似地模拟体内条件。该系统描绘在图39中,并由流动回路组成,该流动回路由连接到有机硅蠕动泵管的试验管组成并由5l无菌人工尿液(au)储器供料。试验管段的长度总共为59”(泵的近端和远端),而有机硅泵管段为18”长。
如实施例12中所述制造未改性和含2%化合物22的添加剂改性的7f聚氨酯管材。同时设置两个回路,一个用未改性的对照试验管材,一个用添加剂改性的试验管材。该系统的所有组件通过高压釜或环氧乙烷灭菌。也如实施例12中所述制备人工尿液和含108cfu/ml大肠杆菌67的细菌接种液。
在实验开始时,这些回路用无菌au流预处理10分钟。然后将回路进料管(无在线过滤器)插入含有在搅拌下保持在37℃水浴中的接种液的烧瓶中。将接种液泵过回路2小时以将细菌接种在管材的腔内表面上。在2小时后,停止泵并使用在线旋塞和管夹将流体锁在回路的主要部分中。将接种液烧瓶换成5l无菌au进料储器,并弃置先前浸在接种液中的进料管段,换成与0.45μm过滤器组装件相连的新管段以防止细菌从已接种的回路回流或迁移到无菌au进料储器中。经过旋塞用无菌au准备新管段和过滤器以防止将气泡引入回路。重启泵并打开旋塞/夹子以重新开始以0.5ml/min流动。
在24h,停止泵并在废物烧瓶塞上游~15cm夹住远端管材。排空夹子下游的流体并切割三个1.5cm管材样品以用于细菌计数,以及用于sem和结晶紫(cv)染色以对生物膜形成进行成像的样品。将剩余回路的远端头再插入废物烧瓶,重新开始流动并继续到第3和7天,此时提取另外的样品。用于细菌计数的样品如实施例4中所述冲洗和加工。用于sem的样品如实施例9中所述冲洗、加工和成像,使用与二次电子检测器一起运行的feixl30esem。使用20kv的加速电压、3的点尺寸和6.5mm的工作距离。纵向剖切用于cv染色的管材样品并在0.1%cv水溶液中浸泡15分钟。取出样品,通过浸在清水中3x轻轻冲洗,并拍照。另外,在实验持续期间全程目视检查管材的生物污损迹象。
经过7天在试验管材上的腔内大肠杆菌粘附显示在图40中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。在所有时间点与对照物相比在改性管材上都观察到大肠杆菌粘附的显著减少:5log(99.999%)至第3天和在第7天3log(99.9%)。
管材上的生物污损的差异从第3天开始视觉可见。具体而言,在未改性管材的管腔中观察到被推测为生物膜的白色淤浆,而用化合物22改性的管材保持干净。结晶紫染色证实在未改性管材上显著堆积生物膜,而在添加剂改性管材上没有观察到生物膜形成。生物膜形成的照片显示在图41中。
另外,通过sem成像确认试验管材上的生物膜形成的差异。对于各时间点,对未改性对照物和添加剂改性管材都将2个1cm长的样品成像,并对各样品获取四个随机图像。在5000x下的代表性图像显示在图42中。基于随机图像的图像分析,未改性对照表面100%被生物膜覆盖,而用化合物22改性的表面的<5%具有可见细菌。
实施例19:对于不同细菌物种在流动条件下在含化合物22的pu导管上的细菌粘附
使用实施例18中描述的方法用非循环流动系统研究各种细菌物种在未改性对照物和含2%化合物22的添加剂改性的7f聚氨酯导管上的粘附。
下列菌株用于测试:奇异变形杆菌296、金黄色葡萄球菌newman、表皮葡萄球菌35984和粪肠球菌33186。所有微生物菌株获自lawsonhealthresearchinstitute(london,ontario)。人工尿液用于对奇异变形杆菌296尿路病原体的实验,而75%pbs/25%tsb(trypticsoybroth)的混合物用于对所有其它细菌的实验。菌株在tsb中在37℃下在摇动下生长过夜。为了制备细菌接种液,将细菌培养物在4,500rpm下离心10分钟,洗涤并以108cfu/ml再悬浮在实验培养基中。使用0.5ml/min的流量并如实施例18中所述在24小时后分析来自各回路的远端部分的4个1.5cm长的样品的细菌粘附。
在流动24小时后在管材上的细菌粘附与来自实施例18的大肠杆菌数据一起显示在图43中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。对于所有受试物种,在24小时看出与未改性对照管材相比在用化合物22改性的管材上的细菌粘附的显著减少,表明改性表面的总体抗粘附性质。
实施例20:与商业输尿管支架产品相比在含化合物22的pu管材上的尿路病原体粘附
与来自主要制造商的市售7f输尿管支架管比较地研究尿路病原体在未改性对照物和含2%化合物22的添加剂改性的7f聚氨酯管材上的粘附。除人工尿液配方外,使用实施例11中描述的方法,其中使用基于brookst.等人,“asimpleartificialurineforthegrowthofurinarypathogens.”lettersinappliedmicrobiology1997,第24卷(3):203-6的配方。
用于测试的商业输尿管支架获自医疗用品经销商并列在表2中。将支架切成1.5cm段,试图尽可能避免排泄孔的存在并通过环氧乙烷灭菌。用于测试的菌株(大肠杆菌67、粪肠球菌33186和奇异变形杆菌296)获自lawsonhealthresearchinstitute(伦敦,ontario)。在人类汇集尿液(hu)中培养24小时后评估大肠杆菌和粪肠球菌粘附,而奇异变形杆菌粘附在人工尿液(au)中评估,因为这一物种可提高尿液的ph并需要缓冲培养基以在静态体外系统中保持存活力。
在24小时后在管材样品上的细菌粘附显示在图44中。细菌计数以对数格式呈现且误差条代表标准误差。对于所有三种受试细菌,与未改性对照物和所有商品相比,用2%化合物22改性的管材都表现出粘附的显著减少(p<0.05的t试验)。某些商品上存在的亲水或润滑涂层在这些实验中看起来不影响细菌粘附。
表2.用于对比试验的商业输尿管支架产品
实施例21:与商业输尿管支架产品相比在流动条件下在含化合物22的pu管材上的大肠杆菌粘附
与商业输尿管支架产品–c.r.bardinc.制造的inlayoptima比较地研究在流动下在未改性对照物和含2%化合物22的添加剂改性的7f聚氨酯管材上的大肠杆菌粘附。使用实施例12中描述的方法,对回路设计做出一些修改以适应输尿管支架产品。具体而言,由于bardinlayoptima沿导管轴的长度具有间隔~2cm的排泄孔,所有试验回路由7f聚氨酯对照管材与使用聚丙烯接头串联连接在泵下游的四个2cm试验管材段组成。相同的布置用于评估的所有试验组。用人工尿液中的大肠杆菌67菌株使用0.5ml/min的流量进行实验。在实验结束时,从聚丙烯接头移除2cm段,并从每边修剪掉0.5cm以除去边缘效应。剩余1cm管材如实施例12中所述加工以进行细菌计数。
在流动24小时后在管材样品上的大肠杆菌粘附显示在图45中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照管材或bardinlayoptima支架管相比,用2%化合物22改性的管材表现出~3log(99.9%)粘附减少(p<0.05的t试验)。
实施例22:在人工尿液中培养2周后含化合物22的pu管材的细菌介导的结壳
某些细菌物种可促进生物流体中的盐结壳或沉淀在器材表面上。这可影响器材功能,以造成器材失效(例如输尿管支架的堵塞,以影响排出),以及对患者舒适度具有不利影响和导致其它并发症和合并症。奇异变形杆菌是在人类尿液中发现中的由于其裂解尿素由此释放氨以致提高尿液的ph的能力而经常与泌尿科器材上的结壳相关联的细菌物种。这又引发尿液中存在的多价离子的沉淀,以致在支架或导管表面上形成鸟粪石(mgnh3po4)或磷灰石(capo4)晶体。
用innovotech(一家位于edmonton,alberta的医疗器材测试实验室)设计的2周体外模型研究用本发明的化合物22改性的表面抗细菌介导的结壳的能力。如实施例12中所述制造未改性对照物和含2%化合物22的添加剂改性的7f聚氨酯管材。将管材切割成3.8cm长的样品,将其以“u形”安装在12孔培养板(innovotech’sbesttm板)的盖子上,每个试验组n=6个样品。安装好的样品和板通过环氧乙烷灭菌。
基于来自brookst.等人,“asimpleartificialurineforthegrowthofurinarypathogens.”lettersinappliedmicrobiology1997,第24卷(3):203-6的配方制备人工尿液(au)。将au过滤灭菌并储存在4℃直至使用。将innovotech储备的奇异变形杆菌的临床菌株(mil#06-0116-3)连续分布到(streakedout)来自低温储备的胰酶大豆琼脂(tsa)上并在37℃下培养~20小时,然后类似地传代培养。来自传代培养物的菌落在tsb中在37℃下在摇动下生长~20小时,然后用于制备以106cfu/ml在人类尿液中的奇异变形杆菌接种液。将四(4)毫升接种液添加到含样品的培养板的各孔中,以导致~2.8cm长的管材浸在接种液中。将板置于旋转摇床上并在37℃下培养14天。每48小时通过将盖子转移到具有新鲜接种液的新板上而更换接种液。在14天后,通过浸在5毫升无菌水中,将样品冲洗3x。然后从盖子中取出样品并在4%硝酸中声处理30分钟以移除结壳沉积物。允许沉积物在硝酸溶液中溶解24小时,然后通过使用标准方法的原子吸附光谱学(agilent220fsatomicabsorptionspectrophotometer,chemicalandmaterialsengineeringdepartment,universityofalberta)分析钙和镁含量。
归一化为表面积的沉积在管材试样上的钙和镁的质量显示在图46中,并与结壳沉积物的总质量相关联。误差条代表标准误差。用2%化合物22改性的聚氨酯管材具有比未改性的聚氨酯管材少59%的在表面上的总钙和镁基沉积物,表明该表面改性减少细菌介导的结壳的潜力。
实施例23:在pbs中培养2小时后在含化合物43、44、45和38的pu棒上的细菌粘附
使用实施例2中描述的方法制备具有除实施例2或4中给出的那些外的另外化合物的聚氨酯棒。使用实施例4中描述的方法评估在未改性对照物和添加剂改性棒上的金黄色葡萄球菌newman和表皮葡萄球菌35984粘附,且结果显示在图47中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。与未改性对照物相比添加剂改性样品上的金黄色葡萄球菌和表皮葡萄球菌粘附的减少为~1.5至2.5log(>99%),取决于添加剂配方和受试细菌物种。
实施例24:在人类汇集尿液中培养24小时后在含化合物43、44、45、38和11的pu棒上的大肠杆菌粘附
使用实施例2中描述的方法制备具有除实施例1或4中给出的那些外的另外化合物的聚氨酯棒。从三位健康志愿者中收集并汇集人类尿液(hu)。将hu过滤灭菌,储存在4℃,并在制备或收集的一周内使用。使用实施例4中描述的方法进行大肠杆菌67粘附测试,使用长度1.5cm的棒样品、在hu中以106cfu/ml制备的细菌接种液和24小时的培养时间。
结果显示在图48中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。与未改性对照物相比添加剂改性样品上的大肠杆菌粘附减少为0至~2.5log(>99%),取决于测试的添加剂配方。
实施例25:在含化合物22、45和38和不透射线填料的pu棒的细菌粘附
使用实施例2中描述的方法和含和不含20%baso4不透射线填料的carbothanepc3585a树脂,制备含2%化合物22、45和38的聚氨酯棒。这两种树脂都获自医用聚氨酯供应商
结果显示在图49中。细菌计数以对数格式呈现且误差条代表标准误差。与各自的未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。与各自的对照物相比添加剂改性样品上的细菌粘附减少为~1.5至3log(99.9%),取决于添加剂配方和受试细菌物种。在含和不含baso4的改性样品之间,细菌粘附的减少类似,表明无机填料的存在不影响表面改性的效力。
实施例26:在pbs或人类汇集尿液中培养2小时后在含化合物54和55的pu棒上的细菌粘附
使用实施例2中描述的方法制备含有附加化合物54和55的聚氨酯棒。使用实施例4中描述的方法进行细菌粘附测试,但对各细菌物种仅进行一个实验,n=3个样品。在pbs中培养2小时后评估金黄色葡萄球菌newman和表皮葡萄球菌359841粘附。在人类汇集尿液(hu)中培养2小时后评估大肠杆菌67粘附。从三位健康志愿者中收集并汇集hu,过滤灭菌,储存在4℃,并在收集的一周内使用。
结果显示在图50中。细菌计数以对数格式呈现且误差条代表标准误差。与未改性对照物相比在粘附方面具有统计显著差异(p<0.05的t试验)的添加剂改性样品用(*)符号标示。与未改性对照物相比添加剂改性样品上的细菌粘附减少为~1至3log(90–99.9%),取决于添加剂配方和受试细菌物种。
实施例27:其它聚合物
根据实施例2的方法制备含有0.05-15%(w/w)的化合物1-57之一或具有smm1–smm16之一化学式的化合物的聚氯乙烯(pvc)棒。根据实施例4的方法测试pvc棒的细菌粘附。包括化合物1-57的任一种或具有smm1–smm16的任一种化学式的化合物的制剂与对照物相比表现出抗细菌粘附性。
类似地,制备含有0.05-15%(w/w)的化合物1-57之一或具有smm1–smm16之一化学式的化合物的聚乙烯棒并测试细菌粘附。包括化合物1-57的任一种或具有smm1–smm16的任一种化学式的化合物的制剂与对照物相比表现出抗细菌粘附性。
在另一实例中,制备含有0.05-15%(w/w)的化合物1-57之一或具有smm1–smm16之一化学式的化合物的尼龙棒(例如nylon6、nylon6-6、nylon11或nylon12)并测试细菌粘附。包括化合物1-57的任一种或具有smm1–smm16的任一种化学式的化合物的制剂与对照物相比表现出抗细菌粘附性。
类似地制备含有0.05-15%(w/w)的化合物1-57之一或具有smm1–smm16之一化学式的化合物的乙烯-乙酸乙烯酯(eva)棒并测试细菌粘附。包括化合物1-57的任一种或具有smm1–smm16的任一种化学式的化合物的制剂与对照物相比表现出抗细菌粘附性。
在另一实例中,制备含有0.05-15%(w/w)的化合物1-57之一或具有smm1–smm16之一化学式的化合物的聚乙烯棒并测试细菌粘附。包括化合物1-57的任一种或具有smm1–smm16的任一种化学式的化合物的制剂与对照物相比表现出抗细菌粘附性。
最后,制备含有0.05-15%(w/w)的化合物1-57之一或具有smm1–smm16之一化学式的化合物的聚(苯乙烯-嵌段-异丁烯-嵌段-苯乙烯)(sibs)棒并测试细菌粘附。包括化合物1-57的任一种或具有smm1–smm16的任一种化学式的化合物的制剂与对照物相比表现出抗细菌粘附性。
其它实施方案
本领域技术人员将显而易见所述发明的各种修改和变动,而不背离本发明的范围和精神。尽管已联系具体实施方案描述了本发明,但应该理解的是,所要求保护的发明不应过度受到这些具体实施方案的限制。确实,本领域技术人员显而易见的对所描述的用于实施本发明的模式的各种修改意在本发明的范围内。
其它实施方案在权利要求书中。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询



 商标分类
商标分类  商标转让
商标转让 



