一种β2-GP1改构蛋白及其构建方法、应用与流程
 2021-02-02 14:02:45|
2021-02-02 14:02:45| 438|
438| 起点商标网
起点商标网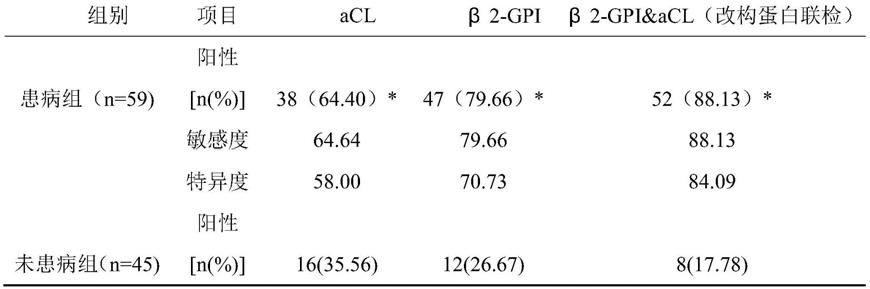
一种
β
2-gp1改构蛋白及其构建方法、应用
技术领域
[0001]
本发明涉及生物医药工程技术领域,具体涉及一种β2-gp1改构蛋白及其构建方法、应用。
背景技术:
[0002]
抗磷脂综合征(aps)为一种以反复动脉或者静脉血栓、病态妊娠和抗磷脂抗体(apl)持续阳性的疾患。抗磷脂抗体(apl)可同时导致多器官血管受累,表现为恶性高血压、轻度偏瘫、呼吸困难、肝梗死、心脏动脉血栓形成等症状。由于长期诊断困难,缺乏有效药物,患者死亡率高达75%以上。
[0003]
抗磷脂综合征(aps)的分类必须满足至少一项临床(血管血栓形成或妊娠合并症)和一项实验室(抗心磷脂抗体,狼疮抗凝或抗β2-gp1抗体阳性)指标。
[0004]
但是目前,在三种实验室标准的测试方法中,均显示出方法学缺陷,即成本过高、检测过程繁琐,敏感性和特异性差异较大,且为单一抗体检测,容易出现患者疾病漏检。
[0005]
研究表明,抗磷脂抗体(apl)检测中双阳性(acl+、aβ2-gp1+)结果的患者,显示出与血栓和病态妊娠的强关联,因此联合检测抗心磷脂抗体(acl)和抗β2-gp1抗体具有重要的意义。
[0006]
β2-gp1是一种由326个氨基酸残基组成的多肽链,分子量约为50kd,具有4个糖基化位点,为高度糖基化的单链亲水蛋白;因其参与脂肪的转运和代谢,又称载脂蛋白h(apolipoprotein h)。β2-gp1由5个从n末端编号为1-5的同源域组成。结构域1到结构域4由约60个氨基酸组成,这些氨基酸包含有同一个基序,该基序的特征是四个保守的半胱氨酸残基组成的框架。第5结构域与结构域1-4的不同之处在于,它含有6个cys,组成3个内部二硫键,并且有一个不规则较长的c末端尾部,含有高度正电荷序列cys281-cys288和进化保守的疏水序列亮氨酸(leu)313-色氨酸(trp)316,为磷脂结合的关键部位,因此β2-gp1呈现强的亲脂特性。在中性ph条件下,第5结构域能与阴性磷脂(pl)稳定结合。
[0007]
研究发现,在β2-gp1的5个结构域中,结构域1(d1)为抗β2-gp1抗体的特异性识别位点。另外,当β2-gp1结合心磷脂后形成的磷脂-蛋白复合物,这一种磷脂-蛋白复合物,将暴露出其中的结构域4(d4)的隐性表位,被β2-gp1依赖性抗心磷脂抗体(acl)所识别,而这一种抗心磷脂抗体才有病理意义,成为β2-gp1依赖性抗心磷脂抗体(acl)的抗原。
技术实现要素:
[0008]
本发明目的在于提供β2-gp1改构蛋白,通过将d1、d4和d5结构域通过一定的氨基酸序列进行链接,形成一种能特异性结合抗β2-gp1抗体和抗acl抗体的改构蛋白,该改构蛋白用于试剂盒能增加试剂盒的特异性,实现抗β2-gp1抗体和抗acl抗体的联检,提高aps的检出率。
[0009]
此外,本发明还提供上述β2-gp1改构蛋白的构建方法、在试剂盒中的应用。
[0010]
本发明通过下述技术方案实现:
[0011]
一种β2-gp1改构蛋白,其氨基酸序列如seq id no.1所示。
[0012]
β2-gp1改构蛋白能够用于抗β2-gp1抗体和抗acl抗体的同时检测,有助于提高检测试剂盒的灵敏度和准确度。
[0013]
β2-gp1改构蛋白,包含结构域1蛋白区段、结构域4蛋白区段和结构域5蛋白区段。
[0014]
一种编码β2-gp1改构蛋白的基因,所述基因的核苷酸序列如seq id no.2所示。
[0015]
β2-gp1是一种由326个氨基酸残基组成的多肽链,分子量约为50kd,具有4个糖基化位点,为高度糖基化的单链亲水蛋白;因其参与脂肪的转运和代谢,又称载脂蛋白h(apolipoprotein h)。β2-gp1由5个从n末端编号为1-5的同源域组成。结构域1到结构域4由约60个氨基酸组成,这些氨基酸包含有同一个基序,该基序的特征是四个保守的半胱氨酸残基组成的框架。第5结构域与结构域1-4的不同之处在于,它含有6个cys,组成3个内部二硫键,并且有一个不规则较长的c末端尾部,含有高度正电荷序列cys281-cys288和进化保守的疏水序列亮氨酸(leu)313-色氨酸(trp)316,为磷脂结合的关键部位,因此β2-gp1呈现强的亲脂特性。在中性ph条件下,第5结构域能与阴性磷脂(pl)稳定结合。
[0016]
在β2-gp1的5个结构域中,结构域1(d1)为抗β2-gp1抗体的特异性识别位点。另外,当β2-gp1结合心磷脂后形成的磷脂-蛋白复合物,这一种磷脂-蛋白复合物,将暴露出其中的结构域4(d4)的隐性表位,被β2-gp1依赖性抗心磷脂抗体(acl)所识别,而这一种抗心磷脂抗体具有病理意义,成为β2-gp1依赖性抗心磷脂抗体(acl)的抗原。
[0017]
本发明的β2-gp1改构蛋白,删除结构域2和结构域3,可以使β2-gp1呈现出与全长序列表达所不同的构象,当连接一个心磷脂后,呈现出的抗原表位,既具有与β2-gp1依赖性抗心磷脂抗体和抗β2-gp1抗体结合的能力,用来制备试剂盒将减少试剂盒检测样本时的非特异性结合。
[0018]
β2-gp1改构蛋白的构建方法,包括如下步骤:
[0019]
s1、重组全基因合成序列:依次连接结构域1、结构域4、结构域5蛋白区段的核苷酸序列获得目的基因;
[0020]
s2、构建重组质粒:将步骤s1中获得的重组全基因合成序列构建至表达载体,获得重组质粒;
[0021]
s3、一次转染:将步骤s2中的重组质粒转染宿主细胞,获得重组杆粒;
[0022]
s4、二次转染:将步骤s3中的重组杆粒再次转染宿主细胞,获得第一代的杆状病毒;
[0023]
s5、表达:将步骤s4中的第一代的杆状病毒进行表达;
[0024]
s6、获得改构蛋白:将步骤s5中表达得到的细胞培养物进行纯化,获得改构蛋白。
[0025]
优选地,所述步骤s1重组全基因合成序列过程中包含一个单位的结构域1蛋白区段的核苷酸序列、一个单位的结构域4蛋白区段的核苷酸序列和一个单位的结构域5蛋白区段的核苷酸序列。
[0026]
优选地,所述步骤s1中重组全基因合成序列中还包括柔性肽基因序列、真核kozak序列、蜂毒信号肽序列、avi标签序列和his标签序列,真核kozak序列、蜂毒信号肽序列、结构域1蛋白区段的核苷酸序列、柔性肽基因序列、结构域4蛋白区段的核苷酸序列、柔性肽基因序列、结构域5蛋白区段的核苷酸序列、avi标签序列和his标签序列依次相连。
[0027]
本发明在结构域5上连接的avi-tag(序列为glndifeaqkiewhe)是一个由15个氨基
酸残基组成的短肽标签,在体内或体外都能被生物素连接酶在赖氨酸残基连接上一个生物素,从而实现蛋白的生物素化,因此在制备试剂盒时,使用链酶亲和素磁珠可以轻易连接上本发明改构蛋白,在不影响线性表位的前提下增加偶联效率。
[0028]
优选地,步骤s1中重组全基因合成序列删除了结构域4中的gly237及gly242残基,删除了结构域5中的pro343及pro358残基。
[0029]
由于β2-gp1三维结构为“鱼钩状”,且转角发生于第4结构域及第5结构域连接处,而pro及gly是高频转角所必须的,且结构域4(d4)与结构域5(d5)连接处含有gly237及gly242残基,pro343及pro358残基。删除结构域5(d5)中的pro343及pro358残基,将减弱结构域4及结构域5的高频转角,增强结构域4对β2-gp1依赖性抗心磷脂抗体的亲和力,且不影响与心磷脂的能力。
[0030]
优选地,所述步骤s2构建重组质粒中的表达载体包括昆虫细胞表达载体和/或杆状病毒表达载体;所述步骤s3一次转染时的宿主细胞包括大肠杆菌宿主和/或动物性细胞宿主。
[0031]
β2-gp1改构蛋白在试剂盒、疫苗或诊断抗原中的应用。
[0032]
一种β2-gp1改构蛋白检测试剂盒制备方法,包括如下步骤:
[0033]
s1、磁珠试剂的制备:将权利要求1所述改构蛋白质使用生物素进行标记,标记完成后,通过生物素与链酶亲的反应,将生物素化的改构蛋白质偶联到链酶亲和素磁珠上,并加入0.1mg/ml的心磷脂,37℃混合反应24h后,作为试剂盒中的组分m;
[0034]
s2、分别在鼠抗人igg、鼠抗人igm及鼠抗人iga三种抗体上标记碱性磷酸酶(ap),将标记完成的igg/igm/iga-ap,使用相同抗体的浓度,混合为同一反应液,作为试剂盒中的组分r2。
[0035]
本发明的改构蛋白,是通过将β2-gp1改构蛋白基因序列在加入his标签序列序列后,构建至pfastbac 1质粒载体中,通过bamh i,ecor i两个限制性内切酶,制备一种含有结构域1(d1)、结构域4(d4)和结构域5(d5)基因序列的重组质粒;重组质粒转化大肠杆菌dh10 bac,获得重组杆粒;将重组杆粒转染昆虫细胞后分泌表达β2-gp1改构蛋白;his标签序列纯化获得β2-gp1改构蛋白。
[0036]
本发明与现有技术相比,具有如下的优点和有益效果:
[0037]
1、本发明β2-gp1改构蛋白能够特异性结合抗β2-gp1抗体和抗acl抗体,实现抗β2-gp1抗体和抗acl抗体的联检,提高aps的检出率。
[0038]
2、使用本发明所述β2-gp1改构蛋白制备检测试剂盒能能有效鉴别apl患者,提高了抗磷脂抗体(apl)的检测灵敏度和特异性,减少漏检和错检。
附图说明
[0039]
此处所说明的附图用来提供对本发明实施例的进一步理解,构成本申请的一部分,并不构成对本发明实施例的限定。在附图中:
[0040]
图1目的基因阳性克隆鉴定结果;
[0041]
图2为改构蛋白鉴定结果;
[0042]
图3为蛋白纯化结果图。
具体实施方式
[0043]
为使本发明的目的、技术方案和优点更加清楚明白,下面结合实施例和附图,对本发明作进一步的详细说明,本发明的示意性实施方式及其说明仅用于解释本发明,并不作为对本发明的限定。
[0044]
实施例1:
[0045]
改构基因(目的基因)的全基因序列的合成:
[0046]
s1、依次连接结构域1、结构域4、结构域5蛋白区段的核苷酸序列得到目的基因,根据ncbi所公开的序列信息,在连接两个基因片段之间去掉终止密码子和起始密码子,并加入5个氨基酸残基(ggggs)的柔性肽基因序列(linker序列);在结构域5上连接一个avi-tag,并在c端加入6*his标签序列;在序列上游加入限制性核酸内切酶位点bamh i,在其下游则加入ecori酶切位点,并根据哺乳动物密码子偏好性,基因合成时各序列之间的排列顺序为真核kozak-信号肽-d1-linker-d4-linker-d5-avi-6*his,目的基因(改构基因)的核苷酸序列如seq id no.2所示。
[0047]
实施例2:
[0048]
含有改构基因的重组质粒构建:
[0049]
2.1将实施例1中获得的全基因序列和质粒载体pfastbac 1进行bamh i、ecor i双酶切,试剂盒回收酶切产物,将酶切产物通过t4连接酶连接。
[0050]
2.2连接产物转化感受态大肠杆菌dh5α,体积不超过感受态细胞的10%,轻轻旋转几次混匀内容物,冰浴30分钟;将管放入42℃水浴,定时60秒热休克,快速将管转移到冰浴120秒使细胞冷却,每管加入400μl lb培养基,37℃缓摇60分钟,使细菌复苏并表达质粒编码的抗生素抗性标记基因,低速离心2分钟,去上清,留约100μl培养基在离心管内,重悬菌体,用玻璃铺菌器将菌液在琼脂板上铺匀。
[0051]
2.3将平板倒置于37℃恒温培养箱,12-16小时后可出现菌落。涂板后挑取阳性克隆进行鉴定,如图1所示。
[0052]
实施例3:
[0053]
改构蛋白的表达
[0054]
3.1将实施例2中获得的重组质粒转化至大肠杆菌dh10 bac感受态细胞,体积不超过感受态细胞的5%,轻轻旋转几次混匀内容物,冰浴30分钟。
[0055]
3.2将管放入42℃水浴,定时90秒热休克,快速将管转移到冰浴120秒,使细胞冷却;每管加入800μl lb培养基,37℃,缓摇4小时,使细菌复苏并表达质粒编码的抗生素标记基因;用玻璃铺菌器将30μl菌液在抗性kan+gent+tet琼脂板上铺匀;将平板倒置于37℃恒温培养箱中,30-48小时后可出现蓝白斑菌落。
[0056]
3.3挑取阳性白斑单菌落接入5ml抗性lb,缓摇12-16h,取菌液进行pcr鉴定,结果显示杆粒改构基因正确;将重组杆粒经转染试剂转染昆虫细胞,3-5天后收取细胞上清液作为第一代杆状病毒。用第一代杆状病毒感染昆虫细胞48-96小时后,获得第二代病毒,用于改构蛋白的表达。β2-gp1改构蛋白的氨基酸序列如seq id no.1所示。
[0057]
3.4第二代病毒1:100体积比感染密度为2
×
10
6
/ml的昆虫细胞sf9,继续培养72小时后,收集细胞培养物。
[0058]
实施例4:
[0059]
改构蛋白鉴定:
[0060]
4.1分别将实施例3中的上清与细胞进行非还原性sds-page电泳,使用12%分离胶浓度,电泳约90分钟;
[0061]
4.2将sds-page电泳凝胶进行转膜(pvdf),湿转100v,30分钟;收集pvdf,使用5%脱脂奶粉封闭;
[0062]
4.3将4.2封闭后的pvdf膜加入β2-gp1 mab,再洗净后加入鼠二抗,ecl显色;确定蛋白表达于细胞上清中,结果如图2所示。
[0063]
实施例5:
[0064]
改构蛋白纯化
[0065]
5.1取实施例3中的细胞培养物在5000g离心力下离心20分钟收集细胞培养上清。
[0066]
5.2细胞培养上清与1ml用平衡缓冲液平衡好的ni-nta resin孵育过夜,次日,弃上清,加入适量平衡缓冲液重悬填料,将填料转移到自流柱里。
[0067]
5.3依次用冲洗缓冲液1(50mm tris-hcl ph8.0;500mm nacl)洗10个柱体积;冲洗缓冲液2(50mm tris-hcl ph8.0;500mm nacl;20mm咪唑)洗10个柱体积;冲洗缓冲液3(50mm tris-hcl ph8.0;500mm nacl;60mm咪唑)洗10个柱体积;冲洗缓冲液4(50mm tris-hcl ph8.0;500mm nacl;300mm咪唑)洗5个柱体积。
[0068]
5.4洗脱缓冲液洗脱目的蛋白,1
×
pbs透析纯化后目的蛋白保存在-80℃。
[0069]
5.5 sds-page电泳检测表达蛋白纯度及浓度,如图3所示。
[0070]
实施例6:
[0071]
使用rayto化学发光仪器,依次加入用生物素化β2-gp1改构蛋白与链酶亲和素磁珠偶联后,并混入0.1mg/ml的心磷脂,37℃混合反应24h后的组分m,待测样本、碱性磷酸酶(ap)标记的鼠抗人igg、鼠抗人igm及鼠抗人iga三种抗体,化学发光底物(amppd),使用免疫间接法来检测血清或血浆样本。
[0072]
当检测样本为apl患者时,血清或血浆中的β2-gp1依赖性抗心磷脂抗体(acl)或抗β2-gp1抗体,经过与磁珠上的抗原形成免疫复合物后,被ap酶标记的igg/igm/iga所识别,当加入3-(2-螺旋金刚烷)-4-甲氧基-4-(3-磷氧酰)-苯基-1,2-二氧环乙烷二钠盐(amppd)后,化学发光仪器将采集到amppd发射出的光子。
[0073]
通过测定正常人血清及apl患者血清建立了实验室参考区间。
[0074]
取2019年5月至2019年11月间,攀枝花市xx医院收治疑似磷脂综合征患者104例作为研究对象,检测结果如下表所示。
[0075][0076]
注:*标识与未患病组阳性比较,p<0.05
[0077]
由上述实验结果可知,使用本发明β2-gp1改构蛋白,有效鉴别apl患者,提高了抗磷脂抗体(apl)的检测灵敏度和特异性,为诊断抗磷脂综合征(aps)提供了重要参考依据。
[0078]
本发明β2-gp1改构蛋白的制备过程及表达过程简单,同时改构蛋白用于试剂盒的制备,有效鉴别apl患者,提高了抗磷脂抗体(apl)的检测灵敏度和特异性,为诊断抗磷脂综合征(aps)提供了重要参考依据。
[0079]
以上所述的具体实施方式,对本发明的目的、技术方案和有益效果进行了进一步详细说明,所应理解的是,以上所述仅为本发明的具体实施方式而已,并不用于限定本发明的保护范围,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



