基于荧光共振能量转移和外切酶辅助循环扩增策略的物质检测方法与流程
 2021-02-02 12:02:01|
2021-02-02 12:02:01| 363|
363| 起点商标网
起点商标网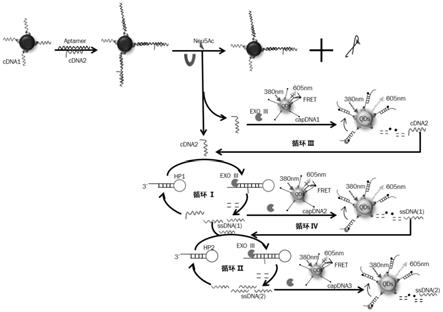
[0001]
本发明涉及一种基于荧光共振能量转移和外切酶辅助循环扩增策略的物质检测方法,属于分析化学技术领域。
背景技术:
[0002]
唾液酸又称燕窝酸,是一种九碳糖,中国传统珍稀食品燕窝中具生物活性的主要成份,母乳中的唾液酸为婴儿早期生长提供免疫力,提高肠道对于维生素及矿物质的吸收能力。唾液酸为神经氨酸,广泛存在于动物组织及微生物中,是细胞膜蛋白的重要组成部分,参与细胞表面多种生理功能,在调节人体生理、生化功能方面起到非常重要的作用。因此,开发检测唾液酸的方法和分析技术对唾液酸或唾液酸修饰的多糖/脂类/蛋白的检测和诊断具有重要意义。目前,针对唾液酸的研究方法有高效液相色谱法、核磁共振法、质谱分析法、凝集素沉淀法、凝集素亲和层析法、凝集素亲和电泳法、凝集素酶联免疫吸附实验、凝集素印迹法、凝集实验、凝集素包被磁珠、荧光标记凝集素流式细胞术等。这些方法通常具有以下缺点:测定样品之前需要对样品进行分离提纯等预处理,只能测定细胞中提取的糖,提取过程中糖蛋白的结构易发生改变或丢失,单次实验中仅能使用少数几种凝集素进行检测,若想使用多种凝集素检测,需要进行多次反应,操作繁琐,无法一次性地对唾液酸进行分析等。此外,这些方法对操作者专业度要求高,成本高,准确度低,检测限高,影响了检测的结果。基于以上研究现状,急需研发新的针对唾液酸或唾液酸修饰的多糖/脂类/蛋白的化学标记和分析检测技术。
[0003]
生物传感分析因其具备高选择性,高灵敏度等优点而受到广泛的关注。生物传感器包括分子识别部分和信号转换部分,分子识别部分识别靶标,而后将生物信号转换成电信号、荧光信号或其他信号。近年来,随着分子生物学和生物传感器技术的发展,多种基于适配体和荧光共振能量转移技术(fret)的生物传感器被设计出来用于检测生物靶标。其中,适配体作为识别原件具有明显的优越性:不受免疫条件和免疫原性的限制,靶标范围广,可以在体外人工合成且技术成熟,成本相对低廉,变性与复性可逆,易于进行多种化学修饰,易于高通量制备,易于长期保存等。这些特性使得适配体在生物医药研究领域得到广泛的应用。
[0004]
量子点是一类类似于球状的纳米材料,通常是由半导体材料所组成。一般直径在1~100nm范围之内,是一种比较稳定的纳米粒子。量子点具有很好的荧光性质,且荧光寿命长,稳定性好。即使激光的高强度和长时间照射,量子点的光学特性也不会发生明显的变化。量子点与dna结合使得构建的生物传感器具有测试方法简单、检测选择性好、灵敏度高等优点。但是,即使将量子点与基于适配体和荧光共振能量转移技术的生物传感器相结合,依然存在灵敏度不够等问题。目前还没有一款能够非常灵敏的用于检测唾液酸的生物传感器。
id no.8所示。
[0022]
本发明首先将适配体与捕获探针、信号探针序列进行高温变性,变复性处理后放置于37℃水浴锅孵育形成一条三明治结构的互补序列。在唾液酸存在的情况下,三明治结构的互补序列中适配体部分与唾液酸结合,改变了互补序列的二级结构,从而导致信号探针从三明治结构的互补序列中释放出来。其次,将含有黑洞猝灭剂(bhq2)的三条核酸分子信标(capdna1、capdna2、capdna3)分别与cdse/zns量子点(qds)孵育,构建三个基于量子点与黑洞猝灭剂的荧光共振能量转移体系,分别为bhq2-capdna1-qds、bhq2-capdna2-qds、bhq2-capdna3-qds。当加入从三明治结构的互补序列中释放出来的信号探针至荧光共振能量转移体系中时,信号探针会与荧光共振能量转移体系bhq2-capdna1-qds中的核酸分子信标capdna1进行序列互补配对。加入核酸外切酶-后,由于核酸分子信标capdna1的3
’
端与信号探针结合完全互补,从而导致其被核酸外切酶-酶切,使得核酸分子信标capdna1的3
’
端修饰的黑洞猝灭剂bhq2被释放出来,致使量子点荧光恢复。当分子信标capdna1被酶切后,与其互补的信号探针被释放出来,释放出的信号探针能够再次与其他分子信标capdna1进行互补杂交,从而导致新一轮的荧光共振能量转移体系终止,结合在量子点上的黑洞猝灭剂大量分离,量子点的荧光强度进一步恢复;此外,为了进一步扩增荧光信号,将双发夹结构核酸探针加入到反应体系中,信号探针能够与发夹结构核酸探针hp1结合,诱发hp1被核酸外切酶-酶切,形成大量的单链ssdna1,ssdna1能够进一步作为信号探针与荧光共振能量转移体系bhq2-capdna2-qds中的核酸分子信标capdna2进行序列互补配对,诱发核酸分子信标capdna2被核酸外切酶-酶切。当分子信标capdna2被酶切后,与其互补的单链ssdna1被释放出来,释放出的单链ssdna1能够再次与其他分子信标capdna2进行互补杂交,从而导致新一轮的荧光共振能量转移体系终止,结合在量子点上的黑洞猝灭剂大量分离,量子点的荧光强度再次增强;与此同时,ssdna1序列能够与发夹结构核酸探针hp2结合,诱发hp2被核酸外切酶-酶切,形成大量的单链ssdna2,ssdna2能够进一步作为信号探针与荧光共振能量转移体系bhq2-capdna3-qds中的核酸分子信标capdna3进行序列互补配对,诱发核酸分子信标capdna3被核酸外切酶-酶切,致使大量量子点荧光恢复。当分子信标capdna3被酶切后,与其互补的单链ssdna2被释放出来,释放出的单链ssdna2能够再次与其他分子信标capdna3进行互补杂交,从而再次导致新一轮的荧光共振能量转移体系终止,结合在量子点上的黑洞猝灭剂大量分离,量子点的荧光强度再次进一步增强;通过以上多轮循环反应增加了酶切的分子信标capdna1、capdna2、capdna3数量,从而增强了荧光信号,提高了生物传感器的灵敏度(图1)。最后,建立荧光信号强度与唾液酸数量间的线性关系,利用该标准曲线计算样品中的唾液酸含量。
[0023]
本发明的有益效果:
[0024]
本发明通过适配体捕获唾液酸从而释放与适配体互补的信号探针,信号探针能够与形成荧光共振能量转移体系中的核酸分子信标结合,与此同时,信号探针还能够与发夹结构核酸探针hp1结合,当加入核酸外切酶-时,信号探针促发核酸分子信标与发夹结构核酸探针酶切,从而使得大量的量子点荧光信号恢复,使该传感器检测范围扩大,提高检测灵敏度。该方法相比于传统的唾液酸检测方法,特异性强,灵敏度高。
附图说明
[0025]
图1为基于荧光共振能量转移和外切酶辅助循环扩增策略的唾液酸高灵敏度检测原理图;
[0026]
图2为唾液酸荧光检测标准曲线。
具体实施方式
[0027]
下面结合具体实施例对本发明作进一步说明,以使本领域的技术人员可以更好地理解本发明并能予以实施,但所举实施例不作为对本发明的限定。
[0028]
以下实施例中所述适配体购于苏州贝信生物科技有限公司,互补核酸与核酸分子信标、发夹结构核酸购于生工生物工程(上海)股份有限公司。
[0029]
本发明实施例中所用的适配体、捕获探针、信号探针、核酸分子信标及发夹结构核酸探针的序列如表1所示。
[0030]
表1序列表
[0031][0032]
实施例1:唾液酸浓度标准曲线的绘制
[0033]
(1)靶标识别磁珠制备:核酸序列如表1所示,包括唾液酸的适配体序列以及与适配体互补的信号探针序列、捕获探针序列,将适配体在75℃高温变性5min,冰浴10min,与此同时,将信号探针与修饰有生物素的序列在95℃高温变性5min,冰浴10min;将以上变复性处理的序列至于37℃孵育,之后加入链霉亲和素修饰的磁珠轻微震荡反应一段时间后,形成一个基于适配体的三明治结构核酸分子杂交体系,使用磁铁将溶液进行磁性分离,丢弃上清液,使用pbs缓冲液清洗沉淀3次后重悬于pbs缓冲液中;
[0034]
(2)靶标识别和信号探针获取:将50μl含有不同浓度唾液酸加入以上pbs缓冲液混匀,室温下孵育1h;用磁铁进行磁性分离,获取上清液,上清液中即含信号探针;
[0035]
(3)荧光共振能量转移体系构建:分别取50μl 1μmol
·
l-1
含有黑洞猝灭剂(bhq2)的核酸分子信标(capdna1、capdna2、capdna3)与50μl 1μmol
·
l-1
cdse/zns荧光量子点(qds)混匀,室温下轻微摇动,孵育25min,构建三个基于量子点与黑洞猝灭剂的荧光共振能量转移体系,分别为bhq2-capdna1-qds、bhq2-capdna2-qds、bhq2-capdna3-qds;所述核酸分子信标序列如表1所示;
[0036]
(4)酶切多级循环放大与信号扩增:取50μl步骤(2)所得溶液加入构建好的荧光共振能量转移体系,同时分别加入50μl的发夹结构核酸探针hp1和hp2,再加入150u的核酸外切酶-酶切反应1.5h,使得修饰在量子点上的分子信标被核酸外切酶-切除,从而使得黑洞猝灭剂bhq2与量子点分离,荧光共振能量转移体系消失,荧光增强;所述发夹结构核酸探针hp1和hp2序列如表1所示;
[0037]
(5)荧光信号检测和标准曲线绘制:将步骤(4)中酶切反应1.5h后的产物使用荧光分光光度计检测,与空白样品作比较,读取荧光值变化,采用的激发波长为380nm,测定发射波长为605
±
5nm下的荧光信号,通过逐倍稀释唾液酸的浓度,根据测定荧光值与加入唾液酸浓度之间的关系,绘制出相应的线性关系曲线。
[0038]
如图2所示,荧光强度随着唾液酸浓度的增加而增加,其线性回归方程是y=0.096logc
neu5ac
+0.893(r
2
=0.995),其中y表示相对荧光强度,c
neu5ac
表示唾液酸的浓度pmoll-1
,该方法的检测限为78.13fmoll-1
。
[0039]
实施例2:实际样品中唾液酸含量的测定
[0040]
为了进一步验证该方法在测定实际样品中唾液酸含量时的准确性,选用了无预处理的牛奶制品和人血清样品。
[0041]
将牛奶制品和人血清样品用pbs缓冲液稀释50倍。然后加入不同浓度的唾液酸混匀。将5μmol
·
l-1
的适配体序列与互补核酸序列在高温变性5min后冰浴10min,然后至于37℃孵育1h,之后通过磁性分离除去上清液,将沉淀用pbs缓冲液冲洗四次后重悬,与50μl含有不同浓度唾液酸的牛奶制品和人血清样品混匀,在室温下轻微震荡孵育30min。再通过磁性分离获取上清液。取50μl上清液,加入150μl构建好的荧光共振能量转移体系中混匀,再分别加入50μl 1μmol
·
l-1
的发夹结构探针hp1与hp2,在37℃下加核酸外切酶150u反应1.5h,最后,将酶切反应溶液置于荧光分光光度计下检测荧光,代入标准曲线可计算出唾液酸的浓度。
[0042]
具体样品和检测结果如表2所示。
[0043]
表2
[0044][0045]
以上所述实施例仅是为充分说明本发明而所举的较佳的实施例,本发明的保护范围不限于此。本技术领域的技术人员在本发明基础上所作的等同替代或变换,均在本发明
的保护范围之内。本发明的保护范围以权利要求书为准。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



