一种侧链修饰的聚氨基酸及其制备方法和用途与流程
 2021-02-02 07:02:25|
2021-02-02 07:02:25| 372|
372| 起点商标网
起点商标网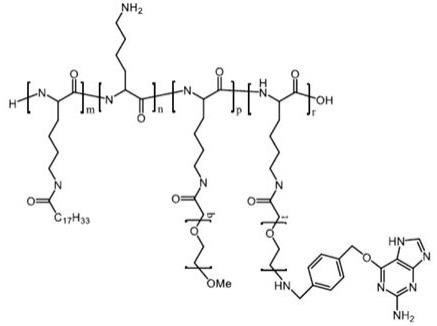
[0001]
本发明属于聚合物领域,涉及一种侧链修饰的聚氨基酸及其制备方法和用途,特别是用于递送核酸分子。
背景技术:
[0002]
病毒是危及人类健康的重大公共卫生安全威胁。使用疫苗是人类抗击病毒的有效手段。自从用种
‘
牛痘
’
的方式战胜天花病毒以来,疫苗帮助人类有效控制和预防多种病毒引起的疾病,包括甲肝病毒、乙肝病毒、乙型脑膜炎、及流感病毒。针对致命性的埃博拉(ebola)病毒和冠状病毒引起的严重急性呼吸道综合症(sars)、中东呼吸道综合症(mers)、2019冠状病毒病(covid-19),开发疫苗成为控制病毒感染疫情的迫切需求。根据不同技术路线,疫苗的类型包括灭活疫苗、重组蛋白疫苗、腺病毒载体疫苗、核酸疫苗。其中,核糖核酸(rna)疫苗通过细胞的蛋白质转录-翻译机制,在人体细胞的胞浆内产生与病毒受体结合区域、病毒衣壳蛋白或其他保守区域的蛋白质片段作为抗原,诱导免疫系统产生抗体,实现对病毒的免疫。
[0003]
核酸包括脱氧核糖核酸(dna)和核糖核酸(rna)是生命体系中重要的遗传物质。根据生命中心法则,遗传信息通过dna-rna-蛋白质的过程,转录和翻译成为功能性的蛋白质。该过程中,细胞利用信使rna(mrna)为模板翻译出蛋白质。信使rna(mrna)是一类rna分子,它将遗传信息保存在核苷酸a-u、g-c的碱基对序列中,将遗传信息从dna传递到核糖体,在那里作为蛋白质合成模板并表达蛋白产物。mrna疫苗无需蛋白质表达纯化,通过体外合成病毒的相关序列mrna,将mrna传递到人体细胞内形成免疫。mrna疫苗具有较多优势:1) mrna易在体外生产和纯化, 除去蛋白药物及病毒载体制备的复杂过程,同时可避免宿主蛋白及病毒源性污染;2) mrna的生产工艺通用性强,可以快速应用于生产不同的目的蛋白,节省药物研发时间,提高效率;3) mrna仅需进入细胞质即可翻译成蛋白质,无需进入细胞核,因此不存在基因的插入和整合,提高药物的安全性;4)通过调节序列修饰和递送载体可以改变其半衰期。rna疫苗生物安全性高、设计灵活、开发迅速、通用性强的特点,使之成为疫苗开发的重要途径(us20200085852)。rna疫苗不但可以预防和抑制病毒在生物体内的感染,还可以使用rna疫苗治疗肿瘤,例如已有报道针对黑色素瘤和小细胞肺癌开发的rna疫苗均已进入临床试验阶段。
[0004]
在临床试验发现,mrna疫苗有效发挥作用受到如下具体因素限制:1)不能自由通过生物膜;2)容易被血浆和组织中rna降解酶(rnase)分解; 3)进入细胞后被内吞小体(endosome)捕获,发展成“溶酶体陷阱”(lysosome trapping),无法发挥作用。因此mrna免疫效率依赖于提高mrna疫苗在体内的稳定性和克服细胞内囊泡转运机制。由于核苷酸2位的羟基取代,rna在生理环境下的稳定性不如dna。为了避免rna在体内循环过程中的水解和酶解消耗,rna疫苗和药物需要递送体系的包裹保护。通过递送体系使疫苗高效进入细胞并且从“溶酶体陷阱”中释放进入胞浆。rna疫苗的成药方式和递送方式对于药代动力学和剂量的控制起到关键作用。现有技术使用脂质体、脂质纳米颗粒作为递送体系制得mrna疫苗
和药物的纳米复合材料。含有正电荷类脂分子的脂质纳米颗粒可通过静电作用获得对带负电的核酸分子良好的装载效果(wo2017049245)。为了从“溶酶体陷阱”中高效释放rna疫苗和药物进入胞浆,需要对递送体系的稳定性和ph响应进行优化。还需要对核酸递送体系进行生物功能化,利用生物功能性配体和抗体,获得对目标细胞(如癌细胞、免疫系统的b细胞、t细胞)和组织(如淋巴组织、肺、小肠等器官)的靶向递送能力。
[0005]
胶束是双亲性分子在水溶液中自发形成的一种纳米聚集体形式,多为球状,还可为柱状。当含有亲水和亲油基团的表面活性剂在溶液中达到和超过临界胶束浓度(critical micelle concentration, cmc)后,自发缔合成为胶束。胶束在溶液中处于动态平衡,能够包裹和释放有效成分,适用于作为递送体系。胶束的疏水性内核使其能够包裹水相中难溶的疏水性化合物。具备负电性或正电性的组成成分的胶束,可以装载带有正电荷或负电荷的有效成分。具备生物相容性的胶束可以保持所接触生物分子的活性,确保低的细胞毒性,能在体内生物降解或无害地排除体外。现有技术报道了通过双亲性嵌段共聚物的结构设计形成高分子胶束。例如商品名为pluronic
®
f-127的一类聚环氧乙烷-聚环氧丙烷-聚环氧乙烷(peo-ppo-peo)三嵌段聚合物材料。此外,已有报道以壳多糖主链的接枝树枝状共聚物(wo2013064648a)形成胶束类纳米材料。在生物纳米材料应用领域,聚氨基酸是一类可完全生物降解的主链类型。聚氨基酸的主链基于酰胺键,在体内环境的生物稳定性优于酯键。
技术实现要素:
[0006]
本发明的目的是提供一种侧链修饰的聚氨基酸及其制备方法和用途,以及该侧链修饰的聚氨基酸形成胶束用于包覆和递送的用途,尤其用于对rna疫苗等核酸分子的包覆和递送。
[0007]
本发明目的是通过如下技术方案实现的:一种侧链修饰的聚氨基酸,其中,所述聚合物主链为聚赖氨酸,或者,赖氨酸与其他氨基酸形成的共聚物;所述其他氨基酸是丝氨酸、苏氨酸、酪氨酸、半胱氨酸、和精氨酸、组氨酸、甘氨酸、亮氨酸、异亮氨酸、缬氨酸、苯丙氨酸、色氨酸、脯氨酸、甲硫氨酸、天冬酰胺、谷氨酰胺中的任意一种或多种。
[0008]
所述聚合物的侧链中至少部分侧链分别含有基团a、和基团g,所述基团a为c
4-40
脂肪烃基,所述基团g为基团g1和/或g2, g1为端基连有c
1-10
烷氧基的聚乙二醇基团,g2为端基连有生物功能性基团的聚乙二醇基团;所述基团a与基团g通过连接基团与所述聚氨基酸的侧链相连。
[0009]
在一个实施方式中,所述连接基团如下:-nh-co-、-nh-、-n=cr
1-、-n-chr
1-、-nh-ch
2-co-、-o-co-、-o-、-o-ch
2-co-、-s-、-s-s-、-s-co-、-s-ch
2-co-或中的任意一种。其中,r1独立地选自h、c
1-6
烷基。
[0010]
根据本发明,所述连接基团中的氨基、氧、硫来自于聚氨基酸侧链上的活性基团,如氨基、羟基、巯基;
在所述连接基团与基团a或基团g中聚乙二醇之间可以是直键,也可以是任意的间隔基团。
[0011]
在一个实施方式中,所述聚乙二醇的重复单元数为1-600之间的整数,优选为2-300,更进一步优选4-200。
[0012]
在一个实施方式中,所述基团a为c
4-25
烷基、c
4-25
烯基、c
4-25
炔基。
[0013]
在一个实施方式中,所述基团g1中的烷氧基为c
1-6
烷氧基,例如甲氧基、乙氧基。
[0014]
根据本发明,所述生物功能性基团为能与蛋白质、多肽、氨基酸等生物分子结合的结合子,包括人工合成的结合子或天然生物分子。
[0015]
根据本发明,所述结合子包括:可以与亲和素结合的生物素;可以与snap蛋白连接的连接子,如苄基鸟嘌呤及其衍生物;可以与clip蛋白连接的连接子,如苄基胞嘧啶及其衍生物;可以与halotag蛋白连接的连接子(halotag ligand (htl)),如6-氯代正己烷及其衍生物;上述所述衍生物可以是乙二醇重复单元数小于46的寡聚乙二醇衍生物。
[0016]
根据本发明,所述天然生物分子包括:糖类分子、长度约为5-80个核苷酸的小的rna链段、氨基酸序列。
[0017]
所述糖类分子为能与受体蛋白质结合的糖类分子,包括单糖、二糖、寡聚糖;所述单糖为二羟丙酮、赤藓糖、苏力糖、阿拉伯糖、核糖、脱氧核糖、木糖、来苏糖、葡萄糖、甘露糖、果糖、半乳糖、鼠李糖。所述二糖为蔗糖、乳糖、麦芽糖;所述寡聚糖为麦芽三糖、松三糖、棉子糖、龙胆三糖、甘露三糖、鼠李三糖、及可以与其他小分子结合的α-环糊精,β-环糊精,γ-环糊精,δ-环糊精。
[0018]
所述小的rna链段为能够与待检测生物分子互补的核苷酸或脱氧核苷酸序列,例如含有10-60个核苷酸的能与蛋白质结合的核酸适配体序列。
[0019]
所述氨基酸序列为能够与蛋白质如抗体结合的氨基酸序列,包括流感病毒血凝素ha氨基酸序列、flag氨基酸序列、myc-tag氨基酸序列、以及含有-epea氨基酸序列的“c-tag”、和含有srleeelrrrl的氨基酸“alfa-tag”。
[0020]
本发明所述抗体为多克隆抗体、单克隆抗体、和纳米抗体,所述抗体为动物来源的抗体或重组蛋白质表达制备得到的抗体。
[0021]
根据本发明,所述侧链修饰的聚氨基酸可为如下中的一种:包括基团a和基团g1的聚氨基酸,包括基团a和基团g2的聚氨基酸,包括基团a、基团g1和基团g2的聚氨基酸。在所述聚合物中,可以存在不被修饰的聚氨基酸侧链。
[0022]
在一个实施方式中,所述聚合物中,含有基团g1和/或g2的侧链数占侧链总量的摩尔百分比为2%-98%,优选5%-90%,更优选10%-80%。
[0023]
在一个实施方式中,所述聚合物中,含有基团a的侧链数占全部侧链总量的摩尔百分比为2%-98%,优选5%-90%,更优选10%-80%。
[0024]
在一个实施方式中,所述聚合物中,含有a基团的侧链数与含有基团g1和/或g2的侧链数之和占全部侧链总量的摩尔百分比为5%-100%,优选20%-100%,更优选40%-100%,例如可以为30%-98%,35%-95%,40%-90%。
[0025]
在一个实施方式中,所述g2基团为-peg-t-b,其中,peg为聚乙二醇链段,b为生物功能性基团,t为连接基团,其将基团b连接到聚乙二醇链上。
[0026]
在一个实施方式中,所述连接基团t例如包括如下基团:
-
co-nh-、-co-o-、-o-、-o-ch
2-co-、-nh-、-n=cr
1-、-n-chr
1-、-nh-ch
2-co-、-s-s-、-s-co-、-s-ch
2-co-或、叠氮基与炔基发生点击反应得到的连接基团、四嗪与双键发生点击反应得到的连接基团中的任意一种。
[0027]
其中,所述叠氮基与炔基发生点击反应得到的连接基团为三唑基或其衍生物;所述四嗪与双键发生点击反应得到的连接基团为二氮杂环或其衍生物。
[0028]
本发明聚合物主链中的精氨酸、组氨酸、甘氨酸、亮氨酸、异亮氨酸、缬氨酸、苯丙氨酸、脯氨酸、甲硫氨酸、色氨酸、天冬酰胺、谷氨酰胺根据其侧链的疏水特性或分子构型、尺寸、芳香性、成氢键能力、ph值响应等特征,可以调节所述聚合物的亲疏水性、成氢键能力和ph值响应。
[0029]
在一个实施方式中,所述聚合物的主链为聚左旋赖氨酸。
[0030]
在一个实施方式中,所述聚合物的主链为人工合成的聚右旋赖氨酸。
[0031]
在一个实施方式中,所述聚合物的主链是α-聚赖氨酸。
[0032]
在一个实施方式中,所述聚合物的主链是ε-聚赖氨酸。
[0033]
在一个实施方式中,所述聚合物的主链为氨基酸共聚物,包括赖氨酸-精氨酸共聚物、赖氨酸-组氨酸共聚物、赖氨酸-丝氨酸共聚物、赖氨酸-苏氨酸共聚物、赖氨酸-酪氨酸共聚物、赖氨酸-半胱氨酸共聚物、赖氨酸-丝氨酸-苏氨酸共聚物、赖氨酸-精氨酸-组氨酸共聚物、赖氨酸-丝氨酸-苏氨酸-酪氨酸共聚物的任意一种。
[0034]
在一个实施方式中,所述聚合物的主链为氨基酸共聚物,包括赖氨酸-甘氨酸共聚物、赖氨酸-亮氨酸共聚物、赖氨酸-异亮氨酸共聚物、赖氨酸-缬氨酸共聚物、赖氨酸-苯丙氨酸共聚物、赖氨酸-色氨酸共聚物的任意一种。
[0035]
在一个实施方式中,所述侧链修饰的聚氨基酸中,赖氨酸占其他氨基酸与赖氨酸总量的摩尔百分比为0.1%-100%,优选10%-100%,更优选30%-100%。
[0036]
本发明所述侧链修饰的聚氨基酸例如具体可为:
ꢀꢀ
。
[0037]
本发明还提供一种侧链修饰的聚氨基酸,其由如下制备方法制备得到,包括:将聚氨基酸与一端连有c
1-10
烷氧基另一端连有反应性基团x1的聚乙二醇和/或一端连有生物功能性基团另一端连有反应性基团x2的聚乙二醇、以及一端连有反应性基团x3的c
4-40
脂肪烃进行反应;其中,反应性基团x1、x2、x3与聚氨基酸侧链上的活性基团氨基、羟基、巯基反应,将端基带有烷氧基和/或生物功能性基团的聚乙二醇以及脂肪烃基连接到聚氨基酸的侧链上。
[0038]
所述聚氨基酸为聚赖氨酸,或者,赖氨酸与其他氨基酸形成的共聚物;所述其他氨基酸是丝氨酸、苏氨酸、酪氨酸、半胱氨酸、和精氨酸、组氨酸、甘氨酸、亮氨酸、异亮氨酸、缬氨酸、苯丙氨酸、色氨酸、脯氨酸、甲硫氨酸、天冬酰胺、谷氨酰胺中的任意一种或多种。
[0039]
本发明中,赖氨酸的侧链含有氨基,丝氨酸、苏氨酸、酪氨酸侧链含有羟基,半胱氨酸侧链含有巯基,上述基团可以通过共价偶联反应进行侧链功能化修饰。
[0040]
本发明的精氨酸、组氨酸、甘氨酸、亮氨酸、异亮氨酸、缬氨酸、苯丙氨酸、脯氨酸、甲硫氨酸、色氨酸、天冬酰胺、谷氨酰胺根据其侧链的疏水特性或分子构型、尺寸、芳香性、成氢键能力、ph值响应等特征,可以用于调节聚氨基酸的亲疏水性、成氢键能力和ph值响应。
[0041]
在一个实施方式中,所述聚氨基酸为聚左旋赖氨酸。
[0042]
在一个实施方式中,所述聚氨基酸为人工合成的聚右旋赖氨酸。
[0043]
在一个实施方式中,所述聚赖氨酸是α-聚赖氨酸。
[0044]
在一个实施方式中,所述聚赖氨酸是ε-聚赖氨酸。
[0045]
在一个实施方式中,所述聚氨基酸为氨基酸共聚物,包括赖氨酸-精氨酸共聚物、赖氨酸-组氨酸共聚物、赖氨酸-丝氨酸共聚物、赖氨酸-苏氨酸共聚物、赖氨酸-酪氨酸共聚物、赖氨酸-半胱氨酸共聚物、赖氨酸-丝氨酸-苏氨酸共聚物、赖氨酸-精氨酸-组氨酸共聚物、赖氨酸-丝氨酸-苏氨酸-酪氨酸共聚物的任意一种。
[0046]
在一个实施方式中,所述聚氨基酸为氨基酸共聚物,包括赖氨酸-甘氨酸共聚物、赖氨酸-亮氨酸共聚物、赖氨酸-异亮氨酸共聚物、赖氨酸-缬氨酸共聚物、赖氨酸-苯丙氨酸共聚物、赖氨酸-色氨酸共聚物的任意一种。
[0047]
本发明还提供一种上述侧链修饰的聚氨基酸的制备方法,包括如下步骤:将聚氨基酸与一端连有c
1-10
烷氧基另一端连有反应性基团x1的聚乙二醇和/或一端连有生物功能性基团另一端连有反应性基团x2的聚乙二醇、以及一端连有反应性基团x3的c
4-40
脂肪烃进行反应;其中,反应性基团x1、x2、x3与聚氨基酸侧链上的活性基团氨基、羟基、巯基反应,将端基带有烷氧基和/或生物功能性基团的聚乙二醇以及脂肪烃基连接到聚氨基酸的侧链上。
[0048]
根据本发明的方法,所述方法可以将上述原料一锅反应,也可以分成两步或更多步进行反应。
[0049]
根据本发明,所述反应性基团x1、x2、x3例如选自羟基、羧基、醛基、酮基、酯基、巯基、马来酰亚胺、α-卤代羰基。
[0050]
例如,氨基与羧基缩合反应得到酰胺连接基团,或者氨基与醛基或酮基反应得到希夫碱连接基团,或者氨基与酯基反应得到酰胺连接基团,或者羟基与羧基缩合反应得到酯连接基团,或者羟基与羟基脱水进行缩合反应得到醚连接基团,或者巯基与马来酰亚胺进行加成反应,或者巯基与α-卤代羰基发生的取代反应,或者巯基与巯基进行反应。
[0051]
示例性地,当聚氨基酸的侧链含有氨基时,所述反应性基团x1、x2、x3为羧基、醛基、酮基、酯基、α-卤代羰基中的至少一种;当聚氨基酸的侧链含有羟基时,所述反应性基团x1、x2、x3为羧基、羟基、α-卤代羰基中的至少一种;当聚氨基酸的侧链含有巯基时,所述反应性基团x1、x2、x3为巯基、马来酰亚胺、α-卤代羰基中的至少一种。
[0052]
在一个实施方式中,所述聚乙二醇为链状聚乙二醇,优选的,重复单元数为1-600之间的整数,优选为2-300,进一步优选为4-200。
[0053]
所述一端具有反应性基团另一端具有烷氧基的聚乙二醇可以商购。也可以采用本领域的常规方法进行制备。
[0054]
所述一端具有反应性基团另一端具有生物功能性基团的聚乙二醇可以商购,也可以采用本领域的常规方法进行制备,例如通过如下方法制备得到:
将一端具有反应性基团x2一端具有反应性基团x4的聚乙二醇与带有反应性基团x5的生物功能性物质进行反应,所述反应性基团x4与反应性基团x5发生反应,从而使生物功能性基团连接到聚乙二醇的一端。
[0055]
根据本发明,所述反应性基团x4、x5例如选自羟基、氨基、羧基、醛基、酮基、酯基、巯基、马来酰亚胺、α-卤代羰基、炔基、烯键、叠氮基、四嗪基。其中,反应性基团x4、x5互为反应性基团,可以发生反应。
[0056]
例如,氨基与羧基缩合反应得到酰胺连接基团,或者氨基与醛基或酮基反应得到希夫碱连接基团,或者氨基与酯基反应得到酰胺连接基团,或者羟基与羧基缩合反应得到酯连接基团,或者羟基与羟基脱水进行缩合反应得到醚连接基团,或者马来酰亚胺与巯基进行加成反应,或者巯基与α-卤代羰基发生的取代反应,或者炔基与叠氮基发生点击反应得到连接基团,或者烯键与四嗪基发生点击反应得到连接基团。其中,炔基与叠氮基发生点击反应是本领域中已知的“点击化学”反应,例如:由金属离子(例如cu(i))催化的叠氮化物-炔环加成反应(sharpless反应,炔基一般在端基),或者,环张力催化的叠氮化物-炔环加成反应(spaac反应,炔基位于张力环的中间)。烯键与四嗪基发生点击反应是本领域中已知的反应,例如环烯烃与四嗪基发生环加成反应。
[0057]
示例性地,当x4为氨基时,x5为羧基、醛基、酮基、酯基、α-卤代羰基中的至少一种;当x4为羟基时,x5为羧基、羟基、α-卤代羰基中的至少一种;当x4为巯基时,x5为巯基、马来酰亚胺、α-卤代羰基中的至少一种;当x4为炔基时,x5为叠氮基;当x4为烯键时,x5为四嗪基。反之也成立。
[0058]
在聚乙二醇与端基的反应性基团x1、x2、x4或生物功能性基团之间可以直接连接,即作为封端基团,也可以通过任意的间隔基团进行连接,这依赖于采用本领域中特定的常规方法将上述反应性基团或生物功能基团引入到聚乙二醇上。在聚乙二醇与反应性基团之间的间隔基团可以是任意的,只要不影响制备本发明所述的聚合物,所述间隔基团例如为c
1-12
烷基、酯基、酰胺基、酮基等。
[0059]
所述聚氨基酸为聚赖氨酸或由赖氨酸和其他氨基酸聚合形成;所述其他氨基酸是丝氨酸、苏氨酸、酪氨酸半胱氨酸、和精氨酸、组氨酸、甘氨酸、亮氨酸、异亮氨酸、缬氨酸、苯丙氨酸、色氨酸、脯氨酸、甲硫氨酸、天冬酰胺、谷氨酰胺的任意一种或多种。作为实例,所述聚氨基酸为多聚左旋赖氨酸,以及人工合成的多聚右旋赖氨酸等。
[0060]
根据本发明,所述聚氨基酸重复单元数为2-3000的整数,优选2-1500,更优选2-1000,再优选2-500。
[0061]
在一个实施方式中,所述聚氨基酸中,赖氨酸占其他氨基酸与赖氨酸总量的摩尔百分比为0.1%-100%,优选10%-100%,更优选30%-100%。
[0062]
根据本发明,上述步骤中,所述反应均为本领域的常规反应步骤,示例性地,所述反应的温度为10-40℃。
[0063]
根据本发明,所述反应可以在偶联剂促进下进行。例如氨基与羧基在偶联剂存在下缩合反应得到酰胺连接基团,或者羟基与羧基在偶联剂存在下缩合反应得到酯连接基团。所述偶联剂例如为碳二亚胺衍生物,选自1-乙基-3-(3-二甲基氨基丙基)碳二亚胺盐酸盐,或n,n-二环己基碳二亚胺,偶联剂与反应物的摩尔比为1至500,优选1至100,更优选1至50,再优选1至20。
[0064]
本发明还提供上述侧链修饰的聚氨基酸的用途,其用于制备胶束。
[0065]
本发明还提供一种胶束,所述胶束包括上述的侧链修饰的聚氨基酸。
[0066]
根据本发明,所述胶束是通过将侧链修饰的聚氨基酸溶解到溶剂中形成的。优选地,将侧链修饰的聚氨基酸溶解在水溶液中,使其浓度为1-1000倍临界胶束浓度。
[0067]
根据本发明,所述胶束是由本发明所述的一种侧链修饰的聚氨基酸组成,或者由本发明所述的两种以上侧链修饰的聚氨基酸组合而成。所述组合可以是二元、三元或多元侧链修饰的聚氨基酸的组合,组合物中的各侧链修饰的聚氨基酸的百分比没有特定的限制只要组合物能够形成胶束。
[0068]
根据本发明,所述侧链修饰的聚氨基酸的临界胶束浓度是通过本领域已知的方法测试得到的,例如包括电导法、表面张力法、滴体积法、超滤曲线法、单点式超滤法、双点式超滤法、紫外分光光度法、染料吸附法、光散射发法、荧光探针法、溶解度法。
[0069]
根据本发明,所述侧链修饰的聚氨基酸的胶束粒径均值小于300nm,优选小于200 nm,更优选小于100 nm,进一步优选小于80 nm。
[0070]
根据本发明,所述侧链修饰的聚氨基酸的胶束粒径是通过本领域已知的方法测试得到的,例如包括动态激光散射法、荧光相关光谱法、扫描电子显微镜成像。
[0071]
本发明还提供上述胶束的制备方法,所述方法包括如下步骤:将上述侧链修饰的聚氨基酸溶解在溶剂中,使其浓度为1-1000倍临界胶束浓度。
[0072]
根据本发明,优选地,所述浓度为1-200倍临界胶束浓度,更优选地,浓度为1-50倍临界胶束浓度,进一步优选地,浓度为1-10倍临界胶束浓度。
[0073]
根据本发明,所述溶剂例如为水溶液或ph3-8的缓冲液,例如醋酸盐缓冲液、磷酸盐缓冲液。
[0074]
本发明还提供上述侧链修饰的聚氨基酸胶束在核酸的包覆和递送中的用途。
[0075]
本发明所述核酸包括rna和dna。
[0076]
在一个实施方式中,本发明所述rna为单链rna。
[0077]
在一个实施方式中,本发明所述rna为双链rna。
[0078]
本发明所述的核酸可为rna疫苗、rna药物、dna疫苗。
[0079]
本发明的核酸可以为疫苗或药物,用于治疗或防治传染病、肿瘤、罕见病、以及其他蛋白缺陷类疾病等,或者用于美容及抗衰老等。
[0080]
本发明用于治疗传染病的rna目标序列是病毒的受体结合区域、病毒的衣壳蛋白或病毒的其他保守区域的蛋白质或蛋白质片段的基因序列。
[0081]
本发明还提供一种递送体系,所述递送体系包括胶束和核酸,所述核酸位于胶束内部。
[0082]
根据本发明,所述递送体系可选地包含有佐剂,所述佐剂选自天然磷脂分子、胆固醇、氨基酸、多肽、离子型表面活性剂和非离子型表面活性剂。
[0083]
根据本发明,可选地,所述佐剂与rna链的摩尔比0.001-8000,优选0.01-4000,更优选为0.1-1000。
[0084]
本发明还提供一种递送体系的制备方法,将含有所述胶束的溶液与核酸接触,孵育混合溶液,制备得到所述的递送体系。
[0085]
本发明还提供一种递送体系的制备方法,将所述侧链修饰的聚氨基酸与核酸形成
混合溶液,制备得到所述的递送体系。
[0086]
所述递送体系可以任选地蒸干溶剂,得到冻干粉。当使用时再溶于溶剂中重新形成递送体系。
[0087]
根据本发明,所述核酸与侧链修饰的聚氨基酸的摩尔比为0.001-1000,优选0.01-100,更优选为0.1-10。
[0088]
其中,接触过程中使用机械搅拌、振荡、加热回流或超声分散。
[0089]
其中,含有所述胶束的溶液例如可以是含有胶束的有机溶液,所述有机溶液的溶剂没有特别限制,只要其能够溶解所述材料即可,可选地为醇、醚、酮、酯、酰胺、亚砜、烷烃、环烷烃、芳香烃、氯代烷烃其中之一,或其混合。
[0090]
[术语和解释]本发明中“侧链修饰的聚氨基酸”、“双亲性聚氨基酸”可互换名称。
[0091]
本发明所述的“脂肪烃”,也可以称为脂肪族化合物,其是指结构中不含有芳香环的烃类,其中碳原子以直链、支链或环状排列,分别称为直链脂肪烃、支链脂肪烃及脂环烃。脂肪族化合物可以是烷烃、烯烃或炔烃。本发明所述脂肪烃的碳原子数可以为1-40个。
[0092]
本发明所述的烷基代表碳原子数为1-40的直链、支链或环状烷基,例如,甲基、乙基、丙基、异丙基、丁基等。
[0093]
本发明所述的烯基代表碳原子数为1-40的直链、支链或环状烯基,例如,乙烯、丙烯、异丙烯、丁烯等。优选的,双键的数目为1到6的整数。
[0094]
本发明所述的炔基代表碳原子数为1-40的直链、支链或环状炔基,例如,乙炔、丙炔、丁炔等。优选的,炔键的数目为1到6的整数。
[0095]
本发明所述氨基代表基团-n(r2)2,其中,r2独立的选自h、c
1-6
烷基。
[0096]
本发明所述的酯基代表基团-co-or3,其中,r3为c
1-6
烷基。
[0097]
术语“反应性基团”也可称为“活性基团”,是指可与另一个“反应性基团”形成化学键的官能团。适合的化学键在本领域中众所周知,例如可以为:羟基、氨基、羧基、醛基、酮基、酯基、巯基、马来酰亚胺、α-卤代羰基、炔基、烯键、叠氮基、四嗪基。
[0098]
术语“连接基团”是指将任意两个基团连接起来的基团,其是由两个“反应性基团”进行反应后形成的基团。
[0099]
术语“间隔基团”是指通过常规反应将反应性基团等引入聚乙二醇链端时可能形成的基团。该基团依赖于引入基团时所使用的试剂。
[0100]
术语“结合子”是指能够与蛋白质、多肽、氨基酸等生物分子通过例如共价键、非共价键等方式结合的物质。
[0101]
术语“连接子”也可称为“配体连接子”,英文为ligand,其是指通过共价连接的方式与蛋白质、氨基酸、抗体、多肽等相连的基团。
[0102]
术语“核酸
”ꢀ
是指脱氧核糖核酸(dna)和核糖核酸(rna)。
[0103]
本发明的有益效果:本发明提供了一种侧链修饰的聚氨基酸及其制备方法,所述侧链修饰的聚氨基酸通过引入亲水性成分和疏水性成分,能够高效形成聚合物胶束。所述侧链修饰的聚氨基酸具有如下优势:(1)主链和侧链结构及其连接方式都可以灵活选取,调节亲水性基团、电荷特性、疏水性基团的数量和种类,使制得的聚合物胶束具有良好生物相容性和靶向递送效率。(2)
聚氨基酸主链的电荷极性为电正性,侧链的反应性基团可以分别为氨基、羟基、巯基。通过精氨酸、组氨酸、丝氨酸等其他共聚氨基酸的数量和分布,调节主链电荷分布,实现对负电性rna的高效、可控包裹。对主链的电荷调节促进胶束的ph值响应,帮助rna从“溶酶体陷阱”中逃离进入胞浆。(3)通过量化侧链修饰脂肪链的链长、饱和度和脂肪链数量来控制侧链的疏水性部分,精确调节疏水部分的体积和缔合作用强度,而亲水部分的体积通过选择聚乙二醇高分子链长和分支数量调节,两者协同配合,实现聚合物胶束尺寸和稳定性精确调控。本发明的聚合物胶束的尺寸小,具有很好的组织穿透性。(4)由于rna和dna在结构和负电性上的相似性,通过灵活调整本发明胶束的基础电荷、尺寸和稳定性,高效构建包裹和递送体系,可实现rna疫苗、rna药物和dna疫苗的高效包裹和递送。通过主链构成、侧链修饰双管齐下,促进胶束的ph值响应,帮助核糖核酸从“溶酶体陷阱”中逃离进入胞浆。(5)通过双亲性功能高分子的侧链修饰引入不同的生物功能基团,包括小分子结合子、蛋白质、抗体等靶向结合效应物,实现递送体系对靶点组织和部位的特异性结合,提高靶向递送效果。
附图说明
[0104]
图1为实施例6制备的双亲性聚氨基酸的氢核磁共振谱局部。
[0105]
图2为实施例12使用实施例3制备的双亲性聚氨基酸的临界胶束浓度测定结果。
[0106]
图3为实施例12使用实施例3制备的双亲性聚氨基酸形成的胶束的动态激光散射结果,尺寸分布用对数坐标表示。
[0107]
图4为实施例13使用实施例9制备的双亲性聚氨基酸形成的胶束的动态激光散射结果,尺寸分布用对数坐标表示。
[0108]
图5为实施例17制备的包含mrna疫苗的双亲性聚氨基酸胶束的动态激光散射结果,尺寸分布用对数坐标表示。
[0109]
图6为实施例20制备的包含mrna疫苗的双亲性聚氨基酸胶束的动态激光散射结果,尺寸分布用对数坐标表示。
具体实施方式
[0110]
下文将结合具体实施例对本发明的制备方法做更进一步的详细说明。应当理解,下列实施例仅为示例性地说明和解释本发明,而不应被解释为对本发明保护范围的限制。凡基于本发明上述内容所实现的技术均涵盖在本发明旨在保护的范围内。
[0111]
下述实施例中所使用的实验方法如无特殊说明,均为常规方法;下述实施例中所用的试剂、材料等,如无特殊说明,均可从商业途径得到。
[0112]
下述实施例中所使用的缓冲液为常用的缓冲溶液,包括磷酸盐缓冲溶液、hepes缓冲液和tris缓冲液,水为高压釜灭菌处理后的miliq去离子水,电导率为18.2欧姆*厘米。
[0113]
下述实施例中使用的百分数(%)均为摩尔百分数。
[0114]
任选表示所述特征存在或不存在,还表示所述特征一定存在,只是具体选择可以随意。
[0115]
实施例1双亲性聚氨基酸pll-ol25-peg2000-biotin20的制备称取10 mg α-聚左旋赖氨酸的氢溴酸盐(pll的氢溴酸盐,平均分子量22500道尔顿),将其溶于150
ꢀµ
l磷酸盐缓冲液中(ph 7.4)得到溶液(a)。称取20 mg端基修饰生物素和琥珀
酰亚胺羧甲基酯的聚乙二醇2000(biotin-peg2000-scm,聚乙二醇平均分子量2000道尔顿,购自北京键凯科技股份有限公司),将其溶于150
ꢀµ
l四氢呋喃(分析纯,南京试剂公司)中得到溶液(b)。向(b)中加入4.1
ꢀµ
l经蒸馏纯化的油酸(ol)。室温下在试管中将溶液(a)与溶液(b)混合,立即向所得混合溶液加入35 mg 1-乙基-3-(
-ꢀ
3-二甲基氨基丙基)碳二亚胺盐酸盐(edc)。室温下振荡过夜,反应8小时,加入100
ꢀµ
l tris缓冲液ph 8.0,继续振荡1小时终止反应。去离子水中透析反应溶液24小时(mwco 50万道尔顿)。所得溶液冷冻处理后置于冻干机中制得25 mg冻干粉。该冻干粉为25%油酸和20%聚乙二醇2000-生物素接枝修饰的功能化双亲性聚氨基酸,该聚合物命名为pll-ol25-peg2000-biotin20,具体结构式如下所示。
[0116]
其中,未连接其他成分的侧链数用n表示。聚氨基酸主链连接有聚乙二醇的侧链数用p表示,聚乙二醇的重复单元数用q表示,聚氨基酸连接有疏水性成分的侧链数用m表示实施例2双亲性聚氨基酸pll-ol25-peg3500-biotin20的制备在2毫升离心管中称取10 mg pll的氢溴酸盐(平均分子量22500道尔顿),将其溶于150
ꢀµ
l磷酸盐缓冲液(ph 7.4)中得到溶液(a)。称取33 mg端基修饰生物素和琥珀酰亚胺羧甲基酯的聚乙二醇3500(biotin-peg3500-scm,聚乙二醇平均分子量3500道尔顿,购自北京键凯科技股份有限公司),将其溶于150
ꢀµ
l 四氢呋喃中得到溶液(b)。向(b)中加入4.1
ꢀµ
l经蒸馏纯化的油酸(ol)。按照实施例1的方法制备得到反应产物,冻干处理制得31 mg冻干粉。该白色粉末为25%油酸和20%聚乙二醇3500-生物素接枝修饰的功能化双亲性聚氨基酸,该聚合物命名为pll-ol25-peg3500-biotin20。
[0117]
实施例3双亲性聚氨基酸pll-no25-peg3500-biotin20的制备与实施例2类似,不同在于使用2.5
ꢀµ
l正辛酸(no)制得35 mg白色冻干粉末,其为25%正辛酸和20%聚乙二醇3500-生物素接枝修饰的功能化双亲性聚氨基酸,该聚合物命名为pll-no25-peg3500-biotin20。
[0118]
实施例4双亲性聚氨基酸pll-ol50-peg3500-biotin50的制备与实施例2类似,不同在于称取82 mg端基修饰琥珀酰亚胺羧甲基酯和生物素的聚乙二醇3500,将其溶于150
ꢀµ
l 四氢呋喃中得到溶液(b)。向(b)中加入7.9
ꢀµ
l油酸(ol),按照实施例1的方法制得白色冻干粉末,其为50%油酸和50%聚乙二醇3500-生物素接枝修饰的功能化双亲性聚氨基酸,命名为pll-ol50-peg3500-biotin50。
[0119]
实施例5双亲性聚氨基酸εpll-la25-peg5000
-ꢀ
biotin30的制备在2毫升离心管中称取10 mg ε-聚左旋赖氨酸的氢溴酸盐(以下称为εpll的氢溴酸盐,平均分子量50000道尔顿),将其溶于150
ꢀµ
l 磷酸盐缓冲液中得到溶液(a)。称取60 mg端基修饰生物素和琥珀酰亚胺羧甲基酯的聚乙二醇5000(biotin-peg5000-scm,平均分子量5000道尔顿,购自北京键凯科技股份有限公司),将其溶于150
ꢀµ
l 四氢呋喃中得到溶液(b)。向(b)中加入2.8
ꢀµ
l月桂酸(la),室温下在试管中将溶液(a)与溶液(b)混合,立即向所得混合溶液加入35 mg edc进行偶联反应。室温下振荡过夜,反应8小时,加入100
ꢀµ
l 20 mm tris缓冲液ph 8.0,继续振荡1小时终止反应。去离子水中透析反应溶液24小时(mwco 50万道尔顿)。所得溶液冷冻处理后置于冻干机中制得43 mg冻干粉,-20 ℃下密封存放。该白色粉末为25%月桂酸和30%聚乙二醇5000-生物素接枝修饰的功能化双亲性聚氨基酸εpll-la25-peg5000-biotin30,结构式如下。
[0120]
其中,未连接其他成分的侧链数用n表示。聚氨基酸主链连接有聚乙二醇的侧链数用p表示,聚乙二醇的重复单元数用q表示,聚氨基酸连接有疏水性成分的侧链数用m表示。
[0121]
实施例6 双亲性聚氨基酸εpll-ol25-peg5000-n3的制备称取10 mg εpll(平均分子量50000道尔顿),将其溶于150
ꢀµ
l 磷酸盐缓冲液中得到溶液(a)。称取72 mg端基修饰叠氮盐和琥珀酰亚胺羧甲基酯的聚乙二醇5000(azide-peg5000-scm,平均分子量5000道尔顿,购自北京键凯科技股份有限公司),将其溶于150
ꢀµ
l 四氢呋喃中得到溶液(b)。向(b)中加入4.1
ꢀµ
l油酸(ol),室温下在试管中将溶液(a)与溶液(b)用振荡器混合。按照实施例5的描述制得产物,冻干制得38 mg冻干粉,-20℃下密封存放。该白色粉末为25%油酸和30%聚乙二醇5000-叠氮盐接枝修饰的双亲性聚氨基酸,该聚合物命名为εpll-ol25-peg5000-n3。产物的质子核磁共振谱如图1所示(1h-nmr,500 mhz, cdcl3)。
[0122]
实施例7双亲性聚氨基酸pll-la25peg2000-ome37的制备在2毫升离心管中称取10 mg pll的氢溴酸盐(平均分子量22500道尔顿),将其溶于150
ꢀµ
l 磷酸盐缓冲液中得到溶液(a)。称取36 mg端基修饰甲氧基和琥珀酰亚胺羧甲基酯的聚乙二醇(m-peg2000-scm,平均分子量2000道尔顿,购自北京键凯科技股份有限公司),将其溶于150
ꢀµ
l四氢呋喃中得到溶液(b)。向(b)中加入2.8
ꢀµ
l月桂酸,室温下在试管中将溶液(a)与溶液(b)振荡器混合。按照与实施例1类似的方法,用edc偶联制得30 mg白色冻干粉末。该白色粉末为25%月桂酸和37%聚乙二醇2000-甲氧基接枝修饰的双亲性聚氨基酸,该聚合物命名为pll-la25-peg2000-ome37。具体结构式如下所示。
[0123]
其中,未连接其他成分的侧链数用n表示。聚氨基酸主链连接有聚乙二醇的侧链数用p表示,聚乙二醇的重复单元数用q表示,聚氨基酸连接有疏水性成分的侧链数用m表示。
[0124]
实施例8 双亲性聚氨基酸pll-la25-peg2000-ome75的制备与实施例7类似,不同在于称取73 mg端基修饰甲氧基和琥珀酰亚胺羧甲基酯的聚乙二醇(m-peg2000-scm,平均分子量2000道尔顿,购自北京键凯科技股份有限公司),将其溶于150
ꢀµ
l四氢呋喃中得到溶液(b)。制得59 mg白色冻干粉末,其为25%油酸和75%聚乙二醇2000-甲氧基接枝修饰的双亲性聚氨基酸,该聚合物命名为pll-la25-peg2000-ome75。
[0125]
实施例9双亲性聚氨基酸pll-no25-peg2000-ome37的制备与实施例7类似,不同在于玻璃小瓶量取2.5
ꢀµ
l正辛酸(no),置于150
ꢀµ
l 四氢呋喃中得到溶液(c)。制得22 mg白色冻干粉末,其为25%正辛酸和37%聚乙二醇2000-甲氧基接枝修饰的双亲性聚氨基酸,该聚合物命名为pll-no25-peg2000-ome37。
[0126]
实施例10 生物功能化双亲性聚氨基酸pll-ol25-peg2000-ome30-peg2000-bg30的制备称取96 mg端基修饰为双琥珀酰亚胺羧甲基酯修饰的聚乙二醇(scm-peg2000-scm,peg平均分子量2000道尔顿,购自北京键凯科技股份有限公司)和 10 mg snaptag蛋白的连接子o6-[4-(氨基甲基)苄基]鸟嘌呤(缩称为bg,购自santa cruz biotechnology公司),将其溶于无水200
ꢀµ
l 四氢呋喃,加入4
ꢀµ
l 三乙胺,氮气保护室温下反应4小时,加入去离子水30分钟,终止反应。置于真空烘箱中,60
°
c除去有机溶剂。用g200硅胶层析板分离反应产物,流动相为二氯甲烷:乙酸乙酯(80:20体积比),rf值0.25处收集产物条带,得到41 mg油状物cooh-peg2000-bg,将其溶于200
ꢀµ
l四氢呋喃,避光保存。
[0127]
称取7.5 mg聚左旋赖氨酸的氢溴酸盐(pll的氢溴酸盐,平均分子量22500道尔顿),将其溶于100
ꢀµ
l的5 mm hepes缓冲溶液(ph 7.4)得到溶液(a)。用玻璃小瓶量称取24 mg 两端分别为甲氧基和琥珀酰亚胺酯的聚乙二醇(m-peg2000-scm,聚乙二醇平均分子量2000道尔顿,购自北京键凯科技股份有限公司),将其溶于150
ꢀµ
l 四氢呋喃中,加入114
ꢀµ
l 上述制备的cooh-peg2000-bg的四氢呋喃溶液,得到溶液(b)。向溶液(b)中加入3.2
ꢀµ
l油
酸。将溶液(a)、(b)混合,立即向所得混合溶液加入28 mg edc偶联试剂,振荡过夜,加入100
ꢀµ
l去离子水30分钟终止反应。透析反应溶液24小时(mwco 50万道尔顿)。冻干处理制得29 mg冻干粉。该冻干粉为25%油酸和30%聚乙二醇2000-甲氧基以及30%聚乙二醇2000-snaptag蛋白的配体连接子接枝修饰的双亲性聚氨基酸,该聚合物命名为pll-ol25-peg2000-ome30-peg2000-bg30。具体结构式如下所示。
[0128]
其中,未连接其他成分的侧链数用n表示。连接有聚乙二醇-甲氧基的侧链数用p表示,聚乙二醇的重复单元数用q表示。连接有聚乙二醇-bg的侧链数用r表示,聚乙二醇的重复单元数用t表示。连接有疏水性成分的侧链数用m表示。
[0129]
实施例11 多肽生物功能化双亲性聚氨基酸pll-ol25-peg3500-ha30的制备用塑料小瓶量称取7.5 mg聚左旋赖氨酸(pll,平均分子量22500道尔顿),将其溶于200
ꢀµ
l的hepes缓冲溶液(100 mm,ph 7.4)得到溶液(a)。另称取42 mg端基修饰分别为马来酰亚胺和琥珀酰亚胺羧甲基酯的聚乙二醇(mal-peg3500-scm,peg平均分子量2000道尔顿,购自北京键凯科技股份有限公司)和 13 mg 氨基酸序列为cypydvpdya的多肽冻干粉(ha-tag,n端为乙酰基修饰),将其溶于200
ꢀµ
l hepes缓冲溶液中(5 mm hepes)调节溶液ph为 6.0,得到溶液(b)。室温下震荡10分钟后,得到端基分别为含有ha多肽序列偶联物和琥珀酰亚胺羧甲基酯的聚乙二醇溶液,将其加入溶液(a)中,室温下振荡4小时。将混合溶液加入到400
ꢀµ
l含有3.2
ꢀµ
l油酸的四氢呋喃溶液中。溶液转移至玻璃小瓶中,立即向所得混合溶液加入28 mg edc偶联试剂,振荡过夜,加入100
ꢀµ
l去离子水30分钟终止反应。透析反应溶液24小时(mwco 50万道尔顿)。冻干处理制得32 mg冻干粉。该冻干粉为25%油酸和30%聚乙二醇3500-ha-tag接枝修饰的双亲性聚氨基酸,该聚合物命名为pll-ol25-peg3500-ha30。
[0130]
实施例12双亲性聚氨基酸胶束的制备和表征本实施例以实施例3制备的生物功能化正辛酸-聚乙二醇接枝修饰的聚赖氨酸pll-no25-peg3500-biotin20为例,说明用探针稳态荧光发射法测定双亲性聚氨基酸胶束的临界胶束浓度cmc和动态激光散射法测量胶束的水合直径。
[0131]
将探针芘(sigma 公司产品,金标签,未经进一步纯化)用无水甲醇溶解,配制成1.0
ꢀ×ꢀ
10-4 mol/l溶液备用。取5
ꢀµ
l 芘甲醇溶液,放入一系列5 ml 容量瓶中, 通氮气将甲醇吹干,依次加入5 ml 不同浓度的pll-no25-peg3500-biotin20的水溶液, 放入超声浴槽中分散1 小时,取1ml样品溶液用于测定芘的荧光发射光谱。荧光光谱用日本日立hitachi f-4500 型荧光分光光度计检测,激发波长为335 nm,狭缝宽度设定为激发:5 nm,发射:2.5 nm, 检测器偏压为700 v。实验温度22
ꢀ±ꢀ1ꢀ°
c。
[0132]
附图2 显示芘在不同浓度的pll-no25-peg3500-biotin20水溶液中的荧光发射光谱变化。芘的第一峰(373 nm)与第三峰(384 nm)荧光强度之比(i1/ i3,附图2a)反应芘分子周围微环境的极性变化。随着双亲性聚氨基酸pll-no25-peg3500-biotin20在水溶液中浓度的提高,该比值依次降低(附图2b)。 当双亲性聚氨基酸浓度增大到一定值时曲线发生突变,该处突变表明芘所处环境极性的变化,显示形成pll-no25-peg3500-biotin20胶束。因此,第一处突变点对应于pll-no25-peg3500-biotin20的cmc 值。通过该方法测得pll-no25-peg3500-biotin20的临界胶束浓度为1.6 mg/ml。当pll-no25-peg3500-biotin20在水溶液中的浓度大于该值时,即可形成胶束。
[0133]
配制浓度为3.0 mg/ml pll-no25-peg3500-biotin20 水溶液(大于cmc浓度),取1 ml溶液进行动态激光散射实验。使用英国malvern instruments 公司的zetasizer nano zs zen3600测得胶束的水合直径为93
ꢀ±ꢀ
36 nm,结果如图3所示。
[0134]
实施例13双亲性聚氨基酸胶束的制备和表征以实施例9制备的正辛酸-聚乙二醇接枝修饰聚赖氨酸pll-no25-peg2000-ome37为例,说明用探针稳态荧光发射法测定双亲性聚氨基酸胶束的临界胶束浓度和动态激光散射法
测量胶束的平均水合直径小于80 nm。按照实施例12描述的芘荧光探针法,测得芘的第一峰(373 nm)与第三峰(384 nm)荧光强度之比(i1/ i3)的第一处突变点为2.3 mg/ml。此处对应于pll-no25-peg2000-ome37的临界胶束浓度(cmc)为2.3 mg/ml。将pll-no25-peg2000-ome37配制浓度为5.0 mg/ml 的磷酸盐缓冲溶液(ph值7.4),取1 ml溶液进行动态激光散射实验。使用英国zetasizer nano zs zen3600(malvern instruments 公司)测得胶束的水合直径为75
ꢀ±ꢀ
28 nm,结果如图4所示。
[0135]
实施例14 禽流感病毒h7n9亚型mrna疫苗的制备第一步,合成dna模板。为了制备mrna疫苗,首先合成dna序列用于随后的体外转录。选择禽流感病毒a/shanghai/02/2013(h7n9)聚合酶pb2的基因序列片段作为目标抗原序列(基因序列-1)。目标抗原序列经gc含量优化(优化方法参见mol. ther. 23, 1456
–
1464 (2015)),在其5
’
端添加非翻译区调控元件(i)5
’
utr (β-globin-1):cagggcagagccatctattgcttacatttgcttctgacacaactgtgttcactagcaacctcaaacagacacc。
[0136]
在其3
’
端添加非翻译区调控元件(ii)3
’
utr (2β-globin):agctcgctttcttgctgtccaatttctattaaaggttcctttgttccctaagtccaactactaaactgggggatattatgaagggccttgagcatctggattctgcctaataaaaaacatttattttcattgcagctcgctttcttgctgtccaatttctattaaaggttcctttgttccctaagtccaactactaaactgggggatattatgaagggccttgagcatctggattctgcctaataaaaaacatttattttcattgc该(i)5
’
utr中的序列可以抑制5
’-
核酸外切降解,而(ii)3
’
utr中的序列可以抑制mrna的去甲腺苷酸化,以增强mrna的稳定性和翻译效率。在3
’
端进一步添加70个重复腺苷和30个重复的胞嘧啶,形成(iii)poly-a尾和poly-c尾,以增强mrna的稳定性:ttaataaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaatattcccccccccccccccccccccccccccccccctctagacaattggaatt将上述所有dna序列按照5
’
utr-目标序列-3
’
utr-polya-polyc的组装顺序合成为线性模板,进行下一步的体外转录。
[0137]
第二步,体外转录。在cap类似物(m7gpppg)存在下,使用t7聚合酶体外转录制备的dna模板,制成“加帽”mrna。随后,使用megaclear transcription clean-up kit (购自赛诺菲公司, waltham, ma, usa)纯化mrna。得到的样品可立即用于形成胶束包裹制剂或冻干保存。
[0138]
实施例15 甲型流感病毒h1n1的mrna疫苗的制备第一步,合成dna模板。使用a/puerto rico/8/1934 h1n1流感病毒血凝素ha的基因序列(基因序列-2)作为目标抗原的dna序列。目标基因序列gc含量经优化后(优化方法参见mol. ther. 23, 1456
–
1464 (2015)),在5
’
端添加非翻译区调控元件(i)5
’
utr (β-globin-2):agagcggccgctttttcagcaagattaagcccagggcagagccatctattgcttacatttgcttctgacacaactgtgttcactagcaacctcaaacagacacc 3
’
端添加非翻译区调控元件(ii)3
’
utr (2β-globin):agctcgctttcttgctgtccaatttctattaaaggttcctttgttccctaagtccaactactaaactgggggatattatgaagggccttgagcatctggattctgcctaataaaaaacatttattttcattgcagctcgctttcttgctg
tccaatttctattaaaggttcctttgttccctaagtccaactactaaactgggggatattatgaagggccttgagcatctggattctgcctaataaaaaacatttattttcattgc进一步添加(iii)含重复腺苷和重复的胞嘧啶序列的poly-a尾和poly-c尾:ttaataaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaaatattcccccccccccccccccccccccccccccccctctagacaattggaatt将上述所有dna序列按照5
’
utr-目标序列-3
’
utr-polya-polyc的组装顺序合成为线性模板,进行下一步的体外转录。
[0139]
第二步,体外转录。在cap类似物(m7gpppg)存在下,使用t7聚合酶体外转录制备得到的dna模板,制成“加帽”mrna。随后,使用megaclear transcription clean-up kit (购自赛诺菲公司, waltham, ma, usa)纯化mrna。经上述体外转录、加帽和纯化得到甲型流感病毒h1n1的mrna疫苗,用于形成胶束包裹制剂或冻干保存。
[0140]
实施例16 冠状病毒sars-cov-2的mrna疫苗的制备按照实施例15描述的方法,第一步,合成dna模板。使用sars-cov-2 冠状病毒表面刺突蛋白受体结合区域的基因序列(nih gene id: 43740568,基因序列-3)作为目标抗原的dna序列。目标基因序列经gc含量优化,添加非翻译区调控元件(i)5
’
utr (β-globin-2),(ii)3
’
utr (2β-globin),以及(iii)重复腺苷和胞嘧啶的poly-a尾和poly-c尾,合成为线性模板。第二步,所得dna模板经体外转录、加帽和纯化得到冠状病毒sars-cov-2的mrna疫苗,用于形成胶束包裹制剂或冻干保存。实施例17 制备包含mrna疫苗的双亲性聚氨基酸胶束在10毫升圆底烧瓶中,将10 mg实施例3制备的pll-no25-peg3500-biotin20溶于300微升乙醇中,向该双亲性聚氨基酸溶液中迅速加入200微升包含3 mg实施例14制备的禽流感病毒h7n9亚型mrna疫苗水溶液(水经高压釜处理,确保无活性核酸水解酶,ph值用盐酸调节为4)。其后用针管通氮气吹除溶剂至形成透明薄膜。加入2 ml纯水,在10℃冷室中涡旋振荡15分钟。该体积下pll-no25-peg3500-biotin20的浓度大于临界胶体浓度(见实施例12测得cmc),聚氨基酸和mrna形成胶束溶液。取200
ꢀµ
l样品在纯水中稀释5倍,溶液进行动态激光散射实验(方法参见实施例12),测得胶束的水合直径为144
ꢀ±ꢀ
34 nm,结果如图5所示。将溶液等分为100
ꢀµ
l样品,每份样品含有30
ꢀµ
g mrna疫苗,4℃冰箱保存,或者液氮急冻保存。
[0141]
实施例18 制备包含mrna疫苗的双亲性聚氨基酸胶束按照实施例17的描述,制备包含mrna疫苗的双亲性聚氨基酸胶束,不同在于向该聚氨基酸溶液中迅速加入200微升包含2 mg实施例16制备的冠状病毒sars-cov-2的mrna疫苗水溶液,该mrna疫苗包含的目标蛋白序列为表面刺突蛋白受体结合区域。
[0142]
实施例19 制备包含mrna疫苗的生物功能化双亲性聚氨基酸纳米材料按照实施例17的方法制备2毫升包含mrna疫苗的双亲性聚氨基酸胶束,向该样品溶液中加入100微摩尔(
µ
m)的链霉素磷酸盐缓冲液,直至链霉素的最终浓度为100 纳摩尔(nm)。将得到的样品溶液转移至截止分子量为1百万道尔顿的半透膜中,在1升ph值6的磷酸盐缓冲液中(高压釜灭菌处理)进行透析24小时。透析后的溶液中再加入10 mg重组人血清白蛋白(hsa),所得混合溶液冷冻处理后置于冻干机中制得冻干粉。-20 ℃下密封存放。该冻干粉样品为链霉素功能化的含mrna疫苗的双亲性聚氨基酸纳米材料。该纳米材料冻干粉可以复溶于纯水中,用于与生物素修饰的小分子配体和抗体蛋白结合(如pd-l1抗体、t细胞受体抗体、白介素6受体抗体凯夫萨拉(sarilumab)等),提高对于目标细胞和组织的靶向递送。
白介素6受体抗体凯夫萨拉功能化的mrna疫苗可以用于白介素6水平增高的冠状病毒症covid-19病人。
[0143]
实施例20 制备包含mrna疫苗的双亲性聚氨基酸-佐剂混合物在10毫升圆底烧瓶中,将10 mg实施例3制备的pll-no25-peg3500-biotin20和作为佐剂的0.5 mg胆固醇、3 mg卵磷脂共同溶于300
ꢀµ
l乙醇中,向该聚氨基酸溶液中迅速加入200
ꢀµ
l包含3 mg实施例14制备的mrna水溶液(水经高压釜处理,确保无活性核酸水解酶,ph值用盐酸调节为4)。其后用针管通氮气吹除溶剂至形成透明薄膜。加入2 ml纯水,在10℃冷室中涡旋振荡15分钟。该体积下pll-no25-peg3500-biotin20的浓度大于临界胶体浓度(见实施例12测得cmc),聚氨基酸和mrna形成胶束溶液。取200
ꢀµ
l样品在纯水中稀释5倍,溶液进行动态激光散射实验,测得胶束的水合直径为176
ꢀ±ꢀ
42 nm,结果如图6所示。将溶液等分为100
ꢀµ
l样品,每份样品含有60
ꢀµ
g mrna,存储于4℃冰箱保存或液氮急冻保存。
[0144]
实施例21 制备含mrna疫苗的双亲性聚氨基酸-佐剂混合物纳米材料按照实施例20的方法制备2 ml包含mrna疫苗的的双亲性聚氨基酸-佐剂混合物,向该样品溶液中加入100
ꢀµ
m(微摩尔)的链霉素磷酸盐缓冲液,直至链霉素的最终浓度为100 nm(纳摩尔)。按照实施例19的方法透析和冻干,制得冻干粉,在-20 ℃下密封存放。该冻干粉样品为链霉素功能化的含mrna疫苗的双亲性聚氨基酸-佐剂混合物纳米材料。使用时将纳米材料复溶于纯水中,与生物素修饰的小分子配体和抗体蛋白结合(如pd-l1抗体、t细胞受体抗体等),提高对于目标细胞和组织的靶向递送。
[0145]
以上,对本发明的实施方式进行了说明。但是,本发明不限定于上述实施方式。凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



