一种多肽固液组合合成丙氨瑞林的方法与流程
 2021-02-02 02:02:58|
2021-02-02 02:02:58| 345|
345| 起点商标网
起点商标网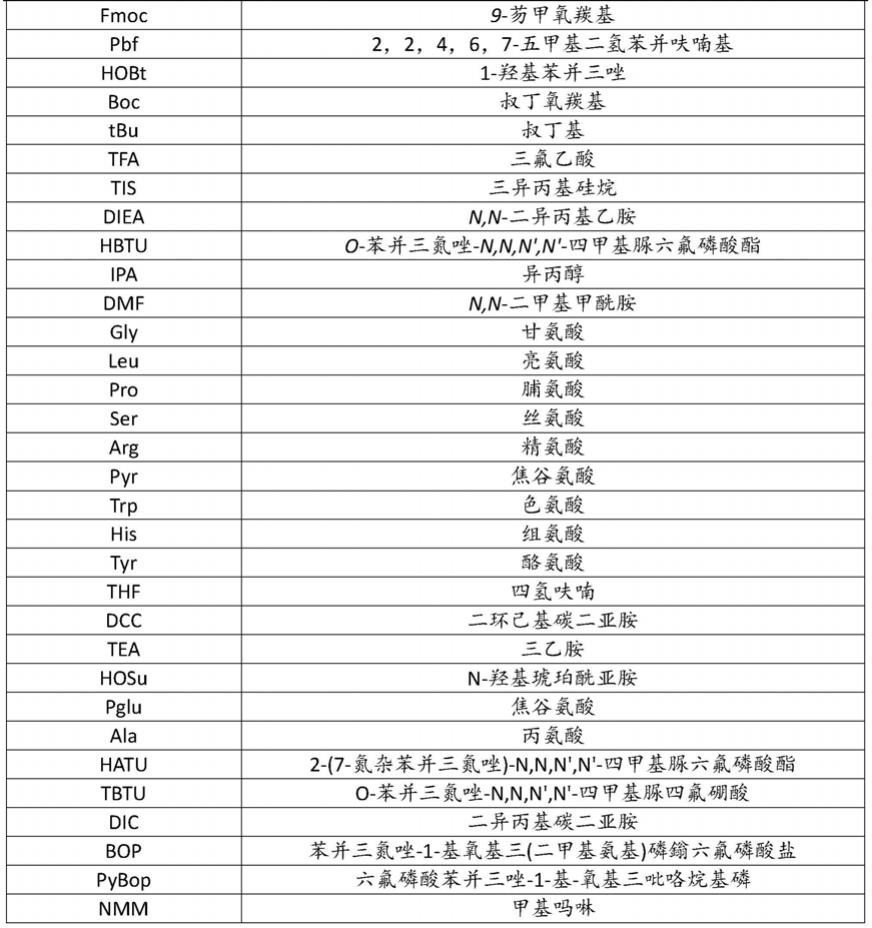
[0001]
本发明涉及医药技术领域,特别是涉及一种多肽固液组合合成丙氨瑞林的方法。
背景技术:
[0002]
丙氨瑞林为人工合成的促性腺激素释放激素(gnrh)的九肽类似物,用药初期可刺激垂体释放促黄体生成素(lh)和促卵泡素(fsh),引起卵巢源性甾体激素短暂升高;重复用药可抑制垂体释放lh和fsh,使血中的雌二醇水平下降,达到药物去卵巢的作用,这种抑制作用可用于治疗子宫内膜异位症等激素依赖性疾病。
[0003]
在现有技术中,申请号为cn201710851059.5提供一种丙氨瑞林的固相制备方法,该方法包括以下步骤:
[0004]
(1)、活化boc-pro:将boc-pro和cs2co3分别溶解,然后混合,制备得活化的boc-pro产物boc-pro-cs;
[0005]
(2)、boc-pro固化:将boc-pro-cs与氯甲基树脂溶解,将boc-pro固化,制备得boc-pro树脂;
[0006]
(3)、接肽:将boc-pro树脂采用逐一偶联的方式依次连接boc-arg、boc-leu、boc-d-ala、boc-tyr、boc-ser-(but)、boc-trp、boc-his-(tos)、pglu,合成得到丙氨瑞林-树脂;
[0007]
(4)、对丙氨瑞林-树脂进行胺解脱树脂,转醋酸盐,得到丙氨瑞林粗品;
[0008]
(5)、丙氨瑞林粗品经hplc纯化、冻干得到丙氨瑞林成品。
[0009]
由该现有技术公开的制备方法能获得收率和纯度高的丙氨瑞林,采用boc策略,脱保护成本更高,需要氨解,反应条件难以控制,副反应较多,需要更低成本和更方便产业化的生产工艺。
技术实现要素:
[0010]
基于此,有必要针对背景技术中存在的问题,提供一种多肽固液组合合成丙氨瑞林的方法。
[0011]
本发明的技术方案是构造一种多肽固液组合合成丙氨瑞林的方法,包括以下步骤:
[0012]
1)、用多肽固相合成法合成化合物1:
[0013]
boc-pglu-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-ala-leu-oh;
[0014]
2)、用多肽液相合成法合成化合物2:h-arg(pbf)-pro-nhet;
[0015]
3)、在液相中合成化合物3:
[0016]
boc-pglu-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-ala-leu-arg(pbf)-pro-nhet;
[0017]
4)、合成丙氨瑞林粗品:pglu-his-trp-ser-tyr-d-ala-leu-arg-pro-nhet。
[0018]
进一步地:步骤1)中,化合物1可以通过固相法从c到n末端的顺序合成;
[0019]
其步骤包括:
[0020]
1):以ctc树脂为固相载体;
[0021]
boc-pglu-oh,fmoc-his(boc)-oh,fmoc-trp(boc)-oh,fmoc-ser(tbu)-oh,fmoc-tyr(tbu)-oh,fmoc-d-ala-oh,fmoc-leu-oh为氨基酸单体;
[0022]
缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic、dcc其中的一种;
[0023]
脱帽试剂为哌嗪溶液,溶剂为偶极非质子溶剂,哌嗪溶液的质量浓度为2-5%;
[0024]
有机碱为diea或nmm;
[0025]
从c到n末端依次合成:
[0026]
boc-pglu-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-ala-leu-ctc树脂;
[0027]
2):用三氟乙酸/二氯甲烷溶液切割,浓缩后用水析出,得到化合物1:
[0028]
boc-pglu-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-ala-leu-oh。
[0029]
进一步地:步骤2)中,化合物2可以通过液相法合成:
[0030]
以fmoc-arg(pbf)-oh,h-pro-nhet
·
hcl为氨基酸单体、缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic、dcc其中的一种、活化剂为hosu或hobt,有机碱主要为diea或tea或nmm,依次合成:
[0031]
1)、fmoc-arg(pbf)-pro-nhet;
[0032]
2)、h-arg(pbf)-pro-nhet。
[0033]
进一步地:步骤3)中,化合物3可以通过液相法合成:以化合物1和化合物2为合成片段、缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic、dcc其中的一种、活化剂为hosu或hobt,有机碱主要为diea或tea或nmm,合成化合物3:
[0034]
boc-pglu-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-ala-leu-arg(pbf)-pro-nhet;
[0035]
化合物1和化合物2的摩尔比为1:1.01~1:1.5,化合物2和缩合剂、活化剂及有机碱的摩尔比=1:1:1:1;
[0036]
进一步地,该丙氨瑞林粗品纯度可以达到90%以上,可以由化合物3溶于tfa溶液中进行反应得到,反应完成后浓缩,加入醚类试剂析出,过滤即得到丙氨瑞林粗品。
[0037]
在其中一个实施例中,使用后的树脂回收步骤如下:
[0038]
1)将树脂用dmf洗涤;
[0039]
2)甲醇洗涤,抽去滤液,真空干燥;
[0040]
3)另配置二氯亚砜的dcm溶液,加入装有树脂的固相合成反应器中,反应2h后,抽去反应液,dcm洗涤。
[0041]
在其中一个实施例中,由化合物3获得粗品的步骤如下:
[0042]
1)取烧瓶,称化合物3投入该烧瓶,加入切肽试剂(tfa:tis:h2o=95:2.5:2.5)切割,得到含有丙氨瑞林粗品的tfa溶液;
[0043]
2)浓缩tfa溶液至少量,加入乙醚;
[0044]
3)离心,真空干燥得丙氨瑞林三氟乙酸盐粗品。
[0045]
在其中一个实施例中,化合物3合成步骤如下:
[0046]
1)取化合物1和缩合剂溶于dmf,加入活化剂和有机碱溶解,-10~5℃冷浴5~15min;
[0047]
2)另取化合物2溶于thf中,反应1.5~2.5h,hplc检测反应完全。浓缩,加入盐酸溶
液,析出类白色固体,过滤,水洗至中性;
[0048]
3)真空干燥,得到化合物3。
[0049]
本发明的优点和有益效果如下:
[0050]
1)以哌嗪作为脱帽试剂用ctc树脂合成片段,结合液相法合成丙氨瑞林,哌嗪不是易制毒试剂,成本比经典合成法用的易制毒试剂哌啶要低,并且更方便运输和储存;
[0051]
2)ctc树脂合成片段可以方便自动化生产;
[0052]
3)ctc树脂可以回收重复利用;
[0053]
4)适合大规模工业化生产,没有剧烈的化学反应;
[0054]
5)降低了生产成本。
附图说明
[0055]
图1为本发明的化合物1的hplc图。
[0056]
图2为本发明的化合物1裂解的无保护样品的ms图。
[0057]
图3为本发明的fmoc-arg(pbf)-pro-nhet.hcl的rp-hplc图。
[0058]
图4为本发明的h-arg(pbf)-pro-nhet的rp-hplc图。
[0059]
图5为本发明的h-arg(pbf)-pro-nhet的ms图。
[0060]
图6为本发明的化合物3(丙氨瑞林前体)的hplc图。
[0061]
图7为本发明的丙氨瑞林粗品的hplc图。
[0062]
图8为本发明的丙氨瑞林的ms图。
[0063]
图9为本发明的另一实施例的化合物1的hplc图。
具体实施方式
[0064]
为了便于理解本发明,下面将参照相关附图对本发明进行更全面的描述。附图中给出了本发明的首选实施例。但是,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施例。相反地,提供这些实施例的目的是使对本发明的公开内容更加透彻全面。
[0065]
除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体实施例的目的,不是旨在于限制本发明。
[0066]
实施例1
[0067]
本发明权利要求书和说明书中出现物质的英文缩写对应的中文名称见表1。
[0068]
表1本发明中出现物质的英文缩写对应的中文名称
[0069]
[0070][0071]
一种多肽固液组合合成丙氨瑞林的方法,包括以下步骤:
[0072]
1)、用多肽固相合成法合成化合物1:
[0073]
boc-pglu-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-ala-leu-oh;
[0074]
2)、用多肽液相合成法合成化合物2:h-arg(pbf)-pro-nhet;
[0075]
3)、在液相中合成化合物3:
[0076]
boc-pglu-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-ala-leu-arg(pbf)-pro-nhet;
[0077]
4)、合成丙氨瑞林粗品:pglu-his-trp-ser-tyr-d-ala-leu-arg-pro-nhet。
[0078]
进一步地:步骤1)中,化合物1可以通过固相法从c到n末端的顺序合成;
[0079]
其步骤包括:
[0080]
1):以ctc树脂为固相载体;
[0081]
boc-pglu-oh,fmoc-his(boc)-oh,fmoc-trp(boc)-oh,fmoc-ser(tbu)-oh,fmoc-tyr(tbu)-oh,fmoc-d-ala-oh,fmoc-leu-oh为氨基酸单体;
[0082]
缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic、dcc其中的一种;
[0083]
脱帽试剂为质量浓度为2%~5%的哌嗪溶液,溶剂为偶极非质子溶剂;
[0084]
更进一步优选地,脱帽试剂的溶剂为dmf,哌嗪的质量浓度为3%;
[0085]
有机碱为diea或nmm;
[0086]
从c到n末端依次合成:
[0087]
boc-pglu-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-ala-leu-ctc树脂;
[0088]
2):用三氟乙酸/二氯甲烷溶液切割,浓缩后用水析出,得到化合物1:
[0089]
boc-pglu-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-ala-leu-oh。
[0090]
具体地,化合物1合成过程如下:
[0091]
投料表如下:
[0092]
名称分子量密度体积μl质量mgctcresin(25g)(取代度1.0mmol/g)
ꢀꢀ
\fmoc-leu-oh353.4\\8835diea129.240.7824120032310fmoc-d-ala-oh311.34\\15567hbtu379.24\\18962diea129.240.7829916.117754.4fmoc-tyr(tbu)-oh459.5\\22975hbtu379.24\\18962diea129.240.7829916.117754.4fmoc-ser(tbu)-oh383.4\\19170hbtu379.24\\18962diea129.240.7829916.117754.4fmoc-trp(boc)-oh526.6\\26330hbtu379.24\\18962diea129.240.7829916.117754.4fmoc-his(boc)-oh477.51\\23875.5hbtu379.24\\18962diea129.240.7829916.117754.4boc-pglu-oh229.2\\11460hbtu379.24\\18962diea129.240.7829916.117754.4
[0093]
一、leu-树脂的合成;
[0094]
1).称25gctc树脂于250ml固相合成反应器中,取fmoc-leu-oh于250ml三角瓶中,100ml量筒量取dcm120ml,摇匀,加diea41ml,摇匀溶解,倒入反应器开始反应。
[0095]
2).反应1h时,用抽滤装置抽去反应液,用dmf洗4次;
[0096]
3).量取200ml质量浓度为3%哌嗪/dmf溶液为脱帽试剂,倒入反应器中,反应20min,然后抽去反应液,dmf洗涤4次。
[0097]
4).茚三酮检测:取树脂于玻璃管中,加入异丙醇,vortex5秒钟,待树脂沉在玻璃管底后,倒去异丙醇,重复洗涤三次,茚三酮检验,在小试管中滴茚三酮溶液,在110℃干式
加热器中加热3min,阳性。
[0098]
二、d-ala-leu-树脂的合成;
[0099]
1).得到leu-树脂后,向反应体系中添加第二氨基酸保护单体fmoc-d-ala-oh、缩合剂hbtu和碱diea,溶剂为dmf,反应时间为2小时,反应完成后,用dmf洗涤4遍;
[0100]
2).反应完全的检测:取树脂于玻璃管中,加入异丙醇,vortex5秒钟,待树脂沉在玻璃管底后,倒去异丙醇,重复洗涤三次,茚三酮检验,在小试管中滴茚三酮溶液,在110℃干式加热器中加热3min,阴性。
[0101]
3).得到fmoc-d-ala-leu-树脂后,量取200ml脱帽试剂哌嗪溶液,倒入反应器中,反应20min,抽去反应液,dmf洗涤4次。
[0102]
4).茚三酮检测:取树脂于玻璃管中,加入异丙醇,vortex5秒钟,待树脂沉在玻璃管底后,倒去异丙醇,重复洗涤三次,茚三酮检验,在小试管中滴茚三酮溶液,在110℃干式加热器中加热3min,阳性。
[0103]
三、获得d-ala-leu-树脂后,按照上述缩合反应方法,依次在d-ala-leu-树脂上连接氨基酸保护单体:
[0104]
fmoc-tyr(tbu)-oh,fmoc-ser(tbu)-oh,fmoc-trp(boc)-oh,fmoc-his(boc)-oh和boc-pglu-oh后得到:
[0105]
boc-pglu-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-ala-leu-树脂。
[0106]
四、将保护多肽从树脂上切割下来,方法如下:
[0107]
加1%tfa/dcm溶液150ml,摇摆反应10min,收集反应液,重复6次,浓缩反应液,加质量浓度为10%柠檬酸溶液,析出白色固体,过滤,水洗至中性,真空干燥。得到化合物1:
[0108]
boc-pglu-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-ala-leu-oh,29.8g,其纯度为91.9%,收率为91%。(rp-hplc图见图1;其裂解的无保护样品ms图见图2)
[0109]
参照图1,化合物1分析方法如下:
[0110]
安捷伦1260型hplc,krosmail100-5c18column4.6*250mm;
[0111]
a:5%乙腈/h2o溶液,0.1%tfa;b:乙腈,0.1%tfa(hplc);
[0112]
梯度洗脱:0~30min;70%b~75%b;
[0113]
λ=210nm;流速=1.0ml/min。
[0114]
进一步地:步骤2)中,化合物2可以通过液相法合成:
[0115]
以fmoc-arg(pbf)-oh,h-pro-nhet
·
hcl为氨基酸单体、缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic、dcc等其中的一种、活化剂为hosu或hobt,有机碱主要为diea或tea或nmm,依次合成:
[0116]
1)、fmoc-arg(pbf)-pro-nhet;
[0117]
2)、h-arg(pbf)-pro-nhet。
[0118]
具体地,化合物2合成过程如下:
[0119]
一、合成h-arg(pbf)-pro-nhet
[0120]
1).合成fmoc-arg(pbf)-pro-nhet.hcl:称fmoc-arg(pbf)-oh,100mmol,65g,bop110mmol,49g溶于500mldmf中,冷浴10min,加入tea110 mmol,12g。
[0121]
2).然后称取h-pro-nhet.hcl,110mmol,20g,用100ml dmf+12gtea溶解,倒入上述反应液,反应2h,hplc显示反应完全,加入0.5m盐酸析出,过滤,得白色固体产物,真空干燥,
得产物87.4g,其收率为108%,纯度为96.8%。(rp-hplc图见图3)。
[0122]
参照图3,分析方法如下:
[0123]
安捷伦1260型hplc,krosmail100-5c18column4.6*250mm;
[0124]
a:5%乙腈/h2o溶液,0.1%tfa;b:乙腈/h2o,0.1%tfa(hplc);
[0125]
梯度洗脱:0~30min;55%b~65%b;
[0126]
λ=210nm;
[0127]
流速=1.0ml/min。
[0128]
三、合成h-arg(pbf)-pro-nhet
[0129]
1).将产物用二乙胺500ml溶解,搅拌30min,hplc显示反应完全。2).浓缩除去二乙胺,加石油醚析出,得到白色固体h-arg(pbf)-pro-nhet,真空干燥,得产物51g,其收率为92.6%,纯度为97.5%。(rp-hplc图见图4,ms图见图5)。
[0130]
参照图4,分析方法如下:
[0131]
安捷伦1260型hplc,krosmail100-5c18column4.6*250mm
[0132]
a:5%乙腈/h2o溶液,0.1%tfa;b:乙腈/h2o,0.1%tfa(hplc)
[0133]
梯度洗脱:0~30min;0%b~10%b
[0134]
λ=210nm;
[0135]
流速=1.0ml/min。
[0136]
进一步地:步骤3)中,化合物3可以通过液相法合成:以化合物1和化合物2为合成片段、缩合剂为hbtu、hatu、tatu、tbtu、pybop、bop、dic、dcc其中的一种、活化剂为hosu或hobt,有机碱主要为diea或tea或nmm,合成化合物3:
[0137]
boc-pglu-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-ala-leu-arg(pbf)-pro-nhet;
[0138]
化合物1和化合物2的摩尔比为1:1.01~1:1.5,化合物2和缩合剂、活化剂及有机碱的摩尔比=1:1:1:1。
[0139]
具体地,化合物3合成过程如下:
[0140]
1).丙氨瑞林前体(化合物3)合成:
[0141]
取化合物1:10mmol,13g和bop11mmol,4.9g溶于20mldmf,加入活化剂hobt和有机碱diea溶解,-5℃冷浴10min,另取化合物2:12mmol,6.6g,溶于20mlthf中,反应2h,hplc检测反应完全。
[0142]
过滤除去白色固体,浓缩,加入0.5m盐酸溶液,析出类白色固体,过滤,水洗至中性。真空干燥,得产物丙氨瑞林前体(化合物3)15.8g,其产率为86.3%,纯度为91%。(rp-hplc图见图6)。
[0143]
参照图6,分析方法如下:
[0144]
安捷伦1260型hplc,krosmail100-5c18column4.6*250mm;
[0145]
a:5%乙腈/h2o溶液,0.1%tfa;b:乙腈/h2o,0.1%tfa(hplc);
[0146]
梯度洗脱:0~30min;70%b~75%b;
[0147]
λ=210nm;流速=1.0ml/min。
[0148]
2).丙氨瑞林粗品合成
[0149]
取100ml圆底烧瓶,称丙氨瑞林前体(化合物3)5mmol(9.2g)投入,加入切肽试剂
(tfa:tis:h2o=95:2.5:2.5)切割,得到含有丙氨瑞林粗品的tfa溶液。
[0150]
浓缩tfa溶液至少量,加入乙醚。离心,真空干燥得丙氨瑞林粗品5.3g,其纯度为91%,收率为83%。(rp-hplc图见图7,ms图见附图8)
[0151]
参照图7,分析方法如下:
[0152]
安捷伦1260型hplc,krosmail100-5c18column4.6*250mm;
[0153]
a:0.1%tfa/h2o溶液b:h2o,0.1%tfa/乙腈(hplc);
[0154]
梯度洗脱:0~30min;20%b~30%b;
[0155]
λ=210nm;流速=1.0ml/min。
[0156]
由以上实施例可知,本发明提供的丙氨瑞林的制备方法,采用固相合成法合成化合物1,液相合成法合成化合物2,然后再将两个中间体缩合得到化合物3,脱保护后得到丙氨瑞林,简化了丙氨瑞林的制备步骤,降低了丙氨瑞林制备成本;采用本发明所述的方法制备得到的丙氨瑞林纯度高达90%以上。
[0157]
实施例2
[0158]
与上述实施例的不同之处在于,通过回收树脂合成化合物1:
[0159]
一、树脂回收;
[0160]
1).将实施例1的树脂用dmf洗涤,甲醇洗涤,抽去滤液,真空干燥。
[0161]
2).另配置二氯亚砜的dcm溶液(二氯亚砜10ml,dcm=200ml),加入装有树脂的250ml固相合成反应器中,反应2h后,抽去反应液,dcm洗涤。
[0162]
投料表如下:
[0163][0164][0165]
二、leu-树脂的合成;
[0166]
1).称25g ctc树脂于250ml固相合成反应器中,取fmoc-leu-oh于250ml三角瓶中,100ml量筒量取dcm120ml,摇匀,加diea 41ml,摇匀溶解,倒入反应器开始反应。
[0167]
2).反应1h时,用抽滤装置抽去反应液,用dmf洗4次;
[0168]
3).量取200ml脱帽试剂哌嗪溶液,倒入反应器中,反应20min,随后,抽去反应液,dmf洗涤4次。
[0169]
4).茚三酮检测:取树脂于玻璃管中,加入异丙醇,vortex5秒钟,待树脂沉在玻璃管底后,倒去异丙醇,重复洗涤三次,茚三酮检验,在小试管中滴茚三酮溶液,在110℃干式加热器中加热3min,阳性。
[0170]
三、d-ala-leu-树脂的合成;
[0171]
1).得到leu-树脂后,向反应体系中添加第二氨基酸保护单体fmoc-d-ala-oh、缩合剂hbtu和碱diea,溶剂为dmf,反应时间为2小时,反应完成后,用dmf洗涤4遍;
[0172]
2).反应完全的检测:取树脂于玻璃管中,加入异丙醇,vortex5秒钟,待树脂沉在玻璃管底后,倒去异丙醇,重复洗涤三次,茚三酮检验,在小试管中滴茚三酮溶液,在110℃干式加热器中加热3min,阴性。
[0173]
3).得到fmoc-d-ala-leu-树脂后,量取200ml脱帽试剂哌嗪溶液,倒入反应器中,反应20min,随后,抽去反应液,dmf洗涤4次。
[0174]
4).茚三酮检测:取树脂于玻璃管中,加入异丙醇,vortex5秒钟,待树脂沉在玻璃管底后,倒去异丙醇,重复洗涤三次,茚三酮检验,在小试管中滴茚三酮溶液,在110℃干式加热器中加热3min,阳性。
[0175]
获得d-ala-leu-树脂后,按照上述缩合反应方法,依次在d-ala-leu-树脂上连接氨基酸保护单体:
[0176]
fmoc-tyr(tbu)-oh,fmoc-ser(tbu)-oh,fmoc-trp(boc)-oh,fmoc-his(boc)-oh和boc-pglu-oh后;
[0177]
获得boc-pglu-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-ala-leu-树脂。然后将保护多肽从树脂上切割下来,方法如下:
[0178]
加1%tfa/dcm溶液150ml,摇摆反应10min,收集反应液,重复6次,浓缩反应液,加10%柠檬酸溶液,析出白色固体,过滤,水洗至中性,真空干燥。得到化合物1:boc-pglu-his(boc)-trp(boc)-ser(tbu)-tyr(tbu)-d-ala-leu-oh,27.3g,纯度为88.5%,收率为84%。(rp-hplc图见图9)
[0179]
参照图9,分析方法如下:
[0180]
安捷伦1260型hplc,krosmail100-5c18column4.6*250mm;
[0181]
a:5%乙腈/h2o溶液,0.1%tfa;b:乙腈,0.1%tfa(hplc);
[0182]
梯度洗脱:0~30min;70%b~90%b;
[0183]
λ=210nm;流速=1.0ml/min。
[0184]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



