芳基或杂芳基取代的噻二唑类化合物及其抗菌用途的制作方法
 2021-02-01 22:02:45|
2021-02-01 22:02:45| 384|
384| 起点商标网
起点商标网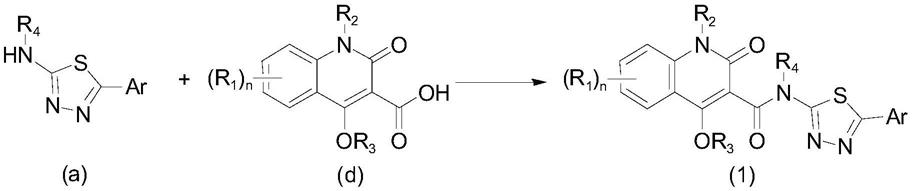
[0001]
本发明属于抗菌药物技术领域,具体涉及芳基或杂芳基取代的噻二唑类化合物、制备方法及其作为抗菌药物的用途。
背景技术:
[0002]
抗生素滥用或者不合理使用促进了耐药性细菌或支原体等病原微生物的不断出现,导致了当前可用的抗菌药物失去疗效。世界卫生组织于2001年将抗生素耐药确定为全球健康的威胁之一。近年来,抗菌药物研发放缓,极少有抗菌药物上市,使得抗生素耐药问题愈发严重。因此,研发新结构类型或新作用机制的抗菌药物对于解决抗生素耐药问题具有重要的临床意义和应用价值。
[0003]
在耐药性革兰氏阳性细菌中,耐甲氧西林金黄色葡萄球菌(mrsa)、耐甲氧西林表面葡萄球菌(mrse)和抗万古霉素肠道球菌(vre)最为常见。对于肺炎支原体而言,关注最多的是对大环内酯类抗生素的耐药株。针对以上耐药性病原微生物研发新型抗生素是当前热点。
[0004]
本专利涉及的化合物属于芳基或杂芳基取代的噻二唑类化合物,因1,3,4-噻二唑的5位为芳基或杂芳基取代,为新结构化合物。本专利涉及的化合物具有很强的抗革兰氏阳性菌耐药菌活性,且抗菌谱广。代表性化合物对标准及临床分离耐药金黄色葡萄球菌、表皮葡萄球菌、粪肠球菌、屎肠球菌菌株的最低抑菌浓度(minimum inhibitory concentration,mic)在0.03-32μg/ml水平,对大环内酯耐药的肺炎支原体也具有一定的抑制活性,灌胃给药对mrsa腹腔注射所致的系统感染小鼠具有较好的保护作用,半数有效量(ed
50
)值达到了1.70mg/kg。因此,该专利所涉及的化合物有进一步开发成为临床用抗菌药物的价值。
技术实现要素:
[0005]
本发明解决的技术问题是克服现有技术中抗耐药菌药物不足的缺陷,提供芳基或杂芳基取代的噻二唑类化合物、制备方法及其作为抗菌药物的用途。
[0006]
为解决本发明的技术问题,本发明提供如下技术方案:
[0007]
第一方面,提供了一种芳基或杂芳基取代的噻二唑类化合物,它是如式(1)所示的化合物:
[0008][0009]
其中:
[0010]
ar代表取代或非取代的芳基或杂芳基,所述取代基选自卤素、c
1-8
烷基、c
2-8
烯基、c
2-8
炔基、卤代c
1-8
烷基、卤代c
2-8
烯基、卤代c
2-8
炔基、c
3-8
环烷基、杂环基、芳基、杂芳基、(ch2)
m
or5、(ch2)
m
sr5、(ch2)
m
nr5r6、(ch2)
m
c(o)r5、(ch2)
m
c(o)or5、(ch2)
m
oc(o)r5、(ch2)
m
c(o)nr5r6、(ch2)
m
nr6c(o)r5、(ch2)
m
s(o)2r5、(ch2)
m
s(o)2nr5r6、(ch2)
m
nr6s(o)2r5的一种或多种;
[0011]
r1各自独立地选自氢、卤素、c
1-8
烷基、c
2-8
烯基、c
2-8
炔基、卤代c
1-8
烷基、卤代c
2-8
烯基、卤代c
2-8
炔基、c
3-8
环烷基、杂环基、芳基、杂芳基、(ch2)
m
or5、(ch2)
m
sr5、(ch2)
m
nr5r6、(ch2)
m
c(o)r5、(ch2)
m
c(o)or5、(ch2)
m
oc(o)r5、(ch2)
m
c(o)nr5r6、(ch2)
m
nr6c(o)r5、(ch2)
m
s(o)2r5、(ch2)
m
s(o)2nr5r6、(ch2)
m
nr6s(o)2r5等;
[0012]
r2、r3、r4各自独立地选自氢、c
1-8
烷基、c
2-8
烯基、c
2-8
炔基、卤代c
1-8
烷基、卤代c
2-8
烯基、卤代c
2-8
炔基、c
3-8
环烷基、杂环基、芳基、杂芳基、(ch2)
m
or5、(ch2)
m
sr5、(ch2)
m
nr5r6、(ch2)
m
c(o)r5、(ch2)
m
c(o)or5、(ch2)
m
oc(o)r5、(ch2)
m
c(o)nr5r6、(ch2)
m
nr6c(o)r5、(ch2)
m
s(o)2r5、(ch2)
m
s(o)2nr5r6、(ch2)
m
nr6s(o)2r5等;各个r5和r6各自独立地为氢、c
1-8
烷基、c
2-8
烯基、c
2-8
炔基、卤代c
1-8
烷基、卤代c
2-8
烯基、卤代c
2-8
炔基、c
3-8
环烷基、杂环基、芳基,或杂芳基等;
[0013]
或r5和r6与其相连的氮原子共同构成任选地具有0-3个额外的各自独立地选自n、o或s的杂原子的3-至9-元环;
[0014]
n为0、1、2、3或4;
[0015]
m各自独立地为0、1、2、3、4、5、6、7、8、9、10;
[0016]
除非另有说明,否则上面所述的芳基包含6-16个碳原子;杂芳基是5-至15-元杂芳基;且杂环基是3-至12-元杂环基;杂芳基或杂环基含有选自n、o或s中的一个或多个杂原子。
[0017]
优选地,所述卤素选自氟、氯、溴、碘;所述卤代代表任意取代位置的单卤代、相同或不同卤素原子的多卤代;所述c
1-8
烷基选自甲基、乙基、丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、直链或含支链的戊基、直链或含支链的己基、直链或含支链的庚基、直链或含支链的辛基;芳基选自苯基、萘基、蒽基、菲基或芘基;杂芳基选自呋喃、噻吩、噁唑、噻唑、异噁唑、噁二唑、噻二唑、吡咯、吡唑、咪唑、吡啶、嘧啶、吡嗪、哒嗪、酞嗪、喹啉、异喹啉、喋啶、嘌呤、吲哚、异吲哚、苯并呋喃基、苯并噻吩基、苯并吡啶基、苯并嘧啶基、苯并吡嗪基、苯并咪唑基或苯并酞嗪基。
[0018]
优选地,所述r2、r3、r4各自独立地选自氢或c
1-8
烷基。
[0019]
进一步地,所述芳基优选苯基或萘基,更优选苯基;杂芳基优选吡啶、噻吩、呋喃、噻唑、喹啉、吲哚。
[0020]
作为优选,本发明提供的芳基或杂芳基取代的噻二唑类化合物为:
[0021]
n-(5-苯基-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j1)
[0022]
n-(5-(4-氯苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j2)
[0023]
n-(5-(4-溴苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j3)
[0024]
n-(5-(3-氟苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j4)
[0025]
n-(5-(2-氟苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j5)
[0026]
n-(5-(4-甲基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j6)
[0027]
n-(5-(3-甲基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j7)
[0028]
n-(5-(4-甲氧基苯基-)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j8)
[0029]
n-(5-(3-甲氧基苯基-)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j9)
[0030]
n-(5-(2-甲氧基苯基-)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j10)
[0031]
n-(5-(3-乙氧基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j11)
[0032]
n-(5-(2-乙氧基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j12)
[0033]
n-(5-(4-二氟甲氧基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j13)
[0034]
n-(5-(4-二甲氨基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j14)
[0035]
n-(5-(4-甲磺酰基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j15)
[0036]
n-(5-(2,4-二氟苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j16)
[0037]
n-(5-(2-氯-4-硝基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j17)
[0038]
n-(5-(吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j18)
[0039]
n-(5-(吡啶-3-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j19)
[0040]
n-(5-(吡啶-4-基)-1,3,4-噻二唑-3-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺
(j20)
[0041]
n-(5-(噻吩-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j21)
[0042]
n-(5-(呋喃-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j22)
[0043]
n-(5-(噻唑-4-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j23)
[0044]
n-(5-(噻唑-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j24)
[0045]
n-(5-(1-甲基-1h-吡唑-3-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j25)
[0046]
n-(5-(喹啉-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j26)
[0047]
n-(5-(1-甲基-1h-吲哚-6-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j27)
[0048]
n-(5-(6-甲基吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j28)
[0049]
n-(5-(5-甲基吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j29)
[0050]
n-(5-(4-甲基吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j30)
[0051]
n-(5-(3-甲基吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j31)
[0052]
n-(5-(4-甲氧基吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j32)
[0053]
n-(5-(6-氟吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j33)
[0054]
n-(5-(5-氟吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j34)
[0055]
n-(5-(3-氟吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j35)
[0056]
n-(5-(5-溴吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j36)
[0057]
n-(5-(5-三氟甲基吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j37)
[0058]
n-(5-(噻唑-2-基)-1,3,4-噻二唑-2-基)-1-乙基-6-氟-4-羟基-2-喹诺酮-3-甲酰胺(j38)
[0059]
n-(5-(噻唑-2-基)-1,3,4-噻二唑-2-基)-1-乙基-7-氯-4-羟基-2-喹诺酮-3-甲酰胺(j39)
[0060]
n-(5-(噻唑-2-基)-1,3,4-噻二唑-2-基)-1-乙基-8-氯-4-羟基-2-喹诺酮-3-甲酰胺(j40)
[0061]
n-(5-(噻唑-2-基)-1,3,4-噻二唑-2-基)-1-乙基-6-甲基-4-羟基-2-喹诺酮-3-甲酰胺(j41)
[0062]
n-(5-(噻唑-2-基)-1,3,4-噻二唑-2-基)-1-乙基-6-甲氧基-4-羟基-2-喹诺酮-3-甲酰胺(j42)
[0063]
第二方面,本发明提供了通式化合物(1)的制备方法,它包括如下步骤:
[0064][0065]
即将中间体(a)与中间体(d)反应制备权利要求1所述的化合物(1);
[0066]
其中,ar和r1、r2、r3、r4的定义如前所述。
[0067]
优选地,上述反应在碱性催化剂和缩合剂存在条件下进行。
[0068]
进一步地,碱性催化剂选自无机碱或有机碱;所述无机碱选自碱金属氢氧化物、碱土金属氢氧化物、碱金属碳酸盐中的至少一种;所述有机碱选自分子中含有伯胺基、仲胺基、叔胺基、季铵碱基中的至少一种,优选三乙胺、吡啶、二乙胺、二异丙胺、吡啶、n,n-二异丙基乙胺、n-甲基哌啶和n-甲基吗啉;所述缩合剂选自1,3-二环己基碳二亚胺、n,n
’-
二异丙基碳二亚胺、苯并三氮唑-n,n,n
’
,n
’-
四甲基脲六氟磷酸酯、卡特缩合剂,优选卡特缩合剂。
[0069]
在此基础上,本发明还提供了中间体(a)的制备方法,包括如下步骤:
[0070][0071]
该反应在有机溶剂中进行,所述有机溶剂选自三氟乙酸、浓硫酸、三氟甲磺酸,优选三氟乙酸;其中,ar、r4的定义如前所述。
[0072]
在此基础上,本发明还提供了中间体(d)的制备方法,包括如下步骤:
[0073][0074]
(1)将中间体(b)转化为中间体(c),其中,当r3为h时,将中间体(b)与丙二酸二乙酯反应即得中间体(c),当r3选自如上所定义的除h以外的其他基团时,先将中间体(b)与丙二酸二乙酯反应,然后再与x-r3进行反应即得中间体(c),所述x为i或br;
[0075]
(2)将中间体(c)在碱性条件下转化为中间体(d),所述碱性条件由氢氧化钠、强氧
化钾或氢氧化锂提供,优选氢氧化锂;
[0076]
其中,r1、r2、r3、n的定义如前所述。
[0077]
进一步地,仅仅作为示例性说明,而不从任何方面限制本发明的发明内容和保护范围,给出上述反应条件中的一个更为具体的示例,:
[0078][0079]
(1)1当量的ar-cn溶于三氟乙酸中,再加入0.9-1.5当量的氨基硫脲,40-80℃下搅拌反应,反应完毕后将反应液倒入冰水中,调节ph为11-12,析出固体,即得到中间体(a);
[0080]
(2)1当量的取代靛紅酸酐的n,n-二甲基甲酰胺溶液中加入0.9-1.5当量的n,n-二异丙基乙胺,并滴加0.9-1.5当量的碘代r2(如c
1-8
烷烃),25-60℃下反应过夜,将反应液倒入冰水中,析出固体,即得到中间体(b);
[0081]
(3)将中间体(b)溶于有机溶剂(如n,n-二甲基甲酰胺、乙腈等)中,依次加入0.9-1.5当量的丙二酸二乙酯和氢化钠,50-90℃反应,反应完毕后,冰水淬灭,调ph至4-5,析出固体,即得到中间体(c);
[0082]
(4)将中间体(c)溶于有机溶剂(如乙醇、乙腈、氯仿等)中,滴加2-10倍当量的5%-20%的氢氧化锂水溶液,于25-60℃下加热反应,反应完毕后,调ph至4-5,析出固体,即得到中间体(d);
[0083]
(5)将等倍量的中间体(a)和中间体(d)溶于乙醇、乙腈、氯仿或n,n-二甲基甲酰胺中,依次加入0.9-2.0当量的n,n-二异丙基乙胺和0.9-2.0当量卡特缩合剂,10-50℃下搅拌过夜,将反应液倒入冰水中,析出固体,即得到所述的化合物(1)。
[0084]
第三方面,本发明提供了上述芳基或杂芳基取代的噻二唑类化合物的抗菌用途或用于制备抗菌药物的用途。
[0085]
作为优选,所述的抗菌用途为治疗和预防细菌、支原体、衣原体、立克次体、螺旋体、真菌等病原微生物所引起的人或动物的感染性疾病。
[0086]
进一步优选地,所述的细菌为金黄色葡萄球菌、表皮葡萄球菌、粪肠球菌、屎肠球菌、艰难梭菌、大肠埃希菌、铜绿假单胞菌、肺炎克雷伯菌等,所述的支原体为肺炎支原体、溶脲脲原体、人型支原体、生殖器支原体等,所述的衣原体为肺炎衣原体、鹦鹉热衣原体、沙
眼衣原体和牛衣原体等。
[0087]
进一步优选地,所述的金黄色葡萄球菌包括甲氧西林敏感型金黄色葡萄球菌、甲氧西林耐药金黄色葡萄球菌,所述的表皮葡萄球菌包括甲氧西林敏感型表皮葡萄球菌、甲氧西林表皮葡萄球菌,所述的粪肠球菌和屎肠球菌包括万古霉素敏感型粪肠球菌和屎肠球菌、万古霉素耐药粪肠球菌和屎肠球菌,所述的支原体选自药物敏感型肺炎支原体或耐药肺炎支原体。
[0088]
第四方面,本发明提供了一种抗菌药物组合物,该药物组合物含有上述的芳基或杂芳基取代的噻二唑类化合物或其药学上可接受的盐以及一种或多种药学上可接受的载体。
[0089]
进一步地,所述载体包括药学领域常规的赋形剂、粘合剂、湿润剂、崩解剂、吸收促进剂、表面活性剂、吸附载体、润滑剂等。
[0090]
作为优选,该药物给药剂型为注射剂、片剂、丸剂、胶囊、悬浮剂、乳剂或软膏,给药途径选自静脉或肌肉注射、口服、经皮给药、粘膜给药、直肠给药、阴道给药等。
[0091]
与现有技术相比,本发明具有如下有益效果:
[0092]
本发明的芳基或杂芳基取代的噻二唑类化合物为新结构的抗菌药物,实验已证实该系列化合物对多种耐药菌有效,具有广谱的抗革兰氏阳性菌的活性,尤其对甲氧西林耐药金黄色葡萄球菌(mrsa)、甲氧西林耐药表皮葡萄球菌(mrse)和万古霉素耐药的肠球菌(vre)具有很强的抑制作用,对大环内酯耐药的肺炎支原体具有一定的抑制活性。经体内动物实验验证,该系列化合物对mrsa腹腔注射所致的系统感染小鼠具有很好的保护作用。由于该结构类型不同于临床用抗菌药物,有望解决细菌耐药问题,具有深入研究的价值以及临床应用的潜力。
具体实施方式
[0093]
下面结合具体实施例对本发明作进一步阐述,但实施例仅用于说明本发明,而不是对本发明进行限制。实施例中所用实验方法如无特殊说明,均为常规方法;所使用的材料、试剂等如无特殊说明,为可从商业途径得到的试剂和材料。
[0094]
一、化合物的制备和检测
[0095]
实施例1:化合物j1的制备和检测
[0096][0097]
向100ml茄形瓶中加入苯甲腈(1.03g,10mmol),用10ml三氟乙酸(tfa)溶解后搅拌5分钟,然后分批加入氨基硫脲(1.00g,11mmol),再补加三氟乙酸10ml,混合溶液于70℃条
件下反应8小时。薄层色谱法监测反应,当苯甲腈消耗完后停止加热并自然冷却。然后,将反应液倒入冰水中,并用1当量浓度的氢氧化钠溶液调节ph至11-12,可见大量黄色沉淀析出。抽滤,滤饼经水洗(150ml)和抽滤后得到粗品。用95%乙醇进行重结晶,得到目标物1.21g(产率:67.9%)。
[0098]
10g(61.3mmol)靛紅酸酐的n,n-二甲基甲酰胺(dmf)溶液中加入二异丙基乙胺12.8ml(73.6mmol),并滴加9.6g(73.6mmol)碘乙烷,45℃下反应过夜。薄层色谱法监测反应完毕后,将反应液倒入冰水中,析出固体,水洗,抽滤,干燥得中间体1-乙基-2h-苯并[1,3]噁嗪-2,4-二酮8.1g(产率:67.5%)。
[0099]
将1.96g(10mmol)1-乙基-2h-苯并[1,3]噁嗪-2,4-二酮溶于n,n-二甲基甲酰胺溶液中,依次加入1.2倍当量的丙二酸二乙酯和氢化钠,80℃反应6小时。薄层色谱法监测反应完毕后,冰水淬灭,2mol/l的盐酸溶液调ph至4-5,析出固体,水洗,抽滤,干燥得中间体1-乙基-4-羟基-2-喹诺酮-3-甲酸乙酯0.83g(产率:31.8%)。
[0100]
将0.5g(1.9mmol)1-乙基-4-羟基-2-喹诺酮-3-甲酸乙酯溶于无水乙醇中,滴加5倍当量10%的氢氧化锂水溶液,50℃下加热反应10小时。薄层色谱法监测反应完毕后,加入2mol/l的盐酸溶液调ph至4-5,析出固体,水洗,抽滤,干燥得中间体1-乙基-4-羟基-2-喹诺酮-3-甲酸0.21g(产率:47.4%)。
[0101]
向50ml茄形瓶中依次加入1-乙基-4羟基-2-喹诺酮-3-甲酸(256.3mg,1.1mmol)和超干溶剂n,n-二甲基甲酰胺(10ml),搅拌溶解。然后,分别加入敷酸剂n,n-二异丙基乙胺(dipea,349.3μl,2mmol)以及缩合剂六氟磷酸苯并三唑-1-氧基三(二甲氨基)磷(bop,884.6mg,2mmol),混合液于室温下搅拌20分钟。接着,加入5-苯基-1,3,4-噻二唑-2-胺(177.2mg,1mmol),反应液于室温下过夜反应。薄层色谱法监测反应进程。当5-苯基-1,3,4-噻二唑-2-胺消耗完时,将反应液倒入50ml水中,析出白色沉淀。抽滤,干燥,滤饼用少量无水乙醇搅洗打浆,再次抽滤得到粗品。用硅胶柱层析纯化,得目标产物n-(5-苯基-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j1)82.6mg。
[0102][0103]
灰白色固体,收率24.7%。esi-ms(m/z):393.08[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.24(s,1h),8.02(s,2h),7.91(s,1h),7.78(s,1h),7.59(s,3h),7.47(s,1h),4.42(s,2h),1.31(s,3h).
[0104]
实施例2:化合物j2的制备和检测
[0105]
以4-氯苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(4-氯苯基)-1,3,4-噻二唑-2-胺(产率:77.2%)。
[0106]
以5-(4-氯苯基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(4-氯苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j2)。
[0107][0108]
淡黄色固体,收率31.5%。esi-ms(m/z):428.12[m+h]
+
.1h nmr(500mhz,dmso-d6)δ7.80(d,j=8.2hz,2h),7.55(d,j=8.3hz,3h),7.50(s,3h),4.27(dd,j=19.5,12.3hz,2h),1.22(t,j=7.1hz,3h).
[0109]
实施例3:化合物j3的制备和检测
[0110]
以4-溴苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(4-溴苯基)-1,3,4-噻二唑-2-胺(产率:55.3%)。
[0111]
以5-(4-溴苯基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(4-溴苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j3)。
[0112][0113]
灰白色固体,收率19.2%。esi-ms(m/z):472.31[m+h]
+
.1h nmr(500mhz,dmso-d6)δ7.73(d,j=8.5hz,2h),7.69(d,j=8.4hz,3h),7.51(s,3h),4.30(p,j=6.8hz,2h),1.23(t,j=7.1hz,3h).
[0114]
实施例4:化合物j4的制备和检测
[0115]
以3-氟苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(3-氟苯基)-1,3,4-噻二唑-2-胺(产率:49.2%)。
[0116]
以5-(3-氟苯基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(3-氟苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j4)。
[0117][0118]
灰白色固体,收率30.1%。esi-ms(m/z):411.06[m+h]
+
.1h nmr(500mhz,dmso-d6)δ7.92-7.87(m,1h),7.80-7.73(m,1h),7.62(d,j=8.4hz,2h),7.54(s,2h),7.31(t,j=8.8hz,2h),4.29(q,j=7.0hz,2h),1.23(t,j=7.1hz,3h).。
[0119]
实施例5:化合物j5的制备和检测
[0120]
以2-氟苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(2-氟苯基)-1,3,4-噻二唑-2-胺(产率:49.2%)。
[0121]
以5-(2-氟苯基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(2-氟苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j5)。
[0122][0123]
淡黄色固体,收率41.1%。esi-ms(m/z):411.31[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.28(dd,j=8.4,4.3hz,1h),8.11(t,j=7.7hz,1h),7.92-7.85(m,1h),7.80-7.72(m,1h),7.51(d,j=16.4hz,4h),7.43-7.34(m,3h),4.29(q,j=7.1hz,2h),1.22(t,j=7.1hz,3h).
[0124]
实施例6:化合物j6的制备和检测
[0125]
以4-甲基苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(4-甲基苯基)-1,3,4-噻二唑-2-胺(产率:75.3%)。
[0126]
以5-(4-甲基苯基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(4-甲基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j6)。
[0127][0128]
白色固体,收率27.4%。esi-ms(m/z):407.19[m+h]
+
.1h nmr(500mhz,dmso-d6)δ7.90(t,j=8.8hz,1h),7.81-7.73(m,1h),7.66(d,j=7.9hz,2h),7.37(s,2h),7.30(d,j=7.9hz,2h),4.30(p,j=7.2,6.4hz,2h),2.37(s,3h),1.23(t,j=7.1hz,3h).
[0129]
实施例7:化合物j7的制备和检测
[0130]
以3-甲基苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(3-甲基苯基)-1,3,4-噻二唑-2-胺(产率:49.2%)。
[0131]
以5-(3-甲基苯基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(3-甲基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j7)。
[0132][0133]
棕灰色固体,收率28.4%。esi-ms(m/z):407.09[m+h]
+
.1h nmr(500mhz,dmso-d6)δ7.60(s,1h),7.57(d,j=7.8hz,1h),7.37(t,j=7.7hz,1h),7.27(d,j=7.7hz,1h),4.29(q,j=7.2hz,2h),2.38(s,3h),1.24-1.20(m,3h).
[0134]
实施例8:化合物j8的制备和检测
[0135]
以4-甲氧基苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(4-甲氧基苯基)-1,3,4-噻二唑-2-胺(产率:75.3%)。
[0136]
以5-(4-甲氧基苯基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(4-甲氧基苯基-)-1,
3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j8)。
[0137][0138]
白色固体,收率31.2%。esi-ms(m/z):423.43[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.28(dd,j=8.2,4.1hz,1h),7.94-7.85(m,1h),7.80-7.74(m,1h),7.72(s,2h),7.31(s,2h),7.05(d,j=8.5hz,2h),4.29(q,j=7.1hz,2h),3.84(s,3h),1.27-1.22(m,3h).
[0139]
实施例9:化合物j9的制备和检测
[0140]
以3-甲氧基苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(3-甲氧基苯基)-1,3,4-噻二唑-2-胺(产率:49.2%)。
[0141]
以5-(3-甲氧基苯基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(3-甲氧基苯基-)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j9)。
[0142][0143]
灰白色固体,收率14.4%。esi-ms(m/z):423.21[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.28(dd,j=8.3,3.9hz,1h),7.94-7.86(m,1h),7.81-7.72(m,1h),7.41(t,j=7.9hz,2h),7.35-7.29(m,3h),7.04(dd,j=8.2,2.5hz,2h),4.29(q,j=7.1hz,2h),3.85(s,3h),1.23(t,j=7.1hz,3h).
[0144]
实施例10:化合物j10的制备和检测
[0145]
以2-甲氧基苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(2-甲氧基苯基)-1,3,4-噻二唑-2-胺(产率:49.2%)。
[0146]
以5-(2-甲氧基苯基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(2-甲氧基苯基-)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j10)。
[0147][0148]
灰白色固体,收率37.3%。esi-ms(m/z):423.11[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.28(dd,j=8.3,3.7hz,1h),8.12(d,j=7.8hz,1h),7.93-7.86(m,1h),7.81-7.72(m,1h),7.50(t,j=7.5hz,1h),7.45(t,j=7.9hz,1h),7.22(d,j=8.7hz,1h),7.09(t,j=7.6hz,1h),4.29(q,j=7.0hz,1h),3.96(s,3h),1.23(t,j=7.1hz,3h).
[0149]
实施例11:化合物j11的制备和检测
[0150]
以3-乙氧基苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(3-乙氧基苯基)-1,3,4-噻二唑-2-胺(产率:49.2%)。
[0151]
以5-(3-乙氧基苯基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(3-乙氧基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j11)。
[0152][0153]
淡黄色固体,收率33.1%。esi-ms(m/z):437.25[m+h]
+
,1h nmr(500mhz,dmso-d6)δ7.45(s,2h),7.39(t,j=7.9hz,2h),7.30(d,j=7.1hz,2h),7.04-6.99(m,2h),4.29(q,j=7.1hz,2h),4.11(q,j=7.0hz,2h),1.37(t,j=7.0hz,3h),1.27-1.14(m,3h).
[0154]
实施例12:化合物j12的制备和检测
[0155]
以2-乙氧基苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(2-乙氧基苯基)-1,3,4-噻二唑-2-胺(产率:49.2%)。
[0156]
以5-(2-乙氧基苯基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(2-乙氧基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j12)。
[0157][0158]
黄色固体,收率54.1%。esi-ms(m/z):437.23[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.15(d,j=7.7hz,1h),7.43(t,j=7.9hz,1h),7.20(d,j=4.4hz,3h),7.07(d,j=7.7hz,1h),4.32-4.27(m,2h),4.24(q,j=7.0hz,2h),1.49(t,j=6.9hz,3h),1.23(t,j=7.1hz,3h).
[0159]
实施例13:化合物j13的制备和检测
[0160]
以4-二氟甲氧基苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(4-二氟甲氧基苯基)-1,3,4-噻二唑-2-胺(产率:61.8%)。
[0161]
以5-(4-二氟甲氧基苯基)-1,3,4-噻二唑-2-胺和和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(4-二氟甲氧基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j13)。
[0162][0163]
黄色固体,收率19.9%。esi-ms(m/z):459.14[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.24(dd,j=14.7,7.3hz,1h),7.89-7.81(m,1h),7.71(d,j=8.4hz,1h),7.60(dd,j=13.2,7.6hz,1h),7.51-7.39(m,2h),7.37-7.29(m,2h),7.19(d,j=12.4hz,1h),4.26(dd,j
=15.6,7.9hz,2h),1.23-1.17(m,3h).
[0164]
实施例14:化合物j14的制备和检测
[0165]
以4-二甲胺基苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(4-二甲氨基苯基)-1,3,4-噻二唑-2-胺(产率:92.2%)。
[0166]
以5-(4-二甲氨基苯基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(4-二甲胺基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j14)。
[0167][0168]
棕色固体,收率16.1%。esi-ms(m/z):436.09[m+h]
+
.1h nmr(500mhz,dmso-d6)δ7.57(d,j=8.5hz,2h),7.18(s,3h),6.77(d,j=8.5hz,3h),4.27(tt,j=23.3,17.0,12.1hz,2h),2.98(s,6h),1.21(dt,j=14.3,7.2hz,3h).
[0169]
实施例15:化合物j15的制备和检测
[0170]
以对甲磺酰基苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(4-甲磺酰基苯基)-1,3,4-噻二唑-2-胺(产率:41.3%)。
[0171]
以5-(4-甲磺酰基苯基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(4-甲磺酰基苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j15)。
[0172][0173]
淡黄色固体,收率为16.6%。esi-ms(m/z):471.35[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.31-8.26(m,1h),8.11(d,j=8.0hz,2h),7.92-7.86(m,1h),7.72(s,2h),7.43-7.39(m,2h),4.40(dd,j=14.1,7.2hz,3h),4.29(q,j=7.4hz,2h),1.27(t,j=7.1hz,3h).
[0174]
实施例16:化合物j16的制备和检测
[0175]
以2,4-二氟苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(2,4-二氟苯基)-1,3,4-噻二唑-2-胺(产率:49.2%)。
[0176]
以5-(2,4-二氟苯基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(2,4-二氟苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j16)。
[0177]
[0178]
白色固体,收率31.4%。esi-ms(m/z):393.09[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.23(dd,j=23.3,11.9hz,2h),7.56(t,j=7.6hz,1h),7.48(q,j=10.3,8.8hz,1h),7.37(d,j=8.4hz,1h),7.28(d,j=8.6hz,1h),7.15(t,j=7.9hz,1h),4.23(q,j=7.9,7.2hz,2h),1.20(s,3h).
[0179]
实施例17:化合物j17的制备和检测
[0180]
以2-氯-4-硝基苯腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(2-氯-4-硝基苯基)-1,3,4-噻二唑-2-胺(产率:61.8%)。
[0181]
以5-(2-氯-4-硝基苯基)-1,3,4-噻二唑-2-胺和和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(2-氯-4-硝基-苯基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j17)。
[0182][0183]
黄色固体,收率25.1%。esi-ms(m/z):472.15[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.46(s,2h),8.39(d,j=8.9hz,1h),8.29(d,j=8.6hz,2h),7.78(s,2h),4.26(q,j=7.6hz,2h),1.23-1.17(m,3h).
[0184]
实施例18:化合物j18的制备和检测
[0185]
以2-氰基吡啶为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(吡啶-2-基)-1,3,4-噻二唑-2-胺(产率:72.9%)。
[0186]
以5-(吡啶-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j18)。
[0187][0188]
白色固体,收率为21.1%。esi-ms(m/z):393.09[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.72-8.59(m,1h),8.28(dd,j=8.3,4.0hz,1h),8.23-8.12(m,1h),8.09-7.96(m,1h),7.89(t,j=9.1hz,1h),7.76(dd,j=24.3,8.3hz,1h),7.62(dd,j=16.6,8.4hz,1h),7.49(q,j=7.3hz,1h),4.36-4.19(m,2h),1.24(t,j=6.9hz,3h).
[0189]
实施例19:化合物j19的制备和检测
[0190]
以3-氰基吡啶为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(吡啶-3-基)-1,3,4-噻二唑-2-胺(产率:72.9%)。
[0191]
以5-(吡啶-3-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(吡啶-3-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j19)。
[0192][0193]
白色固体,收率为为23.3%。esi-ms(m/z):393.09[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.28(dd,j=8.5,4.5hz,1h),8.07(d,j=7.9hz,1h),7.93-7.85(m,1h),7.76(dd,j=23.3,8.3hz,1h),7.66-7.58(m,1h),7.51(q,j=8.1,7.6hz,1h),7.39-7.31(m,1h),7.16-7.07(m,1h),4.29(q,j=6.9hz,2h),1.22(t,j=7.3hz,3h).
[0194]
实施例20:化合物j20的制备和检测
[0195]
以4-氰基吡啶为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(吡啶-4-基)-1,3,4-噻二唑-2-胺(产率:63.2%)。
[0196]
以5-(吡啶-4-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(吡啶-4-基)-1,3,4-噻二唑-3-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j20)。
[0197][0198]
棕色固体,收率26.2%。esi-ms(m/z):393.09[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.28(dd,j=8.2,4.6hz,1h),8.08(s,1h),7.93-7.86(m,1h),7.81-7.72(m,1h),7.64(t,j=7.8hz,1h),7.51(t,j=7.6hz,1h),7.33(s,1h),7.14(s,1h),4.30(q,j=7.1hz,2h),1.23(t,j=7.1hz,3h).
[0199]
实施例21:化合物j21的制备和检测
[0200]
以2-氰基噻吩为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(噻吩-2-基)-1,3,4-噻二唑-2-胺(产率:83.8%)。
[0201]
以5-(噻吩-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(噻吩-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j21)。
[0202][0203]
白色固体,收率19.4%。esi-ms(m/z):399.05[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.28(dd,j=8.4,3.7hz,1h),7.90(t,j=9.3hz,1h),7.75(dd,j=15.8,8.2hz,1h),7.68-7.61(m,1h),7.50(t,j=7.7hz,1h),7.44(d,j=4.9hz,1h),4.29(q,j=7.3hz,2h),1.23(t,j=7.1hz,3h).
[0204]
实施例22:化合物j22的制备和检测
[0205]
以2-氰基呋喃为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(呋喃-2-基)-1,3,4-噻二唑-2-胺(产率:63.2%)。
1,3,4-噻二唑-2-胺的制备,得到中间体5-(1-甲基-1h-吡唑-3-基)-1,3,4-噻二唑-2-胺(产率:41.3%)。
[0221]
以5-(1-甲基-1h-吡唑-3-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(1-甲基-1h-吡唑-3-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j25)。
[0222][0223]
浅绿色固体,收率8.2%。esi-ms(m/z):397.16[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.06(d,j=7.8hz,2h),7.45(t,j=7.8hz,1h),7.33(d,j=8.4hz,1h),7.11(t,j=7.5hz,2h),4.26(s,3h),4.20(q,j=6.9hz,2h),1.18(t,j=7.1hz,3h).
[0224]
实施例26:化合物j26的制备和检测
[0225]
以2-氰基喹啉为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(2-喹啉基)-1,3,4-噻二唑-2-胺(产率:31.1%)。
[0226]
以5-(2-喹啉基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(喹啉-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j26)。
[0227][0228]
棕灰色固体,收率为3.12%。esi-ms(m/z):444.21[m+h]
+
.1h nmr(500mhz,dmso-d6)δ9.46(s,1h),8.48(t,j=10.9hz,2h),8.04(t,j=7.9hz,2h),7.82(d,j=7.9hz,2h),7.71(s,2h),7.66(t,j=7.9hz,2h),4.24(q,j=6.7hz,2h),1.19(t,j=6.7hz,3h).
[0229]
实施例27:化合物j27的制备和检测
[0230]
以1-甲基-1h-吲哚-6-甲腈为起始原料,合成方法同实施例1中提到的中间体5-苯基-1,3,4-噻二唑-2-胺的制备,得到中间体5-(1-甲基-1h-吲哚-6-基)-1,3,4-噻二唑-2-胺(产率:30.2%)。
[0231]
以5-(2-喹啉基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(1-甲基-1h-吲哚-6-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j27)。
[0232][0233]
黄色固体,收率为21.1%。esi-ms(m/z):446.31[m+h]
+
,1h nmr(500mhz,dmso-d6)δ8.24(t,j=9.7hz,1h),8.11(s,1h),7.73-7.66(m,1h),7.57(s,2h),7.40(t,j=14.1hz,2h),7.05-7.12(m,2h),4.38-4.11(m,2h),3.36(s,3h),1.21(s,3h).
[0234]
实施例28:化合物j28的制备和检测
[0235]
以6-甲基-2-氰基吡啶为起始原料,合成方法同实施例1中提到的中间体5-(吡啶-2-基)-1,3,4-噻二唑-2-胺的制备,得到中间体5-(4-甲基吡啶-2-基)-1,3,4-噻二唑-2-胺(产率:10.8%)。
[0236]
以5-(6-甲基吡啶-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(6-甲基吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j28)。
[0237][0238]
棕色固体,收率为9.6%。esi-ms(m/z):408.27[m+h]
+
.1h nmr(500mhz,dmso-d6)δ7.98(s,1h),7.88(d,j=7.9hz,1h),7.81(t,j=7.8hz,1h),7.51(s,2h),7.45(s,1h),7.30(d,j=7.5hz,1h),4.28(d,j=17.4hz,1h),2.76(s,3h),1.27-1.12(m,3h).
[0239]
实施例29:化合物j29的制备和检测
[0240]
以5-甲基-2-氰基吡啶为起始原料,合成方法同实施例1中提到的中间体5-(吡啶-2-基)-1,3,4-噻二唑-2-胺的制备,得到中间体5-(5-甲基吡啶-2-基)-1,3,4-噻二唑-2-胺(产率:45.1%)。
[0241]
以5-(5-甲基吡啶-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(5-甲基吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j29)。
[0242][0243]
棕色固体,收率为12.9%。esi-ms(m/z):408.39[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.22(d,j=7.9hz,1h),8.08(d,j=9.0hz,1h),7.97(d,j=12.7hz,1h),7.77(s,1h),7.56(d,j=8.0hz,1h),7.38(d,j=8.4hz,1h),7.15(s,1h),4.26-4.22(m,2h),2.37(s,3h),1.19(m,3h).
[0244]
实施例30:化合物j30的制备和检测
[0245]
以4-甲基-2-氰基吡啶为起始原料,合成方法同实施例1中提到的中间体5-(吡啶-2-基)-1,3,4-噻二唑-2-胺的制备,得到中间体5-(4-甲基吡啶-2-基)-1,3,4-噻二唑-2-胺(产率:19.1%)。
[0246]
以5-(3-甲基吡啶-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(4-甲基吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j30)。
[0247][0248]
灰色固体,收率为15.7%。esi-ms(m/z):408.71[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.07(s,1h),7.45(s,2h),7.33(s,2h),7.12(s,2h),4.24(s,2h),2.44(s,3h),1.19(s,3h).
[0249]
实施例31:化合物j31的制备和检测
[0250]
以3-甲基-2-氰基吡啶为起始原料,合成方法同实施例1中提到的中间体5-(吡啶-2-基)-1,3,4-噻二唑-2-胺的制备,得到中间体5-(3-甲基吡啶-2-基)-1,3,4-噻二唑-2-胺(产率:19.1%)。
[0251]
以5-(3-甲基吡啶-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(3-甲基吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j31)。
[0252][0253]
灰白色固体,收率为12.6%。esi-ms(m/z):408.31[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.06(d,j=7.8hz,2h),7.45(d,j=7.6hz,2h),7.32(s,1h),7.10(s,2h),4.23(s,2h),1.51(s,3h),1.19(s,3h).
[0254]
实施例32:化合物j32的制备和检测
[0255]
以4-甲氧基-2-氰基吡啶为起始原料,合成方法同实施例1中提到的中间体5-(吡啶-2-基)-1,3,4-噻二唑-2-胺的制备,得到中间体5-(4-甲氧基吡啶-2-基)-1,3,4-噻二唑-2-胺(产率:21.4%)。
[0256]
以5-(4-甲氧基吡啶-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(4-甲氧基吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j32)。
[0257][0258]
灰色固体,收率为9.1%。esi-ms(m/z):424.19[m+h]
+
,1h nmr(500mhz,dmso-d6)δ8.37(d,j=5.8hz,1h),8.05(d,j=7.9hz,1h),7.69(s,1h),7.43(d,j=7.9hz,1h),7.32(d,j=8.5hz,1h),7.10(t,j=7.6hz,1h),6.84(s,1h),4.28-4.17(m,2h),3.92(s,3h),1.20(t,j=7.4hz,3h).
[0259]
实施例33:化合物j33的制备和检测
[0260]
以6-氟-2-氰基吡啶为起始原料,合成方法同实施例1中提到的中间体5-(吡啶-2-基)-1,3,4-噻二唑-2-胺的制备,得到中间体5-(6-氟吡啶-2-基)-1,3,4-噻二唑-2-胺(产率:18.3%)。
[0261]
以5-(6-氟吡啶-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(6-氟吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j33)。
[0262][0263]
棕色固体,收率为8.1%。esi-ms(m/z):412.44[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.13(q,j=7.8hz,2h),8.01(dd,j=7.6,2.2hz,1h),7.68(s,2h),7.24(d,j=8.1hz,2h),4.24(m,2h),1.27-1.15(m,3h).
[0264]
实施例34:化合物j34的制备和检测
[0265]
以5-氟-2-氰基吡啶为起始原料,合成方法同实施例1中提到的中间体5-(吡啶-2-基)-1,3,4-噻二唑-2-胺的制备,得到中间体5-(5-氟吡啶-2-基)-1,3,4-噻二唑-2-胺(产率:18.3%)。
[0266]
以5-(5-氟吡啶-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(5-氟吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j34)。
[0267][0268]
棕色固体,收率为7.3%。esi-ms(m/z):412.24[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.52(s,1h),8.21(d,j=7.7hz,1h),7.96(d,j=13.5hz,1h),7.61-7.56(m,2h),7.38(d,j=8.3hz,1h),7.15(s,1h),4.38-4.09(m,2h),1.21(s,3h).
[0269]
实施例35:化合物j35的制备和检测
[0270]
以3-氟-2-氰基吡啶为起始原料,合成方法同实施例1中提到的中间体5-(吡啶-2-基)-1,3,4-噻二唑-2-胺的制备,得到中间体5-(3-氟吡啶-2-基)-1,3,4-噻二唑-2-胺(产率:35.1%)。
[0271]
以5-(3-氟吡啶-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(3-氟吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j35)。
[0272][0273]
棕色固体,收率12.4%。esi-ms(m/z):412.24[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.52(s,1h),8.21(d,j=7.7hz,1h),7.96(d,j=13.5hz,1h),7.61-7.56(m,2h),7.38(d,j=8.3hz,1h),7.15(s,1h),4.38-4.09(m,2h),1.21(s,3h).
[0274]
实施例36:化合物j36的制备和检测
[0275]
以5-溴-2-氰基吡啶为起始原料,合成方法同实施例1中提到的中间体5-(吡啶-2-基)-1,3,4-噻二唑-2-胺的制备,得到中间体5-(5-溴吡啶-2-基)-1,3,4-噻二唑-2-胺(产率:20.1%)。
[0276]
以5-(5-溴吡啶-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(5-溴吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j36)。
[0277][0278]
棕色固体,收率为7.7%。esi-ms(m/z):472.19[m+h]
+
.esi-ms(m/z):472.19[m+h]
+
,1h nmr(500mhz,dmso-d6)δ8.78(s,2h),8.12(m,3h),7.66(s,2h),4.24(s,2h),1.24(s,3h).
[0279]
实施例37:化合物j37的制备和检测
[0280]
以5-三氟甲基-2-氰基吡啶为起始原料,合成方法同实施例1中提到的中间体5-(吡啶-2-基)-1,3,4-噻二唑-2-胺的制备,得到中间体5-(5-三氟甲基吡啶-2-基)-1,3,4-噻二唑-2-胺(产率:20.1%)。
[0281]
以5-(5-三氟甲基吡啶-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(5-三氟甲基吡啶-2-基)-1,3,4-噻二唑-2-基)-1-乙基-4-羟基-2-喹诺酮-3-甲酰胺(j37)。
[0282][0283]
灰白色固体,收率为4.2%。esi-ms(m/z):462.28[m+h]
+
,1h nmr(500mhz,dmso-d6)δ9.02(s,1h),8.38(s,1h),8.20(s,1h),7.78(s,1h),7.57(s,1h),7.38(s,1h),7.14(s,1h),4.27-4.20(m,2h),1.21(s,3h).
[0284]
实施例38:化合物j38的制备和检测
[0285]
以6-氟靛红酸酐为起始原料,合成方法同实施例1中提到的中间体1-乙基-4-羟基-2-喹诺酮-3-甲酸的制备,得到中间体1-乙基-4-羟基-6-氟-2-喹诺酮-3-甲酸(产率:50.2%)。
[0286]
以5-(噻唑-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-6-氟-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(噻唑-2-基)-1,3,4-噻二唑-2-基)-1-乙基-6-氟-4-羟基-2-喹诺酮-3-甲酰胺(j38)。
[0287][0288]
黄色固体,收率16.9%。esi-ms(m/z):418.12[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.28(d,j=8.4hz,1h),8.08(dd,j=9.0,2.9hz,1h),7.92(d,j=8.4hz,1h),7.74(d,j=8.0hz,1h),7.63(t,j=7.7hz,1h),4.29(q,j=7.1hz,2h),1.22(t,j=7.0hz,3h).
[0289]
实施例39:化合物j39的制备和检测
[0290]
以7-氯靛红酸酐为起始原料,合成方法同实施例1中提到的中间体1-乙基-4-羟基-2-喹诺酮-3-甲酸的制备,得到中间体1-乙基-4-羟基-7-氯-2-喹诺酮-3-甲酸(产率:50.2%)。
[0291]
以5-(噻唑-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-7-氯-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(噻唑-2-基)-1,3,4-噻二唑-2-基)-1-乙基-7-氯-4-羟基-2-喹诺酮-3-甲酰胺(j39)。
[0292][0293]
黄色固体,收率30.7%。esi-ms(m/z):434.18[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.27(d,j=7.4hz,1h),7.99(d,j=6.9hz,1h),7.95-7.90(m,1h),7.82-7.71(m,1h),7.62(t,j=7.7hz,1h),4.27(q,j=6.9hz,2h),1.21(t,j=6.9hz,3h).
[0294]
实施例40:化合物j40的制备和检测
[0295]
以8-氯靛紅酸酐为起始原料,合成方法同实施例1中提到的中间体1-乙基-4-羟基-2-喹诺酮-3-甲酸的制备,得到中间体1-乙基-4-羟基-8-氯-2-喹诺酮-3-甲酸(产率:50.2%)。
[0296]
以5-(噻唑-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-8-氯-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(噻唑-2-基)-1,3,4-噻二唑-2-基)-1-乙基-8-氯-4-羟基-2-喹诺酮-3-甲酰胺(j40)。
[0297][0298]
棕色固体,收率19.6%。esi-ms(m/z):434.28[m+h]
+
.1h nmr(500mhz,dmso-d6)δ8.27(dd,j=8.5,4.3hz,1h),8.04(d,j=8.8hz,1h),7.89(q,j=8.1hz,1h),7.77-7.72(m,1h),7.54(d,j=8.6hz,1h),4.28(q,j=7.0hz,2h),1.20(t,j=7.1hz,3h).
[0299]
实施例41:化合物j41的制备和检测
[0300]
以6-甲基靛红酸酐为起始原料,合成方法同实施例1中提到的中间体1-乙基-4-羟基-2-喹诺酮-3-甲酸的制备,得到中间体1-乙基-4-羟基-6-甲基-2-喹诺酮-3-甲酸(产率:50.2%)。
[0301]
以5-(噻唑-2-基)-1,3,4-噻二唑-2-胺和1-乙基-4-羟基-6-甲基-2-喹诺酮-3-甲酸为起始原料,合成方法同实施例1中提到的终产物j1的制备,得到n-(5-(噻唑-2-基)-1,3,4-噻二唑-2-基)-1-乙基-6-甲基-4-羟基-2-喹诺酮-3-甲酰胺(j41)。
[0302]
8、mrsa15-9;甲氧西林敏感金黄色葡萄球菌:mssa15-1、mssa15-1;万古霉素敏感金黄色葡萄球菌:atcc25923;万古霉素中度敏感金黄色葡萄球菌:atcc700699、atcc700788)、表皮葡萄球菌5株(甲氧西林耐药表皮葡萄球菌:mrse15-1、mrse15-2、mrse15-3;甲氧西林敏感表皮葡萄球菌:msse15-3、msse15-4)、粪肠球菌6株(万古霉素敏感粪肠球菌:efa15-1、efa15-2、atcc29212;万古霉素耐药粪肠球菌:atcc51299、atcc700802、atcc51575)、屎肠球菌3株(万古霉素敏感屎肠球菌efm15-1、efm15-2;万古霉素耐药屎肠球菌atcc700221)。
[0319]
2.培养基及培养条件
[0320]
葡萄球菌:mh肉汤,35-37℃孵育18-24h观察结果。
[0321]
其它菌种:常规mh肉汤,35-37℃孵育18-24h观察结果。
[0322]
mh肉汤配方:蛋白胨1%,牛肉粉0.3%,nacl 0.5%。
[0323]
3.测试方法
[0324]
(1)方法依据
[0325]
采用美国临床和实验室标准协会(clinical and laboratory standards institute,clsi)抗菌药物敏感性试验操作规程【methods for dilution antimicrobial succeptibility tests for bacteria that grow aerobically;approved standard-eleventh edition,m07-a11,2018】推荐的微量肉汤稀释法测定各受试样品对所试菌株的mic值。
[0326]
(2)具体操作步骤
[0327]
分别吸取100μl各不同浓度的受试样品溶液加到灭菌的96孔聚苯乙烯板中的第1至第12孔内,使药物终浓度分别为64、32、16、8、4、2、1、0.5、0.25、0.125、0.06、0.03μg/ml(具体浓度范围根据药品量来计算)。再于各孔内加入100μl的受试菌液(每孔容量200μl),菌液最终浓度约为105cfu/ml。密封后置于35-37℃培养箱内培养18-24h,判断结果。以在小孔内完全抑制细菌生长的最低药物浓度为受试样品的mic。同时设立不加任何样品的空白菌对照和加dmso的溶媒对照。
[0328]
4.化合物的抗革兰氏阳性菌的抗菌谱见表2。
[0329]
实验例3:化合物的抗艰难梭菌活性测定
[0330]
1.菌种类别
[0331]
艰难梭菌标准菌株atcc9689或广州地区收集的临床分离菌株18-2。
[0332]
2.培养基及培养条件
[0333]
布氏肉汤培养基,于37℃厌氧环境下培养48h。
[0334]
培养基配方:5%(v/v)脱纤维羊血、氯化血红素(5mg/l)和维生素k1(1mg/l)。
[0335]
3.测试方法
[0336]
(1)方法依据
[0337]
采用美国临床和实验室标准协会(clsi)抗菌药物敏感性试验操作规程(m11-a8,2012)推荐的琼脂稀释法测定受试样品对所试菌株的mic值。
[0338]
(2)具体操作步骤
[0339]
制备强化布氏肉汤琼脂培养基,对其进行高压灭菌并置于60℃水浴中平衡。将已2倍稀释的不同浓度的受试样品dmso溶液分别加入到强化布氏肉汤琼脂中,充分混匀,制得320-0.15μg/ml范围内的12个浓度梯度的受试药液。然后,分别取1ml的受试药液加入到9ml
的琼脂培养基中,配制32-0.015μg/ml范围内的12个浓度的药物琼脂平板。随后,用多点接种器吸取1-2μl细菌悬液接种于含药琼脂平板表面,每点接种菌量约为105cfu,形成直径为5-8mm的菌斑。接种后置于厌氧环境中于35℃条件下孵育48h。之后观察细菌生长情况,以未见细菌生长的含药琼脂平板对应的浓度即该受试样品的mic。
[0340]
4.化合物抗艰难梭菌的活性见表3。
[0341]
实验例4:化合物的抗肺炎支原体的活性测定
[0342]
1.菌种类别
[0343]
云南地区的肺炎支原体临床分离菌株mp19和mp标准菌株atcc29342(m129株)。
[0344]
2.测试方法
[0345]
于无菌试管中,采用液体培养基按倍比稀释法配制5、10、20、40μg/ml四个浓度的药液。然后,往试管中加入等量的菌液(质量浓度为105cfu/ml),充分混匀后,于37℃条件下培养18-24小时。同时设乙酰螺旋霉素为阳性对照,培养基对照和菌株对照。通过观察培养基颜色变化判断药物活性,培养基对照颜色为红色,菌株对照颜色为黄色。实验为二重复。
[0346]
3.化合物抗肺炎支原体的活性见表4。
[0347]
实验例5:化合物j24对mrsa腹腔注射所致的系统感染小鼠体内保护实验
[0348]
1.菌种类别
[0349]
对化合物敏感的mrsa临床分离菌株mrsa15-1
[0350]
2.测试方法
[0351]
(1)最小致死菌量的确定
[0352]
取体重约18-22克的健康km小鼠(雌雄各半),随机分成4组(每组5只)。吸取4个不同稀释浓度的mrsa15-1菌液,分别腹腔注射入相应组别的小鼠体内,注射的体积为25ml/kg。感染后观察7-14天,并记录小鼠死亡数。导致小鼠100%死亡的最低菌量为最小致死菌量,最小致死菌量为体内保护试验的感染菌量。
[0353]
(2)体内保护试验
[0354]
取体重约18-22克的健康km小鼠(雌雄各半),随机分组。受试药物j24和阳性药利奈唑胺各4个剂量组(每组8只)。感染当天将最小致死菌量的mrsa15-1腹腔注射入小鼠体内,建立腹腔注射mrsa15-1所致的系统感染小鼠模型。按设计剂量在感染前6h和12h各灌胃给药一次(共预防给药两次),感染后按设计剂量在0h和6h各灌胃给药一次(共给药2次)。各组动物给药后,观察并记录小鼠死亡数。连续观察7-14天,根据小鼠死亡数,用孙瑞元等主编das1.0软件按bliss法计算半数有效剂量ed50及95%可信限。另设感染对照组(8只,在设定的时间点灌胃给予等体积的生理盐水),受试药物毒性对照组(5只,不感染细菌,腹腔注射等体积的生理盐水,只在设定的时间点灌胃给予相同体积的受试药物)、空白对照组(5只,不感染细菌,腹腔注射等体积的生理盐水,在设定的时间点灌胃给予相同体积的生理盐水)。
[0355]
3.化合物对mrsa腹腔注射所致的系统感染小鼠体内保护实验结果见表5。
[0356]
(1)受试药物j24:40、20、10和5mg/kg,阳性药利奈唑胺:20、10、5和2.5mg/kg;
[0357]
(2)受试药物j24:9、3、1和0.3mg/kg,阳性药利奈唑胺:9、3、1和0.3mg/kg。
[0358]
表1.化合物对金黄色葡萄球菌标准菌株atcc 29213的最低抑菌浓度
[0359][0360]
[0361]
[0362][0363]
表2.代表性化合物对革兰氏阳性菌不同菌株的最低抑菌浓度mic(μg/ml)。
[0364][0365]
表3.化合物对艰难梭菌临床分离株和标准菌株的最低抑菌浓度mic(μg/ml)。
[0366][0367]
表4.代表性化合物对肺炎支原体临床分离或标准菌株的最低抑菌浓度mic(μg/ml)。
[0368][0369]
表5.j24经小鼠灌胃给药对金黄色葡萄球菌mrsa15-1所致的系统感染模型体内实验结果
[0370]
剂量组(1)
[0371][0372]
剂量组(2)
[0373]
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



