一种卡托普利作用机制的模型教具的制作方法
 2021-01-25 17:01:58|
2021-01-25 17:01:58| 325|
325| 起点商标网
起点商标网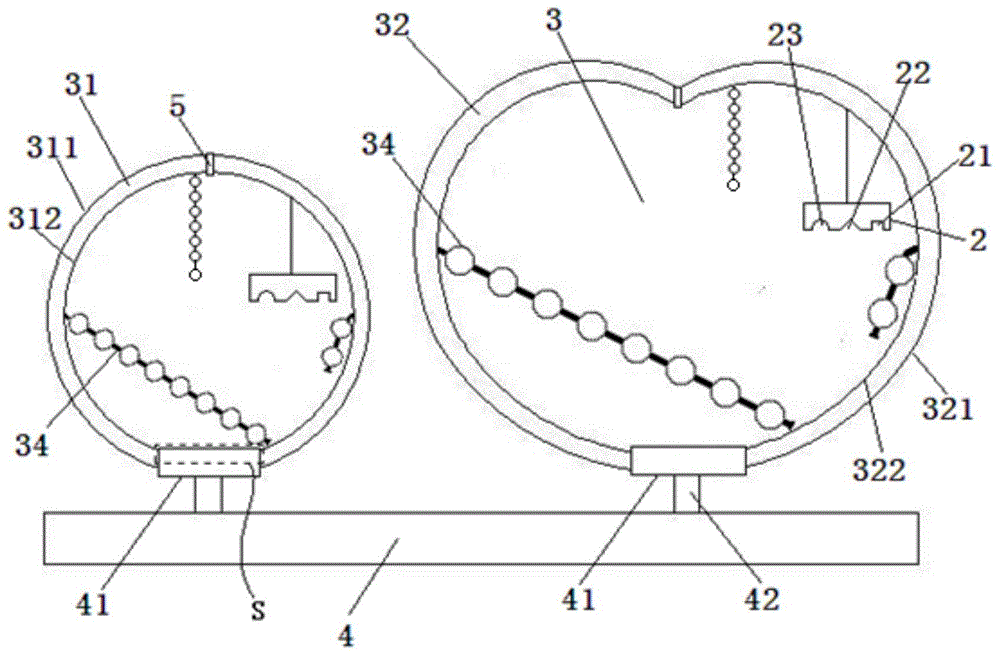
本发明涉及教学用具领域,具体涉及一种卡托普利作用机制的模型教具。
背景技术:
卡托普利属于血管紧张素转化酶抑制药,常用于治疗高血压和慢性心功能不全,属于药理学必讲内容。
血管紧张素转化酶(angiotensinconvertingenzyme,ace)又称激肽酶ⅱ,主要催化血管紧张素ⅰ(10肽)转化为血管紧张素ⅱ(8肽),并使缓激肽(9肽)失活为7肽。血管紧张素ⅱ使小动脉收缩而升高血压,也可促进肾上腺皮质分泌醛固酮,发挥保钠排钾作用,使血容量增多,血压升高,还可促进心脏血管肥大增生。
卡托普利有三个基团能与ace的活性部位结合:(1)脯氨酸的末端羧基与酶的正电荷部位(精氨酸)呈离子键结合;(2)肽键的羰基与酶的供氢部位呈氢键结合;(3)巯基与酶中锌离子结合。卡托普利与ace结合后抑制该酶的活性,使血管紧张素ⅱ生成减少而扩张血管、降低血压、减轻心脏后负荷,并且可减少醛固酮分泌,使水钠潴留减轻,静脉回心血量减少,从而减轻心脏前负荷,心输出量增加,有利于心功能的改善,并逆转心脏血管肥大增生。同时还减少缓激肽的降解,缓激肽使no(一氧化氮)和pgi2(前列腺素i2,前列环素)生成增加,可加强降血压、抗心功能不全、抗心肌和血管细胞肥大增生和心肌重构作用。
在讲解卡托普利作用机制时目前只能借助药理学教材及教学课件上的文字或图片,这种教学方法缺乏直观性、生动性,学生不能很好地理解卡托普利作用机制。
技术实现要素:
针对现有技术不足,本发明提供了一种具有直观性的卡托普利作用机制的立体模型教具。
本发明解决上述技术问题所采用的技术方案为:
一种卡托普利作用机制的模型教具,其包括卡托普利模块、血管紧张素转化酶模块、肌体模块及连接装置,所述的肌体模块包括血管横断面模型、心脏横断面模型、血管紧张素ⅰ指代模型、血管紧张素ⅱ指代模型、缓激肽指代模型、no指代模型以及pgi2指代模型,所述的血管横断面装置和心脏横断面装置设置在连接装置上,所述的血管紧张素ⅰ指代模型、血管紧张素ⅱ指代模型和缓激肽指代模型设置在血管横断面模型以及心脏横断面模型内部,所述的no指代模型以及pgi2指代模型设置在缓激肽指代模型内部,所述的卡托普利模块和血管紧张素转化酶模块设置在血管横断面模型以及心脏横断面模型内部。
进一步地,所述的血管横断面模型包括外圆环和内圆环,所述的外圆环大小固定,所述的内圆环设置在外圆环的内部,所述的内圆环为绕曲一周的螺旋圆形环体,环体的两个接头部位交错相接。
进一步地,所述的内圆环通过与连接装置固接的连接部与外圆环连接并将内圆环设置在外圆环的内部,所述的连接部将内圆环环体的两个接头夹在其内部,并通过固定装置将内圆环的一个接头固定于连接部上,另一个接头悬空。
进一步地,所述的血管横断面模型上部设置有挡固装置,所述的挡固装置为两片挡片,使内圆环与外圆环处于同一纵向平面内,挡固装置并不影响内圆环的弹性伸缩;所述的内圆环和外圆环之间的间距代指血管壁厚度。
进一步地,所述的心脏横断面模型包括心形外框和心形内框,所述的心形外框大小固定,所述的心形内框设置在心形外框的内部,所述的心形内框为绕曲一周的螺旋心形环体,环体的两个接头部位交错相接。
进一步地,所述的心形内框通过与连接装置固接的连接部与心形外框连接并将心形内框设置在心形外框的内部,所述的连接部将心形内框环体的两个接头夹在其内部,并通过固定装置将心形内框的一个接头固定于连接部上,另一个接头悬空。
进一步地,所述的心脏横断面模型上部同样设置有挡固装置;所述的心形内框和心形外框之间的间距代指心脏壁厚度。
进一步地,所述的血管紧张素ⅰ指代模型为10个串珠组成的链状物,血管紧张素ⅰ指代模型设置于血管横断面模型内圆环的内部以及心脏横断面模型心形内框的内部,10个串珠组成的链状物呈直线排列成可产生支撑力的直链一,而且直链一的长度大于内圆环的内径以及心形内框内部最宽部位的长度,所述心形内框内部最宽部位的长度是指心形内框上任何两点之间的连线的最大值,在内圆环内部,直链一通过内圆环圆心将两端分别固定于内圆环内部,在心形内框内部,直链一通过心形内框内部最宽部位将两端分别固定于心形内框内部;所述的直链一的10个串珠的末端第8-9串珠之间通过磁吸固定,其他串珠之间固定连接;所述的血管紧张素ⅱ指代模型即8个串珠组成的链状物为直链一的10个串珠的末端第8-9串珠之间的连接断掉后、去掉末端的两个串珠形成的直链二,所述直链二的长度小于内圆环的内径以及心形内框内部最宽部位的长度;所述的缓激肽指代模型为9个串珠组成的链状物,而且9个串珠之间的连接均为无支撑力的磁吸连接,所述的缓激肽指代模型通过柔性线与内圆环和心形内框连接;所述的no指代模型为长方体、pgi2指代模型为有侧链且横截面为正五边形的立柱,所述的长方体及立柱设置于9个串珠组成的链状物的其中一个或者多个串珠的内部,且此内部装有长方体及立柱的串珠为具有开门的中空结构串珠,由于no及pgi2均为较小的分子,因此将之设计为小型立体结构并设置于缓激肽指代模型内部,代指在卡托普利与ace结合后减少缓激肽的降解,缓激肽可以增加no及pgi2的生成,在讲解no及pgi2的生成时,可以打开盛有长方体及立柱的串珠即可;
进一步地,所述的血管紧张素转化酶模块为一长方体并在其底部设置有三个不同形状的、分别代表酶的正电荷部位(精氨酸)、供氢部位和锌离子的凹陷,所述的凹陷部位设置有磁铁或可与磁铁吸合的金属,所述的锌离子处的凹陷处呈内凹切刀状,用于将10个串珠组成的链状的血管紧张素ⅰ的通过磁吸固定的第8-9串珠之间切断,催化血管紧张素ⅰ(10肽)转化为血管紧张素ⅱ(8肽);还可用于将9个串珠组成的链状物的缓激肽c末端的两个肽切掉,成为7个串珠组成的链状物的失活肽,酶中锌离子部位活性最强,因此选择将锌离子部位设计为切刀状可更形象地表示酶切反应过程,而切刀切的过程仅供示意,在切后可以手动断开第8-9串珠之间的吸合,在10个串珠组成的链状物转化为8个串珠组成的链状物后,直链一对内圆环以及心形内框的支撑作用消失,内圆环恢复原状即绕曲一周的螺旋圆形环体而且环体的两个接头部位交错相接,内圆环和外圆环之间的间距变大,代指血管收缩、管壁肥厚,心形内框恢复原状即绕曲一周的螺旋心形环体且环体的两个接头部位交错相接,心形内框和心形外框之间的间距变大,代指心脏壁变厚;所述的血管紧张素转化酶模块以及卡托普利模块通过柔性线设置于内圆环和心形内框的内部。
进一步地,所述的卡托普利模块为一长链状并伸出三个与凹陷配合、分别代表脯氨酸的末端羧基、肽键的羰基和巯基的凸起,所述的凸起部位设置有磁铁或可与磁铁吸合的金属,用于将卡托普利模块与血管紧张素转化酶模块通过磁吸结合,代指ace与卡托普利的反应,使血管紧张素转化酶模块的凹陷所代表的正电荷部位(精氨酸)、供氢部位和锌离子活性部位与卡托普利模块的凸起所代表的脯氨酸的末端羧基、肽键的羰基和巯基基团结合,进而使ace失活。
进一步地,所述的连接装置为底座固定装置,所述的血管横断面装置和心脏横断面装置通过支架设置在底座固定装置上。
与现有技术相比,本发明具备的优点为:本发明的卡托普利作用机制的模型教具为立体模型结构,具直观性,同时能增加学生的动手能力,加深记忆,使学生更加深入地理解卡托普利作用的机制,有助于药理学课程教学。
附图说明
图1为未施用卡托普利的模型教具的结构示意图;
图2为施用卡托普利的模型教具的结构示意图;
图3为图1中s部位的俯视放大结构示意图;
图4为图2中s部位的俯视放大结构示意图;
图5为图2中a部位的放大结构示意图,图中同时对串珠的开门结构给出了示意结构。
具体实施方式
下面结合附图对本发明做进一步的说明。
如图1、2所示,一种卡托普利作用机制的模型教具,其包括卡托普利模块1、血管紧张素转化酶模块2、肌体模块3及连接装置4,所述的肌体模块3包括血管横断面模型31、心脏横断面模型32、血管紧张素ⅰ指代模型33、血管紧张素ⅱ指代模型34、缓激肽指代模型35、no指代模型36以及pgi2指代模型37,所述的血管横断面模型31和心脏横断面模型32设置在连接装置4上,所述的血管紧张素ⅰ指代模型33、血管紧张素ⅱ指代模型34和缓激肽指代模型35设置在血管横断面模型31以及心脏横断面模型32内部,所述的no指代模型36以及pgi2指代模型37设置在缓激肽指代模型35内部,所述的卡托普利模块1和血管紧张素转化酶模块2设置在血管横断面模型31以及心脏横断面模型32内部。
进一步地,所述的血管横断面模型31包括外圆环311和内圆环312,所述的外圆环311采用硬质材料保证其大小固定,所述的内圆环312设置在外圆环311的内部,所述的内圆环312为绕曲一周的螺旋圆形环体,环体的两个接头312-1和312-2交错相接,如图3所示。
进一步地,所述的内圆环312通过与连接装置4固接的连接部41与外圆环311连接并将内圆环312设置在外圆环311的内部,所述的连接部41设置在血管横断面模型31的底部并与外圆环311固定连接,所述的连接部41将内圆环312环体的两个接头312-1和312-2夹在其内部,并通过固定装置313将内圆环312的一个接头312-1固定于连接部41上,另一个接头312-2悬空;所述的血管横断面模型31上部设置有挡固装置5,所述的挡固装置5包括固定于外圆环311两侧的、将内圆环312的上部夹在内部的两片挡片,所述的挡固装置5用于稳固内圆环312使内圆环312与外圆环311处于同一纵向平面内,但挡固装置5并不影响内圆环312的弹性伸缩;所述的内圆环312和外圆环311之间的间距代指血管壁厚度。
进一步地,所述的心脏横断面模型32包括心形外框321和心形内框322,所述的心形外框321大小固定,所述的心形内框322设置在心形外框321的内部,所述的心形内框322为绕曲一周的螺旋心形环体,环体的两个接头部位与内圆环312的两个接头部位结构相同。
进一步地,所述的心形内框322通过与连接装置4固接的连接部41与心形外框321连接并将心形内框322设置在心形外框321的内部,所述的连接部41设置在心脏横断面模型32的底部并与心形外框321固定连接,所述的连接部41将心形内框322环体的两个接头夹在其内部,并通过固定装置将心形内框322的一个接头固定于连接部41上,另一个接头悬空;所述的心脏横断面模型32上部同样设置有挡固装置5;所述的心形内框322和心形外框321之间的间距代指心脏壁厚度。鉴于与真实心脏横断面呈比例的框形,由于其截面框形不对称而且结构复杂,同时内、外框之间的厚度不易表达,因此本发明采用心形外框321和心形内框322代指心脏横断面的形状,结构简单、直观性强、便于操作;上述的内圆环312/心形内框322具有一定的弹性/伸缩性能,即绕曲一周的、两个接头部位交错相接的螺旋圆形/心形环体,可以通过施力扩大或缩小环体直径,在通过施力扩大环体直径时两个接头部位相离,即图2所示的内圆环312/心形内框322在血管紧张素ⅰ指代模型33的支撑作用下使环体直径扩大、内圆环312/心形内框322与外圆环311/心形外框321之间的间距缩小,两个接头部位相离,环体接头部位结构如本发明图4所示;在施力消失后内圆环312/心形内框322恢复原状即绕曲一周的螺旋圆形/心形环体而且环体的两个接头部位交错相接,即图1所示的内圆环312/心形内框322结构,两个接头部位恢复原状即如图3所示。
进一步地,所述的血管紧张素ⅰ指代模型33为10个串珠组成的链状物,血管紧张素ⅰ指代模型33设置于血管横断面模型内圆环312的内部以及心脏横断面模型心形内框322的内部,10个串珠组成的链状物呈直线排列成可产生支撑力的直链一,而且直链一的长度大于内圆环312的内径以及心形内框322内部最宽部位的长度,所述心形内框322内部最宽部位的长度是指心形内框322上任何两点之间的连线的最大值,在内圆环312内部,直链一通过内圆环312的圆心将两端分别固定于内圆环312内部,直链一与内圆环312的连接为可弯折连接;在心形内框322内部,直链一通过心形内框322内部最宽部位将两端分别固定于心形内框322内部,直链一与心形内框322的连接为可弯折连接;所述的直链一的10个串珠的末端第8-9串珠之间331通过磁吸固定,其他串珠之间固定连接;在内圆环312以及心形内框322内部的血管紧张素ⅰ指代模型33为相同结构的血管紧张素ⅰ指代模型33,为了便于讲解,本发明附图1和附图2中将心形内框322内部的血管紧张素ⅰ指代模型33设计的较内圆环312内部的血管紧张素ⅰ指代模型33大,其实际为同一结构的血管紧张素ⅰ指代模型,同时形成同一结构的直链一;所述的血管紧张素ⅱ指代模型34即8个串珠组成的链状物为直链一的10个串珠的末端第8-9串珠之间331的连接断掉后、去掉末端的两个串珠形成的直链二,所述直链二的长度小于内圆环312的内径以及心形内框322内部最宽部位的长度;所述的缓激肽指代模型35为9个串珠组成的链状物,而且9个串珠之间的连接均为无支撑力的磁吸连接,所述的缓激肽指代模型35通过柔性线与内圆环312和心形内框322连接;如图5所示,所述的no指代模型36为长方体、pgi2指代模型37为有侧链且横截面为正五边形的立柱,所述的长方体及立柱设置于9个串珠组成的链状物的其中一个或者多个串珠的内部,且此内部装有长方体及立柱的串珠为具有开门的中空结构串珠,由于no及pgi2均为较小的分子,因此将之设计为小型立体结构并设置于缓激肽指代模型35内部,代指在卡托普利与ace结合后减少缓激肽的降解,缓激肽可以增加no及pgi2的生成,在讲解no及pgi2的生成时,可以打开盛有长方体及立柱的串珠、展示no指代模型及pgi2指代模型即可;上述均以一条直链代指血管及心脏腔内许多血管紧张素ⅰ分子、血管紧张素ⅱ分子或缓激肽分子,因此直链一对血管壁或心脏壁的支撑不应看做一条而应该理解为许多条在不同方位起作用。
进一步地,所述的血管紧张素转化酶模块2为一长方体并在其底部设置有三个不同形状的、分别代表酶的正电荷部位(精氨酸)21、供氢部位22和锌离子23的凹陷,所述的凹陷部位设置有磁铁或可与磁铁吸合的金属,所述的锌离子23处的凹陷处呈内凹切刀状,用于将10个串珠组成的链状物的血管紧张素ⅰ的通过磁吸固定的第8-9串珠之间331切断,催化血管紧张素ⅰ(10肽)转化为血管紧张素ⅱ(8肽);还可用于将9个串珠组成的链状物的缓激肽c末端的两个肽切掉,成为7个串珠组成的链状物的失活肽,酶中锌离子23部位活性最强,因此选择将锌离子部位设计为切刀状可更形象地表示酶切反应过程,而切刀切的过程仅供示意,在切后可以手动断开第8-9串珠之间331的吸合,在10个串珠组成的链状物转化为8个串珠组成的链状物后,直链一对内圆环312以及心形内框322的支撑作用消失,并且缓激肽失活后不能增加扩血管的no及pgi2的生成,内圆环312恢复原状即绕曲一周的螺旋圆形环体而且环体的两个接头部位交错相接,内圆环和外圆环之间的间距变大,代指血管紧张素ⅱ使血管收缩、管壁肥厚,心形内框322恢复原状即绕曲一周的螺旋心形环体且环体的两个接头部位交错相接,心形内框和心形外框之间的间距变大,代指血管紧张素ⅱ使心脏壁变厚;所述的血管紧张素转化酶模块2以及卡托普利模块1通过柔性线24设置于内圆环312和心形内框322的内部。
进一步地,所述的卡托普利模块1为一长链状并伸出三个与凹陷配合、分别代表脯氨酸的末端羧基11、肽键的羰基12和巯基13的凸起,所述的凸起部位设置有磁铁或可与磁铁吸合的金属,用于将卡托普利模块1与血管紧张素转化酶模块2通过磁吸结合,代指ace与卡托普利的反应,使血管紧张素转化酶模块2的凹陷所代表的正电荷部位(精氨酸)21、供氢部位22和锌离子23活性部位与卡托普利模块1的凸起所代表的脯氨酸的末端羧基11、肽键的羰基12和巯基13基团结合,进而使ace失活,减少血管紧张素ⅱ生成及缓激肽降解,继而no和pgi2生成增加,从而扩张血管、降低血压,并改善心功能、逆转心脏及血管壁肥厚增生。
进一步地,所述的连接装置4为底座固定装置,所述的血管横断面模型31和心脏横断面模型32通过支架42设置在底座固定装置上。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询



 商标分类
商标分类  商标转让
商标转让 



