一种基于高光谱成像的多生理参数检测装置及方法与流程
 2021-01-08 13:01:33|
2021-01-08 13:01:33| 299|
299| 起点商标网
起点商标网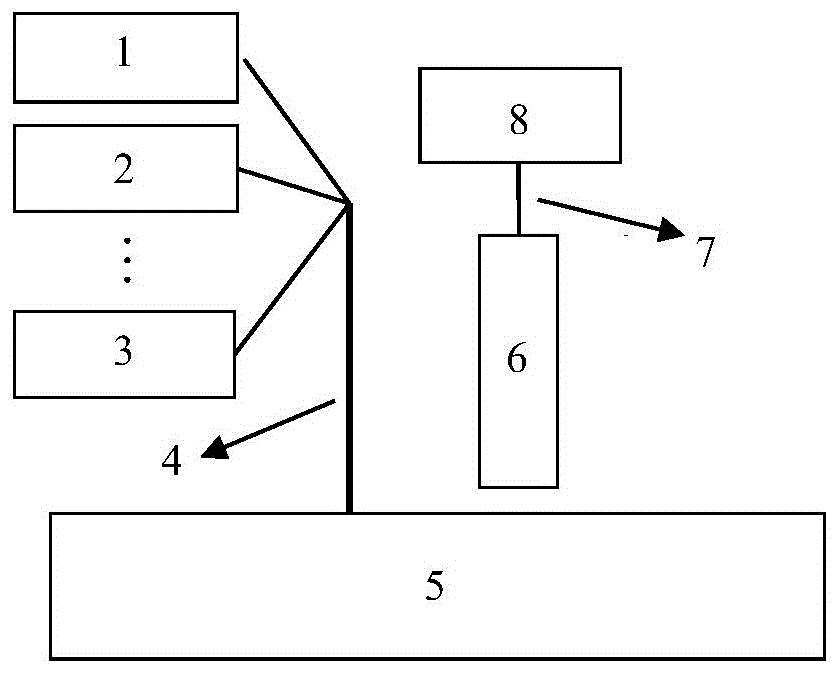
本发明涉及生物医学工程技术领域,尤其涉及一种基于高光谱成像的多生理参数检测装置及方法。
背景技术:
组织血流(bloodflow,bf)、组织血氧饱和度(oxygensaturation,sto2)、组织氧摄取分数(oxygenextractionfraction,oef)及组织氧代谢率(mro2)等多项生理参数,均是与生理和病理状态密切相关的参数,是衡量机体正常与否的重要指标,在脑疾病、乳腺癌以及心血管类疾病等的诊断和治疗中具有关键性的指导意义[1-2]。在众多生理参数中,组织血流和组织血氧饱和度的检测尤为重要,原因在于组织氧摄取及组织氧代谢相关的其他参数均可以在两者的基础上推导计算得出。因此,满足组织血流和组织血氧检测便可检测得到其他相关的生理参数。
在组织血流检测方面,激光多普勒(laserdoppler,ld)穿透深度低、核磁共振成像(magneticresonanceimaging,mri)时间分辨率低且不能长时间实时床边诊断、正电子发射断层成像技术(positronemissiontomography,pet)存在辐射损害。近红外光谱(650nm-950nm)对于生物组织具有良好的穿透性,水、血红蛋白与脂肪等生物组织的主要发色团在近红外波段的吸收相对较弱,有益于实现深层组织血流的检测。基于此,近扩散相关光谱(diffusecorrelationspectroscopy,dcs)利用近红外光谱照射到组织表面,通过计算组织表面散射光斑的光强自相关函数推算组织中红细胞的运动状态,计算得出血流指数(bloodflowindex,bfi),从而实现组织血流(bloodflow,bf)变化的定量检测[3-5]。相比于现有血流检测技术,扩散相关光谱具有无创、实时、长时间床边检测、成本低、易操作等优势,可广泛应用于深层组织血流的检测。在组织血氧检测方面,近红外光谱技术(nearinfraredspectroscopy,nirs),又被称作扩散光学光谱(diffuseopticalspectroscopy,dos)已经较为成熟,且具有巨大的优势。该技术利用近红外光谱特性实现了深层生物组织血红蛋白(hbo2)、脱氧血红蛋白(hb)和血氧饱和度(sto2)的无创测量,并且广泛应用于脑疾病、乳腺癌以及心血管类疾病的早期诊断中[6-7]。
高光谱成像技术[8-9]将光谱分析与光学成像合二为一,不仅能够获取被测对象外在的结构信息,其高分辨率的光谱还能够提供被测对象组分含量的变化信息。本发明将高光谱成像技术与扩散相关光谱、扩散光学光谱相结合,在扩散相关光谱组织血流测量及扩散光学光谱组织血氧饱和度测量的基础上,利用高光谱成像仪以非接触式扫描获取被测组织成像区域内多个波长的光强变化,并在光强数据矩阵的基础上计算出每个像元的组织血流变化及组织血氧饱和度变化,继而计算得出组织氧摄取分数、组织氧代谢率等其他相关生理参数变化,从而实现多生理参数的二维成像。
参考文献:
[1]leouxp.“physiologicalmonitoringoftheseveretraumaticbraininjurypatientintheintensivecareunit,”currentneurologyandneurosciencereports,13(3):331(2013).
[2]buschdr,lynchjm,wintersme,etal,“cerebralbloodflowresponsetohypercapniainchildrenwithobstructivesleepapneasyndrome,”sleep,39(1):209-216(2016).
[3]t.durdurananda.g.yodh,“diffusecorrelationspectroscopyfornon-invasive,micro-vascularcerebralbloodflowmeasurement,”neuroimage85,51,elsevierinc.(2014).
[4]w.b.bakeretal.,“effectsofexercisetrainingoncalfmuscleoxygenextractionandbloodflowinpatientswithperipheralarterydisease,”j.appl.physiol.123(6),1599–1609(2017).
[5]z.lietal.,“calibrationofdiffusecorrelationspectroscopybloodflowindexwithvenous-occlusiondiffuseopticalspectroscopyinskeletalmuscle,”j.biomed.opt.20(12),125005(2015).
[6]giovannellm,continid,pagliazzim,etal.,“babyluxdevice:adiffuseopticalsystemintegratingdiffusecorrelationspectroscopyandtime-resolvednear-infraredspectroscopyfortheneuromonitoringoftheprematurenewbornbrain,”neurophotonics,6(02):025007(2019).
[7]a.tanketal.,“diffuseopticalspectroscopicimagingrevealsdistinctearlybreasttumorhemodynamicresponsestometronomicandmaximumtolerateddoseregimens,”breastcancerres.22(1),1-10,(2020).
[8]calinma,parascasv,savastrud,manead,“hyperspectralimaginginthemedicalfield:presentandfuture,”appliedspectroscopyreviews,49(6),435-447(2014).
[9]ortega,samuel,etal.“detectingbraintumorinpathologicalslidesusinghyperspectralimaging,”biomedicalopticsexpress9(2),818(2018).
技术实现要素:
本发明提供一种基于高光谱成像的多生理参数检测装置及方法,旨在有机融合高光谱成像技术、扩散相关光谱技术和扩散光学光谱技术,在扩散相关光谱组织血流测量及扩散光学光谱组织血氧饱和度测量的基础上,利用高光谱成像仪可实现组织血流、组织血氧饱和度等多生理参数的二维成像。
详见下文描述:
一种基于高光谱成像的多生理参数检测装置及方法,所述装置包括:
(1)光源模块由近红外波段的长相干激光器组成,激光器采用光纤耦合方式输出,激光器所产生的近红外光经n-1光源光纤传输后照射至被测组织表面。其中,激光器波长可采用近红外波段不同的波长;激光器数目与光源光纤输入端数目相同,均为n。
(2)探测模块为高光谱成像仪,用于实现经光源照射后被测组织散射光强的探测。具体而言,光源光谱经被测组织散射后的光强由高光谱成像仪测得,以非接触式扫描采集不同波长下不同像元处的光强;在完成一次成像区域的扫描后,继续下一次扫描,以连续检测的方式实现被测组织光强在不同时间点下的测量。因此,高光谱成像仪可以获得被测组织成像区域内不同像元在不同波长下随时间变化的光强数据矩阵,为后续上位机进行数据分析处理做准备。
(3)上位机模块为计算机,由于需处理高光谱成像仪获得的近红外光谱光强数据矩阵,数据量大,需用较高计算能力的工作站完成。首先,对所获得的光强数据矩阵进行初步的预处理,基于扩散相关光谱和扩散光学光谱技术在光强数据矩阵的基础上计算出每个像元处组织血流变化和组织血氧饱和度变化;然后,计算得出组织氧摄取分数、组织氧代谢率等其他相关生理参数变化,继而得到多生理参数的二维图像。
进一步地,本发明所述光源模块中的长相干激光器,采用光纤耦合输出,其功率大于50mw,相干长度为10m以上,波长范围为650nm-950nm,中心波长可选择为685nm、785nm或者830nm,经多模光纤传导。其中,激光器数目为n。
进一步地,本发明所述探测模块为高光谱成像仪,波长范围为400nm-1000nm,光谱分辨率为3.5nm,探测元件为ccd,像元数为1600×1200,帧频为33fps-247fps。高光谱成像仪测量时放置于被测组织表面上面,与被测组织不接触,两者距离依据被测组织成像区域大小及高光谱成像仪焦距等参数决定。
进一步地,本发明所述光源光纤为n到1的多模光纤,即光源输入端有n个光纤分别与n个激光器相连,在传输中将此n个光纤合并至一个端口输出,照射着被测组织表面。其中,所用多模光纤芯径为50μm、62.5μm、100μm或以上。
进一步地,本发明所述上位机基于多个不同波长下光强衰减程度的不同计算出组织血流指数、含氧血红蛋白浓度和脱氧血红蛋白浓度变化,在两参数的基础上,计算求得组织血流变化、组织血氧饱和度、组织氧摄取分数、组织氧代谢率,从而实现多生理参数的二维成像。
进一步地,本发明所述组织血流指数计算公式为:
式中,kt=δt/<i>为时间散斑对比度,δt为光强标准差,<i>为光强平均强度,<>代表时间上取平均。
进一步地,本发明所述组织血流与血流指数的关系如下:
bf=γbfi
其中,bf为组织血流,单位为ml·100ml-1·min-1;bfi为血流指数,单位为cm2/s;γ为比例常数,单位为(ml·100ml-1·min-1)/(cm2/s)。
进一步地,本发明所述血氧饱和度计算公式为:
式中,
进一步地,本发明所述组织氧代谢率和组织血氧饱和度、组织血流之间的关系为:
rmro2=roef×rbf
式中,r代表相对变化量,即rmro2为相对氧代谢率,roef为相对氧摄取分数,rbf为相对血流。
有益效果
本发明提供一种基于高光谱成像的多生理参数检测装置及方法,借助多个波长的激光器将近红外波段光源照射至被测组织表面,利用高光谱成像仪以非接触式扫描获取被测组织成像区域内多个波长的光强变化,并基于扩散相关光谱和扩散光学光谱在光强数据矩阵的基础上计算出每个像元的组织血流变化和组织血氧饱和度变化,从而实现多生理参数的二维成像。此外,本装置的测量探头为高光谱成像仪,无需与被测组织接触即可完成不同位置点处的测量,且可完成多个波长下光强变化的测量,不仅有利于提高组织血流变化和组织血氧饱和度变化的检测精度,而且有助于测量波长的优选。特别注意的是,本发明中不涉及光开关,不需要通过光开关完成光路的切换即可实现多生理参数的二维成像,易于装置的轻量化、小型号,为向便携式、穿戴式的装置转变奠定了基础。
附图说明
图1为基于高光谱成像的多生理参数检测装置系统示意图;
图2为高光谱成像仪所测得光强数据矩阵示意图;
附图中,各标号所代表的部件列表如下:
1:激光器(685nm)2:激光器(785nm)
3:激光器(830nm)4:n-1光源光纤
5:被测组织6:高光谱成像仪
7:电缆8:计算机
具体实施方式
为使本发明的目的、技术方案和优点更加清楚,以下结合具体实施例,并参照附图,对本发明实施方式作进一步地详细描述。
本发明提供一种基于高光谱成像的多生理参数检测装置,图1展示了本发明所述的基于高光谱成像的多生理参数检测装置系统框图,该装置包括:
激光器(1),(2),(3),波长可在650nm-950nm之间进行选择,相干长度大于10m,功率大于50mw。本公开实施例中列举了激光器的中心波长分别为685nm、785nm和830nm,可根据实际需求选择其他波长,如808nm等近红外波段的波长。
n-1光源光纤(4)为多模光纤,芯径为50μm、62.5μm、100μm或以上。该光纤输入端为n个光纤,分别与n个激光器相连,在传输中将此n个光纤合并至一个端口(即,光纤探头)输出,照射着被测组织表面。
被测组织(5),为被测量的生物组织体,例如脑部、乳腺、骨骼肌等人体部位,但不局限于上述组织。
高光谱成像仪(6),波长范围为400nm-1000nm,光谱分辨率为3.5nm,探测元件为ccd,像元数为1600×1200,帧频为33fps-247fps。高光谱成像仪测量时放置于被测组织表面上面,与被测组织不接触,两者距离依据被测组织成像区域大小及高光谱成像仪焦距等参数决定。
电缆(7),用于数据传输。
计算机(8),在对所获得的光强数据矩阵进行预处理后,基于扩散相关光谱和扩散光学光谱在光强数据矩阵的基础上计算出每个像元的组织血流变化和组织血氧饱和度变化,然后计算得出组织氧摄取分数、组织氧代谢率等其他相关生理参数变化,继而得到多生理参数的二维图像并显示。
进一步,本发明还提供一种基于高光谱成像的多生理参数检测方法,利用所述装置可完成对多生理参数变化的检测。具体步骤如下:
步骤一:将n-1光源光纤的光纤探头固定于被测组织表面,光源光纤的n个输入端分别与n个激光器相连;将高光谱成像仪放置在被测组织表面上方,并不与被测组织接触,依据成像区域面积和高光谱成像仪的焦距等参数调制确定两者的间距。
步骤二:待第一步骤中光纤探头和高光谱成像仪均固定完毕后,打开激光器和高光谱成像仪,近红外光谱经光源光纤传导照射至所被测组织所需的位置点处,高光谱成像仪对被测组织经光源照射后所散射的光强变化进行探测。首先,通过空间扫描获得被测组织的空间信息和光谱信息,即成像区域内各个像元信息及每个像元下多个波长的光强;然后,采用连续测量的方式完成上述信息随时间变化的测量,即测得每个像元不同波长下光强随时间的变化。具体如图2所示,图2中三维坐标轴显示的是高光谱成像仪所测得光强数据矩阵示意图,其中,x轴代表空间水平方位、y轴代表空间垂直方位、时间轴即采样时间。由此可以看出,不同空间位置点处多个波长的光强数据随时间的变化。每个像元同时也包含有多个波长的信息,其所含波长数目与激光器光源的波长数目一致,示意图中显示了本公开实施例中所采用的685nm、785nm和830nm的波长。
步骤三:计算机对步骤二传输的光强信号进行分析处理,推导得出不同像元处的组织血流指数、含氧血红蛋白浓度和脱氧血红蛋白浓度变化,计算组织血氧饱和度、组织氧摄取分数、组织氧代谢率等其他相关生理参数变化,继而得到多生理参数的二维图像并显示。
进一步,本发明所述一种基于高光谱成像的多生理参数检测装置及方法,组织血流、组织血氧饱和度、组织氧摄取分数和组织氧代谢率的具体计算过程如下:
关于组织血流指数的计算,前文已经介绍过其计算公式为:
式中,kt=δt/<i>为时间散斑对比度,δt为光强标准差,<i>为光强平均强度,<>代表时间上取平均。
本实施例中激光器的中心波长分别为685nm、785nm和830nm,计算组织血流指数时,可以选取任意波长下的光强进行计算,也可以分别计算三个波长下的组织血流指数,然后取平均做为最终的组织血流指数。
为了计算相对组织氧代谢率(rmro2),此处先计算组织血流指数(bfi)和相对组织血流(relativebloodflow,rbf)
组织血流(bf)与组织血流指数(bfi)的关系如下:
bf=γbfi
其中,bf为血流,单位为ml·100ml-1·min-1;bfi为血流指数,单位为cm2/s;γ为比例常数,单位为(ml·100ml-1·min-1)/(cm2/s)。
相对组织血流(relativebloodflow,rbf)的计算公式如下:
其中,bf0与bfi0分别代表初始时刻的血流和血流指数。因此,可由组织血流指数的变化即可求得组织血流变化。
依据修正的朗伯比尔定律,含氧血红蛋白浓度和脱氧血红蛋白浓度变化计算公式如下:
其中,
本实施例中激光器的中心波长分别为685nm、785nm和830nm,任意选取两种波长计算含氧血红蛋白浓度和脱氧血红蛋白浓度变化。此外也可以,分别利用685nm和785nm,785nm和830nm,以及685nm和830nm计算三组含氧血红蛋白浓度和脱氧血红蛋白浓度变化,然后将其求平均即为最终采用的含氧血红蛋白浓度和脱氧血红蛋白浓度变化。
组织血氧饱和度的计算公式
可转换为:
式中,
关于组织氧摄取分数的计算,其相对变化roef为:
式中,sao2为动脉血氧饱和度,sao2(0)和sao2(t)分别代表初始时刻(即t=0时)和t时刻的动脉血氧饱和度,sto2(0)和sto2(t)分别代表初始时刻(即t=0时)和t时刻的组织血氧饱和度。通常情况下,可假设:sao2=1,因此,相对氧摄取分数roef可表示为:
关于组织氧代谢率的计算,前文已经介绍过组织氧代谢率和组织血氧饱和度、组织血流之间的关系为:
rmro2=roef×rbf
式中,r代表相对变化量,即rmro2为相对氧代谢率,roef为相对氧摄取分数,rbf为相对血流。
那么,可得相对组织氧代谢率(rmro2)为:
式中,sto2(0)和sto2(t)分别代表初始时刻(即t=0时)和t时刻的组织血氧饱和度,rbf为相对血流。
最后所应说明的是,虽然本发明参照当前的较佳实施方式进行了描述,但本领域的技术人员应能理解,上述较佳实施方式仅用来说明本发明,并非用来限定本发明的保护范围,任何在本发明的精神和原则范围之内,所做的任何修饰、等效替换、改进等,均应包含在本发明的群里保护范围之内。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询



 商标分类
商标分类  商标转让
商标转让 



