复合材料及生物体植入物的制作方法
 2021-01-08 11:01:25|
2021-01-08 11:01:25| 267|
267| 起点商标网
起点商标网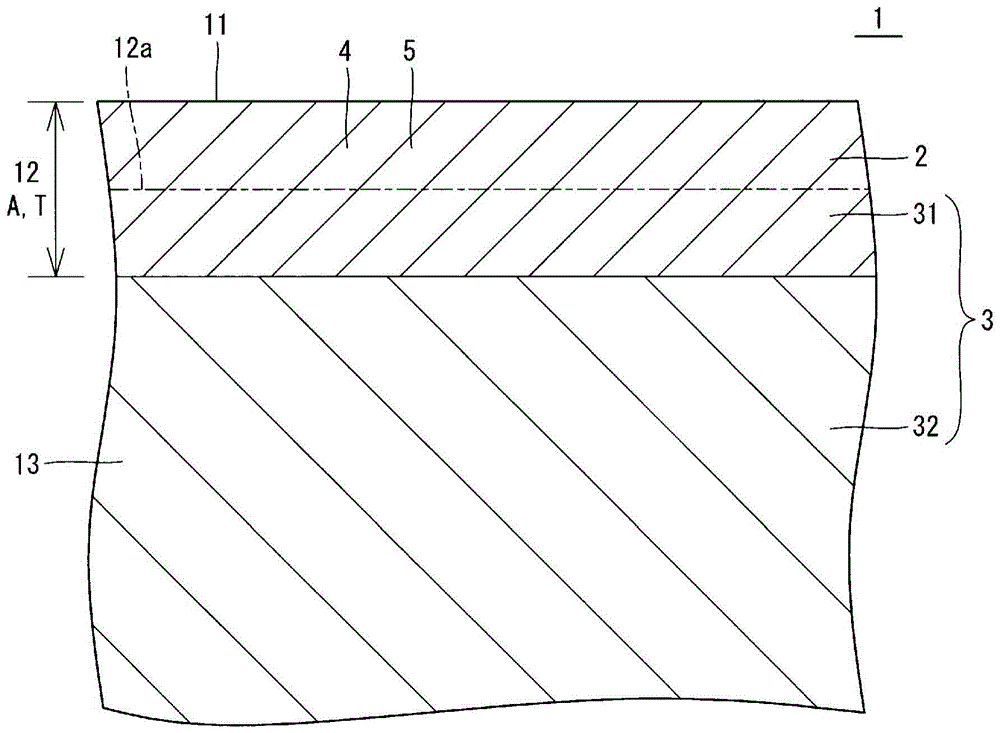
本公开涉及复合材料及生物体植入物(implant)。
背景技术:
已知有在表面注入了氟离子的金属材料(例如,参照专利文献1和非专利文献1)。
现有技术文献
专利文献
专利文献1:日本专利第4568396号公报
非专利文献
非专利文献1:m.yoshinari,y.oda,t.kato,k.okuda,“influenceofsurfacemodificationstotitaniumonantibacterialactivityinvitro”,biomaterials,2001,22,p.2043-2048
技术实现要素:
一实施方式的复合材料具有钛氟化物的晶相和钛的金属晶相。钛氟化物的晶相存在于在深度方向上远离表面的位置的第一区域。
一实施方式的生物体植入物包含一实施方式的复合材料。
附图说明
图1是表示一实施方式的复合材料的示意图。
图2是一实施方式的生物体植入物的一个例子。
图3是表示实施例中的氟浓度的测定结果的图表。
图4是表示实施例和比较例中的硬度的测定结果的图表。
具体实施方式
<复合材料>
以下,使用附图对一实施方式的复合材料进行详细说明。但是,为了便于说明,以下参照的图仅将说明实施方式所需的构成简化表示。因此,一实施方式的复合材料可以具备在所参照的图中未示出的任意构成。另外,图中的构成的尺寸并不忠实地表示实际的构成的尺寸和尺寸比率等。这些点在后述的生物体植入物中也是同样。
图1是表示一实施方式的复合材料的示意图。在图1中,放大示出复合材料的包含表面的部分的截面。
复合材料1含有钛(ti)和氟(f),具有钛氟化物的晶相2(以下,有时称为“晶相2”)和钛的金属晶相3(以下,有时称为“金属晶相3”)。在晶相2中,作为钛和氟的化合物的钛氟化物以晶体的状态存在。在金属晶相3中,钛以由金属键构成的晶体的状态存在。
如上所述,复合材料1含有氟,且具有晶相2,因此能够发挥由氟引起的抗菌性。另外,复合材料1具有大的硬度,因此能够发挥优异的耐磨损性等。作为复合材料1具有大的硬度的理由,推测为以下的理由。
钛氟化物中的钛与氟的结合是共价键。因此,晶相2作为移动金属晶相3的转变(日文:転移)的障碍物发挥作用。因此,如果复合材料1具有晶相2,则转变的移动所需的能量量变大,其结果是,复合材料1的硬度变大。应予说明,如果复合材料1中的氟浓度变大,则存在晶相2的比例变大的趋势。
作为钛氟化物,例如可举出tif(氟化钛)、tif2(二氟化钛)、tif3(三氟化钛)、tif4(四氟化钛)、tiof(氧氟化钛)、tiof2(氧二氟化钛)或f-tio2(氟掺杂氧化钛)等。钛氟化物可以为tiof2。晶相2可以具有ti-f-ti键(共价键)。
作为晶体结构的测定方法,例如可举出透射型电子显微镜(transmissionelectronmicroscope:以下,有时称为“tem”)、x射线衍射(x-raydiffraction:以下,有时称为“xrd”)或x射线光电子能谱分析法(x-rayphotoelectronspectroscopy:以下,有时称为“xps”)等。
复合材料1可以具备包含复合材料1的表面11且从表面11起在深度方向上具有规定厚度的区域(第一区域)12。另外,第一区域12为钛和氟的复合相。应予说明,第一区域12的氟浓度可以为1ppm以上。
第一区域12的厚度t例如为30~800nm。应予说明,在使用“~”表示数值范围时,只要没有特别说明,则分别包含下限和上限的数值。例如,在数值范围为30~800nm时,下限表示30nm以上,上限表示800nm以下。
晶相2可以位于第一区域12内。在满足这样的构成时,由于晶相2位于表面11的附近,所以由钛氟化物的氟引起的抗菌性提高,并且能够增大表面11及其附近的硬度。
晶相2可以位于距离表面11为深度20~200nm的区域。深度以表面11为基准进行判断即可。
金属晶相3可以具有包含氟的第一相31(含氟相)。换言之,金属晶相3可以具有在钛的晶格中含有氟的第一相31。在第一相31中,可以在钛的晶格中导入氟作为侵入型元素。如果金属晶相3具有第一相31,则能够进一步增大复合材料1的硬度。作为其理由,推测为以下的理由。
在第一相31中,氟原子侵入到由金属键构成的钛的晶格中的空间内。由此,钛的晶体产生与侵入的氟原子的大小相对应的晶格应变。钛的晶格的变形是由作为晶格缺陷的转变的移动而引起的。如果钛的晶格因氟原子的侵入而发生应变,则转变的迁移率降低,其结果是,复合材料1的硬度变大。因此,如果金属晶相3具有第一相31,则除了晶相2以外,第一相31也有助于复合材料1的硬度,因此能够进一步增大复合材料1的硬度。另外,如果减小复合材料1中的氟浓度,则存在第一相31的比例变大的趋势。
第一相31可以位于第一区域12内。在满足这样的构成时,由于第一相31位于表面11的附近,所以能够增大表面11及其附近的硬度。另外,第一相31所处的第一区域12与晶相2所处的第一区域12相同。这一点在后述的第二相32所处的第一区域12、氟浓度的最大值所处的第一区域12和硬度的最大值所处的第一区域12中也是同样。即,各构成的说明中的第一区域12均彼此相同。
金属晶相3还可以具有位于比第一相31更靠内侧的位置的不包含氟的第二相32(非含氟相)。在满足这样的构成时,包含位于比第二相32更靠表面11侧的位置的第一相31的部位不易损伤。具体而言,第二相32由于不包含氟,所以具有比第一相31高的韧性。因此,在冲击施加于表面11时,能够通过具有相对高的韧性的第二相32来缓和冲击。其结果是,包含位于比第二相32更靠表面11侧的位置的第一相31的部位不易损伤。
应予说明,第二相32位于比第一相31更靠内侧的位置是指第二相32位于比第一相31更远离表面11的位置。内侧是指相对于表面11而言的复合材料1的里面。换言之,内侧是指在复合材料1中深度变大的方向。另外,不包含氟是指实质上不包含氟,实质上不受氟的影响的状态。具体而言,在氟浓度小于1ppm时,可以判断为不含氟。
第二相32也可以位于比第一区域12更靠内侧的位置。在满足这样的构成时,由于具有相对高的韧性的第二相32,所以位于比第二相32更靠表面11侧的位置的第一区域12不易损伤。
复合材料1还可以具备位于比第一区域12更靠内侧的位置的区域(第二区域)13。第二区域只要是含有钛且不包含氟的区域即可。另外,第二相32也可以位于第二区域内。第二区域13可以与第一区域12接触。即,第一区域12和第二区域13可以是复合材料1中连续的区域。
金属晶相3例如可以包含钛系金属。作为钛系金属,例如可举出纯钛或钛合金等。作为纯钛,例如可举出母相为钛的c.p.2种钛等工业用纯钛。钛合金是母相为钛的合金,例如可举出ti-6al(铝)-4v(钒)、ti-15mo(钼)-5zr(锆)-3al、ti-nb(铌)、ti-6al-7nb、ti-6al-2nb-1ta(钽)、ti-30zr-mo、ni(镍)-ti、ti-3al-2.5v、ti-10v-2fe(铁)-3al或ti-15v-3cr(铬)-3al-3sn(锡)等。
复合材料1还可以具有包含钛和氟的非晶相4(amorphousphase)。在满足这样的构成时,由于非晶相4的高韧性,所以复合材料1不易损伤。
非晶相4可以位于第一区域12内。在满足这样的构成时,由于非晶相4的高韧性,所以第一区域12不易损伤。
复合材料1可以进一步具有含有非晶相4、晶相2和金属晶相3(第一相31)的混合相5。在一实施方式中,混合相5位于第一区域12内。在混合相5中,多个非晶相4(日文:非結晶相4)、晶相2和金属晶相3混合存在。此时,各相的材料特性各不相同,但第一区域12中的复合材料1的材料特性成为与各相的比例相应的特性。具体而言,是将所含有的各相的材料特性平均后的特性,或者是与其相近的特性。即,复合材料1通过含有各相作为混合相5,从而能够减少第一区域中材料特性不同的部分。因此,复合材料1通过具有混合相5,从而能够降低材料从第一区域12局部剥离的可能性。即,能够提高复合材料1的稳定性。
在复合材料1中,氟浓度可以在比表面11靠近内侧的位置显示最大值(参照图3)。在满足这样的构成时,在因磨损等而新的表面11露出时,具有相对大的氟浓度的表面11容易露出,因此容易长期发挥抗菌性。
氟浓度可以随着从表面11朝向内侧而变大并达到最大值(参照图3)。换言之,随着深度变大,氟浓度也可以变大并达到最大值。在满足这样的构成时,在因磨损等而新的表面11露出时,具有相对大的氟浓度的表面11露出,因此能够长期发挥抗菌性。另外,通过调整氟浓度的分布,复合材料1能够调整发挥抗菌性能的时期。
氟浓度的最大值可以位于第一区域12内。在满足这样的构成时,由于氟浓度的最大值位于表面11的附近,所以抗菌性提高。
氟浓度的最大值可以位于比第一区域12的厚度方向a的中央部12a更靠表面11侧的位置(参照图1和图3)。在满足这样的构成时,由于氟浓度的最大值位于表面11的附近,所以抗菌性提高。
在此,氟浓度中的浓度是指原子浓度。在一实施方式中,氟浓度是指相对于每单位体积的钛原子的理想原子数与氟原子数之和的每单位体积的氟原子数。作为氟浓度的测定方法,例如可举出二次离子质谱分析法(secondaryionmassspectrometry:以下,有时称为“sims”)或xps等。sims适合氟浓度较小时。xps适合氟浓度较大时。
氟浓度的最大值例如为10~80原子%。从表面11起深度小于5nm的区域中的氟浓度例如为0.5~20原子%。深度5nm以上且小于20nm的区域中的氟浓度例如为2~30原子%。深度20nm以上且小于50nm的区域中的氟浓度例如为5~80原子%。深度50nm以上且100nm以下的区域中的氟浓度例如为2~80原子%。
复合材料1的硬度可以在比表面11更靠内侧的位置显示最大值(参照图4)。在满足这样的构成时,在因磨损等而新的表面11露出时,具有相对大的硬度的表面11容易露出,因此表面11长期具有大的硬度的可能性提高。应予说明,硬度的说明中的表面11与上述氟浓度的说明中的表面11相同。
硬度可以随着从表面11朝向内侧而变大并达到最大值(参照图4)。换言之,随着深度变大,硬度也可以变大并达到最大值。在满足这样的构成时,在因磨损等而新的表面11露出时,具有相对大的硬度的表面11露出,因此表面11将长期具有大的硬度。
另外,硬度也可以在随着从表面11朝向内侧而变大并达到最大值之后,进一步随着朝向内侧而变小(参照图4)。换言之,复合材料1构成为在内部硬度的变化变得缓慢。据此,与复合材料1内部的硬度急剧变化的构成相比,能够降低局部应力的产生,因此能够降低第一区域12剥离的可能性。
硬度的最大值可以位于第一区域12内。在满足这样的构成时,由于硬度的最大值位于表面11的附近,所以能够增大表面11及其附近的硬度。
硬度的最大值也可以位于比第一区域12的厚度方向a的中央部12a更靠表面11侧的位置(参照图1和图4)。在满足这样的构成时,由于硬度的最大值位于表面11的附近,所以能够增大表面11及其附近的硬度。
硬度的最大值也可以位于比氟浓度的最大值更靠近表面11的位置(参照图3和图4)。在满足这样的构成时,位于比氟浓度的最大值更靠近表面11的位置的部位的硬度相对变大。因此,位于比氟浓度的最大值更靠近表面11的位置的部位不易因磨损等而损伤,能够长期发挥抗菌性。
硬度例如为3~10gpa。硬度的最大值例如为5~10gpa。硬度是压入硬度,表示表面11受到变形时的变形难度。硬度根据将压头压入表面11时的压入深度和所需的力来计算。作为具体的硬度的测定方法,例如可举出纳米压入法(依据iso14577)等。
复合材料1还可以具备位于最外表面的氧化覆膜(未图示)。此时,复合材料1的表面11由氧化覆膜的表面构成。氧化覆膜的厚度例如为2~5nm。作为氧化覆膜的组成,例如可举出tio2(二氧化钛)等。氧化覆膜可以含有氟。氧化覆膜例如通过氧化处理等形成。作为氧化处理,例如可举出自然氧化、热处理、氧等离子体处理、在酸溶液中的浸渍或阳极氧化等。
在复合材料1中,钛的含量可以多于氟的含量。另外,复合材料1可以含有钛作为主成分。主成分是指复合材料1中以质量比计含有最多的成分。
<复合材料的制造方法>
接下来,以得到上述复合材料1的情况为例,对一实施方式的复合材料的制造方法进行详细说明。
首先,准备钛系金属。钛系金属可以根据需要进行清洗。清洗例如可以使用有机溶剂等。作为有机溶剂,例如可举出乙醇或丙酮等。例示的有机溶剂可以混合使用。清洗也可以通过施加超声波来进行。清洗后的钛系金属例如可以在干燥器内进行真空干燥。
接下来,向钛系金属的表面注入氟离子,得到复合材料1。作为氟离子的注入条件,例如可举出以下的条件。
注入能量:大于30kev且80kev以下
注入剂量:1×1016~5×1017原子/cm2(atom/cm2)
所得到的复合材料1可以根据需要进行清洗。清洗的条件可举出与上述钛系金属中例示的条件相同的条件。清洗后的复合材料1例如可以在干燥器内进行真空干燥。
应予说明,在上述的实施方式中,以通过氟离子的注入而得到复合材料1的情况为例进行了说明,但作为复合材料1的制造方法,并不限定于此,只要能够得到复合材料1,则可以采用氟离子的注入以外的其他方法。
<生物体植入物>
接下来,使用附图对一实施方式的生物体植入物进行详细说明。应予说明,在本实施方式中,作为生物体植入物的例子,对牙科植入物进行说明。
图2是表示一实施方式的牙科植入物的外观的示意图。
牙科植入物100具备固定物101、安装于固定物101的端部的桥基102以及通过桥基102安装于固定物101的人工牙103。
牙科植入物100的固定物101、桥基102和人工牙103分别包含复合材料1。如上所述,由于复合材料1具有抗菌性且具有大的硬度,所以牙科植入物100能够抑制细菌的增殖,能够对刷牙、反复使用或清洗等发挥优异的耐久性。
在此,固定物101、桥基102和人工牙103可以分别仅由复合材料1构成。另外,它们也可以一部分由复合材料1构成,其余的部位由复合材料1以外的材料构成。另外,固定物101、桥基102和人工牙103中的至少1个包含复合材料1,其他构件包含复合材料1以外的材料即可。根据如上所述的构成,可抑制植入物表面的细菌的增殖。例如,由于固定物101和桥基102在缺氧的环境中使用,所以能够期待抑制厌氧性细菌的增殖。另外,例如,由于人工牙103在口腔内露出并暴露于空气中,所以能够期待抑制兼性厌氧性细菌、需氧细菌的增殖。因此,复合材料1只要根据想要抑制增殖的菌种、所需的抗菌性能而适当地用于固定物101、桥基102和人工牙103即可。
复合材料1中的第一区域12例如位于牙科植入物100中的有可能与细菌接触的部位、有可能磨损的部位等即可。例如,牙科植入物100只要构成为第一区域12位于固定物101、桥基102和人工牙103的表面即可。另外,例如,牙科植入物100只要构成为第一区域12位于固定物101、桥基102和人工牙103的各接合部位即可。这一点在后述的其他生物体植入物、生物体植入物以外的其他构件中也是同样。
以上,对本公开的一实施方式进行了例示,但本公开不限于上述的实施方式,只要不脱离本公开的主旨,则当然可以采用任意的方式。
例如,在上述的实施方式中,以生物体植入物为牙科植入物的情况为例进行了说明,但生物体植入物并不限于此。例如,生物体植入物只要是钛等生物体用金属制的植入物即可。作为其他生物体植入物,例如可举出股骨柄或髋臼杯等人工关节和脊椎固定器械等脊椎外科植入物等。
另外,在上述的实施方式中,以复合材料1为生物体植入物用的情况为例进行了说明,但复合材料1并不限于生物体植入物用。即,复合材料1只要用作需要抗菌性和高硬度性的构件的材料即可。作为其他构件,例如可举出牙科矫正线、手术器具、注射针、眼镜的框架、餐具类、食品厂的生产线、水壶的饮用口、菜刀、厕所、washlet(注册商标)、水龙头或上下水道管等。
以下,列举实施例详细地说明本公开。应予说明,本公开不受以下的实施例限定。
实施例
[实施例1和实施例2]
<复合材料的制作>
首先,准备以下所示的试验片。
试验片:由c.p.2种钛构成的厚度1mm的纯钛
将上述的试验片成形为直径14mm、厚度1mm的圆盘状后,用乙醇和丙酮进行超声波清洗,在干燥器内使其真空干燥。然后,在不同的条件下向试验片的表面注入氟离子,得到实施例1和实施例2的复合材料1。
氟离子的注入条件如下。
(实施例1)
注入能量:40kev
注入剂量:5×1017原子/cm2
(实施例2)
注入能量:40kev
注入剂量:5×1016原子/cm2
所得到的复合材料1用乙醇和丙酮进行超声波清洗,在干燥器内进行真空干燥后,用于评价。
[比较例1]
将与实施例1和实施例2相同且未注入氟离子的试验片作为比较例1。
<评价>
针对实施例1和实施例2的复合材料1测定氟浓度、硬度和晶体结构。另外,针对实施例1的复合材料1测定抗菌性。针对比较例1测定硬度和抗菌性。
图3是表示实施例1和实施例2中的氟浓度的测定结果的图表。
(氟浓度)
实施例1和实施例2的氟浓度通过xps和sims测定。具体而言,氟浓度较大且超过sims的测定范围的区域通过xps求出氟浓度,除此以外的区域通过sims求出氟浓度。具体而言,至氟浓度10原子%为止的范围通过sims求出氟浓度。另外,氟浓度为10原子%以上的范围通过xps求出氟浓度。在此,xps的测定在深度0~200nm处实施,sims的测定在深度0~900nm处实施。应予说明,在图3中仅示出深度0~200nm的测定结果。另外,在图3中,深度0nm表示复合材料1的表面11。这一点在后述的图4中也是同样。xps和sims各自的测定条件如下。
(xps的测定条件)
分析装置:ulvac-phi公司制的x射线光电子能谱分析装置“phiquanteraii”
x射线源:单色alkα
溅射离子:ar+
加速电压:4kv
(sims的测定条件)
分析装置:ulvac-phi公司制的二次离子质谱分析装置“d-sims6650”
一次离子源(日文:イオン種):cs+
二次离子极性:负性(negative)
加速电压:2kv
射束电流:25na
电荷补偿:无
光栅尺寸:400μm
根据测定结果可以明确,在实施例1中,氟浓度的最大值位于深度90nm处。实施例1的氟浓度的最大值为63原子%。在实施例2中,可以明确氟浓度的最大值位于深度46nm处。实施例2的氟浓度的最大值为11原子%。
将从深度0nm(表面11)至氟浓度成为1ppm的深度作为第一区域12,测定其厚度t。测定结果如下。
(第一区域的厚度t)
实施例1:740nm
实施例2:390nm
图4是表示实施例1、实施例2和比较例1中的硬度的测定结果的图表。
(硬度)
硬度通过纳米压入法(依据iso14577)测定。在此,测定在深度0~1000nm处实施。应予说明,在图4中仅示出深度0~500nm的测定结果。
硬度的测定条件如下。
测定装置:mtssystems公司制的“nanoindenterxp”
测定模式:连续刚性测定
压入深度:最大1000nm
硬度单位:维氏硬度
根据测定结果可以明确,在实施例1中,硬度的最大值位于深度70nm处。实施例1的硬度的最大值为5gpa。在实施例2中可以明确,硬度的最大值位于深度20nm处。实施例2的硬度的最大值为7gpa。
(晶体结构)
晶体结构通过tem、xrd和xps进行了评价。应予说明,在tem、xrd和xps的各测定中,根据上述的第一区域12的厚度t判断第一区域12,将位于比第一区域12更靠内侧的位置的区域作为第二区域。
tem的测定条件如下。
分析装置:fei公司制的透射型电子显微镜“talosf200x”
加速电压:200kv
射束电流值:150pa
测定位置:将复合材料1沿厚度方向切断的截面
xrd的测定条件如下。
分析装置:panalytical公司制的“x’pertpro-mrd”
管球:cukα
入射角度:0.5°
测定范围:10~120°
xps的测定条件与上述的氟浓度相同。
首先,实施基于tem的截面观察。衍射图案参照国际衍射数据中心(internationalcentrefordiffractiondata,icdd)提供的数据库(tiof2:icddno.00-008-0060,钛α相:icddno.00-044-1294)。观察的结果是,在实施例1和实施例2中,均在第一区域12内得到归属于tiof2(晶相2)的衍射图案,在第二区域内得到钛α相的衍射图案(第二相32)。
另外,在实施例1和实施例2中,均在第一区域12内确认到第一相31。在实施例1中,确认到晶相2多于第一相31。在实施例2中,确认到第一相31多于晶相2。另外,在实施例1中,在第一区域12内确认到非晶相4和混合相5。
接下来,实施基于xrd的测定。衍射图案参照icdd提供的jcpds。测定的结果是,在第一区域12中确认到与第二区域不同的晶体结构。
然后,实施基于xps的测定。对于峰的归属,在表1中示出。测定的结果是,在实施例1和实施例2中,均得到了归属于tif3、tif4和f-tio2的峰。另外,在实施例1中,得到了归属于ti-f-ti键的峰,认为该峰是由钛氟化物的晶体引起的。除此以外,图1所示的状态得到了确认。
[表1]
(抗菌性)
抗菌性通过使用了金黄色葡萄球菌的膜密合试验(依据jisz2801)来测定。
测定结果如下。
附着活菌数(cfus)
实施例1:<10(检测限以下)
比较例1:17667
测定的结果是,在实施例1中,附着活菌数为检测限以下。另外,实施例1的抗菌活性值为3.2。因此,可以明确实施例1具有抗菌效果。
附图标记说明
1···复合材料
2···钛氟化物的晶相
3···钛的金属晶相
31···第一相
32···第二相
4···非晶相
5···混合相
11···表面
12···第一区域
12a···中央部
t···厚度
a···厚度方向
13···第二区域
100···牙科植入物
101···固定物
102···桥基
103···人工牙
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询



 商标分类
商标分类  商标转让
商标转让 



