布鲁顿酪氨酸激酶小分子抑制剂及其应用的制作方法
 2021-01-08 11:01:15|
2021-01-08 11:01:15| 285|
285| 起点商标网
起点商标网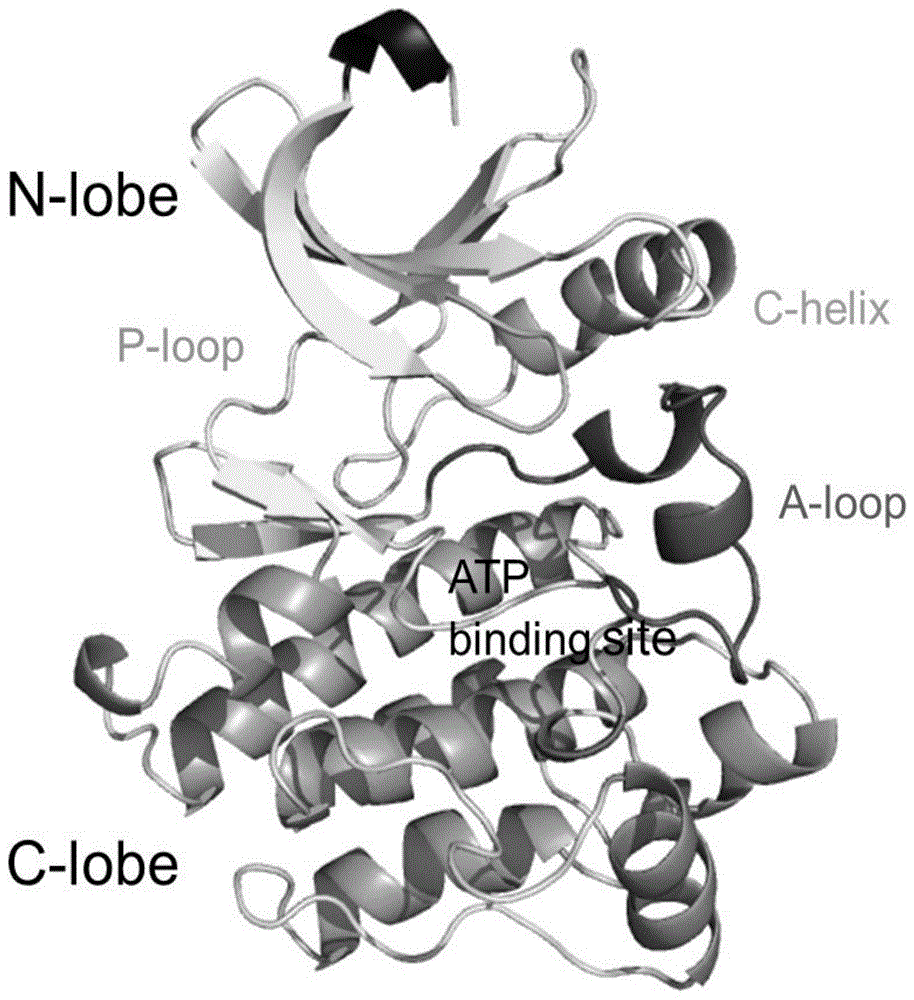
本发明属医药化学技术领域,具体涉及以布鲁顿酪氨酸激酶(brutontyrosinekinase,btk)蛋白为靶点抑制人btk激酶活性的先导化合物及其药用盐在制备btk相关的病症药物中的应用。
背景技术:
btk最初被鉴定为人类x连锁无球蛋白血症(xla)中的缺陷蛋白,是细胞质酪氨酸激酶的src相关的tec家族的成员并在b细胞的发育和激活中起着至关重要的作用。btk主要在造血细胞例如b细胞,肥大细胞和巨噬细胞中表达,但在t细胞,自然杀伤细胞和血浆中并不常见。
btk抑制剂因其在癌症和自身免疫疾病如b细胞恶性肿瘤中的治疗潜力而备受关注。2013年,依鲁替尼(ibrutinib)被fda批准为btk的首创新抑制剂用于治疗套细胞淋巴瘤(mcl)和慢性淋巴细胞白血病(cll),现在处于单一或联合治疗其他适应症的临床评估中。
目前的btk小分子抑制剂分为不可逆和可逆的。不可逆抑制剂通过迈克尔加成与btk中atp结合位点中的c481共价结合,从而产生很好地抑制作用。需要注意的是,大多数处于临床阶段的btk抑制剂是不可逆的。不可逆抑制剂具有强大的功效,但是,近几年,由于广泛使用ibrutinib,与ibrutinib结合的c481被其他的氨基酸所替换,这将改变ibrutinib与btk的不可逆共价结合,降低ibrutinib对btk的亲和力,最终导致耐药性。因此,一个潜在的策略是开发不与c481相互作用的非共价抑制剂,以克服ibrutinib抗btkc481耐药突变。如最近的非共价抑制剂bms-986142(fenebrutinib)表现出令人鼓舞的疗效,目前处于ⅱ期临床研究,可能会为可逆btk抑制剂带来突破。因此,发现有效且安全的可逆抑制剂以及获得临床疗效仍是主要挑战。
随着计算机技术在药物研发领域的应用,计算机虚拟筛选为药物先导化合物的发现提供了一种快速、高效的筛选技术。该技术针对重要疾病特定靶标生物大分子三维结构,从现有小分子数据库中,搜寻与靶标结合较好的化合物,大大降低实验筛选化合物数量,缩短了研发周期。
技术实现要素:
本发明的目的在于提供靶向人btk蛋白的先导化合物及其药用盐在制备btk激酶抑制剂中的应用。其中所述的btk介导的疾病选自一下疾病中的至少一种:类风湿性关节炎、系统性红斑狼疮、银屑病、慢性淋巴细胞白血病和淋巴瘤。
本发明在对靶标btk蛋白的抑制剂结合口袋的研究基础上,筛选得到具有新结构实体的靶向btk蛋白的小分子抑制剂化合物ⅰ和化合物ⅱ,所述的靶向btk蛋白的小分子抑制剂为针对btk与atp结合位点的小分子结构的化合物。
本发明通过基于对接的虚拟筛选,通过lipinski’s五规则筛选、打分函数评分、结合自由能计算、对人btk蛋白激酶活性的抑制试验等多因素综合分析,最终得到了对btk有抑制活性的化合物ⅰ和化合物ⅱ。
本发明的化合物ⅰ和化合物ⅱ经实验证实,在体外有显著的抑制人btk激酶活性效果。本发明的化合物可进一步的结构优化,制备治疗btk蛋白相关疾病(包括类风湿性关节炎、系统性红斑狼疮、银屑病、慢性淋巴细胞白血病和淋巴瘤)的制剂或药物。
本发明通过三轮筛选出2个具有btk抑制活性的化合物;所述化合物具有如下特征:
化合物ⅰ
英文名称:
3-(2-((4-chlorophenethyl)amino)-2-oxoethyl)-4-methyl-2-oxo-2h-chromene-7,8-diyldiacetate.
化合物结构:
化合物ⅱ,
英文名称:
3-(3,4-dimethoxyphenyl)-n-(2-(yridin-2-yl)ethyl)-1h-pyrazole-5-carboxamide化合物结构:
表1显示了筛选得到的两个化合物的理化性质和btk激酶抑制活性数据。
表1
为了便于理解,以下将通过具体的附图和实施例对本发明的靶向人btk蛋白的化合物进行详细的描述。
附图说明
图1为btk激酶非活性状态的结构。
图2为gdc-0834与btk的结合模式图。
图3为化合物-ⅰ与btk的对接结合模式图。
图4为化合物-ⅱ与btk的对接结合模式图。
具体实施方式
实施例1
1、小分子化合物ⅰ和ⅱ的虚拟筛选方法
(1)蛋白准备
在蛋白数据库(https://www.rcsb.org/)中搜寻并获得btk的三维结构(pdbcode:5p9f),该结构为btk与其抑制剂gdc-0834的复合物;使用薛定谔软件包中maestro10.1(2015-01,version10.1,https://www.schrodinger.com/)的proteinpreparationwizard模块进行准备,其中,首先对蛋白进行加氢,并删除蛋白中的水分子、乙二醇、丙三醇,然后在opls_2005力场下对蛋白进行能量优化和最小化。
(2)配体准备
小分子结构在chemdiv数据库中获取,使用薛定谔软件包中maestro10.1的ligprep模块对配体进行优化,分别利用lipinski’s五规则,是否具有可反应基团,对化合物进行对接前筛选工作。
(3)格点生成
使用薛定谔软件以抑制剂gdc-0834为格点盒子的中心生成格点文件。
(4)基于分子对接的虚拟筛选
将准备的小分子配体与靶蛋白进行对接,首先使用薛定谔软件中maestro10.1里的glide的htvs(high-throughputvirtualscreening)模式进行初筛,并选取打分前10%的化合物用sp(standardprecision)模式进行复筛,然后根据打分选取前10%的化合物用xp(extraprecision)模式进行精筛,最后保留打分前4000个化合物,然后对这些分子用薛定谔软件包中canvas2.3模块进行k-meansclustering聚类,最后根据对接打分、能量打分、配体的结合构象对化合物进行挑选,并筛选出具有btk抑制活性的化合物。
2、激酶活性测试
化合物对布鲁顿酪氨酸激酶的抑制试验用酶联免疫方法(elisa)进行检测。将浓度为20μg/ml的底物肽(glu-tyr)4:1(sigma,stlouis,mo)包被到96孔酶标板内。在激酶反应缓冲液(50mmol/ltris-hcl,ph7.4,20mmol/lmgcl2,0.1mmol/lmncl2,1mmol/ldtt)加入酪氨酸激酶、dmso溶解的化合物和atp(终浓度为5μmol/l),37℃孵育1h。将抗酪氨酸磷酸化抗体py99(santacruzbiotechnology,santacruz,ca)加入96孔酶标板内,25℃孵育30min,用pbs洗板,加入辣根过氧化物酶(hrp)标记的二抗,25℃孵育30min,用pbs洗板。加入3,3',5,5'-四甲基联苯胺(tmb)避光显色15min,加入2m的h2so4终止显色。用酶标仪读取od450记作ac,不添加酪氨酸激酶的读数作为阳性对照a0,阴性对照用dmso替代化合物记作amax,并用graphpadprism6计算ic50。计算公式如下:
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询



 商标分类
商标分类  商标转让
商标转让 



