一种镁基微米马达及其制备方法和应用与流程
 2021-01-08 11:01:56|
2021-01-08 11:01:56| 249|
249| 起点商标网
起点商标网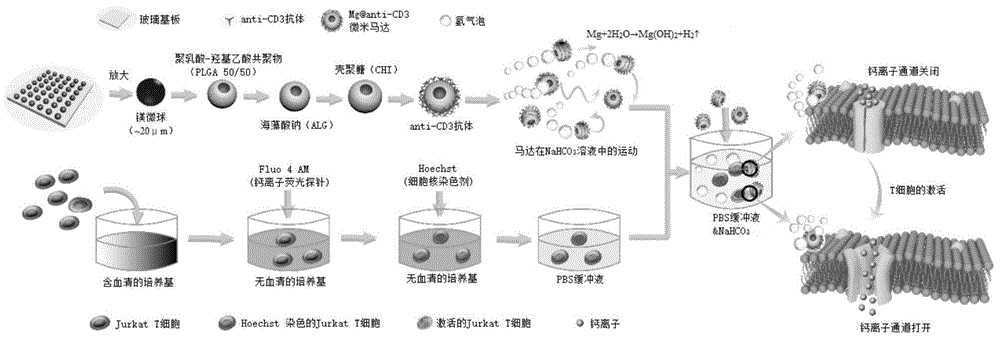
本发明涉及微米马达技术领域,尤其是涉及一种镁基微米马达及其制备方法和应用。
背景技术:
在过去十年中,自推进微纳米马达由于其固有的快速移动和高效的货物牵引能力而备受关注。这些小型化的设备被证明具有革命性的生物医学领域的能力,如按需给药、细胞运输和动态生物传感等,而双金属马达(如钯和金、钛和金等)最先被使用,它们的刚性以及非生物降解性阻碍了它们在生物领域的应用;另外,现有的微米马达中,有一些微米马达通过活性金属(如钾、钠、钙等)与水反应产生氢气在纯水中供电,活性金属-水反应剧烈产生的氢气泡,活性金属用于微纳米马达时不稳定且不可控,且易在表面形成了致密的钝化层;还有一些以h2o2、酸性和碱性溶液为燃料驱动的微米马达,这些微米马达在体内几乎不兼容,因为它们会导致腐蚀和强氧化,也阻碍了自驱动微米马达在复杂生物环境中的临场应用。因此,迫切需要开发一种具有良好生物相容性的微米马达,进一步开发微米马达在生物领域的应用。
技术实现要素:
本发明旨在至少解决现有技术中存在的技术问题之一。为此,本发明提出一种镁基微米马达及其制备方法和应用。
本发明的第一方面,提供一种镁基微米马达,包括镁微球,所述镁微球的表面上依次层叠覆设有聚乳酸-羟基乙酸共聚物层和可降解多孔水凝胶层;所述镁基微米马达上具有用于使所述镁微球连通外部环境的开口。
根据本发明实施例的镁基微米马达,至少具有如下有益效果:该镁基微米马达通过设置镁微球连通外部环境的开口,形成结构不对称的janus结构,可使镁(mg)微球与水反应产生氢气以形成推动力,以实现自推进运动,并在推进后可降解;且相对于钾、钠、钙等活性金属与水的反应,mg和h2o可以中等速度、连续稳定地产生氢气泡,运动速度可控,并且形成钝化层时,这种水作为推动微米马达运动过程中以适当的速度耗尽;此外,水作为推动微米马达的燃料,因其无毒性和丰富性而被视为具有吸引力的动力源,与h2o2、酸性和碱性溶液驱动的微米马达相比,水驱动微米马达在生物流体中具有更好的生物相容性;并且,mg在生物流体中具有良好的吸附性能,可应用于生物医学领域;且在人体中,mg2+离子是第四丰度的,是300多种酶的辅助因子,对组织和器官的正常功能至关重要。另外,基于镁基微米马达的janus结构,其悬浮能力较差,但其在水介质中的粘度低,在镁微球外表面设置聚乳酸-羟基乙酸共聚物(plga)层,可避免下层;且plga是由聚乙醇酸(pga)和聚乳酸(pla)组成的共聚物,在水中,plga可以通过酯键的水解降解,且这种共聚物在生物环境中比在水中降解得更快;plga层涂覆于镁微球表面,有效形成janus结构,为马达的运动提供必要条件。并且,通过可降解多孔水凝胶层的设置,其可本身具有吸附负载特性,其用于药物或功能性抗体等功能性物质,可丰富其功能,扩展其在生物领域应用。由上,该镁基微纳米马达所采用的材料具有生物可降解和生物相容性,在体外应用时,不会产生免疫排斥反应,不会对体系产生不利影响。
根据本发明的一些实施例,所述可降解多孔水凝胶层由海藻酸钠(alg)和壳聚糖(chi)复合制成。制备时,具体可先在聚乳酸-羟基乙酸共聚物(plga)层的表面覆设alg溶液,经干燥后在plga层上形成alg层,而后在alg层上覆设chi溶液,chi与alg形成可降解多孔水凝胶,干燥后形成可降解多孔水凝胶层。其中,plga易于吸附负电性物质,通过在plga层上先覆设alg层,层体之间粘结紧密,可提高结构的稳定牢固性;进而通过在alg层上覆设带正电的chi溶液,alg和chi可产生静电作用,形成可降解多孔水凝胶。
根据本发明的一些实施例,所述可降解多孔水凝胶层的表面负载有功能性物质,所述功能性物质包括药物或功能性抗体。通过在可降解多孔水凝胶层的表面负载以上功能性物质,可使其具有特定功能,进而可扩展其在生物领域的应用。
根据本发明的一些实施例,所述功能性物质和所述可降解多孔水凝胶层的表面具有静电引力作用。由于可降解多孔水凝胶层表面的多孔结构,其本身具备吸附负载特性,通过采用与可降解多孔水凝胶结构的表面具有相反电性的功能性物质,功能性物质与可降解多孔水凝胶层之间通过静电引力作用,可提高负载稳定性。
根据本发明的一些实施例,所述功能性物质为anti-cd3抗体或者anti-cd3抗体与anti-cd28抗体的组合。以上抗体具有负电性,可降解多孔水凝胶层的表面可设计为具有正电性,具体在采用海藻酸钠(alg)和壳聚糖(chi)复合可降解多孔水凝胶层时,可采用过量的chi,以使其表面带正电性。
具体可采用粒径为10~30μm的镁微球,镁微米马达上的开口一般设于所述镁基微米马达的一侧,以利于提升其推动性。
本发明的第二方面,提供本发明第一方面所提供的任一种镁基微米马达的制备方法,包括以下步骤:
s1、将镁微球分散设于基底上;
s2、在所述镁微球的表面涂覆聚乳酸-羟基乙酸共聚物(plga)溶液,经干燥在所述镁微球的表面形成聚乳酸-羟基乙酸共聚物层;
s3、在所述聚乳酸-羟基乙酸共聚物层上设置可降解多孔水凝胶层,得到镁基微米马达粗品;
s4、将所述镁基微米马达粗品从所述基底上剥离。
根据本发明的一些实施例,步骤s3具体包括:在所述聚乳酸-羟基乙酸共聚物层上涂覆海藻酸钠(alg)溶液,干燥后形成海藻酸钠层;再在所述海藻酸钠层的表面涂覆壳聚糖(chi)溶液,干燥后形成可降解多孔水凝胶层。alg溶液一般为alg水溶液,chi溶液为chi水溶液,alg溶液和chi溶液的涂覆可采用旋涂仪旋涂的方式,以利于涂层的快速干燥。
在镁微球的表面设置plga层,而后通过以上方式制备可降解多孔水凝胶层(alg/chi多孔水凝胶层),其中plga层的设置可有利于保证增加海藻酸钠层和壳聚糖形成水凝胶结构而不破坏janus结构,如果没有plga层,直接在镁微球上附着alg/chi多孔水凝胶层,由于在制备过程采用alg溶液和chi溶液,容易与镁微球未钝化层反应,消耗镁微球,对制成微米马达后的马达运动不利。
根据本发明的一些实施例,步骤s3中,在所述聚乳酸-羟基乙酸共聚物层上设置可降解多孔水凝胶层后,再在所述可降解多孔水凝胶层的表面负载功能性物质,所述功能性物质包括药物或功能性抗体。
根据本发明的一些实施例,还包括:步骤s5、将步骤s4剥离下来的微米马达粗品分散于水中,离心纯化。
另外,步骤s1中,所述聚乳酸-羟基乙酸共聚物溶液的溶剂为挥发性溶剂;优选地,所述挥发性溶剂选自乙酸乙酯、二氯甲烷、四氢呋喃、丙酮等中的至少一种。优选采用乙酸乙酯,其安全性高。
本发明的第二方面,提供本发明第一方面所提供的任一种镁基微米马达中,功能性抗体为anti-cd3抗体的镁基微米马达在制备t细胞活化药物上的应用。
附图说明
下面结合附图和实施例对本发明做进一步的说明,其中:
图1是本发明一实施例镁基微米马达的制备方法和用于激活t细胞的示意图;
图2是实施例1镁基微米马达和对比例1~3微米马达的sem图;
图3a是实施例1镁基微米马达多孔alg/chi水凝胶孔径尺寸分布图;
图3b是对比例1mg微球的粒径分布图;
图4是mg@anti-cd3微米马达/rhb的明场图、荧光场图和叠加图像;
图5是实施例1mg@anti-cd3微米马达在不同运动模式下的运动轨迹;
图6是mg@anti-cd3微米马达在运动过程中的速度分布和方向性测试结果;
图7是对比例2mg/plga微米马达在螺旋运动模式下的运动轨迹;
图8是mg/plga微米马达在运动过程中的速度分布和方向性测试结果
图9是anti-cd3浓度测试的标准曲线图;
图10是mg@anti-cd3微米马达激活jurkatt细胞的钙离子通道示意图;
图11是mg@anti-cd3微米马达和mg/plga/alg/chi微米马达分别刺激jurkatt细胞不同时间所测定明场图和荧光场图;
图12是采用荧光显微镜测得mg@anti-cd3微米马达和mg/plga/alg/chi微米马达不同时间内的荧光趋势图;
图13是采用流式细胞仪测得mg@anti-cd3微米马达和mg/plga/alg/chi微米马达不同时间内的荧光趋势图;
图14是mg微球、mg/plga微米马达、mg/plga/alg/chi微米马达和mg@anti-cd3微米马达对t细胞活性实验结果图。
具体实施方式
以下将结合实施例对本发明的构思及产生的技术效果进行清楚、完整地描述,以充分地理解本发明的目的、特征和效果。显然,所描述的实施例只是本发明的一部分实施例,而不是全部实施例,基于本发明的实施例,本领域的技术人员在不付出创造性劳动的前提下所获得的其他实施例,均属于本发明保护的范围。
本发明提供了一种镁基微米马达及其制备方法,该镁基微米马达可用于t细胞活化,图1示出了本发明一实施例镁基微米马达的制备方法和用于激活t细胞的示意图。下面对该镁基微米马达及其具体制备和应用进行具体说明。
(一)使用材料
~20μm(平均粒径)mg微球购自唐山威豪mg粉有限公司;聚乳酸-乙醇酸(plga50/50)由济南罡代港生物科技有限公司获得;海藻酸钠(alg)为200±20mpa.s;壳聚糖(chi)为壳聚糖西格玛·奥尔德里奇;anti-cd3从达科为生物科技有限公司购买;hoechstc1022和fluo4am(钙离子荧光探针)从碧云天公司购买;罗丹明ba81889(rhb)从innochem获得;从阿拉丁购买十二烷基磺酸钠(sds);jurkatt细胞由南方医科大学捐赠。
(二)镁基微米马达的合成
实施例1
首先用丙酮洗涤mg微球三次,然后用氮气流吹干。其次,将mg微球分散镀于玻璃基片上。然后,将溶于乙酸乙酯的1%聚乳酸-羟基乙酸共聚物(plga50/50)滴注在镀有mg微球的玻璃基片上,自然干燥;乙酸乙酯的快速挥发导致在mg微球表面形成均匀的plga涂层,同时,在mg微球与玻璃基片的接触界面上留下一个小的开口,形成janus结构,得到mg/plga微米马达。然后,用旋涂法将含0.1%sds的100μl0.05%alg涂在mg/plga微米马达的plga涂层的表面。在旋涂仪上,快速的旋转速度有助于涂层的快速干燥,干燥后形成alg层(带负电荷),得到mg/plga/alg微米马达。然后,将300μl0.05%的chi(带正电荷)旋涂在mg/plga/alg微米马达的alg层表面,chi与alg通过静电相互作用形成可降解多孔水凝胶层(alg/chi多孔水凝胶层),得到mg/plga/alg/chi微米马达。采用过量的chi来保证mg基微米马达表面的正电荷以吸收anti-cd3。而后将300μlanti-cd3(0.1mg/ml)旋涂分散于chi层的表面,得到镁基微米马达粗品,该镁基微米马达粗品的表面(alg/chi多孔水凝胶层的表面)负载有抗anti-cd3,将镁基微米马达粗品从玻璃基底上刮下,分散在超纯水中,离心纯化,以去除游离的anti-cd3,得到镁基微米马达(mg/plga/alg/chi/anti-cd3,命名为mg@anti-cd3微米马达)。
对比例:
以实施例1中所采用的镁微球作为对比例1;
以实施例1镁基微米马达制备过程中所制备的mg/plga微米马达为对比例2;
以实施例1镁基微米马达制备过程中所制备的mg/plga/alg微米马达为对比例3;
以实施例1镁基微米马达制备过程中所制备的mg/plga/alg/chi微米马达为对比例4;
(三)微米马达的结构表征
具体测试方法如下:
采用扫描电子显微镜(sem)对以上镁基微米马达的合成过程中的mg微球(对比例1)、mg/plga微米马达(对比例2)、mg/plga/alg微米马达(对比例3)和mg@anti-cd3微米马达(实施例1)进行观察,扫描电子显微镜的图像是用s-4800仪器(日本日立高科技公司)在10kv加速电压下获得;测试所得结果如图2所示。图2中,a为mg微球的扫描电镜图,标尺50μm;b、c为单个mg微球的放大图,标尺20μm;d为mg/plga微米马达的扫描电镜图,标尺20μm;e为mg/plga/alg微米马达的扫描电镜图,标尺20μm;f为mg@anti-cd3微米马达的扫描电镜图,标尺20μm;g为f所示mg@anti-cd3微米马达上多孔alg/chi水凝胶结构表面的放大扫描电镜图;标尺1μm。另外,采用imagej软件分析得到mg@anti-cd3微米马达上多孔alg/chi水凝胶孔径尺寸分布如图3a所示;mg微球的粒径分布如图3b所示。
在实施例1mg@anti-cd3微米马达的的制备过程中,在alg溶液和chi溶液中添加罗丹明b(rhb),其余按照实施例1的制备方法,制得mg@anti-cd3微米马达/rhb,采用nikon倒置荧光显微镜、40倍物镜拍摄微米马达分别测试观察得到mg@anti-cd3微米马达/rhb的明场图、荧光图以及明场图和荧光图的叠加图像;以上明场图和荧光图的测试过程,曝光时间分别为70ms(明场通道)和30ms(红色荧光通道)。以上测试所得结果如图4所示。图4中,a为明场和rhb红色荧光场叠加图;b为明场图;c为rhb红色荧光场图像,标尺20μm。
由以上测试结果可知,裸露的mg微球的平均直径为20μm(如图3b所示),且其表面相对光滑(如图2中b和c所示);对于mg/plga微米马达,可以在其上观察到plga涂层的janus结构(如图2中d所示);对于mg/plga/alg微米马达,可以在其上观察到plga/alg涂层的janus结构(如图2中e所示);对于mg@anti-cd3微米马达,由图2中f可知,其具有janus结构(如中虚线环绕),与裸露的mg微球(如图2中b和c所示)、mg/plga微米马达(如图2中d所示)和mg/plga/alg微米马达(如图2中e所示)相比,mg@anti-cd3微米马达的表面粗糙,这是由于多孔alg/chi水凝胶结构的形成所致;图2中g显示了由alg和chi顺序沉积形成的放大多孔水凝胶结构,这些水凝胶具有优良的生物相容性和在生物医学应用中的潜在用途;此外,这些水凝胶为多孔结构,允许在微米马达运动期间装载抗原(anti-cd3)和释放抗原;通过静电作用,将带负电荷的anti-cd3涂层到带正电荷的chi表面。用imagej软件分析,水凝胶孔的平均直径为89.3nm(如图3a所示)。
由图4中b所示明场图像来看,具有不透明mg核心的系统显示为暗球体;对于图4中c所示的荧光成像,rhb共溶于alg溶液和chi溶液中,在水凝胶形成过程中混合,荧光半球显示alg/chi水凝胶的部分表面覆盖,从而证实了janus结构。
一般而言,全裸mg微球与水反应生成的对称氢气泡不利于推进,而不对称的结构确保了在系统的裸侧发生mg-h2o反应,在系统的一侧积聚氢气,以促进高效移动。由上图1、图2、图3a、图3b和图4所示结构表征测试结果可证实成功制备janus结构的mg@anti-cd3微米马达。
(四)mg@anti-cd3微米马达的运动特性
经研究,mg基微米马达在ph值为4~10的水介质中展示了高效和可比的推进力。进而将以上所制得的mg@anti-cd3微米马达在0.5m碳酸氢钠溶液(nahco3)与0.2wt%十二烷基硫酸钠(sds)的混合水溶液中进行实验,以评估微米马达的运动轨迹。具体采用一台高速摄影机(nikon,ds-qi2)与一台尼康ti2-a倒置光学显微镜相连;然后利用nis-elements-ar3.2软件,对mg@anti-cd3微米马达的运动进行观察和记录;再利用imagej插件手动跟踪和chemotaxis趋化工具,统计计算出25个微米马达的运动速度和方向性。
另外,经研究,mg与水(mg-h2o)之间的反应可生成mg(oh)2的钝化层,如反应式(1);而根据反应式(2),在nahco3存在时,mg(oh)2的钝化层将消耗,产生水溶性mgco3;然后,离子扩散到水介质中,形成推动微米马达运动的气泡推力,使mg-h2o反应得以继续。因此,nahco3的存在在mg@anti-cd3微米马达自推进过程中起到了关键作用。由上,当以mg@anti-cd3微米马达在nahco3溶液中推进时,它们的mg核被溶解,显示微米马达的自我破坏和无害残留物,基于类似的原理,可以理解的,也可采用其他可溶解消化mg(oh)2的钝化层的物质;十二烷基硫酸钠作为一种表面活性剂,它可用于降低气泡的表面张力,并提高产生气泡的效率。进而,mg@anti-cd3微米马达在以上水溶液介质中可实现高速运转。
mg+2h2o→mg(oh)2+h2↑反应式(1)
mg(oh)2+2hco3-→mg2++co32-+2h2o反应式(2)
采以上测试方法,观察mg/plga微米马达(对比例2)和mg@anti-cd3微米马达(实施例1)的运动特性,观察到微米马达运动过程中的不同运动模式(包括线性、螺旋和圆形)。
mg@anti-cd3微米马达的运动特性的观察测定结果如图5、图6所示和表1所示。图5中a为微米马达圆形运动模式中的运动轨迹,时间间隔为1s,比例尺为20μm;b为微米马达在组合运动模式(不同阶段具有不同的运动模式)中的运动轨迹,时间间隔为1s,比例尺为50μm;c为微米马达螺旋运动模式中的运动轨迹,时间间隔为1s,比例尺50μm;d为微米马达线性运动模式中的运动轨迹,时间间隔为1s,比例尺50μm。图6中a为25个mg@anti-cd3微米马达的速度分布;b为25个mg@anti-cd3微米马达的方向性测试结果。
mg/plga微米马达的运动特性结果如图7、图8和表2所示。图7为微米马达螺旋运动模式中的运动轨迹,时间间隔为0.29s,比例尺为50μm。图8中,a为25个mg/plga微米马达的速度分布;b为25个mg/plga微米马达的方向性测试结果。
表1mg@anti-cd3微米马达运动特性测试数据表
表2mg/plga微米马达运动特性测试数据表
由图5和图6可知,对于每一个运动模式,在一侧可以清楚地观察到氢气泡的长尾mg@anti-cd3微米马达,janus结构的mg@anti-cd3微米马达在氢气泡释放侧的相反方向被自动推进方向。由以上测试结果可以看出,连续的mg-h2o反应依赖于janus结构,这种结构有助于不对称氢气泡的产生和推进mg@anti-cd3微米马达。同时,可以观察到,伴随气泡产生的强大动量推动微米马达以螺旋路径前进;螺旋轨迹表明,随着时间的增加,合力方向随气泡驱动力和阻力改变。另外,从微米马达的重心或运动方向上分离出合力作用线,这可能是由于不对称结构和质量分布造成的mg@anti-cd3的janus微米马达。还可以观察到,随着动量的减弱,运动路径可以逐渐变为一个子圆或一条直线。通过图像imagej和chemotaxis趋化工具分析,得到了微米马达的速度和方向。根据图5中c所对应运动过程的观察测定,螺旋路径上的微米马达以58μm/s的速度移动,而根据图5中a所对应运动过程的观测测定,沿着亚圆形路径的微米马达的速度约为25μm/s。统计分析25个mg@anti-cd3微米马达后,平均速度确定为42±20μm/s,方向性为0.47,如表1所示。如图6中b所示,提供了多个mg@anti-cd3微米马达自驱动的轨迹。
而对于mg/plga微米马达,由图7、8和表1所示,平均速度约为50±24μm/s,方向性为0.37。对比以上mg/plga微米马达和mg@anti-cd3微米马达的运动特性测试结果可知,负载alg、chi和anti-cd3后,速度略有下降。结果表明,mg微粒表面的薄膜厚度对其运动速度有影响,mg@anti-cd3微米马达比mg/plga微米马达多了三层(alg、chi、anti-cd3),而对于mg@anti-cd3微米马达,经研究,plga层厚度小于3μm时,微米马达可以运动,厚度大于5μm时,马达的运动受限。
(五)t细胞的激活
t细胞激活是免疫治疗必不可少的,它可以清除人体内的病原体,如外来病毒和异常细胞,这种依赖于自然免疫系统功能调节的免疫治疗方法可规避常规药物治疗中的耐药性。因此,发明人考察了以上所制得的mg@anti-cd3微米马达在t细胞活化方面的应用。具体通过将fluo4预染色jurkatt细胞与以上制得的mg@anti-cd3的微米马达混合在十八孔板的一个孔中,并通过倒置荧光显微镜观察。其中,fluo4是细胞内钙水平和钙离子通道状态的指示剂;anti-cd3是针对初始状态的t细胞cd3共受体的单克隆抗体,可参与细胞的活化。经研究,jurkatt细胞在表面活性剂存在的情况下,细胞活性降低,会导致细胞膜不稳定,因此,将jurkatt细胞活化在pbs缓冲液和nahco3混合溶液中进行,而不是包含表面活性剂的溶液。具体按照以下方法进行t细胞激活实验:
1、anti-cd3浓度的测定
在实验过程中,mg@anti-cd3微米马达表面anti-cd3的浓度用蛋白质含量测定方法进行测定。具体可采用bca蛋白检测试剂盒测定anti-cd3浓度,bca蛋白检测试剂盒从碧云天公司购买。其具备步骤包括:
a.加入0.8ml蛋白质标准溶液(20mgbsa),制备25mg/ml蛋白质标准溶液。配制后可立即使用,也可在-20℃下长期保存;
b.取适量25mg/ml蛋白质标准品,稀释至最终浓度0.5mg/ml;
c.根据样品数量,将1体积的bca试剂b(50:1)加入50体积的bca试剂a中,制备bca工作液,工作液在室温下24h内稳定。其中,试剂a和试剂b为购买bca蛋白检测试剂盒所配试剂;
d.向96孔板中加入0、2、4、8、12、16、20μl标准品,并将标准品稀释至20μl;
e.在96孔板中加入适量样品,再加入标准稀释液至20μl;
f.每孔加入200μlbca工作液,置37℃下放置30min;
g.在562nm处测定吸光度,按照以上方法分别测定标准液的吸光度,绘制标准曲线(如图9所示),再根据标准曲线计算样品蛋白质浓度。
采用以上测定方法测得实施例1mg@anti-cd3微米马达样品体系的蛋白质浓度为325μg/ml。
通过细胞计数室测得,1mg以上所制得的mg@anti-cd3微米马达含有2600个粒子。而后通过如下公式(1)计算出每个mg@anti-cd3微米马达上anti-cd3的密度为4.974×10-5μg/μm2。
d=a×0.5/[2600×(4πr2)](μg/μm2)公式(1)
d为anti-cd3密度;a为蛋白质浓度,a=325μg/ml;r(~10μm)为微米马达的半径。
2、jurkatt细胞的培养
jurkatt细胞在37℃的无血清细胞培养基中饥饿2h;然后,在无血清细胞培养基中加入5μg/ml的fluo-4am(钙离子荧光探针),37℃孵育30min,使钙指示剂fluo-4能够被加载到细胞中;然后用hoechstc1022对装有fluo4的jurkatt细胞进行染色8min。
3、jurkatt细胞的激活
以上培养后的jurkatt细胞处于悬浮状态,而后加入mg@anti-cd3微米马达,mg@anti-cd3微米马达与jurkatt细胞在室温下孵育,进而对jurkatt细胞进行激活。mg@anti-cd3微米马达激活jurkatt细胞的钙离子通道示意图如图10所示。
细胞质中钙离子浓度的迅速增加是t细胞活化的一般标准,更强烈和持续的钙升高意味着更强的t细胞活化,因此,钙离子荧光强度的波动可以用来评估t细胞的活化强度。根据研究,当t细胞的钙反应符合以下两个标准时,认为t细胞被激活。一是钙离子升高峰(fluo4,绿色荧光)的振幅必须至少比基础荧光强度高5倍,即增加倍数>5倍;二是钙升高必须持续至少1min后才逐渐衰变,即持续时间>1min。
4、mg@anti-cd3微米马达对t细胞激活的表征
采用荧光显微镜分别测试mg@anti-cd3微米马达(实施例1)刺激t细胞的明场图、荧光图,具用nikon倒置荧光显微镜,分别用40×物镜和荧光滤光片,分别采集蓝光和绿光激发的明场和荧光;曝光时间分别为70ms(明场通道)、30ms(蓝色通道)和100ms(绿色通道)。由于微米马达表面有带正电的壳聚糖层,有利于微米马达与jurkatt细胞的粘附,测得孵育2min后,细胞内的fluo4荧光已清晰可见。另外,测得mg@anti-cd3微米马达分别刺激jurkatt细胞5min、10min、15min和20min后的明场图和绿色荧光场图如图11中a所示。当jurkatt细胞被激活时,可观察到fluo4的绿色荧光。采用荧光显微镜测得其在25min和50min内的荧光趋势如图12中a和b所示。
另外,采用mg/plga/alg/chi微米马达(对比例1)代替mg@anti-cd3微米马达刺激t细胞,作为对照组,并采用类似的方法对微米马达刺激t细胞的表征测试。具体测得mg/plga/alg/chi微米马达分别刺激jurkatt细胞5min、10min、15min和20min后的明场图和绿色荧光场图,如图11中b所示。采用荧光显微镜测得在30min内的荧光趋势如图12中c所示。
采用流式细胞仪(attunenxt,thermofisher)获得活化t细胞的荧光强度值;以t细胞在pbs缓冲液中混合0.5mnahco3作为空白组来探索实验条件。电压维持在370v,流速为50μl/min,注射量为100μl,每次记录5000个细胞;荧光通道为bl2(ftic)。按照以上方法,采用流式细胞仪分别测得mg@anti-cd3微米马达和mg/plga/alg/chi微米马达(对照组)刺激t细胞20min内的荧光趋势,所得结果如图13所示,图13中a表示流式细胞仪测得mg@anti-cd3微米马达刺激t细胞20min内的荧光趋势;b表示流式细胞仪测得mg/plga/alg/chi微米马达刺激t细胞20min内的荧光趋势。
采用细胞计数试剂盒-8(cck-8)评估jurkatt细胞活性,具体步骤包括:
a.将100μljurkatt细胞悬液(5000个细胞/孔)放入96孔板中。在加湿培养箱(37℃,5%co2)中预培养培养培养板24h;
b.添加10μl不同浓度(分别为0.4、0.2、0.1、0.05和0.01mg/ml)的mg微粒、mg/plga/alg/chi微米马达和mg@anti-cd3微米马达分别测试到平板上;
c.在培养箱中培养12h;
d.将10μlcck-8溶液加入板的每个孔中;小心不要将气泡引入油井,因为它们会干扰外径读数;
e.在培养箱中培养1-4h;
f.使用微板阅读器在450nm处测量吸光度。
采用以上方法测得,mg微球、mg/plga微米马达、mg/plga/alg/chi微米马达和mg@anti-cd3微米马达对t细胞活性的影响,所得结果如图14所示。
由图12中a可知,mg@anti-cd3微米马达刺激t细胞,fluo4的荧光强度在25min内从最初的1.231(2min)增加到6.283(22min),增加了5.1倍,持续时间超过1min,表明有jurkatt细胞被成功激活。由图11中a和图12中b可以看出mg@anti-cd3微米马达刺激t细胞,随着时间的增加,fluo4绿色荧光的持续增加趋势;流式细胞仪的测试结果图13中a也验证了这种增加趋势大于大体积溶液,其中,fluo4的荧光强度从2min到18min增加了7.6倍。这可以归因于:首先,mg@anti-cd3微米马达表面的anti-cd3与t细胞相互作用,结合马达的机械动量,可以从一开始激活t细胞;其次,alg/chi水凝胶孔中负载的anti-cd3可以逐渐洗脱,导致fluo4绿色荧光在20min内不断增加,根据以往文献,钙响应仅限于10min,强度较弱。而由于anti-cd3与水凝胶的静电相互作用减弱,水凝胶的分解加速了anti-cd3的释放。此外,图11中a显示,不透明的mg核(mg微球)在mg@anti-cd3微米马达逐渐变得透明,并且在20min内耗尽,证实了系统的崩解性。这一结果也证明了mg作为一种具有吸引力的材料,相比于其他低腐蚀速率的过渡金属(如铁和钨),mg在生物环境中可以中速降解。由此可知,mg@anti-cd3微米马达被无害地溶解在生物介质中,只留下少量残留物,从而证实其自破坏性和生物相容性。
此外,对于对照组(mg/plga/alg/chi微米马达),由图11中b、图12中c和图13中b可知,mg/plga/alg/chi微米马达对细胞的碰撞作用并不能完全激活jurkatt细胞,因此,mg@anti-cd3微米马达体系中激活细胞的主要来源是微米马达上负载的anti-cd3。
除此之外,由图9所示的细胞活性测试结果可知,在微米马达含量为0.2mg/ml时,不同负载的微米马达对细胞的影响都不大,每组细胞的活性都在85%以上。由此验证,本体系中所用所有材料都是具有高生物相容性,可减少免疫过程的免疫排斥反应,提高马达的使用效率和使用范围。
由上,以上所制得的镁基微米马达具有高生物相容性,所有成分均可降解,可避免生物环境的不良毒性,其在nahco3等可溶解消化mg(oh)2钝化层的水溶液中通过纯水裂解实现高效推进,几乎所有反应产物对生物环境无害。另外,其上,alg/chi形成的多孔水凝胶具有较高的抗原载量,通过alg/chi形成的多孔水凝胶结构负载anti-cd3,使得微米马达能够激活钙离子通道,从而诱导t细胞,这对免疫治疗至关重要,进而该镁基微米马达可用于制备t细胞活化药物。可以理解地,由于alg/chi形成的多孔水凝胶结构,可在其上负载其他功能性抗原材料,以赋予镁基微米马达其他功能。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询



 商标分类
商标分类  商标转让
商标转让 



