一种新型冠状病毒RBD融合蛋白亚单位疫苗及其制备方法和应用与流程
 2021-02-02 21:02:04|
2021-02-02 21:02:04| 632|
632| 起点商标网
起点商标网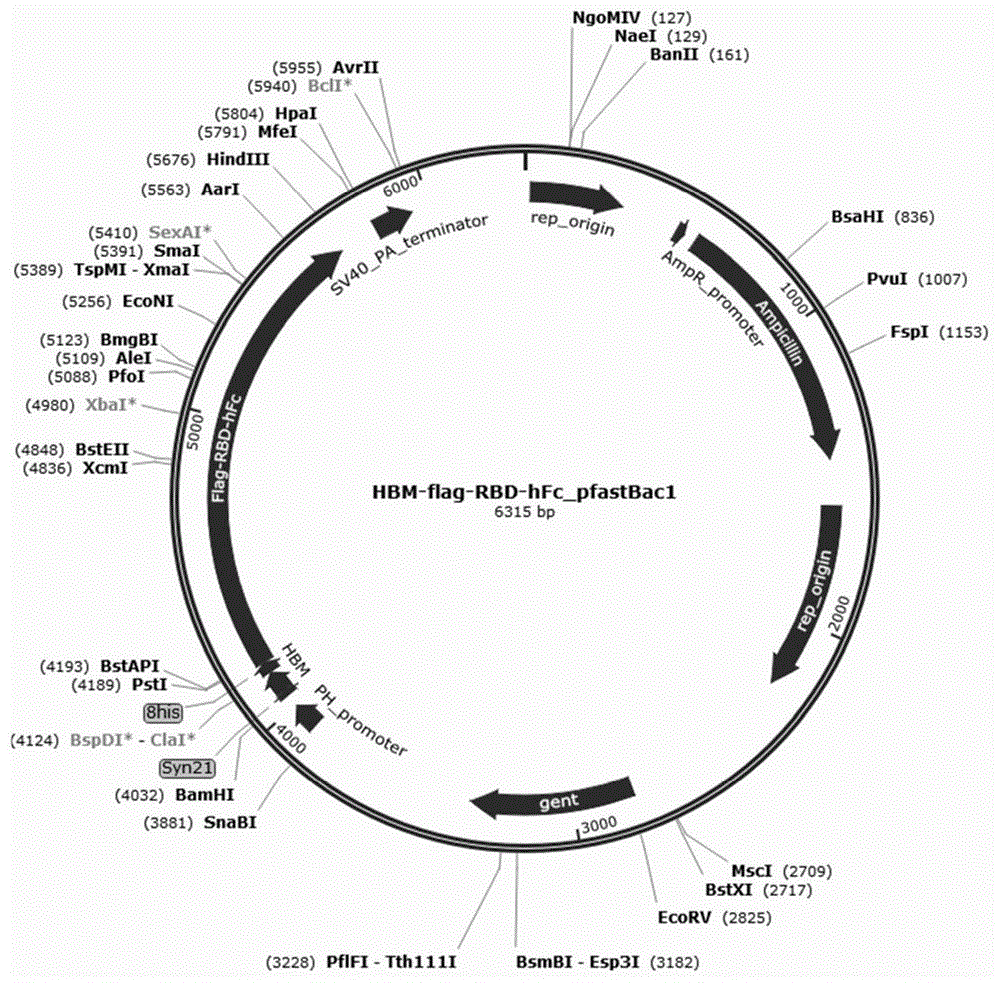
本发明属于生物疫苗的技术领域,具体涉及一种新型冠状病毒rbd融合蛋白亚单位疫苗及其制备方法和应用。
背景技术:
冠状病毒(coronavirus)是一类单股正链rna病毒,可感染包括人类在内的多种哺乳动物。冠状病毒可分为α、β、γ和δ共4个家族,现已知可侵染人类的冠状病毒有7种,均来自于α和β两个家族,包括低致病性的hcov-oc43、hcov-229e、hcov-nl63、hcov-hku1和高致病性的严重急性呼吸综合征冠状病毒(sars-cov)、中东呼吸综合征冠状病毒(mers-cov)、sars-cov-2,其中hcov-229e、hcov-nl63属于冠状病毒α家族,sars-cov-2、sars-cov、mers-cov、hcov-oc43、hcov-hku1属于冠状病毒β家族。sarscov-2普遍呈球形,多具有多形性,直径60~140nm,病毒颗粒表面具有冠状病毒独特的刺突,长约9~12nm。sars-cov-2基因大小约为29.8kb,基因组被注释为含有14个开放阅读框(openingreadingframe,orf),共编码27~28个蛋白质。基因组的3'端编码4种结构蛋白,在冠状病毒间都较为保守,分别为表面刺突糖蛋白(spike,s)、小包膜蛋白(envelope,e)、外膜蛋白(membrane,m)、核衣壳蛋白(nucleocapsid,n)。
2019年末由新型冠状病毒sars-cov-2引发的新型冠状病毒肺炎(以下简称“新型冠状病毒肺炎”),因其高度传染性对世界各国人民健康及社会稳定造成了严重影响,2019-ncov给人类生命健康造成了极大的威胁,已经成为严重的社会公共卫生问题。免疫预防和消毒是防治冠状病毒感染传播的有效手段。也因此,2019-ncov疫苗的研究是十分重要科研工作,对新型冠状病毒肺炎的诊断和预防具有重要意义。关于新型冠状病毒疫苗研发的方向包括重组蛋白疫苗、灭活疫苗、dna疫苗、mrna疫苗和腺病毒载体疫苗,截至目前重组新型冠状病毒(2019-cov)疫苗(腺病毒载体)已进入临床阶段,其他未见成果报道。
技术实现要素:
针对上述问题,本发明的目的在于提供一种新型冠状病毒rbd融合蛋白亚单位疫苗及其制备方法和应用,所述新型冠状病毒rbd融合蛋白亚单位疫苗在预防新型冠状病毒感染方面具有重要作用。
本发明的技术内容如下:
本发明提供了一种新型冠状病毒rbd融合蛋白,所述rbd融合蛋白由包括新型冠状病毒s蛋白的rbd结构域、hbm分泌信号肽、flag免疫增强肽、hfc免疫增强肽融合而成;
所述新型冠状病毒rbd融合蛋白的氨基酸序列如seqidno.1所示;
所述rbd结构域的氨基酸序列如seqidno.2所示;
所述hbm分泌信号肽的氨基酸序列如seqidno.3所示;
所述flag免疫增强肽的氨基酸序列如seqidno.4所示;
所述hfc免疫增强肽(fc受体)的氨基酸序列如seqidno.5所示。
本发明还提供了一种新型冠状病毒rbd融合蛋白的制备方法,包括如下步骤,将新型冠状病毒s蛋白的rbd结构域、hbm分泌信号肽、flag免疫增强肽以及hfc免疫增强肽片段融合,合成于质粒载体上,即得融合蛋白;
所述融合方式包括串联;
所述质粒载体包括pfastbac1载体。
本发明提供了一种新型冠状病毒rbd融合蛋白亚单位疫苗,所述rbd融合蛋白亚单位疫苗为rbd融合蛋白通过杆状病毒昆虫细胞表达系统表达得到。
本发明还提供了一种新型冠状病毒rbd融合蛋白亚单位疫苗的制备方法,所述亚单位疫苗为rbd融合蛋白通过杆状病毒昆虫细胞表达系统表达得到,之后还包括提取纯化工艺,所述提取纯化工艺包括对杆状病毒昆虫系统离心后培养上清进行预处理、过耐edta及碱的ni填料亲和层析以及超滤浓缩透析处理;
所述预处理包括杆状病毒昆虫系统离心后培养上清中加入咪唑至终浓度5mm-50mm,用nacl调节电导至15ms/cm~50ms/cm,调节ph至6.2-8.0,用0.45um以下膜过滤,滤液用于层析纯化;
所述亲和层析的操作包括如下步骤:
1)上游构建在c末端设计了组氨酸标签,便于快速拿到高纯度目标蛋白,亲和层析填料为耐edta及碱的ni填料;填料平衡液咪唑浓度、电导及ph值同预处理液:10mm~0.1mpb(na2hpo4,nah2po4);nacl浓度50mm~0.6m;咪唑浓度5~50mm;ph6.2~8.0;柱高在5~25cm,流速在60cm/h~300cm/h;平衡体积在2cv~20cv;
2)过滤后样品上样,样品上样的流速在60cm/h~300cm/h,上样量为每ml填料2mg~40mg;
3)上完样后用平衡液冲洗柱子至基线平,流速在60cm/h~300cm/h;
4)洗杂,除带组氨酸标签目标蛋白在以上条件下会结合在柱子上,也有部分杂蛋白会非特异性吸附在柱子上,因此选用合适的条件既能把非特异性结合的杂蛋白洗涤下来,目标蛋白又不会在该条件下被洗下来,保证提高纯度又不降低回收率;
洗杂缓冲液主要包括10mm~0.1mpb(na2hpo4,nah2po4);nacl浓度50mm~0.6m;咪唑浓度10~80mm;ph6.2~8.0,流速在60cm/h~300cm/h;
洗脱,洗杂后需用洗脱缓冲液将目标蛋白洗脱下来,洗脱缓冲液包括10mm~0.1mpb(na2hpo4,nah2po4);nacl浓度0mm~0.6m;咪唑浓度100~1m;ph6.2~8.0,流速在60cm/h~300cm/h;
所述超滤浓缩透析处理包括如下步骤:由于亲和层析收集液有高浓度咪唑,且没有稳定组分纯化后蛋白不易保存,因此需进行缓冲液更换,选用超滤法进行缓冲液更换,超滤膜包大小选用3.5kd~30kd,超滤缓冲液包括但不限于:10mm~0.1mpb(na2hpo4,nah2po4),甘露醇1%~3%,精氨酸盐酸盐1%~4%,ph6.0~8.0;
用以上工艺主要特点是工艺路线简单,纯化后纯度高,回收率高,纯化后纯度可达90%以上,回收率85%以上;
超滤后样品为疫苗原液,与佐剂一起制备成疫苗成品可成为最终产品。
一种新型冠状病毒rbd融合蛋白在制备抗新型冠状病毒药物方面的应用。
一种新型冠状病毒rbd融合蛋白在新型冠状病毒的亚单位疫苗的应用。
本发明的有益效果如下:
本发明提供的可表达新型冠状病毒s蛋白的rbd融合蛋白,有助于形成预防新型冠状病毒的疫苗药物,其在小鼠上有良好的免疫原性,为预防新型冠状病毒感染具有重要意义,本发明通过对疫苗的提取纯化,获得高纯度、高回收率的纯的新型冠状病毒rbd融合蛋白亚单位疫苗,超滤浓缩透析将纯度合格的样品进行缓冲液置换,保证样品的稳定性及免疫原性,本提取纯化工艺路线简单,适合放大,可实现产业化生产。
附图说明
图1为实施例1的hbm-flag-rbd-hfc_pfastbac1质粒图谱;
图2为实施例1的质粒转化蓝白斑结果;
图3为实施例1的质粒转化的pcr鉴定结果;
图4为实施例1的杆粒提取pcr电泳结果;
图5为实施例1的蛋白表达情况的wb检测结果;
图6为实施例1的蛋白纯化后样品sds-page检测结果;
图7为实施例1的蛋白纯化后样品wb检测结果。
具体实施方式
以下通过具体的实施案例以及附图说明对本发明作进一步详细的描述,应理解这些实施例仅用于说明本发明而不用于限制本发明的保护范围,在阅读了本发明之后,本领域技术人员对本发明的各种等价形式的修改均落于本申请所附权利要求所限定。
若无特殊说明,本发明的所有原料和试剂均为常规市场的原料、试剂。
实施例1
一种新型冠状病毒rbd融合蛋白亚单位疫苗的制备:
1.重组质粒的构建
选取新型冠状病毒(covid-19)的s蛋白序列中的c端结构域rbd、hbm(分泌信号肽)、flag(免疫增强肽)和hfc(免疫增强肽区)片段,采用串联的方式进行融合,采用密码子优化系统设计合成到pfastbac1载体上,所构建的重组质粒hbm-flag-rbd-hfc_pfastbac1的结构示意图如图1所示;
2.重组杆粒的构建
将重组质粒hbm-flag-rbd-hfc_pfastbac1转化至大肠杆菌dh10bac感受态细胞,在含有x-gal/iptg的lb平板上进行蓝白斑筛选重组子(图2),选取5个白色菌落,进行pcr鉴定,目的片段大小为1650bp,鉴定结果如图3所示,5个白色单菌落均携带目的基因。
挑取2个pcr鉴定出的阳性重组子进行扩大培养,使用碱性裂解法分离杆粒dna,杆粒电泳结果如图4所示,杆粒的浓度较高,条带正确。
3.杆状病毒的表达
将0.5mlesf921培养的密度为1.0×106个/ml的sf9细胞加入到24deepwellblock内,在ep管内混合以下试剂:
a:2μg重组载体加入到100μl无血清转染培养基;
b:6μl转染剂加入到100μl无血清培养基内,溶液最少静置5min;
c:将a、b溶液,轻轻混匀,室温孵育30min。
孵育后,将800μl无血清培养基加入到孵育30min后的转染剂-dna复合物ep管内轻轻混匀,将总体积1ml的dna-转染剂复合物加入到已添加细胞的24welldeepblock内,孵育4到5个小时,加入3mlesf921培养基到24welldeepblock孔内(终体积为4ml),如果细胞生长状态不佳,则需在这一步添加抗生素(使用10mg/ml的庆大霉素),将dna转染剂复合物留在培养基内不会影响细胞转染效率(如果是贴壁细胞则需要吸出dna转染试剂复合物),盖上盖子摇床培养4~5天,取样观察病变情况,收获病毒p0。
传代:p0代病毒传代(p1代病毒制备);p1代病毒传代(p2代病毒制备);p2代病毒传代(p3代病毒制备)同时感染6孔板,第3、4、5、6天收获一孔细胞和上清,分别进行wb检测蛋白表达情况,蛋白连续表达的结果如图5(ps:细胞培养上清,ls:细胞裂解上清,rc:回融沉淀)所示,第3天开始,细胞培养上清中开始有蛋白表达,第4、5、6天,培养上清中蛋白表达较多。
4.新型冠状病毒rbd融合蛋白的纯化
(一)样品预处理:
将新型冠状病毒rbd融合蛋白亚单位疫苗昆虫杆状系统离心后培养上清500ml培养上清加入咪唑至终浓度10mm,加入后充分搅拌至完全溶解;
以上处理液用nacl调节电导至30ms/cm,调节ph至7.2,用0.45um膜过滤,滤液用于层析纯化。
(二)亲和层析
(1)亲和层析填料为耐edta及碱的ni填料;填料平衡液咪唑浓度、电导及ph值同预处理液:20mmpb,nacl浓度0.3m,咪唑浓度10mm,ph7.2平衡;柱高在5cm,流速在150cm/h;平衡体积10cv;
(2)过滤后样品上样,上样流速在150cm/h,上样量为每ml填料2mg~40mg;
(3)上完样后用平衡液冲洗柱子至基线平,流速在150cm/h;
(4)洗杂:洗杂缓冲液20mmpb,nacl浓度0.3m,咪唑浓度30mm,ph7.2,流速150cm/h;
(5)洗脱:洗脱缓冲液20mmpb,nacl浓度0.3m,咪唑浓度300mm,ph7.2,流速在150cm/h;
(三)超滤透析
亲和层析收集液有高浓度咪唑,选用超滤法进行缓冲液更换,超滤膜包大小选用10kd,超滤缓冲液:20mmpb(na2hpo4,nah2po4),甘露醇1.5%,精氨酸盐酸盐2%,ph7.4,透析倍数为6倍体积。透析完后浓缩至浓度2mg/ml;
经考马斯亮蓝染色分析纯度92%,回收率90%。
纯化蛋白的鉴定:将每次纯化的蛋白各取15μl,与等量的2x电泳加样缓冲液混合,经sds-page电泳,电泳结果如图6所示,一部分经考马斯亮蓝染色,观察纯化情况,图6样品泳道分子量为目标分子量,出化后考染结果几乎无其它杂带;另一部分转膜,进行westernblot鉴定,wb检测结果如图7所示,样品条带对应的分子量为目标分子量大小。
5.疫苗的制备:
将制备的抗原用pbs稀释,稀释比例为1:10000,稀释后抗原按1:2比例加入as01b佐剂,充分混合,分装制成疫苗样品。
疫苗的应用:20只小鼠,分成2组,雌雄各半。实验组肌肉注射hbm-flag-rbd-hfc_pfastbac1融合蛋白亚单位疫苗,空白对照组小鼠肌肉注射无菌pbs。每日观察所有参与实验的动物,观察其爬行、进食、体温、呼吸道症状等情况,免疫组和对照组无差别;
分别于免疫后第14天和第28天,通过尾巴静脉采血的方式获得血清。
疫苗的免疫评价:将第14天和第28天获得的血清,检测的抗体滴度,由表1结果所示,表明了免疫组均有高滴度的抗体产生。
表1动物免疫后产生的抗体滴度结果
实施例2
新型冠状病毒rbd融合蛋白亚单位疫苗昆虫杆状系统提取纯化:
(一)样品预处理:
将新型冠状病毒rbd融合蛋白亚单位疫苗昆虫杆状系统离心后培养上清500ml培养上清加入咪唑至终浓度30mm,加入后充分搅拌至完全溶解;
以上处理液用nacl调节电导至50ms/cm,调节ph至6.2,用0.45um膜过滤,滤液用于层析纯化;
(二)亲和层析
(1)亲和层析填料为耐edta及碱的ni填料;填料平衡液咪唑浓度、电导及ph值同预处理液:40mmpb,nacl浓度0.6m,咪唑浓度30mm,ph6.2平衡;柱高在15cm,流速在300cm/h;平衡体积20cv;
(2)过滤后样品上样,上样流速在300cm/h,上样量为每ml填料对应2~40mg目标蛋白;
(3)上完样后用平衡液冲洗柱子至基线平,流速在300cm/h;
(4)洗杂:洗杂缓冲液40mmpb,nacl浓度0.6m,咪唑浓度60mm,ph6.2,流速300cm/h;
(5)洗脱:洗脱缓冲液40mmpb,nacl浓度0.3m,咪唑浓度500mm,ph6.2,流速在300cm/h;
(三)超滤透析
亲和层析收集液有高浓度咪唑,选用超滤法进行缓冲液更换,超滤膜包大小选用3.5kd,超滤缓冲液:40mmpb(na2hpo4,nah2po4),甘露醇1%,精氨酸盐酸盐3%,ph6.2,透析倍数为6倍体积,透析完后浓缩至浓度2mg/ml;
经考马斯亮蓝染色分析纯度93%,回收率86.5%。
实施例3
新型冠状病毒rbd融合蛋白亚单位疫苗昆虫杆状系统提取纯化:
(一)样品预处理:
将新型冠状病毒rbd融合蛋白亚单位疫苗昆虫杆状系统离心后培养上清500ml培养上清加入咪唑至终浓度5mm,加入后充分搅拌至完全溶解;
以上处理液用nacl调节电导至20ms/cm,调节ph至8.0,用0.45um膜过滤,滤液用于层析纯化。
(二)亲和层析
(1)亲和层析填料为耐edta及碱的ni填料;填料平衡液咪唑浓度、电导及ph值同预处理液:0.1mpb,nacl浓度0.2m,咪唑浓度5mm,ph8.0平衡;柱高在10cm,流速在100cm/h;平衡体积10cv;
(2)过滤后样品上样,上样流速在60cm/h,上样量为每ml填料2mg~40mg;
(3)上完样后用平衡液冲洗柱子至基线平,流速在100cm/h;
(4)洗杂:洗杂缓冲液0.1mpb,nacl浓度0.2m,咪唑浓度20mm,ph7.2,流速100cm/h;
(5)洗脱:洗脱缓冲液0.1mpb,nacl浓度0.2m,咪唑浓度0.1m,ph7.2,流速在100cm/h;
(三)超滤透析
亲和层析收集液有高浓度咪唑,选用超滤法进行缓冲液更换,超滤膜包大小选用30kd,超滤缓冲液:0.1mpb(na2hpo4,nah2po4),甘露醇1%,精氨酸盐酸盐4%,ph8.0,透析倍数为6倍体积,透析完后浓缩至浓度2mg/ml;
经考马斯亮蓝染色分析纯度91.5%,回收率87%。
实施例4
新型冠状病毒rbd融合蛋白亚单位疫苗昆虫杆状系统提取纯化:
(一)前处理
将新型冠状病毒rbd融合蛋白亚单位疫苗昆虫杆状系统离心后培养上清500ml培养上清加入咪唑至终浓度50mm,加入后充分搅拌至完全溶解;
以上处理液用nacl调节电导至40ms/cm,调节ph至7.6,用0.45um膜过滤,滤液用于层析纯化。
(二)亲和层析
(1)亲和层析填料为耐edta及碱的ni填料;填料平衡液咪唑浓度、电导及ph值同预处理液:30mmpb,nacl浓度0.5m,咪唑浓度50mm,ph7.6平衡;柱高在25cm,流速在60cm/h;平衡体积15cv;
(2)过滤后样品上样,上样流速在60cm/h,上样量为每ml填料2mg~40mg;
(3)上完样后用平衡液冲洗柱子至基线平,流速在60cm/h;
(4)洗杂:洗杂缓冲液30mmpb,nacl浓度0.5m,咪唑浓度80mm,ph7.6,流速60cm/h;
(5)洗脱,洗脱缓冲液30mmpb,nacl浓度0.5m,咪唑浓度1m,ph7.6,流速在60cm/h;
(三)超滤透析
亲和层析收集液有高浓度咪唑,选用超滤法进行缓冲液更换,超滤膜包大小选用10kd,超滤缓冲液:30mmpb(na2hpo4,nah2po4),甘露醇3%,精氨酸盐酸盐1.5%,ph7.6,透析倍数为6倍体积,透析完后浓缩至浓度2mg/ml;
经考马斯亮蓝染色分析纯度95%,回收率85.1%。
序列表
<110>东莞博盛生物科技有限公司广州源博医药科技有限公司
<120>一种新型冠状病毒rbd融合蛋白亚单位疫苗及其制备方法和应用
<160>5
<170>siposequencelisting1.0
<210>1
<211>546
<212>prt
<213>hbm-flag-rbd-hfc_pfastbac1
<400>1
glyserasnleulyslyslysilelysmetlyspheleuvalasnval
151015
alaleuvalphemetvalvaltyrilesertyriletyralaasparg
202530
serleuhishishishishishishishisglyserglyserglyile
354045
asnasnasnleuglnargvalarggluleualavalglnseralaasn
505560
serthrasnserglnseraspleuaspserphethrvalglulysgly
65707580
iletyrglnthrserasnpheargvalglnprothrgluserileval
859095
argpheproasnilethrasnleucyspropheglygluvalpheasn
100105110
alathrargphealaservaltyralatrpasnarglysargileser
115120125
asncysvalalaasptyrservalleutyrasnseralaserpheser
130135140
thrphelyscystyrglyvalserprothrlysleuasnaspleucys
145150155160
phethrasnvaltyralaaspserphevalileargglyaspgluval
165170175
argglnilealaproglyglnthrglylysilealaasptyrasntyr
180185190
lysleuproaspaspphethrglycysvalilealatrpasnserasn
195200205
asnleuaspserlysvalglyglyasntyrasntyrleutyrargleu
210215220
phearglysserasnleulysprophegluargaspileserthrglu
225230235240
iletyrglnalaglyserthrprocysasnglyvalgluglypheasn
245250255
cystyrpheproleuglnsertyrglypheglnprothrasnglyval
260265270
glytyrglnprotyrargvalvalvalleuserphegluleuleuhis
275280285
alaproalathrvalcysglyprolyslysserthrasnleuvallys
290295300
asnlyscysvalasnpheasnpheglyglyglyglyserargserasp
305310315320
lysthrhisthrcysproprocysproalaprogluleuleuglygly
325330335
proservalpheleupheproprolysprolysaspthrleumetile
340345350
serargthrprogluvalthrcysvalvalvalaspvalserhisglu
355360365
aspprogluvallyspheasntrptyrvalaspglyvalgluvalhis
370375380
asnalalysthrlysproargglugluglntyrasnserthrtyrarg
385390395400
valvalservalleuthrvalleuhisglnasptrpleuasnglylys
405410415
glutyrlyscyslysvalserasnlysalaleuproalaproileglu
420425430
lysthrileserlysalalysglyglnproarggluproglnvaltyr
435440445
thrleuproproserarggluglumetthrlysasnglnvalserleu
450455460
thrcysleuvallysglyphetyrproseraspilealavalglutrp
465470475480
gluserasnglyglnprogluasnasntyrlysthrthrproproval
485490495
leuaspseraspglyserphepheleutyrserlysleuthrvalasp
500505510
lysserargtrpglnglnglyasnvalphesercysservalmethis
515520525
glualaleuhisasnhistyrthrglnlysserleuserleuserpro
530535540
glylys
545
<210>2
<211>239
<212>prt
<213>rbd
<400>2
serphethrvalglulysglyiletyrglnthrserasnpheargval
151015
glnprothrgluserilevalargpheproasnilethrasnleucys
202530
propheglygluvalpheasnalathrargphealaservaltyrala
354045
trpasnarglysargileserasncysvalalaasptyrservalleu
505560
tyrasnseralaserpheserthrphelyscystyrglyvalserpro
65707580
thrlysleuasnaspleucysphethrasnvaltyralaaspserphe
859095
valileargglyaspgluvalargglnilealaproglyglnthrgly
100105110
lysilealaasptyrasntyrlysleuproaspaspphethrglycys
115120125
valilealatrpasnserasnasnleuaspserlysvalglyglyasn
130135140
tyrasntyrleutyrargleuphearglysserasnleulysprophe
145150155160
gluargaspileserthrgluiletyrglnalaglyserthrprocys
165170175
asnglyvalgluglypheasncystyrpheproleuglnsertyrgly
180185190
pheglnprothrasnglyvalglytyrglnprotyrargvalvalval
195200205
leuserphegluleuleuhisalaproalathrvalcysglyprolys
210215220
lysserthrasnleuvallysasnlyscysvalasnpheasnphe
225230235
<210>3
<211>25
<212>prt
<213>hbm
<400>3
metlyspheleuvalasnvalalaleuvalphemetvalvaltyrile
151015
sertyriletyralaaspargserleu
2025
<210>4
<211>25
<212>prt
<213>flag
<400>4
serthrthrthrcysseralacysvalsertrpleucysserproleu
151015
thrproprothrproserprothrtrp
2025
<210>5
<211>221
<212>prt
<213>hfc
<400>5
thrlysleuthrhisalahisargalaglnhisleuasnsertrpgly
151015
aspargglnserserserserproglnasnproargthrproserser
202530
proglyproleuargserhisalatrptrptrpthralathrlysthr
354045
leuargserserserthrglythrtrpthralatrpargcysilemet
505560
proargglnserargglyargserserthrthralaargthrvaltrp
65707580
seralaserserprosercysthrargthrglymetalaargserthr
859095
seralaargserprothrlysproserglnproproserarglyspro
100105110
serprolysprolysglyserprogluasnhisargcysthrprocys
115120125
prohisproglyargargproargthrargseralaproalatrpser
130135140
lysalaserileproalathrserprotrpserglyargalametgly
145150155160
serargargthrthrthrargproargleuprocystrpthrprothr
165170175
alaproserserserthralaserserprotrpthrargalaglygly
180185190
serargglythrserserhisalaprocysthrargleucysthrthr
195200205
thrthrargargargalaserprocysleuargvalasn
210215220
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询



 商标分类
商标分类  商标转让
商标转让 



