具有靶向、释药和检测功能的金属离子配位薄层硼纳米片载体探针的制备方法与流程
 2021-02-02 19:02:27|
2021-02-02 19:02:27| 377|
377| 起点商标网
起点商标网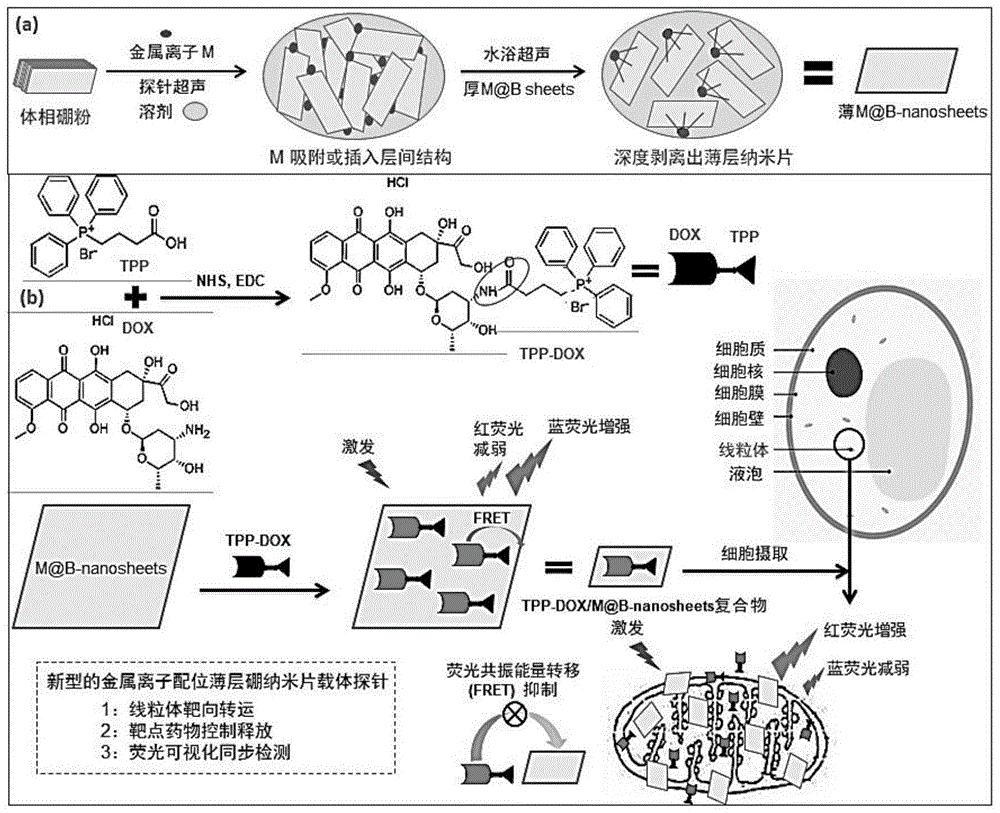
本发明属于功能化纳米片复合材料和生物医用纳米载体探针的制备技术领域,具体涉及一种具有靶向、释药和检测功能的金属离子配位薄层硼纳米片载体探针的制备方法。
背景技术:
硼是元素周期表中的第五位元素,左邻金属的铍和右邻非金属的碳,兼具金属性和非金属性,可形成常规强共价键以及多中心化学键,成键能力和方式均优于碳。在硼有百余种晶体结构中,大部分体相晶体硼含有b12二十面体结构单元,少数含γ-斜方硼的哑铃状b2单元。硼与大部分元素构成丰富的稳定化合物,在多学科领域展现出广阔的应用前景。在纳米尺度,硼纳米材料具有与体相硼不同的优异性能,在小尺寸时趋向形成类苯环有机分子的平面结构,在稍大尺寸和特殊条件下形成类富勒烯的笼状、纳米管、薄膜结构等。这特征预示了硼与碳在理化性质、纳米结构、功能和应用等方面存在高度的相似性,二维(2d)硼烯及硼纳米片有望成为后石墨烯时代的新兴2d纳米材料,将推动纳米科技的快速发展。
近年来,有关硼纳米片的制备及应用的研究已有文献和专利报道。例如,研究者以硼粉末为原料,采用超声辅助的液相剥离法合成了2d硼烯或硼纳米片(q.guo,k.wu,z.shao,e.t.basore,p.jiang,j.qiu,boronnanosheetsforefficientall-opticalmodulationandlogicoperation,adv.opt.mater.,2019,7,1900322.;h.li,l.jing,w.liu,j.lin,r.y.tay,s.h.tsang,e.h.t.teo,scalableproductionoffew-layerboronsheetsbyliquid-phaseexfoliationandtheirsuperiorsupercapacitiveperformance,acsnano,2018,12,1262–1272.),郭强兵等公开了一种硼纳米片均匀涂在反射镜或微纳光纤表面构成可饱和吸收体器件,分散在透明基质内形成复合物膜构成可饱和吸收体器件(郭强兵;邱建荣.一种基于硼纳米片的可饱和吸收体器件及应用.国家发明专利.申请公布号:cn109361141a)。
硼原子核外仅有三个电子,呈现严重的缺电子状态,硼元素sp2价电子易杂化,配位数大,共价半径短,极易与其它元素形成强而有方向的键。在液相剥离过程中,剥离的硼纳米片因暴露于水和氧环境中,硼易与氧反应生成硼氧化物,进而发生氧化和降解,破坏了硼纳米片的结构及性能。密度泛函理论(dft)研究表明,硼-氧之间强共价键会引起硼烯结构的重构和破坏,而硼与碱或碱土金属之间的离子相互作用对硼烯的结构影响甚微。碱或碱土金属电负性低,可补偿硼原子和硼烯的电子缺陷,既弱化了硼烯与基底之间的相互作用,又抑制了硼烯在电荷驱动下的结构转变。过渡金属掺杂的硼烯表现出增强的电催化活性,过渡金属进入硼烯片层结构促进了剥离,硼烯也抑制了过渡金属原子聚集,加快了氧化还原反应。
基于理论预测,硼烯结构暴露空气中是不稳定的,对硼烯表面修饰或掺杂使其2d表面结构更稳定,改性后硼烯具有更独特的光学和电学特征,因此开展2d硼烯结构的金属掺杂或配位及其表面改性具有重要的科学意义和应用价值。碱、碱土和过渡金属的空轨道可与硼的孤对电子形成“金属-硼”配位,配位后硼的孤对电子被占据,不再与氧发生反应。基于此,采用金属离子与硼原子配位的策略制备新型的金属离子配位薄层硼纳米片(m@b-nanosheets),可获得优异的微结构和光电功能的稳定性,表面功能化改性后开发其在生物传感及医学诊疗领域的潜在应用。本发明公开了一种具有靶向、释药和检测功能的金属离子配位薄层硼纳米片载体探针的制备方法,该载体探针可实现癌细胞摄取后的线粒体靶向转运,细胞内微环境变化引发的药物释放,以及原位同步检测的三重功能一体化。目前,尚未有金属离子配位薄层硼纳米片载体探针的制备及其应用的国内外文献和专利报道。
技术实现要素:
本发明的目的在于克服上述现有技术存在的不足,发展一种新型的金属离子配位薄层硼纳米片及其纳米载体探针的制备方法,该载体探针具备靶向、释药和检测的三重功能一体化。
为实现上述目的,本发明公开了的一种具有靶向、释药和检测功能的金属离子配位薄层硼纳米片载体探针的制备方法,其特征在于,该方法具体包括以下步骤:
(1)在磁力搅拌下向50~100ml异丙醇中依次加入100~200mg硼粉末和溶解了1~10mg金属硝酸盐的二次蒸馏水溶液,混合均匀后转入超声波细胞粉碎仪中用探针超声处理5~15min,然后转入超声波清洗器中用水浴超声处理12~24h,反应产物在5000rpm转速下离心5~15min,取上层溶液在10000rpm转速下离心5~15min,离心后的沉淀物用乙醇和二次蒸馏水冲洗三次,真空干燥,制得最终产物即为金属离子配位的薄层硼纳米片(m@b-nanosheets);
(2)称取50mg亲脂性阳离子(3-丙羧基)三苯基溴化膦(tpp),20mgn-羟基丁二酰亚胺(nhs),30mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺(edc)溶于75ml二氯甲烷中,称取50mg阿霉素(dox)溶于25ml二氯甲烷中,加入50μl三乙胺后将dox二氯甲烷溶液逐滴添加至tpp溶液中,在室温和磁力搅拌下反应24h,产物溶液通过硅胶柱层析纯化,制得偶联物tpp-dox;
(3)用磷酸盐水缓冲液和乙醇的混合液分别配制m@b-nanosheets和tpp-dox的分散液,m@b-nanosheets质量浓度调节为0.1~1.0mg/ml,在磁力搅拌下向m@b-nanosheets分散液中逐滴加入tpp-dox的分散液,其中tpp-dox摩尔浓度调节为0.1~1.0mmol/l,制得tpp-dox负载的m@b-nanosheets;
(4)将tpp-dox/m@b-nanosheets复合物通过内吞作用被摄取进入癌细胞如人口腔表皮样癌kbcells,人肺癌a549cells以及耐dox肿瘤mda-mb-231/adrcells,在摄入0~24h后不同时间点,采用激光共聚焦荧光显微镜(clfm)成像观察复合物在内细胞中的分布,采用mtt方法研究复合物对细胞存活率的影响,采用350~400nm激发观测内细胞线粒体区域的荧光颜色变化,基于不同时间点获得的实验结果,clfm成像揭示复合物靶向转运到癌细胞线粒体,mtt实验证实复合物中dox释放,荧光色差发生“蓝→红”可视化变化说明dox释放与同步检测,荧光色差红移越大说明细胞内dox释放的量越高。
本发明的效果是:采用羧-胺偶联反应制备偶联物(tpp-dox),该偶联物具有细胞线粒体靶向的功能,利用癌细胞线粒体跨膜电位较高的特征,达到逆转癌细胞耐药之目的。将tpp-dox负载在m@b-nanosheets片层结构上,具有dox红荧光和纳米片的蓝荧光双发射特征。由于纳米片发射光谱与dox吸收光谱存在较大重叠,发生荧光共振能量转移(fret)。将tpp-dox/m@b-nanosheets复合物通过内吞作用被摄取进入癌细胞。clfm成像显示复合物分布于细胞核和线粒体中,细胞存活率实验揭示复合物对人口腔表皮样癌kbcells和人肺癌a549cells的毒性低于dox,但对耐dox肿瘤mda-mb-231/adrcells毒性显著大于dox。复合物作为药物载体在特定癌细胞中执行靶向转运和细胞标记,当复合物到达靶向细胞核和线粒体时,靶点特殊微环境改变如ph、热敏感等促使tpp-dox从纳米片上脱离开,实现dox药物控制释放。因dox脱离m@b-nanosheets抑制了fret过程,dox红荧光增强而纳米片的蓝荧光减弱,即dox释放过程伴随了荧光色差发生“蓝→红”可视化变化,荧光色差红移越大,说明细胞内dox释放的量越高。因此,tpp-dox/m@b-nanosheets复合物实现了癌细胞荧光标记,亚细胞水平靶向转运,可控药物释放与原位同步检测的三重功能一体化。
附图说明
图1为一种具有靶向、释药和检测功能的金属离子配位薄层硼纳米片载体探针的制备方法与工作原理示意图。
具体实施方式
下面结合附图并通过具体实施例对本发明进行详细说明。
实施例1
本实施例涉及的一种具有靶向、释药和检测功能的金属离子配位薄层硼纳米片载体探针的制备方法与工作原理示意图如图1所示,具体制备步骤如下:
在磁力搅拌下向50ml异丙醇中,依次加入100mg硼粉末和溶解了2mg硝酸镁的二次蒸馏水溶液,混合均匀后转入超声波细胞粉碎仪中用探针超声处理5min,然后转入超声波清洗器中用水浴超声处理12h,反应产物在5000rpm转速下离心5min,取上层溶液在10000rpm转速下离心5min,离心后的沉淀物用乙醇和二次蒸馏水冲洗三次,真空干燥,制得最终产物即为mg@b-nanosheets;
称取50mgtpp,20mgnhs,30mgedc溶于75ml二氯甲烷中,称取50mgdox溶于25ml二氯甲烷中,加入50μl三乙胺后将dox二氯甲烷溶液逐滴添加至tpp溶液中,在室温和磁力搅拌下反应24h,产物溶液通过硅胶柱层析纯化,制得偶联物tpp-dox;
用磷酸盐水缓冲液和乙醇的混合液分别配制mg@b-nanosheets和tpp-dox的分散液,mg@b-nanosheets质量浓度调节为0.2mg/ml,在磁力搅拌下向mg@b-nanosheets分散液中逐滴加入tpp-dox的分散液,其中tpp-dox摩尔浓度调节为0.2mmol/l,制得tpp-dox负载的mg@b-nanosheets;
将tpp-dox/mg@b-nanosheets复合物通过内吞作用摄取进入癌细胞kbcells,a549cells以及mda-mb-231/adrcells,在摄入0~12h后不同时间点,采用clfm成像观察复合物在内细胞中的分布,采用mtt方法研究复合物对细胞存活率的影响,采用360nm激发观测内细胞线粒体区域的荧光颜色变化,基于不同时间点获得的实验结果,clfm成像揭示复合物靶向转运到癌细胞线粒体,mtt实验证实复合物中dox释放,荧光色差发生“蓝→红”可视化变化说明dox释放与同步检测,荧光色差红移越大说明细胞内dox释放的量越高。
实施例2
本实施例涉及的一种具有靶向、释药和检测功能的金属离子配位薄层硼纳米片载体探针的制备方法与原理示意图如图1所示,偶联物tpp-dox的制备同实施例1,其它具体制备步骤如下:
在磁力搅拌下向75ml异丙醇中,依次加入150mg硼粉末和溶解了5mg硝酸钙的二次蒸馏水溶液,混合均匀后转入超声波细胞粉碎仪中用探针超声处理10min,然后转入超声波清洗器中用水浴超声处理18h,反应产物在5000rpm转速下离心10min,取上层溶液在10000rpm转速下离心10min,离心后的沉淀物用乙醇和二次蒸馏水冲洗三次,真空干燥,制得最终产物即为ca@b-nanosheets;
用磷酸盐水缓冲液和乙醇的混合液分别配制ca@b-nanosheets和tpp-dox的分散液,ca@b-nanosheets质量浓度调节为0.5mg/ml,在磁力搅拌下向ca@b-nanosheets分散液中逐滴加入tpp-dox的分散液,其中tpp-dox摩尔浓度调节为0.5mmol/l,制得tpp-dox负载的ca@b-nanosheets;
将tpp-dox/ca@b-nanosheets复合物通过内吞作用摄取进入癌细胞kbcells,a549cells以及mda-mb-231/adrcells,在摄入0~18h后不同时间点,采用clfm成像观察复合物在内细胞中的分布,采用mtt方法研究复合物对细胞存活率的影响,采用370nm激发观测内细胞线粒体区域的荧光颜色变化,基于不同时间点获得的实验结果,clfm成像揭示复合物靶向转运到癌细胞线粒体,mtt实验证实复合物中dox释放,荧光色差发生“蓝→红”可视化变化说明dox释放与同步检测,荧光色差红移越大说明细胞内dox释放的量越高。
实施例3
本实施例涉及的一种具有靶向、释药和检测功能的金属离子配位薄层硼纳米片载体探针的制备方法与原理示意图如图1所示,偶联物tpp-dox的制备同实施例1,其它具体制备步骤如下:
在磁力搅拌下向100ml异丙醇中依次加入200mg硼粉末和溶解了5mg硝酸锂的二次蒸馏水溶液,混合均匀后转入超声波细胞粉碎仪中用探针超声处理15min,然后转入超声波清洗器中用水浴超声处理24h,反应产物在5000rpm转速下离心15min,取上层溶液在10000rpm转速下离心15min,离心后的沉淀物用乙醇和二次蒸馏水冲洗三次,真空干燥,制得最终产物即为li@b-nanosheets;
用磷酸盐水缓冲液和乙醇的混合液分别配制li@b-nanosheets和tpp-dox分散液,li@b-nanosheets质量浓度调节为1.0mg/ml,在磁力搅拌下向li@b-nanosheets分散液中逐滴加入tpp-dox的分散液,其中tpp-dox摩尔浓度调节为1.0mmol/l,制得tpp-dox负载的li@b-nanosheets;
将tpp-dox/li@b-nanosheets复合物通过内吞作用摄取进入癌细胞kbcells,a549cells以及mda-mb-231/adrcells,在摄入0~18h后不同时间点,采用clfm成像观察复合物在内细胞中的分布,采用mtt方法研究复合物对细胞存活率的影响,采用380nm激发观测内细胞线粒体区域的荧光颜色变化,基于不同时间点获得的实验结果,clfm成像揭示复合物靶向转运到癌细胞线粒体,mtt实验证实复合物中dox释放,荧光色差发生“蓝→红”可视化变化说明dox释放与同步检测,荧光色差红移越大说明细胞内dox释放的量越高。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询



 商标分类
商标分类  商标转让
商标转让 



