一类含芘的水溶性染料及制备方法与流程
 2021-02-02 18:02:01|
2021-02-02 18:02:01| 353|
353| 起点商标网
起点商标网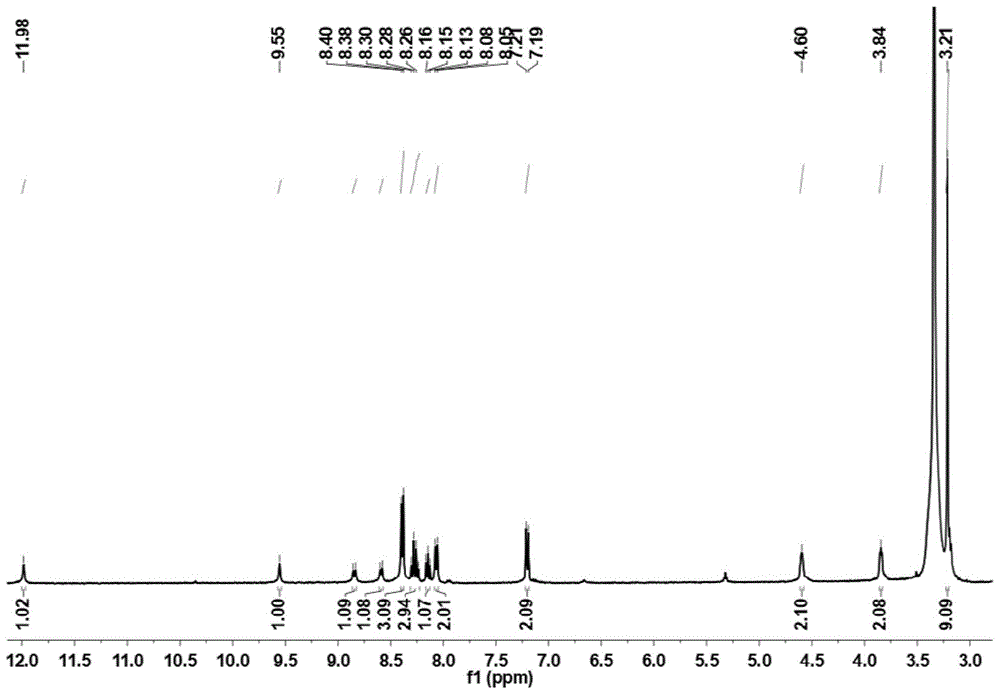
本发明属于有机化学合成技术领域,具体涉及一类新型的含芘的水溶性染料及其制备方法。
背景技术:
芘单元一直作为荧光团被广泛使用,其荧光寿命长,量子产率高,当其以二聚体形式堆叠时,会产生红移的激基缔合物发光,芘衍生物具有优良的光学性质,在荧光探针、荧光染料、荧光化学传感器等方面有重要应用。但其吸收光谱在近紫外区,在低浓度下发射深蓝色光,覆盖的发光区域有限,且基于芘合成的有机化合物大多数不溶于水,无疑限制了基于芘的衍生物的使用。目前对水溶性的含芘化合物的研究较少,因此通过合理的分子设计,简单高效的合成方法得到含芘的水溶性化合物具有重要的研究意义和实用价值。
技术实现要素:
本发明的第一个目的是提供一类荧光发射光谱拓宽的含芘的水溶性染料。
本发明的第二个目的是提供一类所述荧光发射光谱拓宽的含芘的水溶性染料的制备方法。
为了实现上述目的,本发明采用的技术方案如下:
本发明的第一方面提供了一类含芘的水溶性染料,通式如式i所示:
其中,r1为
或,r1、r3同时为
或,r1、r6同时为
或,r1、r8同时为
或,r2、r7同时为
较优选的,所述含芘的水溶性染料中:
其中,r1为以下结构中的一种:
或,r1、r3同时为以下结构中的一种:
或,r1、r6同时为以下结构中的一种:
或,r1、r8同时为以下结构中的一种:
或,r2、r7同时为以下结构中的一种:
更优选的,所述含芘的水溶性染料中:
其中,r1为
或,r1、r3同时为
或,r1、r6同时为
或,r1、r8同时为
或,r2、r7同时为
最优选的,所述含芘的水溶性染料的结构为以下结构中的一种:
本发明的第二方面提供了一种所述含芘的水溶性染料的制备方法,包括以下步骤:
第一步,在室温下,将化合物1和碳酸钾溶于乙腈溶液中,加入二溴烷烃,在温度为70~90℃的条件下,氩气氛围下搅拌回流1~24h,得到化合物2;所述化合物1和碳酸钾的摩尔比为1:3,所述化合物1与二溴烷烃的摩尔比为1:5;
第二步,将化合物2和三甲胺加入乙醇中,在温度为70~90℃的条件下,氩气氛围下搅拌回流1~24h,得到化合物3;其中化合物2与三甲胺的摩尔比为1:5;
第三步,将化合物3、水合肼溶于甲醇中,在温度为70~90℃的条件下,氩气氛围下搅拌回流1~24h,得到化合物4;化合物3和水合肼的摩尔比为1:(5-50);
第四步,将化合物4、1-芘甲醛或芘取代物和过量的三氟乙酸溶于乙醇中,在温度为70~90℃的条件下,氩气氛围下搅拌回流1~24h,得到式i所示化合物即含芘的水溶性染料;
所述化合物4和1-芘甲醛的摩尔比为1:1;所述化合物4和芘取代物的摩尔比为2:1。
所述二溴烷烃为二溴乙烷或二溴丙烷。
所述芘取代物为1,3-芘二甲醛,1,6-芘二甲醛,1,8-芘二甲醛,2,7-芘二甲醛。
由于采用上述技术方案,本发明具有以下优点和有益效果:
为拓宽光谱区域,本发明向芘单元中引入了酰腙基团,延长了π-共轭骨架,使荧光发射波长红移,且酰腙基团分子间氢键的作用会作为次级非共价相互作用稳定芘单元的初级堆叠相互作用。在酰腙基团的另一端共价修饰亲水性的季铵盐链,使整个分子成为一个典型的两亲性结构,具有水溶性。这一特点驱使目标分子在水溶液中进行两亲性组装,疏水性的芘单元在内部堆叠,因此产生激基缔合物发光。合理的分子设计使目标化合物具有水溶性,且拓宽了其荧光光谱,实现了含芘的水溶性染料的合成。
本发明的荧光发射光谱拓宽的含芘的水溶性染料分子设计合理,合成目标物新颖,且有较好的水溶性,合成条件易于控制,产物纯化较为简单,具有普适性,合成步骤简单,反应条件温和。
附图说明
图1为本发明实施例1制备的化合物8的1h-nmr图。
图2为本发明实施例1制备的化合物8的荧光光谱示意图。
图3为本发明实施例2制备的化合物9的1h-nmr图。
图4为本发明实施例2制备的化合物9的荧光光谱示意图。
图5为本发明实施例3制备的化合物10的1h-nmr图。
图6为本发明实施例3制备的化合物10的荧光光谱示意图。
图7为本发明实施例4制备的化合物11的1h-nmr图。
图8为本发明实施例4制备的化合物11的荧光光谱示意图。
图9为本发明实施例5制备的化合物12的1h-nmr图。
图10为本发明实施例5制备的化合物12的荧光光谱示意图。
图11为本发明实施例4制备的化合物11的橙黄色澄清水溶液图片。
图12为本发明对比例化合物8-羟基芘-1,3,6-三磺酸三钠盐的荧光光谱示意图。
具体实施方式
为了更清楚地说明本发明,下面结合优选实施例对本发明做进一步的说明。本领域技术人员应当理解,下面所具体描述的内容是说明性的而非限制性的,不应以此限制本发明的保护范围。
本发明实施例所需的中间化合物的合成路线如下:
化合物7的制备方法包括以下步骤:
(1)在室温下,将化合物1对羟基苯甲酸甲酯(5.0g,33mmol)和碳酸钾(13.8g,100mmol)溶于350ml乙腈溶液,然后将二溴乙烷(30.9g,165mmol)加入上述溶液中,在温度为80℃的条件下,氩气氛围下搅拌回流12h,通过取代反应得到化合物5。其中化合物1与碳酸钾的摩尔比为1:3,化合物1与二溴乙烷的摩尔比为1:5。
(2)将化合物5(5.1g,19.6mmol)和三甲胺(5.8g,98mmol)加入200ml乙醇中,在温度为80℃的条件下,氩气氛围下搅拌回流12h,得到季铵盐类化合物6,其中化合物5与三甲胺的摩尔比为1:5。
(3)将化合物6(4.1g,12mmol)、水合肼(3.2g,60mmol)和120ml甲醇混合,在温度为70℃的条件下,氩气氛围下搅拌回流12h,得到化合物7,其中化合物6和水合肼的摩尔比为1:5。
实施例1
将化合物7(0.1g,0.31mmol)、1-芘甲醛(0.07g,0.31mmol)、三氟乙酸(10ul)与乙醇(40ml)混合,在80℃氩气氛围下搅拌回流24小时,tlc跟踪监测反应至原料耗尽。将反应液冷却到室温,减压蒸馏除去溶剂,重结晶得到0.1g化合物8,产率为72%。
具体合成路线如下:
图1为本发明实施例1制备的化合物8的1h-nmr图,1hnmr(400mhz,dmso-d6)δ=11.98(s,1h),9.55(s,1h),8.84(d,j=9.1hz,1h),8.59(d,j=8.8hz,1h),8.39(d,j=7.8hz,3h),8.27(dd,j=18.3,8.9hz,3h),8.15(m,1h),8.07(d,j=8.7hz,2h),7.20(d,j=8.8hz,2h),4.60(s,2h),3.84(s,2h),3.21(s,9h).
图2为本发明实施例1制备的化合物8的荧光光谱示意图,其荧光最大发射波长为460nm。
实施例2
将化合物7(0.2g,0.62mmol)、1,3-芘二甲醛(0.08g,0.31mmol)、三氟乙酸(10ul)与乙醇(40ml)混合,在80℃氩气氛围下搅拌回流24小时,tlc跟踪监测反应至原料耗尽。将反应液冷却到室温,减压蒸馏除去溶剂,重结晶得到0.15g化合物9,产率为56%。
具体合成路线如下:
图3为本发明实施例2制备的化合物9的1h-nmr图,1hnmr(400mhz,dmso-d6)δ=12.03(s,2h),9.58(s,2h),8.91(d,j=7.8hz,2h),8.64(d,j=7.7hz,2h),8.44(m,4h),8.07(d,j=8.5hz,4h),7.20(d,j=8.7hz,4h),4.60(s,4h),3.85(s,4h),3.21(s,18h)。
图4为本发明实施例2制备的化合物9的荧光光谱示意图,其荧光最大发射波长为625nm。
实施例3
将化合物7(0.2g,0.62mmol)、1,6-芘二甲醛(0.08g,0.31mmol)、三氟乙酸(10ul)与乙醇(40ml)混合,在80℃氩气氛围下搅拌回流24小时。混合物冷却到室温,减压蒸馏除去溶剂,重结晶得到0.18g化合物10,产率为68%。
具体合成路线如下:
图5为本发明实施例3制备的化合物10的1h-nmr图,1hnmr(400mhz,dmso-d6)δ=12.10(s,2h),9.63(s,2h),8.89(d,j=9.0hz,2h),8.63(d,j=7.8hz,4h),8.33(m,4h),8.06(d,j=8.7hz,4h),7.19(d,j=8.7hz,4h),4.59(s,4h),3.85(s,4h),3.22(s,18h)。
图6为本发明实施例3制备的化合物10的荧光光谱示意图,其荧光最大发射波长为625nm。
实施例4
将化合物7(0.2g,0.62mmol)、1,8-芘二甲醛(0.08g,0.31mmol)、三氟乙酸(10ul)与乙醇(40ml)混合,在80℃氩气氛围下搅拌回流24小时。混合物冷却到室温,减压蒸馏除去溶剂,重结晶得到0.14g化合物11,产率为53%。
具体合成路线如下:
图7为本发明实施例4制备的化合物11的1h-nmr图,1hnmr(400mhz,dmso-d6)δ=12.04(s,2h),9.58(s,2h),8.90(d,j=7.8hz,2h),8.64(d,j=7.7hz,2h),8.44(m,4h),8.07(d,j=8.6hz,4h),7.21(d,j=8.7hz,4h),4.60(s,4h),3.85(s,4h),3.22(s,18h)。
图8为本发明实施例4制备的化合物11的荧光光谱示意图,其荧光最大发射波长为625nm。
实施例5
将化合物7(0.2g,0.62mmol)、2,7-芘二甲醛(0.08g,0.31mmol)、三氟乙酸(10ul)与乙醇(40ml)混合,在80℃氩气氛围下搅拌回流24小时。混合物冷却到室温,减压蒸馏除去溶剂,重结晶得到0.16g化合物12,产率为60%。
具体合成路线如下:
图9为本发明实施例5制备的化合物12的1h-nmr图,1hnmr(400mhz,dmso-d6)δ=12.05(s,2h),8.91(s,2h),8.66(s,2h),8.33(s,4h),8.06(d,j=8.3hz,4h),7.19(d,j=8.7hz,4h),4.59(s,4h),3.85(s,4h),3.22(s,18h)。
图10为本发明实施例5制备的化合物12的荧光光谱示意图,其荧光最大发射波长为460nm。
实施例6
将36mg化合物11溶于30ml水中得到橙黄色的澄清水溶液,其浓度为8.33×10-4mol/l,说明本发明合成的含芘染料具有良好的水溶性。图11为本发明实施例4制备的化合物11的橙黄色澄清水溶液。
对比例1
由于芘基团的疏水性,目前大部分含芘染料不溶于水,8-羟基芘-1,3,6-三磺酸三钠盐是现有的少数能溶于水的芘类染料之一,其化学结构式如式ⅱ所示,其在512nm附近有较强的绿光发射,本发明各实施例中的含芘的水溶性染料,其荧光波长较8-羟基芘-1,3,6-三磺酸三钠盐有明显红移,在625nm附近有红光发射,因此在生物成像等领域有更广泛的应用。
图12为本发明对比例中8-羟基芘-1,3,6-三磺酸三钠盐的荧光光谱示意图,其荧光最大发射波长为512nm。
以上所述仅是本发明的较佳实施例而已,并非对本发明作任何形式上的限制,虽然本发明已以较佳实施例揭露如上,然而并非用以限定本发明,任何熟悉本专利的技术人员在不脱离本发明技术方案范围内,当可利用上述提示的技术内容作出些许更动或修饰为等同变化的等效实施例,但凡是未脱离本发明技术方案的内容,依据本发明的技术实质对以上实施例所作的任何简单修改、等同变化与修饰,均仍属于本发明方案的范围内。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询



 商标分类
商标分类  商标转让
商标转让 



