高肿瘤突变负荷和微卫星不稳定参考品的制备方法及应用与流程
 2021-02-02 18:02:07|
2021-02-02 18:02:07| 395|
395| 起点商标网
起点商标网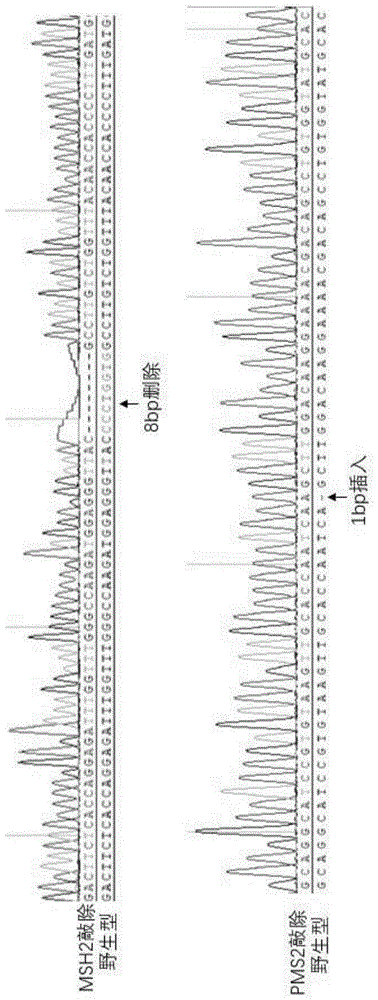
本发明涉及癌细胞检测参考品制备
技术领域:
,具体涉及一种高肿瘤突变负荷和微卫星不稳定参考品的制备方法。
背景技术:
:肿瘤突变负荷(tumormutationburden,tmb)是一种可定量的生物标志物,用来反映肿瘤细胞中所含有的突变数目,通常用肿瘤细胞基因组编码区的每百万碱基突变数来衡量。简单来说就是肿瘤细胞携带的突变数量。非同义突变越多,肿瘤细胞产生的异常蛋白越多。肿瘤突变负荷越高,产生的新抗原也越多,有更大的可能性激活免疫系统对肿瘤的识别。在多癌种中被证实,tmb高的患者总体生存率也更高。tmb是目前除pd-l1表达之外研究最为深入的免疫治疗疗效预测性生物标志物之一。2020年6月16日,fda批准帕博利珠单抗用于既往治疗后疾病进展且无其他令人满意的治疗方案的不可切除或转移性且tmb-h(≧10muts/mb)的成人和儿童实体瘤,这是k药继获批msi-h/dmmr型实体瘤治疗后的第二次不限癌种的获批。研究表明,用来预测癌症治疗效果的tmb值,在不同的癌种中其实是不一样。这也就意味着,可能不存在一个适用于所有癌种的tmb固定值。此外,不同癌种的tmb波动范围比较大,tmb的中位数也相差较大。对不同种类的癌症和不同的用药方案分类分析,不同癌种tmb取值差异较大。微卫星(microsatellite,ms)是指基因组中少于10个核苷酸的简单重复序列,又称短串联重复序列(shorttandemrepeats,strs),其中以二核苷酸序列即(ca/gt)最为丰富,重复次数一般为10~15次。ms的改变会影响基因表达调控以及基因组的稳定,微卫星重复次数减少或者增加被称为微卫星不稳定性(microsatelliteinstability,msi)。微卫星序列在dna复制中极易发生错配、插入/缺失,此改变一旦产生则需要错配系统进行修复,以保证基因组的稳定。目前研究认为,微卫星不稳定性的发生主要是由于dna在复制过程中dna聚合酶产生错误配对并且错配修复(mismatchrepair,mmr)系统未能及时修复所致。mmr系统由mlh1,msh2,msh6和pms2基因组成,这些基因的失活或功能性紊乱,都可能导致细胞突变的增加,最终形成msi。越来越多的研究表明,msi具有非常重要的临床意义,包括:与lynch综合征的筛查,与结直肠癌的预后,与指导用药,均具有显著的相关性。基于聚合酶链式反应(pcr)技术是检测msi的方法学“金标准”,但操作过程复杂,且在结果判断中可能出现荧光过强或过少、非特异性峰、不显著的峰大小改变、杂合性缺失等问题,对结果造成误判。鉴于tmb检测与msi检测过程中存在的问题,制备一种可用来验证及规范tmb的检测及计算流程以及用来对msi检测体系进行质控的标准品尤为重要。目前,市面上存在一些可用于tmb质控的细胞系,包括肿瘤细胞以及与之配对的对照细胞,如atcc细胞库中的nci-h2009与nci-bl2009,nci-h2126与nci-bl2126等。但是,目前市面上并未存在成对的msi细胞系及相关的参考品,特别是将tmb与msi同时集于同一产品。技术实现要素:本发明的目的是提供一种高肿瘤突变负荷和微卫星不稳定参考品的制备方法,其以高tmb值的成对细胞系为基础,将mmr系统的部分或者全部基因敲除,再提取并纯化基因敲除后的细胞的dna,最后按浓度梯度稀释成标准系列参考品,本发明还涉及到该参考品在肿瘤突变负荷和微卫星不稳定性的检测中的应用,本发明提供的参考品使检测可以不依赖公共数据库,一次实验可以得到tmb和msi数据,可以对免疫治疗疗效相关的两个biomarker的检测提供更好的对比和参考。为了实现上述目的,本发明采用的技术方案如下:一种高肿瘤突变负荷和微卫星不稳定参考品的制备方法,其以高tmb(tumormutationburden,肿瘤突变负荷)值的成对细胞系为基础,将mmr(mismatchrepair,错配修复)系统的部分或者全部基因敲除,再提取并纯化基因敲除后的细胞的dna,最后按浓度梯度稀释成标准系列参考品。根据以上方案,所述的高肿瘤突变负荷和微卫星不稳定参考品的制备方法,其特征在于,其包括如下详细步骤:步骤s1,针对mmr系统设计特异的sgrna;所述的特异的sgrna靶向mmr系统的一个或几个或全部的基因;步骤s2,通过体外转录或者化学合成得到步骤s1中设计的特异的sgrna,并将sgrna与cas9蛋白复合形成核糖核蛋白复合物;步骤s3,将步骤s2中获得的核糖核蛋白复合物转染至高tmb值的细胞中;步骤s4,转染48小时后,收集转染后的细胞并进行单克隆培养增殖,再从增殖后的部分细胞中提取dna检测基因敲除结果,选取达到预设敲除目标基因的细胞再进行扩大培养,得到细胞悬液;步骤s5,取步骤s4中的细胞悬液进行dna提取,再测定提取液中的dna浓度,再将测定后的dna和对照细胞的dna按浓度梯度稀释后混合,制成标准系列参考品。根据以上方案,所述的高tmb值的细胞是肿瘤细胞。根据以上方案,所述的步骤s4中的单克隆培养增殖具体是先将转染后的细胞稀释到1-10个/ml,再将细胞悬液混匀,将混匀后的细胞悬液分散至多孔细胞培养板上进行培养。根据以上方案,所述的步骤s4中的基因测定是向有单细胞克隆的孔加入蛋白酶消化细胞,对消化后的细胞进行pcr,再采用sanger法测序。根据以上方案,所述的步骤s5中的dna浓度测定采用分光光度计测提取物的dna浓度,测定标准为:浓度:平均浓度20.0≤x≤60.0ng/μl;od260/280:测定值1.8≤x≤2.0,判定合格;od260/230:测定值1.5≤x≤5.0,判定合格。根据以上方案,所述的浓度梯度如下:肿瘤细胞dna比例(%)对照细胞dna比例(%)梯度11000梯度25050梯度34060梯度42080梯度51090梯度6595梯度7199梯度80.599.5梯度90100将肿瘤细胞dna和对照细胞dna按比例混合。一种高肿瘤突变负荷和微卫星不稳定参考品在肿瘤突变负荷和微卫星不稳定性的检测中的应用。本发明的有益效果是:本发明提供了一种具有tmb-h和msi-h的成对细胞系的制备方法,并将其制备成参考品。该参考品以同一来源正常对照细胞为参照,不依赖公共数据库,一次实验可以得到tmb和msi数据,可以对免疫治疗疗效相关的两个biomarker的检测提供更好的对比和参考。附图说明图1是细胞克隆msh2基因和pms2基因sanger测序结果;图2是肿瘤细胞的分型图谱。图3是对照细胞的分型图谱。具体实施方式下面结合附图和实施例对本发明的技术方案进行说明。本发明提供一种高肿瘤突变负荷和微卫星不稳定参考品的制备方法,其以高tmb值的成对细胞系为基础,将mmr系统的部分或者全部基因敲除,再提取并纯化基因敲除后的细胞的dna,最后按浓度梯度稀释成标准系列参考品;包括如下详细步骤:步骤s1,针对mmr系统设计特异的sgrna;所述的特异的sgrna靶向mmr系统的msh2基因和pms2基因,详细序列为:靶向msh2基因的sgrna序列为:seq01:5’-gcgccgtatagaagtcgccccgg-3’靶向pms2基因的sgrna序列为:seq02:5’-gtaagttgcaccaatcagct-3’;步骤s2,通过化学合成得到步骤s1中设计的特异的sgrna,并将sgrna与cas9蛋白复合形成核糖核蛋白复合物;步骤s3,将步骤s2中获得的核糖核蛋白复合物转染至nci-h2009肿瘤细胞中;步骤s4,转染48小时后,收集转染后的细胞,对细胞准确计数,按照倍比稀释的方法,用培养基将活细胞稀释至5个/ml,并将细胞混匀,取10ml细胞悬液,均匀分到一块96细胞培养孔板中进行培养,待细胞克隆形成时,标记有单细胞克隆的孔,加入约10ul的胰蛋白酶消化细胞,取部分细胞进行pcr,用作sanger测序,剩余细胞继续培养。pcr引物序列如下:primer01_f:5’-cattttcttcaaccaggaggtgag-3’primer01_r:5’-ataagagattctggccgtgtttgta-3’primer02_f:5’-cttgatttgtgcgatgatgtgagaa-3’primer02_r:5’-tagagcaataagaggcgttgaagta-3’根据sanger测序的结果,判断各个克隆中靶基因的敲除情况,并从中挑选msh2和pms2两个基因同时敲除的克隆,进一步地将已经敲除基因的细胞扩大培养,用于提取dna。测序结果如图1所示:由图1可知,挑选的细胞克隆,msh2基因被删除了8bp,而pms2基因被插入了1bp,两个基因均发生了移码突变,即基因敲除。再对基因敲除细胞系进行tmb值计算与msi检测,以确保所制备出的参考品符合要求。将msh2基因和pms2基因敲除细胞系的dna以及对照细胞系的dna,进行全外显子组测序,测序参数如下表所示:通过以下生物信息学方法计算样品的tmb值,dna根据高通量全外显子测序数据分析,所述的tmb检测包含突变过滤的步骤,使用下表的过滤参数对检测出的变异进行过滤:所述tmb检测值=过滤后的体细胞突变/全外显子编码区大小(兆碱基)。根据上述流程,所测得的基因敲除细胞系的tmb值为25。对于msi检测,采用多重荧光pcr—毛细管电泳的方法进行,通过检测nr21、bat26、nr27、bat25、nr24、mono27五个位点分析msi状态,判断标准为:其中2个及2个以上位点发生改变判定为msi-h,仅1个位点发生改变判定为msi-l,无位点改变判定为mss。基因敲除后的肿瘤细胞与对照细胞的msi检测结果如图2和3所示。由图可知,肿瘤细胞在nr27、nr24和mono27三个位点发生了改变,因此判断为msi-h。步骤s5,步骤s51dna提取:采用promega16celllevpurificationkit(货号as1140)及其说明书的使用方法对gdna进行提取;步骤s52dna浓度的测定:使用分光光度计对提取的产物进行dna浓度的测定,浓度测定过程中进行3次重复检测,并且挑选满足如下条件的提取物:浓度:平均浓度20.0≤x≤60.0ng/μlod260/280:测定值1.8≤x≤2.0,判定合格。od260/230:测定值1.5≤x≤5.0,判定合格。步骤s53混合:a)将同一编码和批号细胞沉淀提取的gdna进行混合,混合前需确认:待混合gdna为同一编码和批号的细胞沉淀提取的;待混合gdna浓度测定的od260/280、od160/230结果合格;b)选择合适体积的管子进行混合(≥1.6ml应当用50mlbd管进行混合);c)测定混合后的浓度及od值。步骤s54混合后再行浓度测定,将浓度稀释为20-60ng/μl,再制得的基因敲除肿瘤细胞/对照细胞的gdna,按照下表中的比例进行混合来制备浓度梯度的参考品:肿瘤细胞dna比例(%)对照细胞dna比例(%)梯度11000梯度25050梯度34060梯度42080梯度51090梯度6595梯度7199梯度80.599.5梯度90100将上述的参考品进行全外显子组测序,通过生物信息学方法计算样品的tmb值,分析流程及参数与步骤s4相同。结果显示,tmb值为25。对于msi的检测,也采用步骤s4的方法,结果显示为msi-h。上述制备的高肿瘤突变负荷和微卫星不稳定参考品可以在肿瘤突变负荷和微卫星不稳定性的检测中的应用。以上实施例仅用以说明而非限制本发明的技术方案,尽管上述实施例对本发明进行了详细说明,本领域的相关技术人员应当理解:可以对本发明进行修改或者同等替换,但不脱离本发明精神和范围的任何修改和局部替换均应涵盖在本发明的权利要求范围内。当前第1页1 2 3
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



