一种抗PD-1及c-Met抗原的小分子双特异性抗体Diabody的制作方法
 2021-02-02 16:02:26|
2021-02-02 16:02:26| 478|
478| 起点商标网
起点商标网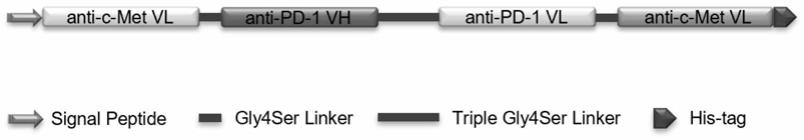
一种抗pd-1及c-met抗原的小分子双特异性抗体diabody
技术领域
[0001]
本发明属生物技术领域,涉及一种双特异性抗体。本发明还包括该双特异性抗体的制备方法、应用以及相应的核酸编码序列。
背景技术:
[0002]
肿瘤的传统治疗手法包括手术、放疗和化疗,手术切除的效果常受限于癌细胞入侵蔓延到邻近组织或远端转移,而放化疗则对体内其他正常组织具有较大毒性。免疫治疗是目前肿瘤治疗的新方向,它能通过调动机体的免疫系统,增强肿瘤微环境抗肿瘤免疫力,从而有效地杀伤肿瘤细胞,具有持久性疗效、适应症广、治疗方式较轻松且能防止转移和复发等优势,甚至为常规治疗无效的晚期肿瘤患者带来了长期生存的希望。目前热门的免疫疗法主要包括免疫检查点抑制剂治疗、过继性免疫细胞治疗、细胞因子治疗与免疫疫苗等。
[0003]
pd-1属于免疫球蛋白超家族,是一种能够抑制t细胞激活的免疫检查点分子,肿瘤细胞能够通过上调其配体pd-l1的表达对t细胞产生抑制效应,因此,pd-1抑制剂代表着肿瘤免疫疗法开发策略上一个重要的转变。当前免疫检查点抑制剂遇到的主要困境是总体缓解率相对较低,临床数据显示pd-1单克隆抗体单药治疗实体瘤仅有10-30%左右的响应率。对此可行的方法即采用联合用药增强其疗效,比如联合放疗、化疗和靶向治疗,然而研究发现联合用药可导致副作用增加近4倍以上。
[0004]
c-met是met基因编码的具有自主磷酸化活性的跨膜受体,属于酪氨酸激酶受体超家族,是hgf的特异性受体。hgf过表达、met基因过表达、突变和扩增均可使其下游信号通路激活,从而促进肿瘤细胞的生长、增殖和迁移,在肿瘤的发生发展中发挥着关键作用。目前针对此靶点的药物主要有c-met小分子抑制剂和单克隆抗体,小分子抑制剂在药物的特异性和有效性方面表现优秀,但常常具有较高副作用及剂量限制性毒性,c-met单克隆抗体的毒性鲜有报道,但其疗效也因其复杂的激活机制而受到限制。
[0005]
双特性抗体是肿瘤免疫治疗的一个新方向,它能通过靶向两种不同的抗原,克服fc限制将t细胞与肿瘤细胞衔接以对其进行集中性杀伤,理论上双特异性抗体能起到“1+1>2”的作用。双特异性抗体按照结构可分为两大类:含fc区的双特异性抗体(igg-like双特异性抗体)与不含fc区的双特异性抗体(non-igg-like双特异性抗体)。分子量较大的igg-like双特异性抗体具有更高的亲和力且半衰期较长,小分子的non-igg-like双特异性抗体半衰期较短,但其组织渗透性极强,具有更大的分布容积,有效剂量不到普通抗体的百分之一,故具有更高的安全性。
[0006]
实体瘤及有形瘤,瘤体生长较血液系统肿瘤更为集中,具有复杂的肿瘤微环境,比如可以通过生成特殊结构的肿瘤血管抑制免疫细胞的浸润等。普通激活型双特异性抗体通过输液进入外周血后可能会过早的结合外周t细胞,且由于免疫抑制微环境无法有效到达肿瘤周围发挥作用,还可能由于外周t细胞的激活产生全身性的免疫因子释放,疗效降低的同时具有很大的安全隐患。并且其双功能特性也具有产生更高副作用的风险。因此在确定双特异性抗体靶点选择的同时,还需要对其结构进行改造,设计出合理的双特异性抗体结
构,在增强其杀伤作用的同时降低其副作用。
[0007]
蛋白质结构的解析对其功能的理解至关重要。然而由于技术的限制,运用实验的方法解析蛋白质结构投入大、周期长、风险大。同源建模技术可以很好的解决这些问题,蛋白质三级结构的保守性远远超过一级结构的保守性,因此可利用信息技术直接从一级结构预测其高级结构。分子对接是一种预测蛋白质相互识别以及相互作用的技术,基于能量优化来实现蛋白质对接运算。故可通过蛋白质同源建模、优化及对接技术来对双特异性抗体的结构进行辅助设计,并对其结构合理性进行评估。
技术实现要素:
[0008]
本发明要解决的技术问题是提供一种同时识别c-met和pd-1的双特异性抗体。
[0009]
本发明要解决的另一个技术问题是将上述双特异性抗体应用于制备抗肿瘤药物。
[0010]
基于上述问题,本发明公开了一种能够结合肿瘤相关抗原c-met和t细胞免疫检查点分子pd-1的双特异性抗体。所述双特异性抗体靶向肿瘤细胞上的抗原c-met,基于c-met复杂的激活机制所导致的c-met单克隆抗体用药限制的问题,本发明通过衔接t细胞来促进其杀伤作用。实验表明,t细胞激活后可分泌ifn-γ促使肿瘤上调pd-l1来抑制t细胞的激活,所述双特异性抗体同时可靶向t细胞上的pd-1抗原,有效地避免了现有激活型双特异性抗体药物可能引起的进一步免疫抑制作用,而导致肿瘤杀伤作用降低。同时c-met功能域也赋予了pd-1功能域肿瘤特异性,以此提升pd-1抗体的响应率。本发明基于上述构思完成。
[0011]
一方面,本发明提供了一种双特异性抗体,它包含特异性识别t淋巴细胞pd-1抗原的第一功能域和特异性识别肿瘤细胞c-met抗原的第二功能域,亦称为diabody。
[0012]
该双特异性抗体包括抗体轻重链可变区及gly4ser连接肽。
[0013]
本发明的双特异性抗体含有抗pd-1抗体轻链可变区单元,较好的,其核苷酸序列如seq id no:1所示。
[0014]
本发明的双特异性抗体含有抗pd-1抗体重链可变区单元,较好的,其核苷酸序列如seq id no:2所示。
[0015]
本发明的双特异性抗体含有抗c-met抗体轻链可变区单元,较好的,其核苷酸序列如seq id no:3所示。
[0016]
本发明的双特异性抗体含有抗c-met抗体重链可变区单元,较好的,其核苷酸序列如seq id no:4所示。
[0017]
本发明的双特异性抗体含有gly4ser连接肽,较好的,其核苷酸序列如seq id no:5所示。
[0018]
本发明的双特异性抗体中,分别将抗pd-1及c-met抗体的轻重链可变区交叉配对并通过gly4ser连接肽进行连接。
[0019]
本发明的双特异性抗体中,抗pd-1vh的n末端连接于抗c-met vl的c末端,抗c-met vh的n末端连接于抗pd-1vl的c末端,最后通过gly4ser连接肽形成柔性肽将抗pd-1vh的c末端连接于其vl的n末端。
[0020]
在本发明的一个优选例中,所述的gly4ser连接肽有3个单元。
[0021]
本发明的双特异性抗体中,两端抗c-met轻重链聚合形成二聚化抗c-met可变区,中间部位形成抗pd-1scfv。
[0022]
较好的,本发明的双特异性抗体具有开口式二聚化结构,与肿瘤抗原c-met具有更高的结合能力,故形成具有双靶点亲和力差异的单链小分子双特异性抗体diabody。
[0023]
本发明提供了该双特异性抗体的制备方法,包括:
[0024]
设计所述的双特异性抗体;
[0025]
利用计算机蛋白质同源建模、优化和对接技术辅助设计。
[0026]
较好的,该制备方法还包括评估双特异性抗体的结构与合理性。
[0027]
在评估基础上不断优化建模,如此循环,最终获得本发明的双特异性抗体。
[0028]
本发明的结构设计合理性通过使用计算机分子模拟软件discovery studio进行评估。在ds数据库中搜索高分同源性模板序列,将目标序列与其进行比对及叠合,对所述结构双特异性抗体diabody进行蛋白质同源建模及优化,使用ramanchandran plot评估模型结构。再利用zdock将双特异性抗体diabody分别与pdb数据库中的c-met抗原(pdb id:2rfs)及pd-1胞外段(pdb id:3rrq)晶体结构进行对接运算,对接构型利用rdock进行优化,使用能量打分函数进行打分。最后运用预处理的隐马尔科夫模型对抗体cdr区进行识别和注释,通过分析改造后抗原抗体相互作用界面rmsd及非键相互作用变化来评估双特异性抗体diabody的合理性和特性。
[0029]
本发明提供了该双特异性抗体的应用,即在制备治疗实体瘤药物中的应用。
[0030]
较好的,所述的实体瘤药物针对表达c-met抗原的瘤体或者肿瘤细胞。
[0031]
本发明主要为实体瘤的应用治疗提供基础,所述双特异性抗体diabody为小分子的non-igg-like双特异性抗体,仅含有抗体轻重链可变区,故本发明具有极强的组织渗透性、较大的分布容积且有效剂量低。所述双特异性抗体不含fc段,能够在联合t细胞发挥持续性杀伤作用的同时,避免通过fc段引发adcc、cdc作用和介导-型超敏反应等可能引起的强烈机体毒性反应。
[0032]
进一步地,所述双特异性抗体diabody具有双靶点亲和力差异,本发明与肿瘤抗原c-met具有更高的亲和力,使其能够优先靶向肿瘤,然后募集并激活t细胞发挥杀伤作用,致使进入体内的药物大量暴露于肿瘤部位,增强杀伤作用的同时降低对正常组织的毒性。
[0033]
具体地,本发明通过形成不同构型的抗体功能域产生了具有双靶点亲和力差异的单链小分子双特异性抗体diabody。所述双特异性抗体diabody的抗pd-1及c-met抗体的轻重链可变区交叉配对并通过gly4ser连接肽进行连接,pd-1可变区轻重链再由3个gly4ser连接肽形成中间部位的pd-1scfv,连接在pd-1scfv n末端和c末端的c-met可变区轻重链二聚化,最终形成高亲和力靶向肿瘤抗原c-met的双特异性抗体diabody。
[0034]
另一方面,本发明提供了该双特异性抗体的核酸序列。
[0035]
本发明还提供了含有该双特异性抗体核酸编码序列的表达载体,例如,在本发明的一个实施例中采用pcep4载体。
[0036]
本发明提供了表达该双特异性抗体抗体的细胞。
[0037]
在本发明的一个优选实施例中,该细胞是经过ebna1改造的人胚肾293细胞hek293e。
[0038]
本发明涉及的术语和缩略语如下:
[0039]
pd-1:程序性死亡受体1(programmed cell death protein 1)。
[0040]
c-met:肝细胞生长因子受体(mesenchymal epithelial transition factor)。
[0041]
hgf:肝细胞生长因子(hepatocyte growth factor)。
[0042]
scfv:单链可变区抗体片段(single-chain variable fragment)。
[0043]
vh:重链可变区(heavy chain variable region)。
[0044]
vl:轻链可变区(light chain variable region)。
[0045]
ebna1:eb病毒核抗原(epstein-barr virus nuclear antigen 1)。
[0046]
fc:可结晶片段(fragment crystallizable)。
[0047]
cdr:互补性决定区(complementarity determining region)。
[0048]
adcc:抗体依赖的细胞毒性作用(antibody-dependent cell-mediated cytotoxicity)。
[0049]
cdc:补体依赖的细胞毒性作用(complement-dependent cytotoxicity)。
[0050]
rmsd:均方根偏差(root mean square deviation)。
[0051]
pbmcs:外周血单个核细胞(peripheral blood mononuclear cells)。
[0052]
tils:肿瘤浸润淋巴细胞(tumor infiltrating lymphocyte)。
[0053]
pei:聚乙烯亚胺(polyethylenimine)。
[0054]
fitc:异硫氰酸荧光素(fluorescein isothiocyanate)。
[0055]
pha-l:植物血凝素(phytohemagglutinin-l)。
[0056]
sds-page:十二烷基硫酸钠聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate polyacrylamide gel electrophoresis)。
[0057]
pbs:磷酸缓冲盐溶液(phosphate buffer saline)。
[0058]
ldh:乳酸脱氢酶(lactate dehydrogenase)。
[0059]
本发明提供了一种抗pd-1抗原和抗c-met抗原的小分子双特异性抗体diabody,并在计算机蛋白质同源建模、对接和优化的基础上设计与评估双特异性抗体的结构及其合理性。具有单链开口式二聚化结构的diabody能够优先结合肿瘤细胞表面的c-met抗原,再通过结合t细胞表面的负性共刺激分子pd-1,在肿瘤周围募集t细胞,同时避免肿瘤细胞表面上调的pd-l1发挥抑制作用,促进t细胞激活,对肿瘤产生持续性杀伤。双特异性抗体diabody具有双靶点亲和力差异及小分子特性,在实体瘤中能达到更高的药物暴露水平,在增强杀伤作用的同时降低对正常组织的毒性。
附图说明
[0060]
图1是抗pd-1及c-met抗原的双特异性抗体diabody的分子结构示意图。
[0061]
图2是抗pd-1及c-met抗原的双特异性抗体diabody蛋白质模拟结果图。
[0062]
图3是抗pd-1及c-met抗原的双特异性抗体diabody的质粒图谱及引物序列。
[0063]
图4是双特异性抗体diabody蛋白质表达的sds-page电泳分析图。
[0064]
图5是双特异性抗体diabody蛋白质纯化的sds-page电泳分析图。
[0065]
图6是抗pd-1及c-met抗原的双特异性抗体diabody的流式结合图。
[0066]
图7是双特异性抗体diabody在体外抑制肿瘤细胞增殖的cck-8检测结果。
[0067]
图8是双特异性抗体diabody在体外抑制肿瘤细胞迁移的划痕实验结果图。
[0068]
图9是双特异性抗体diabody在体外抑制肿瘤细胞侵袭的transwell结果图。
[0069]
图10是diabody体外激活tils中cd4和cd8t细胞的流式散点图。
[0070]
图11是在不同效靶比情况下diabody对肿瘤细胞ldh释放水平的测定。
[0071]
图12是diabody作用下t细胞的细胞因子il-2和ifn-γ分泌水平的检测。
具体实施方式
[0072]
下面结合附图,对本发明的较优的实施例作进一步的详细说明。本发明的实验通常按照冷泉港实验室的《分子克隆实验指南》及常规实验步骤进行操作。
[0073]
本发明涉及序列如下:
[0074]
seq id no.1抗pd-1抗体轻链单元核苷酸序列:
[0075]
gagattgtcctcacccagtcaccggcaaccctgtcactgtcacccggagagcgcgccactctgtcttgcagagcatcccagagcgtgtccagctacctggcatggtaccagcagaagccaggccaggccccacggttgctgatttacgacgcgtccaaccgagctacaggaatccctgcacggttctcaggctccggatccggcacagattttaccctcacaatttcaagcctcgagccagaagactttgcggtgtactactgtcagcagagtagcaattggccccgcacatttggacagggtacaaaagtggaaataaagcgcactgtggctgctccaagcgtgttcatctttccgcccagcgacgaacaactgaaaagcgggactgcctccgtggtttgtctgctcaacaatttctatccccgcgaggccaaagtgcagtggaaggtcgacaatgccctccagtccggcaattcccaggaatccgttaccgagcaagatagtaaggatagcacctacagcctgtcctctacgctgacgctttccaaggcagactacgagaagcacaaagtgtatgcttgcgaggtcactcaccaggggttgagtagcccagtaacaaaatcatttaaccggggagaatgt。
[0076]
seq id no.2抗pd-1抗体重链单元核苷酸序列:
[0077]
caggtgcagctggtcgagtcaggcggaggtgtcgttcaaccaggacgctccctgagactggactgcaaggcgtccggaataaccttctccaatagcggcatgcactgggttcgacaggcacctgggaaaggcctggaatgggtggccgtgatctggtatgacggcagcaagcgctactatgccgatagtgtgaagggtcgcttcacaatttcccgcgataatagcaagaacactctgttcctgcagatgaactctcttagagcggaggacacagccgtgtactattgcgcaactaatgacgattactggggccaaggtacgttggtcactgtcagctccgccagcacaaaaggacccagcgtgttccccttggccccctctagcaaaagcacatcagggggtaccgcagcgctggggtgcctcgtgaaagattactttcctgagccagtgaccgtctcttggaactcaggagcgctgacctctggtgtccacaccttccctgccgtgttgcagtccagcggactgtacagcttgagcagcgtcgtgacggttccctcttcatccctgggtacccagacctacatttgcaatgtcaaccataagccaagcaacacaaaggtggacaagaaggtcgaacccaaatcttgcgataagactcatacctgcccaccgtgcccggcccccgaattgctcggaggaccgagcgtttttttgttccccccaaagcccaaggatactctcatgatttcacgaaccccagaggtgacatgtgtcgtagtcgacgtgtcacatgaggatcctgaggtgaaattcaactggtatgtagacggtgtcgaggtgcacaacgcgaagaccaaaccccgcgaggaacagtacaatagcacgtatagagttgtttcagttctgaccgttctgcatcaggactggctgaatggcaaagaatacaaatgcaaggtttcaaataaagcactgcccgccccgatagagaagaccatctctaaggcaaagggccagcccagggaaccccaggtttatacgctccctccctcaagagaggaaatgactaaaaaccaggtttcactgtggtgcctggtcaaggggttttatccatctgatatcgctgtggaatgggagtccaatggccaacccgagaacaactataagactacgccgccagttctggattcagacgggtcctttttcctgtacagcaaactgacagtggataagtcccgatggcagcagggaaatgttttttcatgctctgtgatgcatgaggccctccacaaccattacacccagaagagtttgagcctcagcccaggcaag。
[0078]
seq id no.3抗c-met抗体轻链可变区核苷酸序列:
[0079]
gacatccagatgacccagtccccatcaagcttgtcagccagcgttggcgaccgcgttacaatcacctgcaagagctctcagagcctcttgtatacatcaagccagaaaaactatctggcctggtatcaacagaaacctgggaag
gcccccaagctgctgatctactgggcttccacacgagagagcggtgtccctagccgcttcagcggatccgggagcggcaccgattttacacttactatttccagtctccaaccagaggactttgcaacctattactgtcagcagtattacgcatatccctggactttcgggcagggcaccaaagtggagatcaagcga。
[0080]
seq id no.4抗c-met抗体重链可变区核苷酸序列:
[0081]
gaggttcaactggtcgagagcggaggaggactggtgcagccaggaggatcactgcgccttagctgtgctgcctccgggtacacttttaccagttactggctgcactgggtgcggcaggcaccaggcaagggtctggagtgggtaggtatgattgatccctcaaactccgacacgaggtttaatcctaatttcaaagaccgctttaccatatcagcggatacctccaagaatactgcctaccttcaaatgaacagccttcgcgccgaggatacagctgtttattactgcgccacctaccgatcatatgtgacacccttggattactggggccagggaaccctggtcacagtcagcagc。
[0082]
seq id no.5gly4ser连接肽核苷酸序列:
[0083]
ggaggaggcggcagtggaggagggggctccggagggggaggtagc。
[0084]
实施例1:双特异性抗体diabody的结构设计
[0085]
为了提高双特异性抗体diabody与肿瘤的结合力,将抗肿瘤抗原c-met抗体可变区以二聚化的形式结合,所以将其轻重链分别连接在pd-1scfv的n末端和c末端,以形成具有双靶点亲和力差异的双特异性抗体。diabody的n末端添加信号肽,c末端携带六组氨酸his-tag标签,以便后续纯化及鉴定工作。
[0086]
实施例2:通过蛋白质结构同源建模评估设计结构合理性
[0087]
利用discovery studio软件,首先载入diabody氨基酸序列,并在在ds数据库中搜索与目标序列同源性最高的模板序列,接着将所选择的高分模板序列与目标序列进行比对,随后进行叠合,最后利用modeler构建目标序列的3d模型,根据pdf或dope值挑选最优模型,最后使用ramanchandran plot评估模型,可见95%以上的氨基酸骨架结构是合理的。
[0088]
实施例3:双特异性抗体diabody表达质粒构建
[0089]
以实验室前期筛选的c-met及pd-1抗体序列为模板,设计合理的引物并通过重叠延伸pcr构建目的基因。
[0090]
db-ml-f:ctgtggttccccggctcgcgatgtgacatccagatgacccag,seq id no 6。
[0091]
db-ml-r:gcttcctcctccgcctcgcttgatctccacttt,seq id no 7。
[0092]
db-ph-f:ggcggaggaggaagccaggtgcagttggtcgaa,seq id no 8。
[0093]
db-ph-r:cacgatctctgagccgccgccaccggaacctccgcctccggaaccaccacctccacttgacaccg,seq id no 9。
[0094]
db-pl-f:gtgtcaagtggaggtggtggttccggaggcggaggttccggtggcggcggctcagagatcgtg,seq id no 10。
[0095]
db-pl-r:gcttcctcctccgcctctcttgatctccacctt,seq id no 11。
[0096]
db-mh-f:ggcggaggaggaagcgaggttcaactggtcgag,seq id no 12。
[0097]
db-mh-r:ccttgccggcctcgagcggccgcttaatggtgatggtgatgatggctgctgactgtgaccaggg,seq id no 13。
[0098]
引物db-ml-f及db-ml-r扩增c-met vl,引物db-mh-f及db-mh-r扩增c-met vh,引物db-pl-f及db-pl-r扩增pd-1vl,引物db-ph-f及db-ph-r扩增pd-1vh,引物db-ml-f及db-ph-r扩增c-met vl-pd-1vh,引物db-pl-f及db-mh-r扩增pd-1vl-c-met vh,引物db-ml-f及db-mh-r扩增全长diabody,并在diabody的n末端和c末端分别引入了信号肽和his-tag标
签。接着利用重组反应将目的基因连接到线性化真核表达载体pcep4中。最后转化大肠杆菌,挑取阳性单克隆,扩增并抽提质粒,测序鉴定。
[0099]
实施例4:双特异性抗体diabody蛋白的表达
[0100]
将hek293e细胞由贴壁驯化为无血清悬浮培养,待达到对数生长期时,将阳离子转染试剂pei与携带有diabody目的基因的表达质粒按比例混合,以等量pei为空白对照,转染hek293e细胞,24hr后添加辅料,隔天收集100μl上清待鉴定。通过sds-page凝胶电泳和考马斯亮蓝染色分析蛋白表达情况,在目的蛋白分子量位置处,实验组比起对照组有明显的蛋白质生成。待细胞活性下降到75%以下后,离心收细胞上清,过滤除菌后-20℃保存待纯化。
[0101]
实施例5:双特异性抗体diabody蛋白的纯化
[0102]
将预装镍柱连接到akta蛋白纯化系统中,用3-5倍柱体积的去离子水冲洗出储存缓冲液,使用至少5倍柱体积的结合缓冲液平衡柱子,将含his-tag标签蛋白的样品过柱,控制流速,收集流出液待后续分析,用10倍柱体积的洗涤缓冲液冲洗柱子以去除杂蛋白,直到流出液的a280达到最低且稳定后,用5-10倍柱体积含咪唑的洗脱液进行梯度洗脱,收集洗脱液待鉴定。通过bca蛋白定量试剂盒测定其表达量约为10mg/l。
[0103]
实施例6:通过流式细胞术检测diabody抗体抗原结合特异性
[0104]
将diabody作为一抗,分别与稳定表达pd-1胞外段的cho细胞和表达c-met的胃癌细胞mkn45共孵育,以pbs为空白对照,洗涤3次,加入fitc标记的anti-his-tag二抗,洗涤3次,使用流式细胞仪分析荧光强度变化。pd-1和c-met实验组的荧光强度增强说明diabody能够结合细胞表面表达的pd-1及c-met,具有抗体抗原结合特异性。
[0105]
实施例7:通过检测cck-8测定diabody对肿瘤细胞增殖的抑制作用
[0106]
将a549接种于96孔板中,贴壁过夜,分别加入不同浓度的双特异性抗体diabody,以pbs为空白对照,同时加入hgf刺激,3天后利用cck-8检测a549增殖。随着diabody浓度的提高,实验组明显能够抑制hgf刺激所导致的a549增殖。a549贴壁后加入diabody,以pbs为空白对照,以c-met小分子抑制剂jnj-38877605为阳性对照,比较加药后5天内肿瘤细胞增殖的变化,diabody和jnj-38877605均能有效抑制a549增殖,且在72hr后,diabody的抑制作用明显强于jnj-38877605,说明比起c-met小分子抑制剂其具有更加持久的药效。
[0107]
实施例8:通过划痕实验检测diabody对肿瘤细胞迁移的抑制
[0108]
将a549细胞接种于六孔板中,贴壁24hr待到汇合率达到100%,用1ml枪头快速用力均匀地在培养皿中划痕,pbs洗涤2次,去除划下的细胞,加入含diabody的1640培养基,以等体积pbs为空白对照,以jnj-38877605为阳性对照,同时加入hgf刺激,通过拍照记录0、24、48hr时细胞迁移的情况。diabody能够明显抑制hgf引起的a549细胞迁移。
[0109]
实施例9:通过transwell测定diabody对肿瘤细胞侵袭的抑制
[0110]
将准备好的matrigel冰浴融化,以50μl体积铺于transwell小室(24孔板)的聚碳酸酯膜上,37℃放置1h,使其聚合成凝胶。在下室中加入含20%血清的1640培养基,将对数生长期的a549消化离心后用1640培养基重悬,调整细胞浓度,取200ul至上室中,并在其中添加diabody处理,以等体积pbs为对照,以jnj-38877605为阳性对照,同时加入hgf刺激,置于5%co2培养箱于37℃培养24h。待培养时间结束后,弃去上室液体,用湿棉签擦去膜上未穿过膜的细胞,4%多聚甲醛室温固定,0.1%结晶紫染色,pbs洗涤3次,干燥后倒置显微镜下观察穿过膜的细胞。diabody能够明显抑制hgf刺激所促进的a549侵袭运动。
[0111]
实施例10:流式细胞术测定diabody对肝癌中肿瘤浸润t淋巴细胞的激活
[0112]
肿瘤医院收集肝细胞癌病人肝癌组织和外周血,通过ficoll分离pbmcs,肝癌组织消化后,通过percoll分离肝癌组织中的tils。将tils与原代肝癌细胞共培养,加入diabody处理,以等体积pbs为对照,最后通过流式细胞术分析cd69表达,检测外周血和肿瘤组织中cd4和cd8t细胞的激活情况。相较于对照组pbmcs与tils,diabody能够激活tils中被肿瘤细胞抑制的cd4和cd8t细胞。
[0113]
实施例11:diabody在不同效靶比情况下对肿瘤细胞的杀伤作用
[0114]
mcc-97h细胞贴壁24hr后,ifn-γ刺激24hr使其表达pd-l1,分离健康人外周血中的t细胞,pha-l刺激48hr使其表达pd-1。然后将二者以不同效靶比进行共孵育培养,再加入diabody处理,以等体积pbs为对照,48hr后检测培养上清中ldh的释放水平,并计算杀伤率。随着效靶比的升高,t细胞的杀伤作用增强,且diabody能增强其杀伤作用。
[0115]
实施例12:diabody促进t细胞分泌细胞因子ifn-γ和il-2
[0116]
mkn45细胞贴壁24hr,ifn-γ刺激24hr,分离的人t细胞用pha-l刺激48hr,将二者以效靶比64:1共孵育培养,加入不同浓度的diabody处理,以等体积pbs为对照,5%co2培养箱37℃培养48hr,最后通过elisa检测细胞上清中ifn-γ和il-2的分泌水平。diabody能促进t细胞激活分泌细胞因子,且随着浓度的升高,激活作用增强。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



