用于有机发光二极管的物质组合物的制作方法
 2021-02-02 14:02:55|
2021-02-02 14:02:55| 356|
356| 起点商标网
起点商标网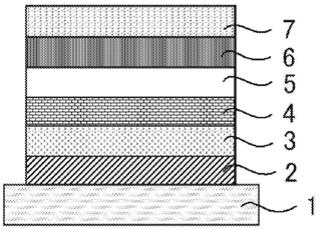
用于有机发光二极管的物质组合物
[0001]
相关申请
[0002]
本申请主张2018年3月30日提交的美国临时专利申请第62/650,414号;2018年4月5日提交的美国临时专利申请第62/653,133号;2018年4月5日提交的美国临时专利申请第62/653,224号;2018年4月17日提交的美国临时专利申请第62/658,842号;2018年4月17日提交的美国临时专利申请第62/658,845号;2018年4月25日提交的美国临时专利申请第62/662,550号;及2018年4月25日申请的美国临时专利申请第62/662,552号的优先权。
背景技术:
[0003]
有机发光二极管(oled)是一种将有机化合物膜置于两个导体之间的发光二极管(led),该膜响应于电流等激发而发光。oled可用于照明和显示器中,例如电视屏幕、计算机显示器、移动电话和平板电脑。oled显示器的内在问题是有机化合物有限的寿命。尤其,发射蓝光的oled与绿色或红色oled相比,以显著增加的速率劣化。
[0004]
oled材料取决于由主体传输材料中的电子和空穴的重组而生成的分子激发态(激子)的辐射衰减。激发的性质引起电子与空穴之间的相互作用,该作用使激发态分裂成亮单重态(总自旋为0)和暗三重态(总自旋为1)。由于电子和空穴的重组会提供四种自旋状态的统计混合物(一个单重态和三个三重态子级),因此常规oled的最大理论效率为25%。
[0005]
目前为止,oled材料设计通常集中在收集来自暗三重态的剩余能量。制作一般从暗三重态发光的高效磷光体的近期研究已经实现了绿色和红色oled。然而,蓝色等其它颜色需要较高的能量激发态(加速oled的劣化过程)。
[0006]
对三重态-单重态跃迁速率的基本限制因素是参数|hfi/δest|2的值,其中hfi是由超精细相互作用或自旋-轨道作用所致的耦合能量,并且δest是单重态与三重态之间的能量分裂。传统的磷光oled取决于由自旋-轨道(so)作用所致的单重态与三重态的混合、hfi的增加及得到在重金属原子与有机配位体之间共用的最低发射态。由此,从所有更高的单重态和三重态收集能量,接下来是磷光(源自激发三重态的寿命相对短的发射)。缩短的三重态寿命会减少由电荷和其它激子引发的三重态激子湮灭。根据其他研究人员的近期研究表明,已经达到磷光材料的性能极限。
技术实现要素:
[0007]
本发明涉及一种用于oled的新颖材料。在一些实施方式中,这些oled能够达到更高的激发态而不会快速劣化。现已发现,取决于δe
st
的最小化而不是h
fi
的最大化的热激活延迟荧光(tadf)能够在单重态能级与三重态子级之间,在相关时间尺度(例如1μs~100ms)内转移粒子数(population)。本说明书中记载的化合物能够在比以往记载的化合物更高的能量激发态下发光。
[0008]
在一些实施方式中,本发明提供通式(i)的化合物:
[0009][0010]
其中
[0011]
r1、r2、r3、r4及r5独立地选自氢、氘、a1、ar1及d1;
[0012]
r1、r2、r3、r4及r5中的至少一个为a1;
[0013]
r1、r2、r3、r4及r5中的至少一个为d1;
[0014]
a1独立地选自
[0015][0016][0017]
x
a
独立地选自o、s及nr
a
’
;
[0018]
r
a
独立地选自氢、氘、卤素、氰基、经取代或未经取代的烷基、经取代或未经取代的烷氧基、经取代或未经取代的芳基、经取代或未经取代的芳氧基、经取代或未经取代的杂芳基、经取代或未经取代的杂芳氧基及甲硅烷基;
[0019]
r
a
的2个以上的例子能够结合而形成环体系;
[0020]
r
a
’
独立地选自氢、氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基;
[0021]
r
a
’
及r
a
的2个以上的例子能够结合而形成环体系;
[0022]
l
a
独立地选自单键、经取代或未经取代的亚芳基及经取代或未经取代的杂亚芳基;其中亚芳基和杂亚芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代;这些取代基中的2个以上能够结合而形成环体系;
[0023]
d1独立地选自
[0024][0025][0026]
x
d
独立地选自o、s、nr
d
’
、c(o)、经取代或未经取代的亚甲基、经取代或未经取代的亚乙基、经取代或未经取代的亚乙烯基、经取代或未经取代的邻亚芳基及经取代或未经取代的邻杂亚芳基;其中亚甲基、亚乙基、亚乙烯基、邻亚芳基或邻杂亚芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代;
[0027]
r
d
独立地选自氢、氘、经取代或未经取代的烷基、经取代或未经取代的烷氧基、经取代或未经取代的氨基、经取代或未经取代的芳基、经取代或未经取代的芳氧基、经取代或未经取代的杂芳基、经取代或未经取代的杂芳氧基及甲硅烷基;
[0028]
r
d
的2个以上的例子能够结合而形成环体系;
[0029]
r
d
’
独立地选自氢、氘、经取代或未经取代的烷基、经取代或未经取代的氨基、经取代或未经取代的芳基及经取代或未经取代的杂芳基;
[0030]
r
d
’
及r
d
的2个以上的例子能够结合而形成环体系;
[0031]
l
d
独立地选自单键、经取代或未经取代的亚芳基及经取代或未经取代的杂亚芳基;其中亚芳基和杂亚芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代;这些取代基中的2个以上能够结合而形成环体系;
[0032]
ar1独立地选自不包含任何氮原子的经取代或未经取代的杂芳基;其中芳基及杂芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代;这些取代基中的2个以上能够结合而形成环体系;
[0033]
每个“*”表示与通式(i)的连接点。
[0034]
在一些实施方式中,本发明提供通式(ii)的化合物:
[0035][0036]
其中
[0037]
a选自
[0038][0039]
d独立地选自h、me、ph、
[0040]
[0041][0042]
r独立地选自h、me及ph;
[0043]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0044]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0045]
所出现的至少一个d选自d1-d31。
[0046]
在一些实施方式中,本发明提供通式(iii)的化合物:
[0047][0048]
其中
[0049]
a选自
[0050][0051]
d独立地选自
[0052]
[0053]
[0054][0055]
r独立地选自h、me及ph;
[0056]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0057]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0058]
d的至少一个例子选自d1-d31。
[0059]
在一些实施方式中,本发明提供通式(iii)的化合物:
[0060][0061]
其中
[0062]
a选自
[0063]
[0064][0065]
d独立地选自h、氘、ph、
[0066]
[0067][0068]
r独立地选自h、me及ph;
[0069]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0070]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0071]
d的至少一个例子选自d1-d31;
[0072]
d的至少一个例子选自h、氘或ph。
[0073]
在一些实施方式中,本发明提供通式(iv)的化合物:
[0074][0075]
其中
[0076]
a选自
[0077][0078][0079]
d独立地选自
[0080]
[0081][0082]
r独立地选自h、me及ph;
[0083]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0084]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0085]
d的至少一个例子选自d1-d31。
[0086]
在一些实施方式中,本发明提供通式(iv)的化合物:
[0087][0088]
其中
[0089]
a选自
[0090][0091]
d独立地选自h、氘、ph、
[0092]
[0093][0094]
r独立地选自h、me及ph;
[0095]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0096]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0097]
d的至少一个例子选自d1-d31;
[0098]
d的至少一个例子选自h、ph或氘。
[0099]
在一些实施方式中,本发明提供包含通式(i)、(ii)、(iii)或(iv)的化合物的延迟荧光发射体。
[0100]
在一些实施方式中,本发明提供包含通式(i)、(ii)、(iii)或(iv)的化合物的有机发光二极管(oled)。
[0101]
在一些实施方式中,本说明书提供一种有机发光二极管(oled),其包含阳极、阴极及至少一个包含位于所述阳极与所述阴极之间的发光层的有机层,所述发光层包含:
[0102]
主体材料;及
[0103]
通式(i)、(ii)、(iii)或(iv)的化合物。
[0104]
在一些实施方式中,本说明书提供一种有机发光二极管(oled),其包含阳极、阴极及至少一个包含位于所述阳极与所述阴极之间的发光层的有机层,所述发光层包含:
[0105]
主体材料;及
[0106]
通式(i)、(ii)、(iii)或(iv)的化合物(其中通式(i)、(ii)、(iii)或(iv)的化合物为发光材料)。
[0107]
在一些实施方式中,本说明书提供一种有机发光二极管(oled),其包含阳极、阴极及至少一个包含位于所述阳极与所述阴极之间的发光层的有机层,所述发光层包含:
[0108]
主体材料;
[0109]
通式(i)、(ii)、(iii)或(iv)的化合物;及
[0110]
发光材料,其不是通式(i)、(ii)、(iii)或(iv)的化合物。
[0111]
在一些实施方式中,本说明书提供一种有机发光二极管(oled),其包含阳极、阴极及至少一个包含位于所述阳极与所述阴极之间的发光层的有机层,所述发光层包含:
[0112]
通式(i)、(ii)、(iii)或(iv)的化合物;及
[0113]
发光材料,其不是通式(i)、(ii)、(iii)或(iv)的化合物。
[0114]
在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物用于屏幕或显示器中。
[0115]
在又一方式中,本发明涉及一种oled显示器的制造方法,所述方法包括:
[0116]
在母板的主基板上形成阻挡层的步骤;
[0117]
在所述阻挡层上,以单元面板为单位形成多个显示单元的步骤;
[0118]
在所述单元面板的每个所述显示单元上形成封装层的步骤;及
[0119]
在单元面板之间的界面部分贴附有机膜的步骤。
附图说明
[0120]
图1是示意图,其中1表示基板,2表示阳极,3表示空穴注入层,4表示空穴传输层,5表示发光层,6表示电子传输层,7表示阴极。
具体实施方式
[0121]
在一方式中,本发明提供通式(i)的化合物:
[0122][0123]
其中
[0124]
r1、r2、r3、r4及r5独立地选自氢、氘、a1、ar1及d1;
[0125]
r1、r2、r3、r4及r5中的至少一个为a1;
[0126]
r1、r2、r3、r4及r5中的至少一个为d1;
[0127]
a1独立地选自
[0128][0129]
x
a
独立地选自o、s及nr
a
’
;
[0130]
r
a
独立地选自氢、氘、卤素、氰基、经取代或未经取代的烷基、经取代或未经取代的烷氧基、经取代或未经取代的芳基、经取代或未经取代的芳氧基、经取代或未经取代的杂芳基、经取代或未经取代的杂芳氧基及甲硅烷基;
[0131]
r
a
的2个以上的例子能够结合而形成环体系;
[0132]
r
a
’
独立地选自氢、氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基;
[0133]
r
a
’
及r
a
的2个以上的例子能够结合而形成环体系;
[0134]
l
a
独立地选自单键、经取代或未经取代的亚芳基及经取代或未经取代的杂亚芳基;其中亚芳基和杂亚芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代;这些取代基中的2个以上能够结合而形成环体系;
[0135]
d1独立地选自
[0136][0137]
x
d
独立地选自o、s、nr
d
’
、c(o)、经取代或未经取代的亚甲基、经取代或未经取代的亚乙基、经取代或未经取代的亚乙烯基、经取代或未经取代的邻亚芳基及经取代或未经取代的邻杂亚芳基;其中亚甲基、亚乙基、亚乙烯基、邻亚芳基或邻杂亚芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代;
[0138]
r
d
独立地选自氢、氘、经取代或未经取代的烷基、经取代或未经取代的烷氧基、经取代或未经取代的氨基、经取代或未经取代的芳基、经取代或未经取代的芳氧基、经取代或未经取代的杂芳基、经取代或未经取代的杂芳氧基及甲硅烷基;
[0139]
r
d
的2个以上的例子能够结合而形成环体系;
[0140]
r
d
’
独立地选自氢、氘、经取代或未经取代的烷基、经取代或未经取代的氨基、经取代或未经取代的芳基及经取代或未经取代的杂芳基;
[0141]
r
d
’
及r
d
的2个以上的例子能够结合而形成环体系;
[0142]
l
d
独立地选自单键、经取代或未经取代的亚芳基及经取代或未经取代的杂亚芳基;其中亚芳基和杂亚芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代;这些取代基中的2个以上能够结合而形成环体系;
[0143]
ar1独立地选自不包含任何氮原子的经取代或未经取代的杂芳基;其中芳基及杂芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代;这些取代基中的2个以上能够结合而形成环体系;
[0144]
每个“*”表示与通式(i)的连接点。
[0145]
在一些实施方式中,通式(i)的化合物选自
[0146][0147]
在一些实施方式中,通式(i)的化合物选自
[0148][0149]
在一些实施方式中,通式(i)的化合物选自
[0150][0151]
在一方式中,本发明提供通式(ii)的化合物:
[0152][0153]
其中
[0154]
a选自
[0155][0156][0157]
d独立地选自h、me、ph、
[0158]
[0159][0160]
r独立地选自h、me及ph;
[0161]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0162]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0163]
所出现的至少一个d选自d1-d31。
[0164]
在一方式中,本发明提供通式(iii)的化合物:
[0165][0166]
其中
[0167]
a选自
[0168][0169][0170]
d独立地选自
[0171]
[0172][0173]
r独立地选自h、me及ph;
[0174]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0175]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0176]
d的至少一个例子选自d1-d31。
[0177]
在一方式中,本发明提供通式(iii)的化合物:
[0178][0179]
其中
[0180]
a选自
[0181][0182]
d独立地选自h、氘、ph、
[0183]
[0184][0185]
r独立地选自h、me及ph;
[0186]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0187]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0188]
d的至少一个例子选自d1-d31;
[0189]
d的至少一个例子选自h、氘或ph。
[0190]
在一方式中,本发明提供通式(iv)的化合物:
[0191][0192]
其中
[0193]
a选自
[0194][0195]
d独立地选自
[0196]
[0197]
[0198][0199]
r独立地选自h、me及ph;
[0200]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0201]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0202]
d的至少一个例子选自d1-d31。
[0203]
在一方式中,本发明提供通式(iv)的化合物:
[0204][0205]
其中
[0206]
a选自
[0207]
[0208][0209]
d独立地选自h、氘、ph、
[0210]
[0211][0212]
r独立地选自h、me及ph;
[0213]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0214]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0215]
d的至少一个例子选自d1-d31;
[0216]
d的至少一个例子选自h、ph或氘。
[0217]
实施例用于说明本发明而并不限制本发明。实际上,对本领域技术人员来说显而易见,在不脱离本发明的范围或宗旨的情况下,能够对本发明进行各种修改和变更。例如,作为一实施方式的一部分而进行说明或描述的特征可以用于另一实施方式以作为又一实施方式。因此,本发明意欲包括在所附权利要求及其等效内容的范围内的这些修改和变更。本发明的其它目的、特征及方式公开于以下详细说明中或可以衍生自以下详细说明。本领域技术人员应理解,本说明书仅是对示例性实施方式的说明,不应解释为限定本发明的更广的方式。
[0218]
定义
[0219]
若本说明书中没有特别说明,则在本申请中所用的科学和技术性术语应具有本领域技术人员通常理解的含义。通常,本说明书中记载的化学相关性使用中的命名法及化学技术是在本领域中熟知和常用的内容。
[0220]
本领域公认的术语“酰基”是指由通式烃基c(o)-(优选为烷基c(o)-)表示的基团。
[0221]
本领域公认的术语“酰胺基”是指被酰基取代的氨基,并且例如可以由通式烃基c(o)nh-表示。
[0222]
本领域公认的术语“酰氧基”是指由通式烃基c(o)o-(优选为烷基c(o)o-)表示的基团。
[0223]
术语“烷氧基”是指键合有氧的烷基。在一些实施方式中,烷氧基具有1~20个碳。在一些实施方式中,烷氧基具有1~12个碳原子。代表性烷氧基包括甲氧基、三氟甲氧基、乙氧基、丙氧基、叔丁氧基等。
[0224]
术语“烷氧基烷基”是指被烷氧基取代的烷基,并且可以由通式烷基-o-烷基表示。
[0225]
本说明书中使用的术语“烯基”是指包含至少一个双键且包括“未经取代的烯基”和“经取代的烯基”这两者的脂肪族基团,其中后者是指具有取代基(取代烯基的一个以上碳上的氢)的烯基部分。通常,若没有特别说明,则直链或支链烯基具有1~约20个碳原子,优选具有1~约12个碳原子。此类取代基可以在包括或未包括在一个以上双键中的一个以上的碳上出现。而且,如下所述,除了稳定性受阻的情况以外,此类取代基包括所有预期用作烷基的取代基。例如,可以预期用一个以上烷基、碳环基、芳基、杂环基或杂芳基取代烯基。
[0226]“烷基”或“烷烃”是完全饱和的直链或支链非芳香族烃。通常,若没有特别说明,则直链或支链烷基具有1~约20个碳原子,优选具有1~约12个碳原子。在一些实施方式中,烷基具有1~8个碳原子、1~6个碳原子、1~4个碳原子或1~3个碳原子。直链和支链烷基的例子包括甲基、乙基、正丙基、异丙基、正丁基、仲丁基、叔丁基、戊基、己基、戊基和辛基。
[0227]
另外,在整个说明书、实施例及权利要求中使用的术语“烷基”意欲包括“未经取代的烷基”和“经取代的烷基”这两者,其中后者是指具有取代基(取代烃骨架的一个以上可取代碳上的氢)的烷基部分。若没有特别说明,则此类取代基例如可以包括卤素(例如氟)、羟基、羰基(如羧基、烷氧基羰基、甲酰基或酰基)、硫代羰基(如硫酯、硫代乙酸酯或硫代甲酸酯)、烷氧基、磷酰基、磷酸酯、膦酸酯、亚膦酸酯、氨基、酰胺基、脒、亚胺、氰基、硝基、叠氮
基、硫氢基、烷硫基、硫酸酯、磺酸酯、氨磺酰基、磺酰胺基、磺酰基、杂环基、芳烷基或芳香族或杂芳香族部分。在优选的实施方式中,经取代的烷基上的取代基选自c
1-6
烷基、c
3-6
环烷基、卤素、羰基、氰基或羟基。在更优选的实施方式中,经取代的烷基上的取代基选自氟、羰基、氰基或羟基。本领域的技术人员应理解,烃链上取代的部分在适当的时候本身可以被取代。例如,经取代的烷基的取代基可以包括经取代和未经取代形式的氨基、叠氮基、亚氨基、酰胺基、磷酰基(包括膦酸酯和亚膦酸酯)、磺酰基(包括硫酸酯、磺酰胺基、氨磺酰基和磺酸酯)和甲硅烷基,以及醚、烷硫基、羰基(包括酮、醛、羧酸盐及酯)、-cf3、-cn等。以下,对示例性经取代的烷基进行说明。环烷基可以进一步被烷基、烯基、烷氧基、烷硫基、氨基烷基、被羰基取代的烷基、-cf3、-cn等基团取代。
[0228]
与化学部分(例如,酰基、酰氧基、烷基、烯基、炔基或烷氧基)结合使用时,术语“c
x-y”表示包括在链中含有x~y个碳的基团。例如,术语“c
x-y
烷基”是指经取代或未经取代的饱和烃基(包括在链中包含x~y个碳的直链烷基和支链烷基),包括卤代烷基。优选的卤代烷基包括三氟甲基、二氟甲基、2,2,2-三氟乙基和五氟乙基。c0烷基表示基团位于末端位置的氢,若基团位于内部则表示键。术语“c
2-y
烯基”和“c
2-y
炔基”是指经取代或未经取代的不饱和脂肪族基团(具有与上述烷基类似的长度和取代可能性,但分别含有至少一个双键或三键)。
[0229]
本说明书中使用的术语“烷基氨基”是指被至少一个烷基取代的氨基。
[0230]
本说明书中使用的术语“烷硫基”是指被烷基取代的硫醇基,并且可以由通式烷基s-表示。
[0231]
本说明书中使用的术语“芳硫基”是指被烷基取代的硫醇基,并且可以由通式芳基s-表示。
[0232]
本说明书中使用的术语“炔基”是指包含至少一个三键的脂肪族基团,且包括“未经取代的炔基”和“经取代的炔基”这两者,其中后者是指具有取代基(取代炔基的一个以上碳上的氢)的炔基部分。通常,若没有特别说明,则直链或支链炔基具有1~约20个碳原子,优选具有1~约10个碳原子。此类取代基可以在包括或未包括在一个以上三键中的一个以上的碳上出现。而且,如上所述,除了稳定性受阻的情况以外,此类取代基包括所有预期用作烷基的取代基。例如,可以预期用一个以上烷基、碳环基、芳基、杂环基或杂芳基取代炔基。
[0233]
本说明书中使用的术语“酰胺”是指以下基团。
[0234][0235]
其中各个r
a
独立地表示氢或烃基,或两个r
a
与其所连接的n原子一同形成在环结构中具有4~8个原子的杂环。
[0236]
本领域公认的术语“胺”及“氨基”是指未经取代和经取代的胺和其盐,例如可以由下述式表示的部分。
[0237]
[0238]
其中各个r
a
独立地表示氢或烃基,或两个r
a
与其所连接的n原子一同形成在环结构中具有4~8个原子的杂环。
[0239]
本说明书中使用的术语“氨基烷基”是指被氨基取代的烷基。
[0240]
本说明书中使用的术语“芳烷基”是指被芳基取代的烷基。
[0241]
本说明书中使用的术语“芳基”包括环的每个原子均为碳的经取代或未经取代的单环芳香族基团。环优选为6~20元环,更优选为6元环。芳基优选具有6~40个碳原子,更优选具有6~25个碳原子。术语“芳基”还包括具有2个以上环(相邻的2个环共用2个碳)的多环体系,其中至少一个环是芳香族环,其它环例如可以是环烷基、环烯基、环炔基、芳基、杂芳基和/或杂环基。芳基包括苯、萘、菲、苯酚、苯胺等。
[0242]
本领域公认的术语“氨基甲酸酯”是指以下基团。
[0243][0244]
其中各个r
a
独立地表示氢或烃基(例如烷基),或两个r
a
与介入原子一同形成环结构中具有4~8个原子的杂环。
[0245]
本说明书中使用的术语“碳环(carbocycle/carbocyclic)”是指环的每个原子均为碳的饱和或不饱和环。碳环基优选具有3~20个碳原子。术语碳环包括芳香族碳环和非芳香族碳环两者。非芳香族碳环包括所有碳原子均饱和的环烷烃环和含有至少一个双键的环烯烃环两者。“碳环”包括5~7元单环和8~12元双环。双环碳环的每个环均可以选自饱和环、不饱和环及芳香族环。碳环包括在两个环之间共用一个、两个或三个以上原子的双环分子。术语“稠合碳环”是指每个环均与另一个环共用2个相邻原子的双环碳环。稠合碳环的每个环均可以选自饱和环、不饱和环及芳香族环。在一个示例性实施方式中,芳香族环(例如苯基(ph))可以与饱和或不饱和环(例如环己烷、环戊烷或环己烯)稠合。只要化合价允许,饱和双环、不饱和双环及芳香族双环的任意组合均在碳环的定义范围内。示例性“碳环”包括环戊烷、环己烷、双环[2.2.1]庚烷、1,5-环辛二烯、1,2,3,4-四氢萘、双环[4.2.0]辛-3-烯、萘和金刚烷。示例性稠合碳环包括十氢萘、萘、1,2,3,4-四氢萘、双环[4.2.0]辛烷、4,5,6,7-四氢-1h-茚和双环[4.1.0]庚-3-烯。“碳环”可以在能够载置氢原子的任何一个以上位置上被取代。
[0246]“环烷基”是完全饱和的环状烃。“环烷基”包括单环和双环。环烷基优选具有3~20个碳原子。通常,若没有特别说明,则单环环烷基具有3~约10个碳原子,更典型为具有3~8个碳原子。双环环烷基的第二个环可以选自饱和环、不饱和环及芳香族环。环烷基包括在两个环之间共用一个、两个或三个以上原子的双环分子。术语“稠合环烷基”是指每个环均与另一个环共用两个相邻原子的双环环烷基。稠合双环环烷基的第二个环可以选自饱和环、不饱和环及芳香族环。“环烯基”是包含一个以上双键的环状烃。
[0247]
本说明书中使用的术语“碳环基烷基”是指被碳环基取代的烷基。
[0248]
本说明书中使用的术语“碳酸酯”是指基团-oco
2-r
a
,其中r
a
表示烃基。
[0249]
本说明书中使用的术语“羧基”是指由式-co2h表示的基团。
[0250]
本说明书中使用的术语“酯”是指基团-c(o)or
a
,其中r
a
表示烃基。
[0251]
本说明书中使用的术语“醚”是指经由氧连接到另一个烃基的烃基。因此,烃基的
醚取代基可以是烃基-o-。醚可以对称或不对称。醚的例子包括杂环-o-杂环和芳基-o-杂环,但并不限于此。醚包括“烷氧基烷基”,其可以由通式烷基-o-烷基表示。
[0252]
本说明书中使用的术语“卤代”和“卤素”表示卤素,并且包括氯、氟、溴及碘。
[0253]
本说明书中使用的术语“杂芳烷基(hetaralkyl/heteroaralkyl)”是指被杂芳基取代的烷基。
[0254]
本说明书中使用的术语“杂烷基”是指碳原子和至少一个杂原子的饱和或不饱和链,其中没有2个杂原子是相邻的。
[0255]
术语“杂芳基(heteroaryl/hetaryl)”包括经取代或未经取代的芳香族单环结构,优选为5~20元环,更优选为5~6元环,其环结构包括至少一个杂原子,优选包括1~4个杂原子,更优选包括1个或2个杂原子。杂芳基优选具有2~40个碳原子,更优选具有2~25个碳原子。术语“杂芳基”还包括具有2个以上环(相邻的2个环共用2个碳)的多环体系,其中至少一个环是芳香族环,其它环例如可以是环烷基、环烯基、环炔基、芳基、杂芳基和/或杂环基。杂芳基例如包括吡咯、呋喃、噻吩、咪唑、噁唑、噻唑、吡唑、吡啶、吡嗪、哒嗪、嘧啶及咔唑等。
[0256]
术语“芳氧基”是键合有氧的芳基。芳氧基优选具有6~40个碳原子,更优选具有6~25个碳原子。
[0257]
术语“杂芳氧基”是键合有氧的芳基。杂芳氧优选具有3~40个碳原子,更优选具有3~25碳原子。
[0258]
本说明书中使用的术语“杂原子”表示除碳或氢以外的任何元素的原子。优选的杂原子是氮、氧及硫。
[0259]
术语“杂环基”、“杂环(heterocycle/heterocyclic)”包括经取代或未经取代的非芳香族环结构,优选为3~20元环,更优选为3~7元环,其环结构包括至少一个杂原子,优选包括1~4个杂原子,更优选包括1个或2个杂原子。术语“杂环基”和“杂环”还包括具有两个以上环(两个相邻环共有两个以上碳)的多环系统,其中至少一个环是杂环,例如,其它环可以是环烷基、环烯基、环炔基、芳基、杂芳基和/或杂环基。杂环基例如包括哌啶、哌嗪、吡咯烷、吗啉、内酯、内酰胺等。
[0260]
本说明书中使用的术语“杂环基烷基”是指被杂环基取代的烷基。
[0261]
本说明书中使用的术语“烃基”是指经由碳原子键结的基团,其中碳原子不具有=o或=s取代基。烃基可以任选包括杂原子。烃基包括烷基、烯基、炔基、烷氧基烷基、氨基烷基、芳烷基、芳基、芳烷基、碳环基、环烷基、碳环基烷基、杂芳烷基、经由碳原子键结的杂芳基、经由碳原子键结的杂环基、杂环烷基或羟基烷基,但并不限于此。因此,甲基、乙氧基乙基、2-吡啶基及三氟甲基等基团是烃基,但乙酰基(其在连接碳上具有=o取代基)和乙氧基(其经由氧而不是连接碳)等取代基不是烃基。
[0262]
本说明书中使用的术语“羟基烷基”是指被羟基取代的烷基。
[0263]
与酰基、酰氧基、烷基、烯基、炔基或烷氧基等化学部分结合使用时,术语“低级(lower)”表示包括在取代基中存在6个以下非氢原子的基团。例如,“低级烷基”是指含有6个以下碳原子的烷基。在一些实施方式中,烷基具有1~6个碳原子,1~4个碳原子或1~3个碳原子。本说明书中记载的酰基、酰氧基、烷基、烯基、炔基或烷氧基取代基无论单独出现或与羟基烷基和芳烷基等的说明中的其它取代基组合出现,均分别是低级酰基、低级酰氧基、低级烷基、低级烯基、低级炔基或低级烷氧基(此时,例如对烷基取代基中的碳原子进行计
数时,不包括芳基内的原子)。
[0264]
术语“多环基”、“多环(polycycle/polycyclic)”是指2个以上环(例如环烷基、环烯基、环炔基、芳基、杂芳基和/或杂环基),其中2个相邻环(例如为“稠环”)共有2个以上原子。多环的每个环均可以经取代或未经取代。在某些实施方式中,多环的每个环在环中均包含3~10个原子,优选包含5~7个原子。
[0265]
术语“聚(间苯醚)(poly(meta-phenylene oxides))”中,术语“亚苯基(phenylene)”概括性地指6元芳基或6元杂芳基部分。在本发明的第一~第二十方式中,对示例性聚(间苯醚)进行了说明。
[0266]
术语“甲硅烷基”是指键结有三个烃基部分的硅部分。
[0267]
术语“经取代的”是指如下部分:具有取代骨架的一个以上碳上的氢的取代基。应理解,“取代”或“被~取代的”包括以下默认的限制条件:此类取代取决于被取代原子和取代基的允许化合价,并且该取代会生成稳定的化合物,例如不会自发地(例如通过重排、环化、消除等)进行转变的化合物。可以被取代的部分能够包括本说明书中记载的任意合适的取代基,例如酰基、酰胺基、酰氧基、烷氧基、烷氧基烷基、烯基、烷基、烷基氨基、烷硫基、芳硫基、炔基、酰胺、氨基、氨基烷基、芳烷基、氨基甲酸酯、碳环基、环烷基、碳环基烷基、碳酸酯、酯、醚、杂芳烷基、杂环基、杂环基烷基、烃基、甲硅烷基、砜或硫醚。本说明书中使用的术语“经取代的”预期包括有机化合物的所有可允许的取代基。广义上来讲,可允许的取代基包括有机化合物的非环状和环状、支链和非支链、碳环和杂环、芳香族和非芳香族取代基。对于合适的有机化合物,可允许的取代基可以是一个以上,并且可以相同或不同。出于本发明的目的,氮等杂原子可以具有氢和/或本说明书中记载的满足杂原子的化合价的有机化合物的任意允许的取代基。取代基可以包括本说明书中记载的任意取代基,例如卤素、羟基、羰基(例如羧基、烷氧基羰基、甲酰基或酰基)、硫代羰基(例如硫酯、硫代乙酸酯或硫代甲酸酯)、烷氧基、磷酰基、磷酸酯、膦酸酯、亚膦酸酯、氨基、酰胺基、脒、亚胺、氰基、硝基、叠氮基、硫氢基、烷硫基、硫酸酯、磺酸酯、氨磺酰基、磺酰胺基、磺酰基、杂环基、芳烷基或芳香族或杂芳香族部分。在优选的实施方式中,经取代的烷基上的取代基选自c
1-6
烷基、c
3-6
环烷基、卤素、羰基、氰基或羟基。在更优选的实施方式中,经取代的烷基上的取代基选自氟、羰基、氰基或羟基。本领域的技术人员应理解,取代基在适当的时候本身可以被取代。若没有具体说明“未经取代的”,则关于本说明书中的化学部分,应理解为包括经取代的变体。例如,关于“芳基”或芳基部分,默认包括经取代和未经取代的变体两者。
[0268]
本领域公认的术语“磺酸酯”是指基团so3h或其药学上可接受的盐。
[0269]
本领域公认的术语“砜”是指基团-s(o)
2-r
a
,其中r
a
表示烃基。
[0270]
本说明书中使用的术语“硫醚”等同于醚,其中氧被硫取代。
[0271]
本说明书中使用的术语“对称分子”是指群对称或合成对称的分子。本说明书中使用的术语“群对称”是指根据分子对称性群论具有对称性的分子。本说明书中使用的术语“合成对称”是指以无需区域选择性合成方案的方式选择的分子。
[0272]
本说明书中使用的术语“供体”是指可以用于有机发光二极管中且可能在激发时从其最高占用分子轨道向受体供给电子的分子片段。在优选的实施方式中,供体包含取代氨基。在一示例性实施方式中,供体的电离势为-6.5ev以上。
[0273]
本说明书中使用的术语“受体”是指可以用于有机发光二极管中且可能从被激发
的供体接受电子到其最低未占用分子轨道的分子片段。在一示例性实施方式中,受体的电子亲和能为-0.5ev以下。
[0274]
本说明书中使用的术语“连接部分”或“桥接部分”是指可以包含在共价连接于受体与供体部分之间的分子的分子片段。例如,连接部分能够进一步与受体部分、供体部分或这两者共轭。认为在不受任何特定理论限制的情况下,连接部分能够将受体和供体部分立体限制为特定结构,由此防止供体与受体部分的共轭π体系之间的重叠。合适的连接部分的例子包括苯基、乙烯基及乙炔基。
[0275]
本说明书中使用的术语“多价”是指与至少2个其它分子片段连接的分子片段。例如,连接部分为多价。
[0276]
本说明书中使用的或“*”是指两个原子之间的连接点。
[0277]“空穴传输层(htl)”及类似术语表示由传输空穴的材料制成的层。建议较高的空穴迁移率。htl用于阻断由发射层传输的电子的通过。通常要求低电子亲和能以阻断电子。htl优选具有较大三重态以阻断激子从相邻发射层(eml)迁移。htl化合物的例子包括二(对甲苯基)氨基苯基]环己烷(tapc)、n,n-二苯基-n,n-双(3-甲基苯基)-1,1-联二苯-4,4-二胺(tpd)及n,n'-二苯基-ν,ν'-双(1-萘基)-(1,1'-联二苯)-4,4'-二胺(npb,α-npd),但不限于此。
[0278]“发光层”及类似用语表示发光的层。在一些实施方式中,发光层包含主体材料和客体材料。客体材料可以作为掺杂剂材料,但本发明并不限于此。主体材料或“主体”可以是双极性或单极性,可以单独使用或组合使用2种以上的主体材料。主体材料的光电特性可以根据所使用的客体材料类型(tadf,磷光或荧光)而不同。对于荧光客体材料来说,主体材料应在客体材料的吸收与材料释放之间具有良好的光谱重叠以诱导好的荧光转移到客体材料。对于磷光客体材料来说,主体材料应具有较高的三重态能量以限制客体材料的三重态。对于tadf客体材料来说,主体材料应具有光谱重叠和更高的三重态能量两者。
[0279]“掺杂剂”及类似用语是指用于载流子传输层、发光层或其他层的添加剂材料。在载流子传输层中,掺杂剂及类似用语在作为添加剂添加到有机层时,发挥提高有机电子装置的有机层的导电率的电子受体或供体的功能。同样地,有机半导体在其导电性方面也可能受到掺杂的影响。此类有机半导体基质材料可以由具有电子供体特性的化合物或具有电子受体特性的化合物构成。在发光层中,掺杂剂及类似用语还表示例如分散在主体等基质中的发光材料。三重态收集材料被掺杂到发光层或包含在相邻层中以提高激子生成效率时,将其称为辅助掺杂剂。由于三重态收集材料提高激子生成效率,因此辅助掺杂剂在发光层或相邻层中的含量并没有特别限制。辅助掺杂剂在发光层中的含量优选高于发光材料,更优选至少为两倍。在发光层中,主体材料的含量优选为50重量%以上,辅助掺杂剂的含量优选为5重量%以上且小于50重量%,发光材料的含量优选大于0重量%且小于25重量%,更优选0重量%以上且小于10重量%。辅助掺杂剂在相邻层中的含量可以大于50重量%,也可以为100重量%。在发光层或相邻层中包含三重态收集材料的装置具有比没有三重态收集材料更高的光发射效率时,这种三重态收集材料发挥辅助掺杂剂的作用。包含主体材料、辅助掺杂剂及发光材料的发光层满足以下(a),优选满足以下(b):
[0280]
es1(a)>es1(b)>es1(c)
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(a)
[0281]
et1(a)>et1(b)
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(b)
[0282]
其中es1(a)表示主体材料的最低激发单重态能级;es1(b)表示辅助掺杂剂的最低激发单重态能级;es1(c)表示发光材料的最低激发单重态能级;et1(a)表示主体材料在77k下的最低激发三重态能级;et1(b)表示辅助掺杂剂在77k下的最低激发三重态能级。辅助掺杂剂的最低单重态激发态与在77k下的最低三重态激发态之间的能量差δest优选为0.3ev以下,更优选为0.2ev以下,进一步优选为0.1ev以下。
[0283]
在本发明的化合物中,不具体指定为特定同位素的任意原子均表示该原子的任意稳定的同位素。若没有特别说明,则在位置被具体指定为“h”或“氢”时,应理解为该位置在其天然丰度同位素组合物中具有氢。另外,若没有特别说明,则位置被具体指定为“d”或“氘”时,应理解为该位置具有丰度比氘的天然丰度0.015%至少大3340倍的氘(例如,至少混有50.1%氘)。
[0284]“d”和“d”均指氘。
[0285]“被氘取代”是指一个以上氢原子被相应数量的氘原子取代。
[0286]
本说明书中使用的术语“同位素富集系数”表示在指定同位素的同位素丰度与天然丰度之间的比率。
[0287]
在各实施方式中,本发明的化合物相对于每个指定氘原子的同位素富集系数至少为3500(在每个指定氘原子中混有52.5%氘)、至少为4000(混有60%氘)、至少为4500(混有67.5%氘)、至少为5000(混有75%氘)、至少为5500(混有82.5%氘)、至少6000(混有90%氘)、至少为6333.3(混有95%氘)、至少为6466.7(混有97%氘)、至少为6600(混有99%氘)或至少为6633.3(混有99.5%氘)。
[0288]
术语“同位素体”是指仅是其同位素组合物与本发明的特定化合物不同的物种。
[0289]
表示本发明的化合物时,术语“化合物”是指除了在分子的组成原子之间可能存在同位素变异之外,具有相同的化学结构的分子集合。因此,本领域技术人员应理解由含有指定氘原子的特定化学结构表示的化合物还在该结构中的一个以上指定氘位置具有氢原子的少量的同位素体。此类同位素体在本发明的化合物中的相对量取决于多种因素,包括用于制备化合物的氘化试剂的同位素纯度和用于制备化合物的各种合成步骤中的氘混入效率。然而,如上所述,此类同位素体整体的相对量小于化合物的49.9%。在另一实施方式中,此类同位素体整体的相对量小于化合物的47.5%、小于化合物的40%、小于化合物的32.5%、小于化合物的25%、小于化合物的17.5%、小于化合物的10%、小于化合物的5%、小于化合物的3%、小于化合物的1%或小于化合物的0.5%。
[0290]
oled的原理
[0291]
oled通常由两个电极(阳极和阴极)之间的有机材料或化合物层组成。有机分子通过由部分或全部分子的共轭引起的π电子离域而可以导电。施加电压时,电子从存在于阳极的最高占用分子轨道(homo)流入存在于阴极的有机分子的最低未占用分子轨道(lumo)。从homo去除电子也被称为将电子空穴插入到homo中。静电力使电子和空穴朝彼此接近,直到它们重组并形成激子(电子和空穴的键合态)为止。随着激发态衰减且电子能级弛豫(relax),发射频率在可见光谱中的辐射线。这一辐射的频率取决于材料能隙,该能隙是homo与lumo之间的能量差距。
[0292]
由于电子和空穴是具有半整数自旋的费米子,因此激子可以呈单重态还是三重态取决于电子与空穴的自旋的结合情况。从统计上来讲,对每个单重态激子形成3个三重态激
子。从三重态衰减是自旋受阻,其结果会导致跃迁的时间尺度增加和限制荧光装置的内部效率。磷光有机发光二极管利用自旋-轨道作用,促进单重态与三重态之间的体系间窜越,因此获得来自单重态和三重态两者的发射并且改进内部效率。
[0293]
一种原型磷光材料是三(2-苯基吡啶)铱(ir(ppy)3),其中激发态是从ir原子向有机配位体的电荷转移。此类方法使三重态寿命减少至比完全允许的跃迁(例如荧光)的辐射寿命慢若干数量级的约数μβ。基于ir的磷光体可用于多种显示器应用已得到证实,但由较大的三重态密度导致的损失仍阻碍oled应用于更高亮度的固态照明。
[0294]
tadf欲最小化δe
st
。交换分裂从常规值0.4~0.7ev减少到热能的能级差(与kbt成比例,其中kb表示玻尔兹曼常数,t表示温度)表示,即使能态之间的耦合较小,热搅动仍可以在相关时间尺度内使粒子数在单重态等级与三重态子级之间跃迁。
[0295]
tadf分子由通过共价键直接连接或经由共轭连接部分(或“桥接部分”)连接的供体和受体部分组成。“供体”部分可能在激发时将电子从其homo转移到“受体”部分。“受体”部分可能从“供体”部分接受电子到其lumo。tadf分子的供体-受体性质会导致具有显示极低δe
st
的电荷转移特征的低位激发态。由于热分子运动可以随机改变供体-受体体系的光学特性,因此供体和受体部分的刚性三维排列能够用于限制通过激发寿命期间的内部转化进行的电荷转移状态的非辐射衰减。
[0296]
因此,优选减少δe
st
,并生成能够利用三重态激子的反向系间窜越(risc)增加的体系。认为这种体系会增加量子效率并减少发射寿命。具有这些特征的体系能够发光而不会发生现有oled中普遍存在的快速劣化。
[0297]
本发明的化合物
[0298]
在一些实施方式中,化合物具有通式(i)结构:
[0299][0300]
其中
[0301]
r1、r2、r3、r4及r5独立地选自氢、氘、a1、ar1及d1;
[0302]
r1、r2、r3、r4及r5中的至少一个为a1;
[0303]
r1、r2、r3、r4及r5中的至少一个为d1;
[0304]
a1独立地选自
[0305][0306]
x
a
独立地选自o、s及nr
a
’
;
[0307]
r
a
独立地选自氢、氘、卤素、氰基、经取代或未经取代的烷基、经取代或未经取代的烷氧基、经取代或未经取代的芳基、经取代或未经取代的芳氧基、经取代或未经取代的杂芳基、经取代或未经取代的杂芳氧基及甲硅烷基;
[0308]
r
a
的2个以上的例子能够结合而形成环体系;
[0309]
r
a
’
独立地选自氢、氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基;
[0310]
r
a
’
及r
a
的2个以上的例子能够结合而形成环体系;
[0311]
l
a
独立地选自单键、经取代或未经取代的亚芳基及经取代或未经取代的杂亚芳基;其中亚芳基和杂亚芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代;这些取代基中的2个以上能够结合而形成环体系;
[0312]
d1独立地选自
[0313][0314]
x
d
独立地选自o、s、nr
d
’
、c(o)、经取代或未经取代的亚甲基、经取代或未经取代的亚乙基、经取代或未经取代的亚乙烯基、经取代或未经取代的邻亚芳基及经取代或未经取代的邻杂亚芳基;其中亚甲基、亚乙基、亚乙烯基、邻亚芳基或邻杂亚芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代;
[0315]
r
d
独立地选自氢、氘、经取代或未经取代的烷基、经取代或未经取代的烷氧基、经取代或未经取代的氨基、经取代或未经取代的芳基、经取代或未经取代的芳氧基、经取代或未经取代的杂芳基、经取代或未经取代的杂芳氧基及甲硅烷基;
[0316]
r
d
的2个以上的例子能够结合而形成环体系;
[0317]
r
d
’
独立地选自氢、氘、经取代或未经取代的烷基、经取代或未经取代的氨基、经取代或未经取代的芳基及经取代或未经取代的杂芳基;
[0318]
r
d
’
及r
d
的2个以上的例子能够结合而形成环体系;
[0319]
l
d
独立地选自单键、经取代或未经取代的亚芳基及经取代或未经取代的杂亚芳基;其中亚芳基和杂亚芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代;这些取代基中的2个以上能够结合而形成环体系;
[0320]
ar1独立地选自不包含任何氮原子的经取代或未经取代的杂芳基;其中芳基及杂芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代;这些取代基中的2个以上能够结合而形成环体系;
[0321]
每个“*”表示与通式(i)的连接点。
[0322]
在一些实施方式中,a1为
[0323]
在一些实施方式中,a1为
[0324]
在一些实施方式中,a1为
[0325]
在一些实施方式中,a1为
[0326]
在一些实施方式中,a1为
[0327]
在一些实施方式中,a1为
[0328]
在一些实施方式中,a1为
[0329]
在一些实施方式中,a1为
[0330]
在一些实施方式中,a1为
[0331]
在一些实施方式中,a1为
[0332]
在一些实施方式中,a1选自
[0333][0334]
在一些实施方式中,a1选自
[0335][0336]
在一些实施方式中,a2为
[0337]
在一些实施方式中,a2为
[0338]
在一些实施方式中,a2为
[0339]
在一些实施方式中,a2为
[0340]
在一些实施方式中,a2为
[0341]
在一些实施方式中,a2为
[0342]
在一些实施方式中,a2为
[0343]
在一些实施方式中,a2为
[0344]
在一些实施方式中,a2为
[0345]
在一些实施方式中,a2为
[0346]
在一些实施方式中,r1为氢。在一些实施方式中,r1为氘。在一些实施方式中,r1为a2。在一些实施方式中,r1为ar1。在一些实施方式中,r1为d1。
[0347]
在一些实施方式中,r2为氢。在一些实施方式中,r2为氘。在一些实施方式中,r2为a2。在一些实施方式中,r2为ar1。在一些实施方式中,r2为d1。
[0348]
在一些实施方式中,r3为氢。在一些实施方式中,r3为氘。在一些实施方式中,r3为a2。在一些实施方式中,r3为ar1。在一些实施方式中,r3为d1。
[0349]
在一些实施方式中,r4为氢。在一些实施方式中,r4为氘。在一些实施方式中,r4为a2。在一些实施方式中,r4为ar1。在一些实施方式中,r4为d1。
[0350]
在一些实施方式中,r5为氢。在一些实施方式中,r5为氘。在一些实施方式中,r5为a2。在一些实施方式中,r5为ar1。在一些实施方式中,r5为d1。
[0351]
在一些实施方式中,x
a
为o。在一些实施方式中,x
a
为s。在一些实施方式中,x
a
为nr
a
’
。
[0352]
在一些实施方式中,r
a
为氢。在一些实施方式中,r
a
为氘。在一些实施方式中,r
a
为卤素。在一些实施方式中,r
a
为氰基。在一些实施方式中,r
a
为经取代或未经取代的烷基。在一些实施方式中,r
a
为经取代或未经取代的烷氧基。在一些实施方式中,r
a
为经取代或未经取代的芳基。在一些实施方式中,r
a
为经取代或未经取代的芳氧基。在一些实施方式中,r
a
为
经取代或未经取代的杂芳基。在一些实施方式中,r
a
为经取代或未经取代的杂芳氧基。在一些实施方式中,r
a
为甲硅烷基。在一些实施方式中,r
a
的2个以上的例子结合而形成环体系。
[0353]
在一些实施方式中,r
a
’
为氢。在一些实施方式中,r
a
’
为氘。在一些实施方式中,r
a
’
为经取代或未经取代的烷基。在一些实施方式中,r
a
’
为经取代或未经取代的芳基。在一些实施方式中,r
a
’
为经取代或未经取代的杂芳基。在一些实施方式中,r
a
’
及r
a
的2个以上的例子结合而形成环体系。
[0354]
在一些实施方式中,l
a
为键。在一些实施方式中,l
a
为经取代或未经取代的亚芳基。在一些实施方式中,l
a
为经取代或未经取代的杂亚芳基。亚芳基及杂亚芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代;这些取代基中的2个以上能够结合而形成环体系。
[0355]
在一些实施方式中,d1为
[0356]
在一些实施方式中,d1为
[0357]
在一些实施方式中,d1为
[0358]
在一些实施方式中,d1为
[0359]
在一些实施方式中,d1为
[0360]
在一些实施方式中,x
d
为o。在一些实施方式中,x
d
为s。在一些实施方式中,x
d
为nr
d
’
。在一些实施方式中,x
d
为c(o)。在一些实施方式中,x
d
为经取代或未经取代的亚甲基。在一些实施方式中,x
d
为经取代或未经取代的亚乙基。在一些实施方式中,x
d
为经取代或未经取代的亚乙烯基。在一些实施方式中,x
d
为经取代或未经取代的邻亚芳基。在一些实施方式中,x
d
为经取代或未经取代的邻杂亚芳基。亚甲基、亚乙基、亚乙烯基、邻亚芳基或邻杂亚芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代。
[0361]
在一些实施方式中,r
d
为氢。在一些实施方式中,r
d
为氘。在一些实施方式中,rd为经取代或未经取代的烷基。在一些实施方式中,rd为经取代或未经取代的烷氧基。在一些实施方式中,r
d
为经取代或未经取代的氨基。在一些实施方式中,r
d
为经取代或未经取代的芳基。在一些实施方式中,r
d
为经取代或未经取代的芳氧基。在一些实施方式中,r
d
为经取代或未经取代的杂芳基。在一些实施方式中,r
d
为经取代或未经取代的杂芳氧基。在一些实施方式中,r
d
为甲硅烷基。在一些实施方式中,r
d
的2个以上的例子结合而形成环体系。
[0362]
在一些实施方式中,r
d
’
为氢。在一些实施方式中,r
d
’
为氘。在一些实施方式中,r
d
’
为经取代或未经取代的烷基。在一些实施方式中,r
d
’
为经取代或未经取代的芳基。在一些实施方式中,r
d
’
为经取代或未经取代的杂芳基。在一些实施方式中,r
d
’
及r
d
的2个以上的例子结合而形成环体系。
[0363]
在一些实施方式中,l
d
为单键。在一些实施方式中,l
d
为经取代或未经取代的亚芳基。在一些实施方式中,l
d
为经取代或未经取代的杂亚芳基。亚芳基及杂亚芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及经取代或未经取代的杂芳基中的1个以上的取代基取代;这些取代基中的2个以上能够结合而形成环体系。
[0364]
在一些实施方式中,ar1为经取代或未经取代的芳基。在一些实施方式中,ar1为不包含任何氮原子的经取代或未经取代的杂芳基。芳基及杂芳基的每个例子能够被独立地选自氘、经取代或未经取代的烷基、经取代或未经取代的芳基及不包含任何氮原子的经取代或未经取代的杂芳基中的1个以上的取代基取代;这些取代基中的2个以上能够结合而形成
环体系。在一些实施方式中,烷基为c1-c20烷基。
[0365]
在一些实施方式中,ar1选自
[0366][0367]
其中
[0368]
1个r
ar
是与通式(i)的连接点,剩余的r
ar
独立地选自氢、氘、烷基或烷基被取代或未被取代的芳基。
[0369]
在一些实施方式中,ar1为芳基,为c6-c40芳基。在一些实施方式中,ar1独立地选自经取代或未经取代的苯基、经取代或未经取代的联苯及经取代或未经取代的三联苯。
[0370]
在一些实施方式中,ar1选自经取代或未经取代的苯基、经取代或未经取代的联苯及经取代或未经取代的三联苯。
[0371]
在一些实施方式中,ar1为杂芳基,为c2-c40杂芳基。
[0372]
在一些实施方式中,ar1为烷氧基,为c1-c20烷氧基。
[0373]
在一些实施方式中,ar1为芳氧基,为c6-c40芳氧基。
[0374]
在一些实施方式中,ar1为杂芳氧基,为c2-c40杂芳氧基。
[0375]
在一些实施方式中,通式(i)的化合物为通式(ia)的化合物:
[0376][0377]
在一些实施方式中,通式(i)的化合物为通式(ib)的化合物:
[0378][0379][0380]
其中
[0381]
r
l
独立地选自氘、烷基或烷基被取代或未被取代的芳基;及
[0382]
n为0~4。
[0383]
在一些实施方式中,通式(i)的化合物为通式(ic)的化合物:
[0384][0385]
其中
[0386]
r
l
独立地选自氘、烷基或烷基被取代或未被取代的芳基;及
[0387]
n为0~4。
[0388]
在一些实施方式中,化合物具有通式(ii)的结构:
[0389][0390]
其中
[0391]
a选自
[0392][0393]
d独立地选自h、me、ph、
[0394]
[0395]
[0396][0397]
r独立地选自h、me及ph;
[0398]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0399]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0400]
所出现的至少一个d选自d1-d31。
[0401]
在一些实施方式中,a为cn。在一些实施方式中,a为a1。在一些实施方式中,a为a2。在一些实施方式中,a为a3。在一些实施方式中,a为a4。在一些实施方式中,a为a5。在一些实施方式中,a为a6。在一些实施方式中,a为a7。在一些实施方式中,a为a8。在一些实施方式中,a为a9。在一些实施方式中,a为a10。
[0402]
在一些实施方式中,d为h。在一些实施方式中,d的至少一个例子为h。在一些实施方式中,d为me。在一些实施方式中,d的至少一个例子为me。在一些实施方式中,d为ph。在一些实施方式中,d的至少一个例子为ph。
[0403]
在一些实施方式中,d为d1。在一些实施方式中,d为d2。在一些实施方式中,d为d3。在一些实施方式中,d为d4。在一些实施方式中,d为d5。在一些实施方式中,d为d6。在一些实施方式中,d为d7。在一些实施方式中,d为d8。在一些实施方式中,d为d9。在一些实施方式中,d为d10。在一些实施方式中,d为d11。在一些实施方式中,d为d12。在一些实施方式中,d为d13。在一些实施方式中,d为d14。在一些实施方式中,d为d15。在一些实施方式中,d为d16。在一些实施方式中,d为d17。在一些实施方式中,d为d18。在一些实施方式中,d为d19。在一些实施方式中,d为d20。在一些实施方式中,d为d21。在一些实施方式中,d为d22。在一些实施方式中,d为d23。在一些实施方式中,d为d24。在一些实施方式中,d为d25。在一些实施方式中,d为d26。在一些实施方式中,d为d27。在一些实施方式中,d为d28。在一些实施方式中,d为d29。在一些实施方式中,d为d30。在一些实施方式中,d为d31。
[0404]
在一些实施方式中,d选自d1、d2、d3、d4、d5、d6及d7。在一些实施方式中,d选自d8、d9、d10、d11、d12及d13。在一些实施方式中,d选自d14、d15及d16。在一些实施方式中,d选自d17、d18及d19。在一些实施方式中,d选自d20、d21、d22、d23及d24。在一些实施方式中,d选自d25、d26及d27。在一些实施方式中,d选自d28、d29、d30及d31。
[0405]
在一些实施方式中,r为h。在一些实施方式中,r为me。在一些实施方式中,r为ph。
[0406]
在一些实施方式中,r的2个例子不同。在一些实施方式中,r的2个例子相同。
[0407]
在一些实施方式中,d的每个例子均不同。在一些实施方式中,d的2个例子相同。在一些实施方式中,d的3个例子相同。在一些实施方式中,d的所有例子均相同。
[0408]
在一些实施方式中,d的2个例子独立地选自d1-d31。在一些实施方式中,d的3个例子独立地选自d1-d31。在一些实施方式中,d的所有例子独立地选自d1-d31。
[0409]
在一些实施方式中,z1为c(ch3)2。在一些实施方式中,z1为c(ph)2。在一些实施方式中,z1为o。在一些实施方式中,z1为c(ch3)2。在一些实施方式中,z1为n(ph)。
[0410]
在一些实施方式中,z2为h。在一些实施方式中,z2为cn。在一些实施方式中,z2为(c
1-c
20
)-烷基。在一些实施方式中,z2为5~30元芳基。在一些实施方式中,z2为3~30元杂芳基。在一些实施方式中,z2为二芳基氨基。在一些实施方式中,二芳基氨基为-n(ph)2。
[0411]
在一些实施方式中,z2的2个例子相同。在一些实施方式中,z2的2个例子不同。
[0412]
在一些实施方式中,通式(ii)的化合物选自
[0413]
[0414]
[0415]
[0416]
[0417]
[0418]
[0419]
[0420]
[0421]
[0422][0423]
在一些实施方式中,通式(ii)的化合物选自
[0424]
[0425]
[0426][0427]
在一些实施方式中,通式(ii)的化合物为
[0428]
在一些实施方式中,化合物具有通式(iii)结构:
[0429][0430]
其中
[0431]
a选自
[0432]
[0433][0434]
d独立地选自
[0435]
[0436][0437]
r独立地选自h、me及ph;
[0438]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0439]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0440]
d的至少一个例子选自d1-d31。
[0441]
在一些实施方式中,a为a1。在一些实施方式中,a为a2。在一些实施方式中,a为a3。在一些实施方式中,a为a4。在一些实施方式中,a为a5。在一些实施方式中,a为a6。在一些实施方式中,a为a7。在一些实施方式中,a为a8。在一些实施方式中,a为a9。在一些实施方式中,a为a10。
[0442]
在一些实施方式中,a选自a1、a2及a3。在一些实施方式中,a选自a4及a5。在一些实施方式中,a选自a6及a7。在一些实施方式中,a选自a8、a9及a10。
[0443]
在一些实施方式中,d为d1。在一些实施方式中,d为d2。在一些实施方式中,d为d3。在一些实施方式中,d为d4。在一些实施方式中,d为d5。在一些实施方式中,d为d6。在一些实施方式中,d为d7。在一些实施方式中,d为d8。在一些实施方式中,d为d9。在一些实施方式中,d为d10。在一些实施方式中,d为d11。在一些实施方式中,d为d12。在一些实施方式中,d为d13。在一些实施方式中,d为d14。在一些实施方式中,d为d15。在一些实施方式中,d为d16。在一些实施方式中,d为d17。在一些实施方式中,d为d18。在一些实施方式中,d为d19。在一些实施方式中,d为d20。在一些实施方式中,d为d21。在一些实施方式中,d为d22。在一些实施方式中,d为d23。在一些实施方式中,d为d24。在一些实施方式中,d为d25。在一些实施方式中,d为d26。在一些实施方式中,d为d27。在一些实施方式中,d为d28。在一些实施方式中,d为d29。在一些实施方式中,d为d30。在一些实施方式中,d为d31。
[0444]
在一些实施方式中,d选自d1、d2、d3、d4、d5、d6及d7。在一些实施方式中,d选自d8、d9、d10、d11、d12及d13。在一些实施方式中,d选自d14、d15及d16。在一些实施方式中,d选自d17、d18及d19。在一些实施方式中,d选自d20、d21、d22、d23及d24。在一些实施方式中,d选自d25、d26及d27。在一些实施方式中,d选自d28、d29、d30及d31。
[0445]
在一些实施方式中,r为h。在一些实施方式中,r为me。在一些实施方式中,r为ph。
[0446]
在一些实施方式中,r的2个例子不同。在一些实施方式中,r的2个例子相同。
[0447]
在一些实施方式中,d的每个例子均不同。在一些实施方式中,d的2个例子相同。在一些实施方式中,d的3个例子相同。在一些实施方式中,d的所有例子均相同。
[0448]
在一些实施方式中,d的2个例子独立地选自d1-d31。在一些实施方式中,d的3个例子独立地选自d1-d31。在一些实施方式中,d的所有例子独立地选自d1-d31。
[0449]
在一些实施方式中,z1为c(ch3)2。在一些实施方式中,z1为c(ph)2。在一些实施方式中,z1为o。在一些实施方式中,z1为c(ch3)2。在一些实施方式中,z1为n(ph)。
[0450]
在一些实施方式中,z2为h。在一些实施方式中,z2为cn。在一些实施方式中,z2为(c
1-c
20
)-烷基。在一些实施方式中,z2为5~30元芳基。在一些实施方式中,z2为3~30元杂芳基。在一些实施方式中,z2为二芳基氨基。在一些实施方式中,二芳基氨基为-n(ph)2。
[0451]
在一些实施方式中,z2的2个例子相同。在一些实施方式中,z2的2个例子不同。
[0452]
在一些实施方式中,式(iii)的化合物选自
[0453]
[0454]
[0455]
[0456]
[0457]
[0458]
[0459]
[0460]
[0461][0462]
在一些实施方式中,通式(iii)的化合物选自
[0463]
[0464]
[0465]
[0466][0467]
在一些实施方式中,化合物具有通式(iii)结构:
[0468][0469]
其中
[0470]
a选自
[0471][0472]
d独立地选自h、氘、ph、
[0473]
[0474]
[0475][0476]
r独立地选自h、me及ph;
[0477]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0478]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0479]
d的至少一个例子选自d1-d31;
[0480]
d的至少一个例子选自h、氘或ph。
[0481]
在一些实施方式中,a为a1。在一些实施方式中,a为a2。在一些实施方式中,a为a3。在一些实施方式中,a为a4。在一些实施方式中,a为a5。在一些实施方式中,a为a6。在一些实施方式中,a为a7。在一些实施方式中,a为a8。在一些实施方式中,a为a9。在一些实施方式中,a为a10。
[0482]
在一些实施方式中,a选自a1、a2及a3。在一些实施方式中,a选自a4及a5。在一些实施方式中,a选自a6及a7。在一些实施方式中,a选自a8、a9及a10。
[0483]
在一些实施方式中,d为h。在一些实施方式中,d为氘。在一些实施方式中,d为苯基。
[0484]
在一些实施方式中,d为d1。在一些实施方式中,d为d2。在一些实施方式中,d为d3。在一些实施方式中,d为d4。在一些实施方式中,d为d5。在一些实施方式中,d为d6。在一些实施方式中,d为d7。在一些实施方式中,d为d8。在一些实施方式中,d为d9。在一些实施方式中,d为d10。在一些实施方式中,d为d11。在一些实施方式中,d为d12。在一些实施方式中,d为d13。在一些实施方式中,d为d14。在一些实施方式中,d为d15。在一些实施方式中,d为d16。在一些实施方式中,d为d17。在一些实施方式中,d为d18。在一些实施方式中,d为d19。在一些实施方式中,d为d20。在一些实施方式中,d为d21。在一些实施方式中,d为d22。在一些实施方式中,d为d23。在一些实施方式中,d为d24。在一些实施方式中,d为d25。在一些实施方式中,d为d26。在一些实施方式中,d为d27。在一些实施方式中,d为d28。在一些实施方式中,d为d29。在一些实施方式中,d为d30。在一些实施方式中,d为d31。
[0485]
在一些实施方式中,d选自d1、d2、d3、d4、d5、d6及d7。在一些实施方式中,d选自d8、d9、d10、d11、d12及d13。在一些实施方式中,d选自d14、d15及d16。在一些实施方式中,d选自d17、d18及d19。在一些实施方式中,d选自d20、d21、d22、d23及d24。在一些实施方式中,d选自d25、d26及d27。在一些实施方式中,d选自d28、d29、d30及d31。
[0486]
在一些实施方式中,r为h。在一些实施方式中,r为me。在一些实施方式中,r为ph。
[0487]
在一些实施方式中,r的2个例子不同。在一些实施方式中,r的2个例子相同。
[0488]
在一些实施方式中,d的每个例子均不同。在一些实施方式中,d的2个例子相同。在一些实施方式中,d的3个例子相同。在一些实施方式中,d的所有例子均相同。
[0489]
在一些实施方式中,d的2个例子独立地选自d1-d31。在一些实施方式中,d的3个例子独立地选自d1-d31。
[0490]
在一些实施方式中,z1为c(ch3)2。在一些实施方式中,z1为c(ph)2。在一些实施方式中,z1为o。在一些实施方式中,z1为c(ch3)2。在一些实施方式中,z1为n(ph)。
[0491]
在一些实施方式中,z2为h。在一些实施方式中,z2为cn。在一些实施方式中,z2为(c
1-c
20
)-烷基。在一些实施方式中,z2为5~30元芳基。在一些实施方式中,z2为3~30元杂芳基。在一些实施方式中,z2为二芳基氨基。在一些实施方式中,二芳基氨基为-n(ph)2。
[0492]
在一些实施方式中,z2的2个例子相同。在一些实施方式中,z2的2个例子不同。
[0493]
在一些实施方式中,式(iii)的化合物选自
[0494]
[0495]
[0496]
[0497]
[0498]
[0499]
[0500]
[0501]
[0502]
[0503]
[0504]
[0505]
[0506]
[0507]
[0508]
[0509][0510]
在一些实施方式中,通式(iii)的化合物选自
[0511]
[0512]
[0513]
[0514]
[0515]
[0516][0517]
在一些实施方式中,通式(iii)的化合物选自
[0518]
[0519]
[0520][0521]
在一些实施方式中,化合物具有通式(iv)的结构:
[0522][0523][0524]
其中
[0525]
a选自
[0526][0527]
d独立地选自
[0528]
[0529]
[0530][0531]
r独立地选自h、me及ph;
[0532]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0533]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0534]
d的至少一个例子选自d1-d31。
[0535]
在一些实施方式中,a为a1。在一些实施方式中,a为a2。在一些实施方式中,a为a3。在一些实施方式中,a为a4。在一些实施方式中,a为a5。在一些实施方式中,a为a6。在一些实施方式中,a为a7。在一些实施方式中,a为a8。在一些实施方式中,a为a9。在一些实施方式中,a为a10。
[0536]
在一些实施方式中,a选自a1、a2及a3。在一些实施方式中,a选自a4及a5。在一些实施方式中,a选自a6及a7。在一些实施方式中,a选自a8、a9及a10。
[0537]
在一些实施方式中,d为d1。在一些实施方式中,d为d2。在一些实施方式中,d为d3。在一些实施方式中,d为d4。在一些实施方式中,d为d5。在一些实施方式中,d为d6。在一些实施方式中,d为d7。在一些实施方式中,d为d8。在一些实施方式中,d为d9。在一些实施方式中,d为d10。在一些实施方式中,d为d11。在一些实施方式中,d为d12。在一些实施方式中,d为d13。在一些实施方式中,d为d14。在一些实施方式中,d为d15。在一些实施方式中,d为d16。在一些实施方式中,d为d17。在一些实施方式中,d为d18。在一些实施方式中,d为d19。在一些实施方式中,d为d20。在一些实施方式中,d为d21。在一些实施方式中,d为d22。在一些实施方式中,d为d23。在一些实施方式中,d为d24。在一些实施方式中,d为d25。在一些实施方式中,d为d26。在一些实施方式中,d为d27。在一些实施方式中,d为d28。在一些实施方式中,d为d29。在一些实施方式中,d为d30。在一些实施方式中,d为d31。
[0538]
在一些实施方式中,d选自d1、d2、d3、d4、d5、d6及d7。在一些实施方式中,d选自d8、d9、d10、d11、d12及d13。在一些实施方式中,d选自d14、d15及d16。在一些实施方式中,d选自d17、d18及d19。在一些实施方式中,d选自d20、d21、d22、d23及d24。在一些实施方式中,d选自d25、d26及d27。在一些实施方式中,d选自d28、d29、d30及d31。
[0539]
在一些实施方式中,r为h。在一些实施方式中,r为me。在一些实施方式中,r为ph。
[0540]
在一些实施方式中,r的2个例子不同。在一些实施方式中,r的2个例子相同。
[0541]
在一些实施方式中,d的每个例子均不同。在一些实施方式中,d的2个例子相同。在
一些实施方式中,d的3个例子相同。在一些实施方式中,d的所有例子均相同。
[0542]
在一些实施方式中,d的2个例子独立地选自d1-d31。在一些实施方式中,d的3个例子独立地选自d1-d31。在一些实施方式中,d的所有例子独立地选自d1-d31。
[0543]
在一些实施方式中,z1为c(ch3)2。在一些实施方式中,z1为c(ph)2。在一些实施方式中,z1为o。在一些实施方式中,z1为c(ch3)2。在一些实施方式中,z1为n(ph)。
[0544]
在一些实施方式中,z2为h。在一些实施方式中,z2为cn。在一些实施方式中,z2为(c
1-c
20
)-烷基。在一些实施方式中,z2为5~30元芳基。在一些实施方式中,z2为3~30元杂芳基。在一些实施方式中,z2为二芳基氨基。在一些实施方式中,二芳基氨基为-n(ph)2。
[0545]
在一些实施方式中,z2的2个例子相同。在一些实施方式中,z2的2个例子不同。
[0546]
在一些实施方式中,式(i)的化合物选自
[0547]
[0548]
[0549]
[0550]
[0551]
[0552]
[0553]
[0554]
[0555][0556]
在一些实施方式中,通式(iv)的化合物选自
[0557]
[0558]
[0559]
[0560]
[0561][0562]
在一些实施方式中,化合物具有通式(iv)的结构:
[0563][0564]
其中
[0565]
a选自
[0566]
[0567][0568]
d独立地选自h、氘、ph、
[0569]
[0570][0571]
r独立地选自h、me及ph;
[0572]
z1独立地选自c(ch3)2、c(ph)2、o及n(ph);
[0573]
z2独立地选自h、cn、(c
1-c
20
)-烷基、5~30元芳基、3~30元杂芳基及二芳基氨基;
[0574]
d的至少一个例子选自d1-d31;
[0575]
d的至少一个例子选自h、ph或氘。
[0576]
在一些实施方式中,a为a1。在一些实施方式中,a为a2。在一些实施方式中,a为a3。在一些实施方式中,a为a4。在一些实施方式中,a为a5。在一些实施方式中,a为a6。在一些实施方式中,a为a7。在一些实施方式中,a为a8。在一些实施方式中,a为a9。在一些实施方式
中,a为a10。
[0577]
在一些实施方式中,a选自a1、a2及a3。在一些实施方式中,a选自a4及a5。在一些实施方式中,a选自a6及a7。在一些实施方式中,a选自a8、a9及a10。
[0578]
在一些实施方式中,d为h。在一些实施方式中,d为氘。在一些实施方式中,d为苯基。
[0579]
在一些实施方式中,d为d1。在一些实施方式中,d为d2。在一些实施方式中,d为d3。在一些实施方式中,d为d4。在一些实施方式中,d为d5。在一些实施方式中,d为d6。在一些实施方式中,d为d7。在一些实施方式中,d为d8。在一些实施方式中,d为d9。在一些实施方式中,d为d10。在一些实施方式中,d为d11。在一些实施方式中,d为d12。在一些实施方式中,d为d13。在一些实施方式中,d为d14。在一些实施方式中,d为d15。在一些实施方式中,d为d16。在一些实施方式中,d为d17。在一些实施方式中,d为d18。在一些实施方式中,d为d19。在一些实施方式中,d为d20。在一些实施方式中,d为d21。在一些实施方式中,d为d22。在一些实施方式中,d为d23。在一些实施方式中,d为d24。在一些实施方式中,d为d25。在一些实施方式中,d为d26。在一些实施方式中,d为d27。在一些实施方式中,d为d28。在一些实施方式中,d为d29。在一些实施方式中,d为d30。在一些实施方式中,d为d31。
[0580]
在一些实施方式中,d选自d1、d2、d3、d4、d5、d6及d7。在一些实施方式中,d选自d8、d9、d10、d11、d12及d13。在一些实施方式中,d选自d14、d15及d16。在一些实施方式中,d选自d17、d18及d19。在一些实施方式中,d选自d20、d21、d22、d23及d24。在一些实施方式中,d选自d25、d26及d27。在一些实施方式中,d选自d28、d29、d30及d31。
[0581]
在一些实施方式中,r为h。在一些实施方式中,r为me。在一些实施方式中,r为ph。
[0582]
在一些实施方式中,r的2个例子不同。在一些实施方式中,r的2个例子相同。
[0583]
在一些实施方式中,d的每个例子均不同。在一些实施方式中,d的2个例子相同。在一些实施方式中,d的3个例子相同。
[0584]
在一些实施方式中,d的2个例子独立地选自d1-d31。在一些实施方式中,d的3个例子独立地选自d1-d31。在一些实施方式中,d的所有例子独立地选自d1-d31。
[0585]
在一些实施方式中,z1为c(ch3)2。在一些实施方式中,z1为c(ph)2。在一些实施方式中,z1为o。在一些实施方式中,z1为c(ch3)2。在一些实施方式中,z1为n(ph)。
[0586]
在一些实施方式中,z2为h。在一些实施方式中,z2为cn。在一些实施方式中,z2为(c
1-c
20
)-烷基。在一些实施方式中,z2为5~30元芳基。在一些实施方式中,z2为3~30元杂芳基。在一些实施方式中,z2为二芳基氨基。在一些实施方式中,二芳基氨基为-n(ph)2。
[0587]
在一些实施方式中,z2的2个例子相同。在一些实施方式中,z2的2个例子不同。
[0588]
在一些实施方式中,通式(iv)的化合物选自
[0589]
[0590]
[0591]
[0592]
[0593]
[0594]
[0595]
[0596]
[0597]
[0598]
[0599]
[0600]
[0601]
[0602][0603]
在一些实施方式中,通式(iv)的化合物选自
[0604]
[0605]
[0606]
[0607][0608]
在一些实施方式中,通式(iv)的化合物选自
[0609]
[0610][0611]
在一些实施方式中,通式(iv)的化合物为
[0612][0613]
在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物被氘取代。
[0614]
在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物为发光材料。
[0615]
在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物能够发出延迟荧光。
[0616]
在本发明的一些实施方式中,通过热或电子手段激发时,通式(i)、(ii)、(iii)或(iv)的化合物能够在紫外线区域、可见光谱的蓝色、绿色、黄色、橙色或红色区域(例如约420nm~约500nm、约500nm~约600nm或约600nm~约700nm)或者近红外线区域产生光。
[0617]
在本发明的一些实施方式中,通过热或电子手段激发时,通式(i)、(ii)、(iii)或(iv)的化合物能够在可见光谱的红色或橙色区域(例如,约620nm~约780nm;约650nm)产生光。
[0618]
在本发明的一些实施方式中,通过热或电子手段激发时,通式(i)、(ii)、(iii)或(iv)的化合物能够在可见光谱的橙色或黄色区域(例如,约570nm~约620nm;约590nm;约570nm)产生光。
[0619]
在本发明的一些实施方式中,通过热或电子手段激发时,通式(i)、(ii)、(iii)或(iv)的化合物能够在可见光谱的绿色区域(例如,约490nm~约575nm;约510nm)产生光。
[0620]
在本发明的一些实施方式中,通过热或电子手段激发时,通式(i)、(ii)、(iii)或(iv)的化合物能够在可见光谱的蓝色区域(例如,约400nm~约490nm;约475nm)产生光。
[0621]
化学小分子库的电子特性能够使用已知的量子力学从头计算法(ab initio)进行计算。例如,使用时间依赖性密度泛函理论,能够筛选出具有homo高于特定阈值且lumo低于特定阈值的分子片段(部分),其中所计算的该部分的三重态高于2.75ev,上述时间依赖性密度泛函理论使用作为基组的所谓6-31g*的函数组和becke三参数lee-yang-parr杂化泛函来求算哈特里-福克方程(td-dft/b3lyp/6-31g*)。
[0622]
因此,例如,供体部分(“d”)由于其homo能量(例如电离势)为-6.5ev以上而能够被选择。受体部分(“a”)由于其lumo能量(例如电子亲和能)为-0.5ev以下而能够被选择。桥接部分(“l”)可以是能够将受体和供体部分立体地限制为特定结构的刚性共轭体系,由此防止供体与受体部分的共轭π体系之间的重叠。
[0623]
在一些实施方式中,利用以下特性中的一个以上来过滤化合物库:
[0624]
1.在接近特定波长的发射;
[0625]
2.计算出高于特定能级的三重态;
[0626]
3.低于特定值的δe
st
值;
[0627]
4.高于特定值的量子产率;
[0628]
5.homo能级;及
[0629]
6.lumo能级。
[0630]
在一些实施方式中,在77k下最低单重态激发态与最低三重态激发态之间的差(δst)小于约0.5ev,小于约0.4ev,小于约0.3ev,小于约0.2ev,或小于约0.1ev。在一些实施方式中,δest值小于约0.09ev,小于约0.08ev,小于约0.07ev,小于约0.06ev,小于约0.05ev,小于约0.04ev,小于约0.03ev,小于约0.02ev或小于约0.01ev。
[0631]
在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物显示出高于25%的量子产率,例如约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%、约75%、约80%、约85%、约90%、约95%或更大。
[0632]
具有公开化合物的组合物
[0633]
在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物通过与一种以上材料(例如小分子、聚合物、金属、金属络合物等)组合、分散在该材料中、与该材料共价键合、涂布该材料、形成于该材料上或与其结合来形成固态的膜或层。例如,通式(i)、(ii)、(iii)或(iv)的化合物可以与电活性材料结合而形成膜。在一些情况下,通式(i)、(ii)、(iii)或(iv)的化合物可以与空穴传输聚合物结合。在一些情况下,通式(i)、(ii)、(iii)或(iv)的化合物可以与电子传输聚合物结合。在一些情况下,通式(i)、(ii)、(iii)或(iv)的化合物可以与空穴传输聚合物及电子传输聚合物结合。在一些情况下,通式(i)、(ii)、(iii)或(iv)的化合物可以与均包含空穴传输部分及电子传输部分这两者的共聚物结合。在这些实施方式中,形成于固体膜或层内的电子和/或空穴可以与通式(i)、(ii)、(iii)或(iv)的化合物相互作用。
[0634]
所公开化合物的示例性用途
[0635]
有机发光二极管
[0636]
本发明的一方式涉及作为有机发光装置的有机发光材料的本发明的通式(i)、(ii)、(iii)或(iv)的化合物的用途。在一些实施方式中,本发明的由通式(i)、(ii)、(iii)或(iv)表示的化合物可以在有机发光装置的发光层中有效地用作发光材料。在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物包含发出延迟荧光的延迟荧光材料(延迟荧光发射体)。在一些实施方式中,本发明提供一种具有通式(i)、(ii)、(iii)或(iv)的结构的延迟荧光发射体。在一些实施方式中,本发明涉及作为延迟荧光发射体的通式(i)、(ii)、(iii)或(iv)的化合物的用途。在一些实施方式中,发光层包含通式(i)、(ii)、(iii)或(iv)的化合物作为辅助掺杂剂。
[0637]
在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物能够用作主体材料,能够与一种以上发光材料一同使用,并且发光材料可以为荧光材料、磷光材料或tadf材料。在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物能够用作空穴传输材料。在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物能够用作电子传输材料。在一些实施方式中,本发明涉及一种用于从通式(i)、(ii)、(iii)或(iv)的化合物发射延迟荧光的方法。在一些实施方式中,包含化合物作为发光材料的有机发光装置发射延迟荧光且具有高发光效率。
[0638]
在一些实施方式中,发光层包含通式(i)、(ii)、(iii)或(iv)的化合物,其中通式(i)、(ii)、(iii)或(iv)的化合物与基板平行地取向。在一些实施方式中,基板是用于形成
膜的表面。在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物相对于膜形成表面的取向会影响或决定由排列的化合物发射的光的传播方向。在一些实施方式中,由通式(i)、(ii)、(iii)或(iv)的化合物发射的光的传播方向的排列会增强来自发光层的光提取效率。
[0639]
本发明的一方式涉及一种有机发光装置。在一些实施方式中,有机发光装置包含发光层。在一些实施方式中,发光层包含通式(i)、(ii)、(iii)或(iv)的化合物作为发光材料。在一些实施方式中,有机发光装置是有机光致发光装置(有机pl装置)。在一些实施方式中,有机发光装置是有机电致发光装置(有机el装置)。在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物辅助包含在发光层中的另一发光材料的发光,即作为所谓的辅助掺杂剂。在一些实施方式中,在发光层中包含的通式(i)、(ii)、(iii)或(iv)的化合物在其最低激发单重态能级,该能级包括在发光层中包含的主体材料的最低激发单重态能级与在发光层中包含的另一发光材料的最低激发单重态能级之间。
[0640]
在一些实施方式中,有机光致发光装置包含至少一个发光层。在一些实施方式中,有机电致发光装置包含至少一个阳极、阴极及阳极与阴极之间的有机层。在一些实施方式中,有机层至少包含发光层。在一些实施方式中,有机层仅包含发光层。在一些实施方式中,有机层包括除发光层以外的一个以上有机层。有机层的例子包括空穴传输层、空穴注入层、电子阻挡层、空穴阻挡层、电子注入层、电子传输层和激子阻挡层。在一些实施方式中,空穴传输层可以是具有空穴注入功能的空穴注入和传输层,并且电子传输层可以是具有电子注入功能的电子注入和传输层。有机电致发光装置的例子示于图1。
[0641]
基板
[0642]
在一些实施方式中,本发明的有机电致发光装置由基板支撑,其中该基板并无特别限制,可以是在有机电致发光装置中常用的任意基板,例如由玻璃、透明塑料、石英及硅形成的基板。
[0643]
阳极
[0644]
在一些实施方式中,有机电致发光装置的阳极由金属、合金、导电化合物或其组合制成。在一些实施方式中,金属、合金或导电化合物具有较大功函数(4ev以上)。在一些实施方式中,金属是au。在一些实施方式中,导电性透明材料选自cui、氧化铟锡(ito)、sno2及zno。在一些实施方式中,例如使用idixo(in2o
3-zno)等能够形成透明导电膜的非晶材料。在一些实施方式中,阳极是薄膜。在一些实施方式中,薄膜通过气相沉积或溅射制造。在一些实施方式中,通过光刻法对膜进行图案化。在不要求图案具有高精度(例如,约100μm以上)的一些实施方式中,可以在电极材料的气相沉积或溅射中,利用具有所需形状的掩模形成图案。在一些实施方式中,能够将有机导电化合物等材料涂布成涂层时,使用印刷法和涂布法等湿膜形成法。在一些实施方式中,所发射的光透过阳极时,阳极的透射率大于10%,并且该阳极具有数百ohm/平方以下的薄膜电阻。在一些实施方式中,阳极的厚度是10~1,000nm。在一些实施方式中,阳极的厚度是10~200nm。在一些实施方式中,阳极的厚度根据所使用的材料而改变。
[0645]
阴极
[0646]
在一些实施方式中,阴极由具有较小功函数(4ev以下)的金属(称为电子注入金属)、合金、导电化合物或其组合即电极材料制成。在一些实施方式中,电极材料选自钠、钠-钾合金、镁、锂、镁-铜混合物、镁-银混合物、镁-铝混合物、镁-铟混合物、铝-氧化铝(al2o3)
混合物、铟、锂-铝混合物及稀土金属。在一些实施方式中,使用电子注入金属与第二金属(功函数比所使用的电子注入金属更大的稳定金属)的混合物。在一些实施方式中,混合物选自镁-银混合物、镁-铝混合物、镁-铟混合物、铝-氧化铝(al2o3)混合物、锂-铝混合物及铝。在一些实施方式中,混合物会提高电子注入特性和抗氧化耐性。在一些实施方式中,通过将电极材料利用气相沉积或溅射形成为薄膜而生成阴极。在一些实施方式中,阴极具有数百ohm/平方以下的薄膜电阻。在一些实施方式中,阴极的厚度在10nm~5μm的范围内。在一些实施方式中,阴极的厚度在50~200nm的范围内。在一些实施方式中,为了透射所发射的光,有机电致发光装置的阳极和阴极中的一个为透明或半透明。在一些实施方式中,透明或半透明的电致发光装置会增强发光亮度。
[0647]
在一些实施方式中,如对阳极的说明中所示,阴极由导电透明材料形成以形成透明或半透明的阴极。在一些实施方式中,装置包含阳极和阴极(两者均为透明或半透明)。
[0648]
发光层
[0649]
在一些实施方式中,发光层是分别从阳极和阴极注入的空穴和电子重组而形成激子的层。在一些实施方式中,上述层发光。
[0650]
在一些实施方式中,作为发光层单独使用发光材料。在一些实施方式中,发光层含有发光材料和主体材料。在一些实施方式中,发光材料是通式(i)、(ii)、(iii)或(iv)的一种以上化合物。在一些实施方式中,为了使有机电致发光装置和有机光致发光装置显示出高发光效率,将在发光材料中生成的单重态激子和三重态激子限定于发光材料。在一些实施方式中,除发光材料以外,在发光层中还使用主体材料。在一些实施方式中,主体材料是有机化合物。在一些实施方式中,有机化合物具有激发单重态能量和激发三重态能量,其中至少一个高于本发明的发光材料。在一些实施方式中,将在本发明的发光材料中生成的单重态激子和三重态激子限定于本发明发光材料的分子。在一些实施方式中,充分限定单重态和三重态激子以诱导发光效率。在一些实施方式中,即使没有充分限定单重态激子和三重态激子,但仍获得了较高发光效率,因此,能够实较现高发光效率的主体材料可以用于本发明中而没有特别限制。在一些实施方式中,发光在本发明的装置中的发光层的发光材料中发生。在一些实施方式中,所发射的光均包含荧光和延迟荧光两者。在一些实施方式中,所发射的光包括从主体材料发射的光。在一些实施方式中,所发射的光由从主体材料发射的光组成。在一些实施方式中,所发射的光包括来自通式(i)、(ii)、(iii)或(iv)的化合物的发射光和来自主体材料的发射光。在一些实施方式中,使用tadf分子和主体材料。在一些实施方式中,tadf是辅助掺杂剂。
[0651]
在一些实施方式中,在使用主体材料的情况下,作为包含在发光层中的发光材料,本发明的化合物的量为0.1重量%以上。在一些实施方式中,在使用主体材料的情况下,作为包含在发光层中的发光材料,本发明的化合物的量为1重量%以上。在一些实施方式中,在使用主体材料的情况下,作为包含在发光层中的发光材料,本发明的化合物的量为50重量%以下。在一些实施方式中,在使用主体材料的情况下,作为包含在发光层中的发光材料,本发明的化合物的量为20重量%以下。在一些实施方式中,在使用主体材料的情况下,作为包含在发光层中的发光材料,本发明的化合物的量为10重量%以下。
[0652]
在一些实施方式中,发光层中的主体材料是包含空穴传输功能和电子传输功能的有机化合物。在一些实施方式中,发光层中的主体材料是防止所发射的光的波长变长的有
机化合物。在一些实施方式中,发光层中的主体材料是具有较高玻璃化转变温度的有机化合物。
[0653]
在一些实施方式中,主体材料选自由以下材料组成的组:
[0654]
[0655]
[0656]
[0657][0658]
注入层
[0659]
注入层是电极与有机层之间的层。在一些实施方式中,注入层降低驱动电压并且增强发光亮度。在一些实施方式中,注入层包括空穴注入层和电子注入层。注入层可以位于阳极与发光层或空穴传输层之间,也可以位于阴极与发光层或电子传输层之间。在一些实施方式中,存在注入层。在一些实施方式中,不存在注入层。
[0660]
阻挡层
[0661]
阻挡层是能够抑制存在于发光层中的电荷(电子或空穴)和/或激子扩散到发光层外侧。在一些实施方式中,电子阻挡层在发光层与空穴传输层之间,并且抑制电子穿过发光层移向空穴传输层。在一些实施方式中,空穴阻挡层在发光层与电子传输层之间,并且抑制空穴穿过发光层移向电子传输层。在一些实施方式中,阻挡层抑制激子扩散到发光层外侧。在一些实施方式中,电子阻挡层和空穴阻挡层是激子阻挡层。本说明书中使用的术语“电子阻挡层”或“激子阻挡层”包括具有电子阻挡层功能和激子阻挡层功能两者的层。
[0662]
空穴阻挡层
[0663]
空穴阻挡层起到电子传输层的作用。在一些实施方式中,空穴阻挡层在传输电子的同时抑制空穴到达电子传输层。在一些实施方式中,空穴阻挡层增强电子和空穴在发光层中的重组概率。用于空穴阻挡层的材料可以是与关于电子传输层记载的材料相同的材料。
[0664]
[0665][0666]
电子阻挡层
[0667]
电子阻挡层传输空穴时,在一些实施方式中,电子阻挡层在传输空穴的同时抑制电子到达空穴传输层。在一些实施方式中,电子阻挡层增强电子和空穴在发光层中的重组概率。接着,以下,对可用作电子阻挡材料的化合物的优选例子进行说明。
[0668][0669]
激子阻挡层
[0670]
激子阻挡层抑制通过空穴和电子在发光层中重组而生成的激子扩散到电荷传输层。在一些实施方式中,激子阻挡层能够将激子有效限制在发光层中。在一些实施方式中,装置的发光效率得到了提高。在一些实施方式中,激子阻挡层在阳极侧和阴极侧中的任一侧及两侧与发光层相邻。在激子阻挡层位于阳极侧的一些实施方式中,该层可以位于空穴传输层与发光层之间且与发光层相邻。在激子阻挡层位于阴极侧的一些实施方式中,该层可以位于发光层与阴极之间且与发光层相邻。在一些实施方式中,空穴注入层、电子阻挡层
或类似层位于阳极与在阳极侧与发光层相邻的激子阻挡层之间。在一些实施方式中,空穴注入层、电子阻挡层、空穴阻挡层或类似层位于阴极与在阴极侧与发光层相邻的激子阻挡层之间。在一些实施方式中,激子阻挡层包含激发单重态能量和激发三重态能量,其中至少一个分别高于发光材料的激发单重态能量和激发三重态能量。
[0671]
空穴传输层
[0672]
空穴传输层包含空穴传输材料。在一些实施方式中,空穴传输层是单层。在一些实施方式中,空穴传输层包含多个层。
[0673]
在一些实施方式中,空穴传输材料具有空穴的注入或传输特性及电子的阻挡特性中的一种。在一些实施方式中,空穴传输材料是有机材料。在一些实施方式中,空穴传输材料是无机材料。可以用于本说明书中的现有空穴传输材料的例子包括三唑衍生物、噁二唑衍生物、咪唑衍生物、咔唑衍生物、吲哚并咔唑衍生物、聚芳基烷烃衍生物、吡唑啉衍生物、吡唑啉酮衍生物、苯二胺衍生物、芳胺衍生物、氨基取代查耳酮衍生物、噁唑衍生物、苯乙烯基蒽衍生物、芴酮衍生物、腙衍生物、芪衍生物、硅氮烷衍生物、苯胺共聚物及导电性聚合物低聚物(尤其噻吩低聚物)或这些的组合,但并不限于此。在一些实施方式中,空穴传输材料选自卟啉化合物、芳香族叔胺和苯乙烯胺化合物。在一些实施方式中,空穴传输材料是芳香族叔胺化合物。接着,以下,对可用作空穴传输材料的化合物的优选例子进行说明。
[0674]
[0675]
[0676][0677][0678]
电子传输层
[0679]
电子传输层包含电子传输材料。在一些实施方式中,电子传输层是单层。在一些实施方式中,电子传输层包含多个层。
[0680]
在一些实施方式中,电子传输材料仅需要具有将从阴极注入的电子传输到发光层的功能。在一些实施方式中,电子传输材料也起到空穴阻挡材料的作用。可以用于本说明书中的电子传输层的例子包括硝基取代芴衍生物、二苯醌衍生物、硫代吡喃二氧化物衍生物、碳二亚胺、亚芴基甲烷衍生物、蒽醌二甲烷、蒽酮衍生物、噁二唑衍生物、唑衍生物、氮杂苯衍生物或者这些的组合或这些的聚合物,但并不限于此。在一些实施方式中,电子传输材料是噻二唑衍生物或喹喔啉衍生物。在一些实施方式中,电子传输材料是聚合物材料。接着,以下,对可用作电子传输材料的化合物的优选例子进行说明。
[0681]
[0682]
[0683][0684]
分子重量
[0685]
关于由通式(i)、(ii)、(iii)或(iv)表示的化合物的分子重量,例如使用通过气相沉积法形成的包含由通式(i)、(ii)、(iii)或(iv)表示的化合物的有机层时,优选为1500道尔顿以下,更优选为1200以下,进一步优选为1000以下,更进一步优选为900以下。
[0686]
聚合物
[0687]
通式(i)、(ii)、(iii)或(iv)的化合物可以与化合物的分子重量无关地通过涂布方法形成为膜。因此,即使是具有相对大的分子重量的化合物也能够形成为膜。
[0688]
在一些实施方式中,膜包含多种独立地选自通式(i)、(ii)、(iii)或(iv)的化合物。在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物被改性以混合聚合性基团。然后,改性化合物进行聚合来获得包含通式(i)、(ii)、(iii)或(iv)的化合物的聚合物。例如,单体通过用聚合性官能团取代通式(i)、(ii)、(iii)或(iv)的化合物的任一个氢来获得。然
后,单体与任意另一单体进行均聚或共聚以获得具有重复单元的聚合物。或者,通式(i)、(ii)、(iii)或(iv)的不同化合物进行耦合以获得二聚体或三聚体。具有重复单元(包含通式(i)、(ii)、(iii)或(iv)的化合物)的聚合物的例子包括包含通式(a)或(b)的单元的聚合物。
[0689][0690]
其中:
[0691]
q表示包含通式(i)、(ii)、(iii)或(iv)的化合物的基团;
[0692]
l1及l2分别表示连接基团;
[0693]
r
101
、r
102
、r
103
及r
104
分别独立地表示取代基。
[0694]
在一些实施方式中,连接基团优选为0~20个碳,更优选为1~15个碳,进一步优选为2~10个碳。在一些实施方式中,连接部分是-x
11-l
11-;其中x
11
是氧或硫,l
11
表示连接基团。
[0695]
在一些实施方式中,x
11
为氧。在一些实施方式中,l
11
为经取代或未经取代的亚烷基或经取代或未经取代的亚芳基。在一些实施方式中,经取代或未经取代的亚烷基为c1-c10亚烷基。在一些实施方式中,经取代或未经取代的亚芳基为经取代或未经取代的亚苯基。
[0696]
在一些实施方式中,r
101
、r
102
、r
103
及r
104
独立地为具有1~6个碳原子的经取代或未经取代的烷基、具有1~6个碳原子的经取代或未经取代的烷氧基或卤素原子。在一些实施方式中,r
101
、r
102
、r
103
及r
104
独立地为具有1~3个碳原子的未经取代的烷基、具有1~3个碳原子的未经取代的烷氧基、氟原子或氯原子。在一些实施方式中,r
101
、r
102
、r
103
及r
104
独立地为具有1~3个碳原子的未经取代的烷基或具有1~3个碳原子的未经取代的烷氧基。
[0697]
l1及l2可以通过取代通式(i)、(ii)、(iii)或(iv)的结构中的任一个氢来导入。2个以上连接基团可以与1个q键合而形成交联结构或网状结构。
[0698]
重复单元的具体的结构例包括由下述通式(c)~(f)表示的结构。
[0699][0700]
具有通式(c)~(f)的重复单元的聚合物可以通过用羟基取代任一个氢来合成为通式(i)、(ii)、(iii)或(iv)的结构,之后利用起到连接作用的羟基,通过与任意下述化合物进行反应而将聚合性基团导入该结构,并使聚合性基团进行聚合。
[0701][0702]
包含由通式(i)、(ii)、(iii)或(iv)表示的结构的聚合物可以为单独包含具有由通式(i)、(ii)、(iii)或(iv)表示的结构的重复单元的聚合物或可以为包含具有任意其他结构的重复单元的聚合物。在聚合物中包含的具有由通式(i)、(ii)、(iii)或(iv)表示的结构的重复单元可以为仅1种类型,或可以包含2种类型的重复单元。不具有由通式(i)、(ii)、(iii)或(iv)表示的结构的重复单元包括衍生自一般共聚中使用的单体。例如,记载有衍生自具有烯属不饱和键(例如乙烯、苯乙烯等)单体的重复单元。
[0703]
在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物包含在本发明的装置的发光层中。在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物包含在发光层及至少一个另一层中。在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物针对各层独立地选择。在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物相同。在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物不同。例如,由通式(i)、(ii)、(iii)或(iv)表示的化合物可以用于上述注入层、阻挡层、空穴阻挡层、电子阻挡层、激子阻挡层、空穴传输层、电子传输层等。层的膜形成方法并无特别限制,层可以通过任意干式工艺和/或湿式工艺制造。
[0704]
以上示出了用于有机电致发光装置中的材料的具体例,但可以用于本发明中的材料不应解释为限定于示例性化合物。在一些实施方式中,具有特定功能的材料也能够具有另一功能。
[0705]
膜形成方法
[0706]
本发明的化合物可以通过任意方法在基板上形成为膜。
[0707]
在形成膜之前,可以加热或冷却基板,并通过改变基板的温度来控制膜质量和膜中的分子聚集。基板的温度并无特别限制,优选在0~200℃的范围内,更优选在15~100℃的范围内,尤其优选在20~95℃的范围内。
[0708]
在基板上形成本发明的化合物的膜之前,可以通过真空工艺或溶液工艺来形成膜,两种工艺均优选。
[0709]
通过真空工艺形成膜的具体例包括真空沉积、溅射方法、离子镀方法及分子束外延(mbe)等物理气相沉积,以及等离子聚合等化学气相沉积(cvd),并且优选使用真空沉积。
[0710]
通过溶液工艺形成膜表示一种将有机化合物溶解于能够溶解有机化合物的溶剂中,并利用所获得的溶液形成膜的方法。其具体例包括涂布法(例如流延法、浸涂法、模涂法、辊涂、棒涂法、旋涂法)、印刷法(例如喷墨法、网版印刷法、凹版印刷法、柔性版印刷法、平版印刷法及微接触印刷法)及朗缪尔-布洛杰特(lb)方法等常规方法,优选使用喷墨法、凹版印刷法、柔性版印刷法、平版印刷法及微接触印刷法。
[0711]
以下,对能够在基于溶液工艺的膜形成中使用的本发明的有机半导体装置用涂布溶液进行说明。
[0712]
通过溶液工艺在基板上形成膜的情况下,层形成用材料可以溶解或分散在合适的有机溶剂(例如,己烷、辛烷、癸烷、甲苯、二甲苯、均三甲苯、乙基苯、十氢萘及1-甲基萘等烃
溶剂;丙酮、甲基乙基酮、甲基异丁酮及环己酮等酮类溶剂;二氯甲烷、氯仿、四氯甲烷、二氯乙烷、三氯乙烷、四氯乙烷、氯苯、二氯苯及氯甲苯等卤代烃溶剂;乙酸乙酯、乙酸丁酯及乙酸戊酯等酯类溶剂;甲醇、乙醇、丙醇、丁醇、戊醇、己醇、环己醇、甲基溶纤剂、乙基溶纤剂及乙二醇等醇类溶剂;二乙醚、二丁醚、四氢呋喃、二噁烷及苯甲醚等醚类溶剂;n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、1-甲基-2-吡咯烷酮及1-甲基-2-咪唑啉酮等酰胺或酰亚胺类溶剂;二甲基亚砜等亚砜类溶剂;乙腈等腈类溶剂)和/或水中以制备涂布液,之后可以用各种涂布方法涂布该涂布液以形成薄膜。
[0713]
装置
[0714]
在一些实施方式中,本发明的化合物包含在装置中。例如,装置包括oled灯泡、oled灯、电视屏幕、计算机显示器、移动电话和平板电脑,但并不限于此。
[0715]
在一些实施方式中,电子装置包含oled,该oled包含阳极、阴极及至少一个包含位于阳极与阴极之间的发光层的有机层,其中该发光层包含:
[0716]
主体材料;及
[0717]
通式(i)、(ii)、(iii)或(iv)的化合物。
[0718]
在一些实施方式中,发光层包含通式(i)、(ii)、(iii)或(iv)的化合物作为发光材料。
[0719]
在一些实施方式中,发光层包含通式(i)、(ii)、(iii)或(iv)的化合物作为辅助掺杂剂。
[0720]
在一些实施方式中,oled的发光层进一步包含荧光材料,其中针对荧光发射体,通式(i)、(ii)、(iii)或(iv)的化合物将三重态转变成单重态。
[0721]
在一些实施方式中,本说明书中记载的组合物可以包含在oled或光伏装置等各种光敏性或光活化装置中。在一些实施方式中,组合物可以用于促进装置内的电荷转移或能量转移和/或用作空穴传输材料。例如,装置可以是有机发光二极管(oled)、有机集成电路(o-ic)、有机场效应晶体管(o-fet)、有机薄膜晶体管(o-tft)、有机发光晶体管(o-let)、有机太阳能电池(o-sc)、有机光检测器、有机感光器、有机场淬灭装置(o-fqd)、发光电化学电池(lec)或有机激光二极管(o-laser)。
[0722]
灯泡或灯
[0723]
在一些实施方式中,电子装置包含oled,该oled包含阳极、阴极及至少一个包含位于阳极与阴极之间的发光层的有机层,其中该发光层包含:
[0724]
主体材料;
[0725]
通式(i)、(ii)、(iii)或(iv)的化合物(其中,通式(i)、(ii)、(iii)或(iv)的化合物为发光材料);及
[0726]
oled驱动电路。
[0727]
在一些实施方式中,发光层包含通式(i)、(ii)、(iii)或(iv)的化合物作为辅助掺杂剂。
[0728]
在一些实施方式中,装置包含颜色不同的oled。在一些实施方式中,装置包括包含oled组合的阵列。在一些实施方式中,oled的组合是3种颜色的组合(例如rgb)。在一些实施方式中,oled的组合是非为红色、绿色或蓝色(例如,橙色和黄色绿色)的颜色的组合。在一些实施方式中,oled的组合是2种、4种或更多颜色的组合。
[0729]
在一些实施方式中,装置是包含以下部分的oled灯:
[0730]
电路板,具有具备安装面的第一侧和与其相反的第二侧且界定至少一个开口;
[0731]
至少一个oled,其位于安装面上,构成为发出光的该至少一个oled包含:
[0732]
阳极、阴极及至少一个包含位于阳极与阴极之间的发光层的有机层,其中该发光层包含:
[0733]
主体材料;
[0734]
通式(i)、(ii)、(iii)或(iv)的化合物(其中通式(i)、(ii)、(iii)或(iv)的化合物为发光材料);
[0735]
电路板用外壳;及
[0736]
设置于外壳末端的至少一个连接器,该外壳和连接器界定适合设置于灯具的套件(package)。
[0737]
在一些实施方式中,发光层包含通式(i)、(ii)、(iii)或(iv)的化合物作为辅助掺杂剂。
[0738]
在一些实施方式中,oled灯包含安装在电路板上以使光沿多个方向发出的多个oled。在一些实施方式中,沿第一方向发出的光的一部分被偏转成沿第二方向发出。在一些实施方式中,反射器用于使沿第一方向发出的光偏转。
[0739]
显示器或屏幕
[0740]
在一些实施方式中,通式(i)、(ii)、(iii)或(iv)的化合物能够用于屏幕或显示器。在一些实施方式中,利用包括真空蒸镀、沉积、气相沉积或化学气相沉积(cvd)(但不限于此)的工艺,将通式(i)、(ii)、(iii)或(iv)的化合物沉积到基板上。在一些实施方式中,基板是可以在提供纵横比独特的像素的双侧蚀刻中使用的感光板结构。屏幕(也可以被称为掩模)用于oled显示器中的制造工艺中。相应的原图(artwork)图案设计使垂直方向上的像素与水平面上的大范围的斜面开口之间的陡而窄的系杆(tie-bar)变得容易。由此,优化向tft背板上的化学沉积的同时,可实现高清显示器所需像素的近似图案化。
[0741]
像素的内部图案化可以以水平和垂直方向上的不同纵横比构成三维像素开口。另外,在像素区域内使用成像的“条纹”或半色调圆会抑制特定区域中的蚀刻,直至这些特定图案被底切而从基板掉落。此时,整个像素区域中的蚀刻速率相同,但深度会根据半色调图案而不同。改变半色调图案的尺寸和间距可以在像素内以不同速率抑制蚀刻,因此能够进行用于生成陡而垂直的斜面的局部深的蚀刻。
[0742]
用于沉积掩模的优选材料是殷钢。殷钢是在钢厂中冷轧成长薄板的金属合金。殷钢无法作为镍掩模电沉积至旋转芯轴上。用于在沉积用掩模上形成开口区域的优选且成本上可行的方法是利用湿式化学蚀刻的方法。
[0743]
在一些实施方式中,屏幕或显示器图案是基板上的像素矩阵。在一些实施方式中,使用蚀刻法(例如光刻法和电子束蚀刻法)来制造屏幕或显示器图案。在一些实施方式中,使用湿式化学蚀刻来制造屏幕或显示器图案。在另一实施方式中,使用等离子蚀刻来制造屏幕或显示器图案。
[0744]
使用公开化合物的装置的制造方法
[0745]
通常形成较大母板之后,以单元面板为单位切割母板,由此制造oled显示器。通常,如下形成母板上的每个单元面板:在主基板上形成包括活化层和源电极/漏电极的薄膜
晶体管,将平坦化膜贴附到该tft上,接着依次形成像素电极、发光层、对电极及封装层,之后从母板上切割。
[0746]
通常形成较大母之后,以单元面板为单位切割母板,由此制造oled显示器。通常,如下形成母板上的每个单元面板:在主基板上形成包括活化层和源电极/漏电极的薄膜晶体管,将平坦化膜贴附到该tft上,接着依次形成像素电极、发光层、对电极及封装层,之后从母板上切割。
[0747]
在另一方式中,本发明提供一种有机发光二极管(oled)显示器的制造方法,该方法包括:
[0748]
在母板的主基板上形成阻挡层的步骤;
[0749]
在该阻挡层上,以单元面板为单位形成多个显示单元的步骤;
[0750]
在该单元面板的每个显示单元上形成封装层的步骤;及
[0751]
在该单元面板之间的界面部分贴附有机膜的步骤。
[0752]
在一些实施方式中,阻挡层是例如由sinx形成的无机膜,并且阻挡层的边缘部分覆盖有由聚酰亚胺或丙烯酸形成的有机膜。在一些实施方式中,有机膜有助于以单元面板为单位轻轻地切割母板。
[0753]
在一些实施方式中,薄膜晶体管(tft)层包括发光层、闸电极及源电极/漏电极。多个显示单元中的每一个均可以包括薄膜晶体管(tft)、形成于tft层上的平坦化膜和及形成于平坦化膜上的发光单元,其中贴附于界面部分的有机膜由与平坦化膜的材料相同的材料形成且形成平坦化膜的同时形成。在一些实施方式中,发光单元与tft层隔着位于该两者之间的钝化层和平坦化膜而连接,并且发光单元与覆盖并保护发光单元的封装层连接。在制造方法的一些实施方式中,有机膜既不接触显示单元也不接触封装层。
[0754]
有机膜和平坦化膜中的每一个均可以包含聚酰亚胺和丙烯酸中的任一种。在一些实施方式中,阻挡层可以是无机膜。在一些实施方式中,主基板可以由聚酰亚胺形成。该方法可以进一步包括如下步骤:在由聚酰亚胺形成的主基板的一个表面形成阻挡层之前,使由玻璃材料形成的载体基板接触主基板的另一个表面且在沿着界面部分切割之前,从主基板分离出载体基板。在一些实施方式中,oled显示器是柔性显示器。
[0755]
在一些实施方式中,钝化层是设置于tft层上以覆盖tft层的有机膜。在一些实施方式中,平坦化膜是在钝化层上形成的有机膜。在一些实施方式中,平坦化膜与在阻挡层边缘部分上形成的有机膜相同地由聚酰亚胺或丙烯酸形成。在一些实施方式中,平坦化膜和有机膜在制造oled显示器的同时形成。在一些实施方式中,有机膜可以在阻挡层的边缘部分形成,以使有机膜的一部分直接接触主基板且使有机膜的剩余部分包围阻挡层的边缘部分的同时接触阻挡层。
[0756]
在一些实施方式中,发光层包含像素电极、对电极及设置于像素电极与对电极之间的有机发光层。在一些实施方式中,像素电极连接于tft层的源电极/漏电极。
[0757]
在一些实施方式中,经由tft层向像素电极施加电压时,在像素电极与对电极之间形成适当的电压,由此有机发光层发光而形成图像。以下,将包括tft层和发光单元的图像形成单元称为显示单元。
[0758]
在一些实施方式中,覆盖显示单元且防止外部水分渗透的封装层可以形成为具有有机膜和无机膜交替层叠的薄膜包封结构。在一些实施方式中,封装层具有层叠有多个薄
膜的薄膜包封结构。在一些实施方式中,贴附于界面部分的有机膜分别从多个显示单元分开。在一些实施方式中,形成有机膜以使有机膜的一部分直接接触主基板且使有机膜的剩余部分包围阻挡层边缘部分的同时接触阻挡层。
[0759]
在一个实施方式中,oled显示器具有挠性且使用由聚酰亚胺形成的柔性主基板。在一些实施方式中,在由玻璃材料形成的载体基板上形成主基板,之后分离载体基板。
[0760]
在一些实施方式中,阻挡层形成于与载体基板相对的主基板表面上。在一实施方式中,阻挡层根据每个单元面板的尺寸进行图案化。例如,主基板在母板的整个表面上形成,而阻挡层则根据各单元面板的尺寸形成,因此在单元面板的阻挡层之间的界面部分会形成凹槽。各单元面板可以沿着凹槽切割。
[0761]
在一些实施方式中,制造方法进一步包括沿着界面部分切割的步骤,其中在阻挡层中形成凹槽,有机膜的至少一部分形成于凹槽,凹槽不会穿透主基板。在一些实施方式中,形成各单元面板的tft层,将作为无机膜的钝化层和作为有机膜的平坦化膜设置于tft层上以覆盖tft层。形成例如由聚酰亚胺或丙烯酸形成的平坦化膜的同时,界面部分的凹槽例如被由聚酰亚胺或丙烯酸形成的有机膜覆盖。这是为了使有机膜吸收沿着界面部分的凹槽切割各单元面板时产生的冲击而防止产生龟裂。即,若整个阻挡层在没有有机膜的情况下完全暴露,则在沿着界面部分的凹槽切割各单元面板时产生的冲击会转移到阻挡层,由此增加龟裂的风险。然而,在一实施方式中,位于阻挡层之间的界面部分的凹槽被有机膜覆盖且有机膜吸收原本会转移到阻挡层的冲击,因此可以轻轻地切割各单元面板而可以防止在阻挡层中产生龟裂。在一个实施方式中,覆盖位于界面部分凹槽的有机膜与平坦化膜彼此分离。例如,若有机膜与平坦化膜彼此连接而作为一个层,则由于外部水分有可能经由平坦化膜和残留有有机膜的一部分渗透到显示单元,因此有机膜与平坦化膜彼此分离以使有机膜与显示单元分离。
[0762]
在一些实施方式中,显示单元通过形成发光单元来形成,并将封装层设置于显示单元上以覆盖显示单元。如此,若母板制造完成,则使支撑主基板的载体基板从主基板分离。在一些实施方式中,向载体基板发射激光束时,因载体基板与主基板之间的热膨胀系数之差而使载体基板从主基板分离。
[0763]
在一些实施方式中,以单元面板为单位切割母板。在一些实施方式中,通过使用切割机,沿着单元面板之间的界面部分切割母板。在一些实施方式中,由于位于界面部分(模板沿其切割)的凹槽被有机膜覆盖,因此有机膜吸收切割期间产生的冲击。在一些实施方式中,可以在切割期间防止在阻挡层中产生龟裂。
[0764]
在一些实施方式中,该方法降低产品的缺陷率且使产品的品质稳定。
[0765]
又一方式是一种oled显示器,其包括:形成于主基板上的阻挡层;形成于阻挡层的显示单元;形成于显示单元的封装层;及贴附于阻挡层的边缘部分的有机膜。
[0766]
实施例
[0767]
本发明的一实施方式提供根据以下实施例的步骤,使用适当的材料来制备通式(i)、(ii)、(iii)或(iv)的化合物的内容。本领域技术人员应理解,以下制备步骤的条件和工艺的已知变形可以用于制备这些化合物。另外,通过利用详细说明的步骤,本领域技术人员可以制备本发明的其他化合物。
[0768]
分析方法的一般信息
[0769]
参考以下实施例,对本发明的特征进行更具体的说明。只要不脱离本发明的主旨,以下所示的材料、工艺、工序等可以进行适当变更。因此,本发明的范围不应解释为限定于以下所示的具体例。试样的特性通过利用nmr(核磁共振500mhz,bruker公司制)、lc/ms(液相色谱-质谱联用仪,waters corp制)、ac3(riken keiki co.,ltd.制)、高性能uv/vis/nir光谱仪(lambda950,perkinelmer,co.,ltd.制)、荧光光谱仪(fluoromax-4,horiba,ltd.制)、光学多道分析仪(pma-12c10027-01,hamamatsu photonics k.k.制)、绝对量子产率测试系统(c11347,hamamatsu photonics k.k.制)、自动电流电压亮度测试系统(ets-170,system engineers co.,ltd制)、寿命测试系统(eas-26c,system engineers co.,ltd制)及条纹相机(model c4334,hamamatsu photonics k.k.制)来进行了评价。
[0770]
实施例1
[0771]
将有机电致发光装置为一例,如下记载上述特征的原理。
[0772]
在有机电致发光装置中,将载流子从阳极和阴极注入到发光材料中以形成用于发光的发光材料的激发态。在载流子注入型有机电致发光装置的情况下,通常,被激发成激发单重态的激子是所产生总激子的25%,剩余75%被激发成激发三重态。因此,使用作为来自激发三重态的发光的磷光提供较高的能量利用率。然而,由于激发三重态的寿命较长,会通过与位于激发三重态的激子相互作用而导致激发态饱和和能量失活,因此磷光的量子产率通常不高。延迟荧光材料通过以下机制发射荧光:激子能量通过系间窜越等而转变成激发三重态,之后通过由三重态-三重态湮灭或热能吸收所致的反向系间窜越而转变成激发单重态,由此发射荧光。认为在上述材料中,通过吸收热能发光的热活化型延迟荧光材料尤其可用于有机电致发光装置。在有机电致发光装置中使用延迟荧光材料的情况下,激发单重态的激子通常发射荧光。另一方面,激发三重态的激子通过跃迁到激发单重态(通过吸收装置中产生的热而形成)的系间窜越发射荧光。此时,通过从激发三重态到激发单重态的反向系间窜越发射的光具有与荧光相同的波长,这是因为光发射来自激发单重态但具有比正常荧光和磷光更长的寿命(发光寿命),因此观察到的光为比正常荧光和磷光延迟的荧光。光可以定义为延迟荧光。使用热活化型激子跃迁机制,可以通过注入载流子后吸收热能,将通常仅以25%的比例形成的激发单重态的化合物的比例提高为25%以上。在低于100℃的低温下发射强荧光和延迟荧光的化合物通过利用装置热量充分进行从激发三重态到激发单重态的系间窜越而发射延迟荧光,因此使用化合物可以大幅提高发光效率。
[0773]
实施例2
[0774]
本发明的化合物能够通过本领域技术人员已知的任何方法来合成。化合物由一般可用的起始材料合成。各种部分能够经由线性或分支型合成途径来组合。
[0775]
化合物1的合成
[0776][0777]
2,6-二氟-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼烷-2-基)苯甲腈(a)的合成
[0778]
将4-溴-2,6-二氟苯甲腈(499mg,2.29mmol)、双(频哪醇合)二硼(700mg,2.75mmol)、[1,1'-双(二苯基膦)二茂铁]二氯化钯(ii)(84.9mg,0.115mmol)、无水乙酸钾(675mg,6.88mmol)及1,4-二噁烷(10ml)投入三口烧瓶中,并将所获得的溶液在110℃、氮气气氛下搅拌了2小时。冷却至室温之后,将反应混合物用硅藻土垫过滤,用氯仿冲洗,并对所获得的滤液进行了真空蒸发。使用己烷/乙酸乙酯作为洗脱液,通过硅胶柱层析纯化所获得的剩余部分,由此获得了米色固体(0.618g,定量产率)。
[0779]1h nmr(500mhz,cdcl3,δ):7.43(d,j=8.0hz,2h),1.35(s,12h);apci-ms m/z:266.2m
+
。
[0780]
4-(4,6-二苯基-1,3,5-三嗪-2-基)-2,6-二氟苯甲腈(b)的合成
[0781]
将化合物a(618mg,1.83mmol)、2-溴-4,6-二苯基-1,3,5-三嗪(689mg,2.20mmol)、pd(pph3)4(110mg,0.0918mmol)、碳酸钾(774mg,5.51mmol)溶解于脱气去离子水(3ml)及脱气thf(9ml)中的混合物在80℃、氮气气氛下搅拌了17小时。冷却至室温之后,将反应混合物用硅藻土垫过滤,用氯仿冲洗,并对所获得的滤液进行了真空蒸发。使用3:2(v/v)己烷/甲苯作为洗脱液,通过硅胶柱层析纯化所获得的剩余部分,由此获得了白色固体(0.484g,57.0%)。
[0782]1h nmr(500mhz,cdcl3,δ):8.75(d,j=8.0hz,4h),8.45(d,j=8.5hz,2h),7.67(t,j=7.5hz,2h),7.61(t,j=7.5hz,4h);apci-ms m/z:373.1m
+
。
[0783]
2,6-二(9h-咔唑-9-基)-4-(4,6-二苯基-1,3,5-三嗪-2-基)苯甲腈(1)的合成
[0784]
将化合物c(251mg,0.675mmol)、咔唑(284g,1.69mmol)及碳酸钾(283g,2.03mmol)混合于n,n-二甲基甲酰胺(dmf)10ml中的混合物在140℃、环境气体下搅拌了2小时。将反应混合物倒入大量meoh中,由此获得了黄色沉淀物。过滤后,用meoh清洗所获得的固体,由此获得了黄色饼状物。使用2:3(v/v)石油醚/氯仿作为洗脱液,通过硅胶柱层析纯化混合物,由此获得了绿黄色固体(442g,98.5%)。
[0785]1h nmr(500mhz,cdcl3,δ):9.14(s,2h),8.68(d,j=7.0hz,4h),8.23(d,j=8.0hz,4h),7.60(t,j=7.5hz,2h),7.56-7.51(m,8h),7.47-7.39(m,8h);apci-ms m/z:665.3m
+
。
[0786]
化合物2的合成
[0787][0788]
2'-(4,6-二苯基-1,3,5-三嗪-2-基)-4',6'-二氟-[1,1':3',1
”-
三联苯]-5'-甲腈(c)的合成
[0789]
在带有搅拌棒的双口烧瓶中投入了化合物b(0.50g,1.35mmol)、碳酸钾(0.47g,3.38mmol)、乙酸钯(12.6mg,0.0405mmol)及三环己基膦(35.6mg,0.122mmol),抽真空并重新充氮气3次。对反应混合物添加溴苯(0.57ml,5.40mmol)、2-乙基己酸(0.02ml,0.135mmol)及二甲苯(10ml),在室温下搅拌15分钟之后加热至150℃。搅拌18小时之后,将反应混合物冷却至室温,用chcl3(10ml)和水(10ml)稀释,用硅藻土垫过滤之后用chcl3进行
了清洗。分离水层,并用chcl3(20ml)进行了萃取。将合并的有机层用盐水清洗并用无水硫酸镁进行了干燥。对溶剂进行真空蒸发,使用1:1(v/v)己烷/chcl3作为洗脱液,通过硅胶柱层析纯化粗产物,由此获得了白色固体(0.211g,30.0%)。
[0790]1h nmr(500mhz,cdcl3,δ):8.17(d,j=7.0hz,4h),7.54(t,j=8.0hz,2h),7.43(t,j=8.0hz,4h),7.25-7.21(m,8h),7.16(t,j=7.0hz,2h)。
[0791]
4',6'-二(9h-咔唑-9-基)-2'-(4,6-二苯基-1,3,5-三嗪-2-基)-[1,1':3',1
”-
三联苯]-5'-甲腈(2)的合成
[0792]
将化合物d(459mg,0.896mmol)、咔唑(374mg,2.24mmol)及碳酸钾(379mg,2.03mmol)混合于n,n-二甲基甲酰胺(dmf)10ml中的混合物在140℃、环境气体下搅拌了2小时。将反应混合物倒入大量meoh中,由此获得了沉淀物。过滤后,用meoh清洗所获得的固体,由此获得了绿灰色饼。使用1:3(v/v)己烷/氯仿作为洗脱液,通过硅胶柱层析纯化混合物,由此获得了淡黄色固体(0.660g,90.2%)。
[0793]1h nmr(500mhz,cdcl3,δ):8.15(d,j=8.0hz,4h),7.98(d,j=8.0hz,4h),7.51(t,j=7.5hz,2h),7.43-7.37(m,8h),7.35(d,j=8.5hz,4h),7.23(t,j=8.0hz,4h),7.00-6.98(m,4h),6.71-6.70(m,6h);maldi-ms m/z:815.7m
+
。
[0794]
化合物3的合成
[0795][0796]
2,3,5,6-四(9h-咔唑-9-基)-4-(4,6-二苯基嘧啶-2-基)苯甲腈(3)的合成
[0797]
将k2co3(1.07g,7.77mmol)和9h-咔唑(0.861g,5.15mmol)混合于nmp(40ml)中的混合物在室温下搅拌1小时,之后添加了化合物1(0.42g,1.03mmol)。将混合物在100℃下搅拌了48小时。用h2o淬冷了反应混合物。过滤沉淀产物,用meoh清洗,由ch2cl2/meoh再结晶,由此以76%的产率获得了黄色粉末的化合物2(0.786g,0.79mmol)。
[0798]1h-nmr(500mhz,cdcl3,δ):7.79(d,j=7.5hz,4h),7.46(d,j=7.5hz,4h),7.38(d,j=7.5hz,4h),7.25-7.09(m,14h),6.99(t,j=7.5hz,4h),6.95-6.87(m,9h),6.64(d,j=7.5hz,4h)。ms(asap):993.4(m
+
)。c
71
h
43
n7的计算值:993.4。
[0799]
化合物4的合成
[0800]
[0801]
4-(4,6-二苯基-1,3,5-三嗪-2-基)-2,3,5,6-四氟苯甲腈(e)的合成
[0802]
将2-碘-4,6-二苯基-1,3,5-三嗪(4.10g,11.42mmol)、2,3,5,6-四氟苯甲腈(3.0g,17.12mmol)、k3po4(4.85g,22.83mmol)、cui(0.65g,3.42mmol)及1,10-二氮杂菲(0.62g,3.44mmol)混合于dmf(80ml)和二甲苯(80ml)中的混合物在100℃下搅拌了72小时。将反应混合物用h2o淬冷,用盐水清洗,用etoac洗脱,用mgso4干燥,并在减压下进行了浓缩。对所获得的混合物进行硅胶柱层析(己烷:甲苯=2:1),由此以30.1%的产率获得了白色粉末的化合物f(1.40g,3.44mmol)。
[0803]1h-nmr(500mhz,cdcl3,δ):8.68-8.66(m,4h),7.67-7.56(m,6h)。ms(asap):406.8(m
+
)。c
22
h
10
f4n4的计算值:406.1。
[0804]
2,3,5,6-四(9h-咔唑-9-基)-4-(4,6-二苯基-1,3,5-三嗪-2-基)苯甲腈(4)的合成
[0805]
将k2co3(2.81g,20.3mmol)和9h-咔唑(2.26g,13.54mmol)混合于nmp(35ml)中的混合物在室温下搅拌1小时,之后添加了化合物e(1.1g,2.71mmol)。将混合物在100℃下搅拌了24小时。用h2o淬冷了反应混合物。过滤沉淀产物,用meoh清洗,并进行了硅胶柱层析(己烷:chcl3=1:1),由此以88.9%的产率获得了黄色粉末的化合物4(2.40g,2.41mmol)。
[0806]1h-nmr(500mhz,cdcl3,δ):7.79(d,j=7.5hz,4h),7.44(d,j=7.5hz,4h),7.39(d,j=7.5hz,4h),7.29-7.10(m,18h),7.02-6.98(m,8h),6.91(t,j=7.5hz,4h)。
[0807]
ms(asap):994.4(m
+
)。c
70
h
42
n8的计算值:994.4。
[0808]
化合物5的合成
[0809][0810]
3-(4,6-二苯基-1,3,5-三嗪-2-基)-2,4,5,6-四氟苯甲腈(f)的合成
[0811]
在带有搅拌棒的双口烧瓶中投入了2,3,4,6-四氟苯甲腈(1.52g,8.57mmol)、2-溴-4,6-二苯基-1,3,5-三嗪(2.68g,8.57mmol)、碳酸钾(1.79g,12.85mmol)、乙酸钯(58mg,0.26mmol)及三环己基膦(218mg,0.771mmol)的,抽真空并重新充氮气3次。对反应混合物添加2-乙基己酸(0.14ml,0.857mmol)和二甲苯(50ml),在室温下搅拌15分钟之后加热至130℃。搅拌15小时之后,将反应混合物冷却至室温,用chcl3(10ml)和水(10ml)稀释,用硅藻土垫过滤之后用chcl3和水进行了清洗。分离水层,并用chcl3(20ml)进行了萃取。将合并的有机层用盐水清洗并用无水硫酸镁进行了干燥。对溶剂进行真空蒸发,使用2:1(v/v/v)己烷/chcl3作为洗脱液,通过硅胶柱层析纯化粗产物,由此获得了淡黄色固体(0.45g,412.9%)。
[0812]1h nmr(500mhz,cdcl3,δ):8.67(d,j=7.5hz,4h),7.65(t,j=7.5hz,2h),7.58(t,j=8.0hz,4h);esi-ms m/z:407m
+
。
[0813]
2,3,4,6-四(9h-咔唑-9-基)-5-(4,6-二苯基-1,3,5-三嗪-2-基)苯甲腈(5)的合成
[0814]
将咔唑(0.65g,3.88mmol)、化合物f(0.35g,0.861mmol)及碳酸钾(0.60g,
4.31mmol)混合于n,n-二甲基甲酰胺(dmf)10ml中的混合物在140℃、环境气体下搅拌了3小时。将反应混合物倒入meoh,由此获得了黄色沉淀物。过滤后,用meoh清洗所获得的固体,由此获得了黄色饼状物。使用2:1(v/v)氯仿/己烷作为洗脱液,通过硅胶柱层析纯化混合物,由此获得了黄色固体(0.81g,94.3%)。
[0815]1h nmr(500mhz,cdcl3,δ):7.88(d,j=7.5hz,2h),7.73(d,j=7.0hz,2h),7.50(d,j=8.0hz,2h),7.45-7.41(m,4h),7.38(d,j=8.0hz,2h),7.32(t,j=7.5hz,2h),7.29(d,j=8.0hz,2h),7.25-7.24(m,2h),7.22(m,6h),7.09-7.03(m,10h),7.93(t,j=7.5hz,2h),6.88(t,j=7.5hz,2h),6.82(t,j=7.5hz,2h),6.68(t,j=8.5hz,2h);esi-ms m/z:995m
+
。
[0816]
化合物6的合成
[0817][0818]
4'-(4,6-二苯基-1,3,5-三嗪-2-基)-2,3,5,6-四氟[1,1'-联苯]-4-甲腈(g)的合成
[0819]
将2-(4-溴苯基)-4,6-二苯基-1,3,5-三嗪(5.00g,12.88mmol)、双(频哪醇合)二硼(3.93g,15.46mmol)、[1,1'-双(二苯基膦)二茂铁]二氯化钯(ii)(0.485g,0.644mmol)、无水乙酸钾(3.81g,38.64mmol)及1,4-二噁烷(50ml)投入三口烧瓶中,并将所获得的溶液在110℃、氮气气氛下搅拌了14小时。冷却至室温之后,将反应混合物用硅藻土垫过滤,用乙酸乙酯冲洗,并对所获得的滤液进行了真空蒸发。使用10:1(v/v)己烷/乙酸乙酯作为洗脱液,通过硅胶柱层析纯化所获得的剩余部分,由此获得了米色固体(4.74g,84.5%)。1h nmr(500mhz,cdcl3,δ):8.79(d,j=8.0hz,4h),8.76(d,j=8.5hz,2h),8.01(d,j=8.5hz,2h),7.64-7.57(m,6h),1.40(s,12h)。
[0820]
2,4-二苯基-6-(4-(4,4,5,5-四甲基-1,3,2-二氧杂硼烷-2-基)苯基)-1,3,5-三嗪(h)的合成
[0821]
将化合物g(6.50g,14.93mmol)、4-溴-2,3,5,6-四氟苯甲腈(3.86g,15.23mmol)、pd(pph3)4(871mg,0.747mmol)、碳酸钾(6.21g,44.79mmol)溶解于脱气去离子水(20ml)及脱气thf(60ml)中的混合物在80℃、氮气气氛下搅拌了24小时。冷却至室温之后,对反应混合物添加甲醇(400ml),并进行了过滤。依次用水(20ml)和甲醇(20ml)清洗所获得的固体,并最终进行了真空干燥。使用3:1(v/v)己烷/甲苯作为洗脱液,通过硅胶柱层析纯化所获得的剩余部分,由此获得了白色固体(4.80g,66.6%)。
[0822]1h nmr(500mhz,cdcl3,δ):8.94(d,j=6.5hz,2h),8.80(d,j=7.0hz,4h),7.70(d,j=8.5hz,2h),7.66-7.59(m,6h);apci-ms m/z:483.4m
+
。
[0823]
2,3,5,6-四(9h-咔唑-9-基)-4'-(4,6-二苯基-1,3,5-三嗪-2-基)-[1,1'-联苯]-4-甲腈(6)的合成
[0824]
将9h-咔唑(1.88g,11.20mmol)、化合物i(12.06g,11.20mmol)及碳酸钾(4.67g,33.60mmol)混合于n-甲基-2-吡咯烷酮(nmp)190ml中的混合物在150℃、环境气体下搅拌了
2小时。将反应混合物倒入meoh,由此获得了沉淀物。过滤后,用meoh清洗所获得的固体,由此获得了粗产物。使用3:1(v/v)甲苯/己烷作为洗脱液,通过硅胶柱层析纯化混合物,由此获得了绿黄色固体(8.93g,74.4%)。
[0825]1h nmr(500mhz,cdcl3,δ):8.48(d,j=7.0hz,4h),7.92(d,j=7.0hz,2h),7.74-7.71(m,4h),7.56(d,j=7.5hz,4h),7.50(t,j=7.5hz,2h),7.42(t,j=7.5hz,4h),7.24-7.21(m,4h),7.11-7.05(m,12h),7.00-6.92(m,10h);apci-ms m/z:1071.8m
+
。
[0826]
化合物7的合成
[0827][0828]
2,4-二苯基-6-(3-(4,4,5,5-四甲基-1,3,2-二氧杂硼烷-2-基)苯基)-1,3,5-三嗪(i)的合成
[0829]
将2-(3-溴苯基)-4,6-二苯基-1,3,5-三嗪(3.02g,7.73mmol)、双(频哪醇合)二硼(2.35g,9.27mmol)、[1,1'-双(二苯基膦)二茂铁]二氯化钯(ii)(286mg,0.386mmol)、无水乙酸钾(2.29g,23.2mmol)及1,4-二噁烷(40ml)投入三口烧瓶中,并将所获得的溶液在110℃、氮气气氛下搅拌了2小时。冷却至室温之后,将反应混合物用硅藻土垫过滤,用氯仿冲洗,并对所获得的滤液进行了真空蒸发。使用1:1(v/v)己烷/甲苯作为洗脱液,通过硅胶柱层析纯化所获得的剩余部分,由此获得了白色固体(2.73g,81.1%)。
[0830]1h nmr(500mhz,cdcl3,δ):9.14(s,1h),8.88(d,j=7.5hz,1h),8.81(d,j=6.0hz,4h),8.06(d,j=7.5hz,1h),7.64-7.54(m,7h),1.42(s,12h);apci-ms m/z:436.3m
+
。
[0831]
3'-(4,6-二苯基-1,3,5-三嗪-2-基)-2,3,5,6-四氟[1,1'-联苯]-4-甲腈(j)的合成
[0832]
将化合物i(2.00g,4.59mmol)、4-溴-2,3,5,6-四氟苯甲腈(1.19g,4.69mmol)、pd(pph3)4(268mg,0.230mmol)、碳酸钾(1.90mg,13.78mmol)溶解于脱气去离子水(6ml)及脱气thf(18ml)中的混合物在80℃、氮气气氛下搅拌了18小时。冷却至室温之后,将反应混合物用硅藻土垫过滤,用氯仿冲洗,并对所获得的滤液进行了真空蒸发。使用3:2(v/v)己烷/甲苯作为洗脱液,通过硅胶柱层析纯化所获得的剩余部分,由此获得了白色固体(0.962g,43.4%)。
[0833]1h nmr(500mhz,cdcl3,δ):8.94(d,j=8.0hz,1h),8.86(s,1h),8.77(d,j=8.0hz,4h),7.77(t,j=7.5hz,1h),7.70(d,j=7.5hz,1h),7.66-7.57(m,6h)。
[0834]
2,3,5,6-四(9h-咔唑-9-基)-3'-(4,6-二苯基-1,3,5-三嗪-2-基)-[1,1'-联苯]-4-甲腈(7)的合成
[0835]
在氮气气氛、室温下,向无水四氢呋喃(20ml)中的9h-咔唑(1.51g,8.97mmol)溶液添加了氢化钠(60%分散于矿物油中,404mg,9.97mmol)。搅拌1小时后,添加化合物j(951mg,1.99mmol),并将混合物在80℃下搅拌了6小时。冷却至室温之后,将反应溶液倒入
meoh中,由此获得了沉淀物。过滤所获得的混合物,并用meoh清洗了所获得的固体。使用1/2(v/v)己烷/甲苯作为洗脱液,通过柱层析纯化剩余部分,由此获得了淡黄色固体(1.52g,45.1%)。1h nmr(500mhz,cdcl3,δ):8.30(d,j=8.5hz,4h),8.22(s,1h),8.04(d,j=8.5hz,1h),7.75-7.72(m,4h),7.56-7.51(m,4h),7.48-7.44(m,6h),7.32-7.30(m,2h),7.25-7.23(m,2h),7.19(d,j=8.0hz,2h),7.13-7.05(m,10h),6.99-6.91(m,7h),6.80(t,j=7.5hz,2h),6.64(t,j=8.0hz,1h);apci-ms m/z:1071.8m
+
。
[0836]
化合物8的合成
[0837][0838]
4'-(4,6-二苯基-1,3,5-三嗪-2-基)-3,4,5,6-四氟[1,1'-联苯]-2-甲腈(k)的合成
[0839]
将双(三苯基膦)二氯化钯(ii)(0.57mmol,0.40g)、2,3,4,5-四氟苯甲腈(11.42mmol,2.00g)、2-(4-溴苯基)-4,6-二苯基-1,3,5-三嗪(17.13mmol,6.65g)、碳酸钾(34.27mmol,4.74g)、2-乙基己酸(2.28mmol,0.33g)及三环己基膦(1.71mmol,0.48g)在氮气气氛下投入三口圆底烧瓶中。在氮气中流过一分钟之后,将其溶解于二甲苯中。将混合物的温度提高至100℃之后搅拌了一夜。在室温下,用盐水淬灭反应产物,并用氯仿萃取了混合物,用mgso4干燥之后用真空蒸发系统进行了浓缩。使用正己烷/氯仿作为洗脱液,通过硅胶柱层析纯化了混合物。获得了白色粉末产物(0.96g,17.34%的产率)。
[0840]1h nmr(500mh
z
,cdcl3)δ7.58-7.65(m,6h),7.68(d,j=8.5h
z
,2h),8.79(d,j=7h
z
,4h),8.94(d,j=8.5h
z
,2h)。
19
f nmr(470mh
z
,cdcl3)δ-152.45(td,j
f
=23.5,4.7h
z
,1f),-143.95(td,j
f
=18.8,9.4h
z
,1f),-137.47(qd,j
f
=21.2,9.4,4.7h
z
,1f),-129.61~-129.69(m,1f)ms(apci)m/z 483.10[(m+h)
+
]。
[0841]
(3s,4r,5r,6r)-3,4,5,6-四(9h-咔唑-9-基)-4'-(4,6-二苯基-1,3,5-三嗪-2-基)-[1,1'-联苯]-2-甲腈(8)的合成
[0842]
将碳酸钾(11.81mmol,1.63g)、4'-(4,6-二苯基-1,3,5-三嗪-2-基)-3,4,5,6-四氟[1,1'-联苯]-2-甲腈(k,1.97mmol,0.95g)及9h-咔唑(9.85mmol,1.65g)投入三口圆底烧瓶中。利用干燥系统干燥混合物之后,将n-甲基-2-吡咯烷酮作为溶剂,在氮气气氛下倒入烧瓶中。将反应混合物的温度保持在130℃的同时搅拌了一夜。用盐水淬灭反应产物,并用氯仿萃取了混合物。用mgso4干燥分离出的有几层,并用真空蒸发系统对溶剂进行了浓缩。使用氯仿与己烷(1:4)混合物作为洗脱液,通过柱层析分离了反应产物。获得了最终产物(1.99g,94.29%)。1h nmr(500mh
z
,cdcl3)δ6.59(q,j=8h
z
,4h),6.72-6.75(m,4h),6.93-6.97(m,4h),7.03-7.09(m,8h),7.18-7.20(m,3h),7.26-7.30(m,5h),7.51-7.58(m,10h),7.73(d,j=7h
z
,2h),8.55(d,j=8.5h
z
,2h),8.67(d,j=7h
z
,4h),ms(apci)m/z 1071.49[(m
+h)
+
]。
[0843]
实施例3
[0844]
纯净膜的制备
[0845]
在本实施例中,将在实施例2中合成的化合物2在真空度为10-3
pa以下的条件下,利用真空气相沉积法,气相沉积在石英基板上,由此形成了具有70nm厚度的膜。
[0846]
掺杂膜的制备
[0847]
将化合物2和主体材料也在真空度为10-3
pa以下的条件下,利用真空气相沉积法,由分离出的气相沉积源气相沉积在石英基板上,由此形成了具有100nm厚度的膜,化合物2的浓度为20重量%。
[0848]
光学特性的评价
[0849]
对试样照射在300k下具有300nm的波长的光,测定发光光谱,将其称为荧光。还测定了在77k下的光谱,将其称为磷光。分别根据荧光和磷光光谱的起始部分,推定了最低单重态能量(s1)及最低三重态能量(t1)。根据s1与t1之间的能隙计算了δe
st
。plqy也通过300nm的激发光进行了测定。利用条纹相机,并用337nm的激发光获得了时间分辨光谱,将发光寿命短的成分称为荧光,而将发光寿命长的成分称为延迟荧光。根据衰变曲线算出了荧光成分的寿命(τ
准时
)及延迟荧光成分的寿命(τ
延迟
)。
[0850]
oled的制备和测定
[0851]
在1.0x10-4
pa以下的真空度下,通过真空气相沉积法,将薄膜层叠在形成有由100nm厚度的氧化铟锡(ito)形成的阳极的玻璃基板上。首先,在ito上形成10nm厚度的hat-cn,并在其上形成25nm厚度的trispcz。以5nm厚度形成pyd2,之后将化合物2和主体材料由分离出的气相沉积源气相共沉积在其上,由此形成了具有30nm厚度的层,将该层称为发光层。此时,化合物2的浓度为20重量%。以10nm厚度形成sf3-trz,并在其上将sf3-trz及气相共沉积成30nm厚度,然后,将liq真空气相沉积成2nm厚度,之后将铝(al)气相沉积成100nm厚度以形成阴极,由此制造了有机电致发光装并测定了其光电特性。
[0852]
作为比较例,测定了用实施例2中合成的化合物3及5~8来代替化合物2来进行相同评价的结果和用化合物1进行相同评价的结果。
[0853][0854]
[0855][0856][0857]
*1:ito/hat-cn(10)/trispcz(25)/pyd2(5)/eml(30)/sf3-trz(10)/sf3-trz:liq=7:3(40)/liq(2)/al
[0858]
*2:ito/hat-cn(10)/trispcz(25)/pyd2(5)/eml(30)/sf3-trz(10)/sf3-trz:liq=7:3(35)/liq(2)/al
[0859]
*3:ito/hat-cn(10)/a-npd(30)/trispcz(10)/pyd2(5)/eml(30)/sf3-trz(10)/sf3-trz:liq=7:3(30)/liq(2)/al
[0860]
*4:ito/hat-cn(60)/trispcz(30)/pyd2(5)/eml(30)/sf3-trz(10)/sf3-trz:liq=7:3(30)/liq(2)/al
[0861]
*4
’
:ito/hat-cn(60)/trispcz(30)/pyd2(5)/主体材料:化合物x:tbpe=69.5:30:0.5(30)/sf3-trz(10)/sf3-trz:liq=7:3(30)/liq(2)/al
[0862]
[0863]
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
相关标签:
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



