具有二甲基环丁烷环的二酯化合物及其制备方法及其衍生的二甲基环丁烷化合物的制备方法与流程
 2021-02-02 14:02:34|
2021-02-02 14:02:34| 364|
364| 起点商标网
起点商标网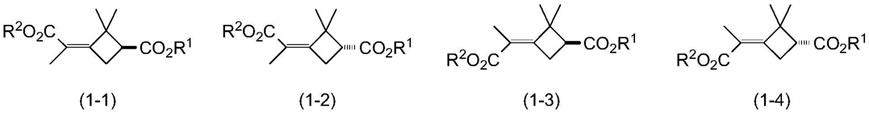
[0001]
本发明涉及具有二甲基环丁烷环的二酯化合物,其是用于合成昆虫性信息素的有用中间体,并且涉及制备该二酯化合物的方法。本发明还涉及由具有二甲基环丁烷环的二酯化合物衍生的二甲基环丁烷化合物的制备方法。
背景技术:
[0002]
昆虫性信息素是具有生物活性的物质,通常具有将雄性个体吸引到雌性个体的功能,并以少量表现出高度吸引活性。性信息素被广泛用作预测害虫暴发并确认地理传播(入侵特定区域)的手段,以及作为控制害虫的手段。广泛使用的方法有大量诱捕法、诱引并杀死或吸引并杀死方法、诱引并感染或吸引并感染方法、以及交配破坏方法。在实际使用性信息素之前,需要经济地制备足够量的信息素物质,以进行基础研究和应用。
[0003]
性信息素的化学结构中独特结构的一个例子是环丁烷结构。例如,如bierl-leonhardt等报道,在经济上危害严重的害虫并在世界范围内广泛传染柑橘类的橘臀纹粉蚧(planococcus citri,通用名:citrus mealybug)的性信息素是(+)-顺式-(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸盐(非专利文献1,如下所示)。橘小粉蚧(pseudococcus cryptyptus,通用名:citriculus mealbug)和白点椰盾蚧(acutaspis albopicta,通用名称:albopicta scale)的性信息素也具有顺式-(3-异丙烯基-2,2-二甲基环丁基)甲基羧酸酯的结构,类似于橘臀纹粉蚧的性信息素(非专利文献2和3,如下所示)。此外,还已知诸如木槿曼粉蚧(maconellicoccus hirstus,通用名:pink hibiscus mealybug)和棉花粉蚧(phenacoccus solenopsis,通用名:cotton mealybug)的种类,其性信息素为(3-异亚丙基-2,2-二甲基环丁基)甲基酯,双键的位置与橘臀纹粉蚧的性信息素的位置不同(非专利文献4和5,如下所示)。
[0004]
在制备具有这些环丁烷结构的性信息素的常用方法中,将蒎烯用作原料。例如,passaro等人报道了以下方法;蒎烯被氧化以制备马鞭草酚或马鞭草酮,然后进一步被氧化以裂解双键,随后是酮基的甲基化、羧基的还原和乙酰化以获得橘臀纹粉蚧的性信息素(非专利文献6,如上所列)。zhang等人报道了以下方法:马鞭草酮被氧化,然后进行酮的甲基化,内酯化和内酯环的裂解以构建异亚丙基,并还原羧基以制备(3-异亚丙基-2,2-二甲基环丁基)甲醇,这对应于木槿曼粉蚧和棉花粉蚧的性信息素中的醇部分(非专利文献7,如下所示)。
[0005]
现有技术列表
[0006]
[非专利文献]
[0007]
[非专利文献1]tetrahedron.lett.22,389(1981)
[0008]
[非专利文献2]j.chem.ecol.29,2213(2003)
[0009]
[非专利文献3]j.econ.entomol.105,497(2012)
[0010]
[非专利文献4]proc.natl.acad.sci.101,9601(2004)
[0011]
[非专利文献5]j.chem.ecol.42,1193(2016)
[0012]
[非专利文献6]j.agric.food chem.2004,52,2896(2004)
[0013]
[非专利文献7]tetrahedron.lett.45,9401(2004)。
技术实现要素:
[0014]
但是,在非专利文献6中记载的方法中,使用四乙酸铅或氧化铬将蒎烯氧化为马鞭草醇或马鞭草酮,会残留大量有害的重金属废物,给环境带来很大负担。此外,这些氧化剂可能引起爆炸并且在工业上不实用。使用昂贵的钌催化剂来进一步氧化马鞭草酚或马鞭草酮,因此,从经济角度考虑,工业实践是困难的。在非专利文献7中描述的制备方法中,蒎烯氧化成马鞭草酮是在氧气气氛中进行的。考虑到安全性,这在工业上难以实施,并且需要长达7天的反应时间,效率低下且不经济。此外,如非专利文献6中那样,昂贵的钌催化剂用于马鞭草酮的氧化,这是不经济的。
[0015]
迫切需要一种能够提供足够量的信息素物质的高效且工业实用的制备方法,以用于对具有环丁烷结构的性信息素化合物(如橘臀纹粉蚧的性信息素)进行基础生物学和农业研究,并进一步用于应用目的和实际使用。
[0016]
本发明就是在这样的情况下完成的,目的在于提供一种高效和工业上实用的制备二甲基环丁烷化合物的方法并提供该化合物,该化合物可用作具有环丁烷结构的性信息素化合物的合成中间体。
[0017]
为了解决上述问题而进行的深入研究的结果是,本发明人发现了一种使用具有二甲基环丁烷结构的如下通式(1)的二酯化合物来高效且工业上实用地制备具有环丁烷结构的性信息素的方法,从安全性、经济性和环境负担考虑,没有在工业上难以进行的氧化反应,因此完成了本发明。
[0018]
根据本发明的另一方面,提供了一种制备具有二甲基环丁烷环的如下通式(1)的二酯化合物的方法,
[0019][0020]
其中r
1
和r
2
彼此独立地代表具有1至10个碳原子的一价烃基,所述方法包括
[0021]
使如下通式(2)的二甲基环丁酮化合物:
[0022][0023]
其中r
1
如上限定,
[0024]
与具有如下通式(3)的膦酸酯化合物:
[0025]
r
2
o
2
c-(ch
3
)chp(o)(or
3
)
2
ꢀꢀ
(3)
[0026]
其中r
2
如上限定,并且r
3
代表具有1至10个碳原子的一价烃基,
[0027]
特别是在烯化反应,优选霍纳-沃兹沃思-埃蒙斯反应中,
[0028]
进行反应,以制备具有二甲基环丁烷环的二酯化合物(1)。
[0029]
根据本发明的另一方面,提供了一种制备具有二甲基环丁烷环的下式(4)的二醇
化合物的方法:
[0030][0031]
所述方法包括
[0032]
使具有二甲基环丁烷环的如下通式(1)的二酯化合物:
[0033][0034]
其中r
1
和r
2
彼此独立地代表具有1至10个碳原子的一价烃基,
[0035]
进行还原反应,以制备具有二甲基环丁烷环的二醇化合物(4)。
[0036]
根据本发明的另一方面,提供了一种制备如下通式(5)的二甲基环丁烷化合物的方法:
[0037][0038]
其中x
1
代表具有包括羰基的碳原子在内的1至10个碳原子的酰氧基、具有包括羰基的碳原子在内的2至10个碳原子的脂族烃氧基(alkoxy)羰氧基(carbonyloxy)、具有1至10个碳原子的脂族烃磺酰氧基(alkane sulfonyloxy)、具有6至20个碳原子的芳烃磺酰氧基、具有1至12个碳原子的脂族烃氧基、具有6至12个碳原子的芳氧基、具有3至20个碳原子的硅氧基、具有3至30个碳原子的三脂族烃基膦基(phosphonio)、具有12至30个碳原子的三芳基膦基或卤素原子;并且x
2
代表羟基、具有包括羰基的碳原子在内的1至10个碳原子的酰氧基、具有包括羰基的碳原子在内的2至10个碳原子的脂族烃氧基羰氧基、具有1至10个碳原子的脂族烃磺酰氧基、具有6至20个碳原子的芳烃磺酰氧基、具有1至12个碳原子的脂族烃氧基、具有6至12个碳原子的芳氧基、具有3至20个碳原子的硅氧基或卤素原子,
[0039]
所述方法包括
[0040]
根据前述的制备具有二甲基环丁烷环的二醇化合物(4)的方法,以及
[0041]
将具有二甲基环丁烷环的二醇化合物(4)中的hoch
2-(ch
3
)c=部分中的羟基以及任选地-ch
2
oh部分中的羟基分别改变为x
1
和x
2
,以制备二甲基环丁烷化合物(5)。
[0042]
根据本发明的另一方面,提供了一种制备异丙烯基二甲基环丁烷化合物和/或异亚丙基二甲基环丁烷化合物的方法,所述异丙烯基二甲基环丁烷化合物具有下式(6):
[0043][0044]
其中x
3
代表羟基、具有包括羰基的碳原子在内的1至10个碳原子的酰氧基、具有包括羰基的碳原子在内的2至10个碳原子的脂族烃氧基羰氧基、具有1至10个碳原子的脂族烃磺酰氧基、具有6至20个碳原子的芳烃磺酰氧基、具有1至12个碳原子的脂族烃氧基、具有6至12个碳原子的芳氧基、具有3至20个碳原子的硅氧基或卤素原子,
[0045]
所述异亚丙基二甲基环丁烷化合物具有下式(7):
[0046][0047]
其中x
3
如上限定;
[0048]
所述方法包括
[0049]
根据前述的制备二甲基环丁烷化合物(5)的方法;以及
[0050]
使二甲基环丁烷化合物(5)进行还原反应,以制备异丙烯基二甲基环丁烷化合物(6)和/或异亚丙基二甲基环丁烷化合物(7)。
[0051]
根据本发明的另一方面,提供了一种制备异丙烯基二甲基环丁烷化合物(6
′
)和/或异亚丙基二甲基环丁烷化合物(7
′
)的方法,该方法包括
[0052]
根据前述的制备异丙烯基二甲基环丁烷化合物(6)和/或异亚丙基二甲基环丁烷化合物(7)的方法,以及
[0053]
将异丙烯基二甲基环丁烷化合物(6)和/或异亚丙基二甲基环丁烷化合物(7)中的特定基团x
3
更改为如上限定的x
3
的选项中的另一个基团x
3
,以制备异丙烯基二甲基环丁烷化合物(6')和/或异亚丙基二甲基环丁烷化合物(7')。
[0054]
根据本发明的另一方面,提供了一种具有二甲基环丁烷环的如下通式(1)的二酯化合物,
[0055][0056]
其中r
1
和r
2
彼此独立地代表具有1至10个碳原子的一价烃基。
[0057]
根据本发明,可以高效且工业上实用地制备具有环丁烷结构的性信息素化合物,从安全性、经济性和环境负担考虑,没有在工业上难以进行的氧化反应。本发明适用于制备为橘臀纹粉蚧、橘小粉蚧和白点椰盾蚧的性信息素的顺式-(3-异丙烯基-2,2-二甲基环丁基)甲基酯,和为木槿曼粉蚧和棉花粉蚧的性信息素的(3-异亚丙基-2,2-二甲基环丁基)甲基酯。
具体实施方式
[0058]
在本说明书中的中间体、试剂和目标化合物的化学式中,可能存在一些在结构上具有不同取代位置的异构体,或立体异构体,例如对映体或非对映异构体。除非另有说明,否则在每种情况下,每个化学式应解释为代表所有这些异构体。此外,这些异构体可以是异构体或其组合。
[0059]
[i]具有二甲基环丁烷环的二酯化合物(1)
[0060]
首先,将说明具有二甲基环丁烷环的二酯化合物(1)。具有二甲基环丁烷环的二酯化合物(1)由下式代表。
[0061][0062]
r
1
和r
2
彼此独立地代表具有1至10个碳原子的一价烃基。r
1
和r
2
的碳原子数为1至
10,优选1至5。
[0063]
一价烃基的实例包括直链饱和脂族烃基,例如甲基(me)、乙基(et)、正丙基(pr)、正丁基(bu)、正戊基(pen)、正己基(hex)、正庚基(hep)、正辛基(oct)、正壬基(non)和正癸基(dec);支链饱和脂族烃基,例如异丙基(i-pr)、仲丁基、异丁基(i-bu)和叔丁基(t-bu);直链不饱和脂族烃基,例如2-丙烯基和2-丙炔基;支链不饱和脂族烃基,例如2-甲基-2-丙烯基;环脂族烃基,例如环丙基、2-甲基环丙基、环丁基、环戊基和环己基(c-hex);和芳族脂族烃基,例如苯基(ph)、2-甲基苯基和4-甲基苯基;并且还可以包括与上述基团具有异构关系的脂族烃基。
[0064]
这些一价烃基中的一部分氢原子可以被甲基、乙基或卤素原子取代。卤素原子的实例包括氯原子、溴原子和碘原子。
[0065]
考虑到将在下文中描述的还原反应中的反应性和/或反应后的纯化容易性,优选具有更高反应性并且可通过洗涤和浓缩容易地除去其副产物醇的具有1-4个碳原子的一价烃基。r
1
和r
2
的特别优选实例包括甲基、乙基、正丙基、异丙基、正丁基、仲丁基、异丁基和叔丁基,特别是甲基、乙基和正丙基。
[0066]
具有二甲基环丁烷环的二酯化合物(1)的实例包括下式(1-1)的(s,z)-3-(1-烷氧羰基亚乙基)-2,2-二甲基环丁烷羧酸酯化合物、下式(1-2)的(r,z)-3-(1-烷氧羰基亚乙基)-2,2-二甲基环丁烷羧酸酯化合物、下式(1-3)的(s,e)-3-(1-烷氧羰基亚乙基)-2,2-二甲基环丁烷羧酸酯化合物和下式(1-4)的(r,e)-3-(1-烷氧羰基亚乙基)-2,2-二甲基环丁烷羧酸酯化合物及其外消旋体、非对映体混合物和对映体混合物。
[0067][0068]
特别地,具有二甲基环丁烷环的二酯化合物(1)的实例包括乙基3-(1-乙氧基羰基亚乙基)-2,2-二甲基环丁烷甲酸酯(参见实施例1)和以下具有二甲基环丁烷环的二酯化合物。
[0069][0070]
[ii]具有二甲基环丁烷环的二酯化合物(1)的制备方法
[0071]
接下来,下面将解释根据以下化学反应式制备具有二甲基环丁烷环的二酯化合物(1)的方法。该方法包括使如下通式(2)的二甲基环丁酮化合物与如下通式(3)的膦酸酯化合物反应,特别是在烯烃化反应中,优选在霍纳-沃兹沃思-埃蒙斯反应中,以制备具有二甲基环丁烷环的二酯化合物(1)。
[0072][0073]
二甲基环丁酮化合物(2)中的r
1
如上限定。
[0074]
二甲基环丁酮化合物(2)的实例包括如下通式(2-1)的(s)-3-氧代-2,2-二甲基环丁烷羧酸酯化合物和(r)-3-氧代-2,2-二甲基环丁烷羧酸酯化合物(2-2),以及外消旋体和对映体混合物。
[0075][0076]
二甲基环丁酮化合物(2)的实例包括乙基2,2-二甲基-3-氧代环丁烷羧酸酯(参见下面的实施例1)。
[0077]
二甲基环丁酮化合物(2)可以单独使用或组合使用。二甲基环丁酮化合物(2)可以是商购的,也可以在室内合成。
[0078]
膦酸酯化合物(3)中的r
2
如上所限定。
[0079]
膦酸酯化合物(3)中的r
3
代表具有1至10个碳原子的一价烃基。碳原子数为1至10,
优选1至5。
[0080]
一价烃基的实例包括直链饱和脂族烃基,例如甲基、乙基、正丙基、正丁基、正戊基、正己基、正庚基、正辛基、正壬基和正癸基;支链饱和脂族烃基,例如异丙基、仲丁基、异丁基、叔丁基;直链不饱和脂族烃基,例如2-丙烯基和2-丙炔基;支链不饱和脂族烃基,例如2-甲基-2-丙烯基;环脂族烃基,例如环丙基、2-甲基环丙基、环丁基、环戊基和环己基;芳族脂族烃基,例如苯基、2-甲基苯基、4-甲基苯基;并且还可以包括与上述基团具有异构关系的脂族烃基。
[0081]
这些一价烃基的一部分氢原子可以被甲基、乙基或卤素原子取代。卤素原子的实例包括氯原子、溴原子和碘原子。
[0082]
考虑到膦酸酯化合物(3)的可获得性,r
3
的特别优选的实例包括甲基、乙基、正丙基、异丙基、正丁基和苯基。
[0083]
特别地,膦酸酯化合物(3)的实例是2-膦基丙酸三乙酯。
[0084]
膦酸酯化合物(3)可以单独使用或组合使用。膦酸酯化合物(3)可以是商购的,也可以在室内合成。
[0085]
相对于每摩尔二甲基环丁酮化合物(2),膦酸酯化合物(3)的用量优选为0.7至5.0摩尔,更优选为0.8至4.0摩尔,并且甚至更优选为0.9至3.0摩尔。
[0086]
在上述反应中使用的碱的实例包括醇盐,例如甲醇钠、乙醇钠、叔丁醇钠、叔戊醇钠、甲醇锂、乙醇锂、叔丁醇锂、叔戊醇锂、甲醇钾、乙醇钾、叔丁醇钾和叔戊醇钾;有机金属化合物,例如甲基锂、乙基锂、正丁基锂、甲基氯化镁和二甲亚砜(dimsyl)钠;金属酰胺,例如酰胺钠、酰胺锂、二异丙基酰胺锂、六甲基二硅叠氮化锂、六甲基二硅叠氮化钠、六甲基二硅叠氮化钾和二环己基酰胺锂;金属氢化物,例如氢化钠、氢化钾和氢化钙;和有机碱性化合物,例如三乙胺、二异丙基乙胺、三丁胺、n,n-二甲基苯胺、n,n-二乙基苯胺、吡啶、4-二甲基氨基吡啶、咪唑、喹啉、吡咯烷、哌啶、可力丁(collidine)、二甲基吡啶、吗啉和1,8-二氮杂双环[5.4.0]-7-十一烯。
[0087]
该碱可以单独使用或组合使用。该碱可以是商购的。
[0088]
相对于每摩尔膦酸酯化合物(3),碱的使用量优选为0.7至5.0摩尔,更优选为0.8至4.0摩尔,并且甚至更优选为0.9至3.0摩尔。
[0089]
前述反应可以在路易斯酸的存在下进行。
[0090]
路易斯酸的实例包括卤化锂,例如氯化锂、溴化锂和碘化锂。
[0091]
路易斯酸可以单独使用或组合使用。路易斯酸可以是商购的。
[0092]
相对于每摩尔膦酸酯化合物(3),路易斯酸的用量优选为0.7至5.0摩尔,更优选为0.8至4.0摩尔,并且甚至更优选为0.9至3.0摩尔。
[0093]
反应中使用的溶剂的实例包括醚,例如乙醚、丁醚、四氢呋喃和1,4-二恶烷;烃,例如己烷、庚烷、苯、甲苯、二甲苯和异丙苯;氯化物溶剂,例如二氯甲烷、氯仿和三氯乙烯;非质子极性溶剂,例如n,n-二甲基甲酰胺、1,3-二甲基-2-咪唑啉酮、二甲基亚砜和六甲基磷酸三酰胺;腈,例如乙腈和丙腈;酯,例如乙酸乙酯和乙酸正丁酯;醇,例如甲醇、乙醇和叔丁醇;和水。
[0094]
溶剂可以单独使用或组合使用。溶剂可以是商购的。
[0095]
相对于每摩尔二甲基环丁酮化合物(2),溶剂的用量优选为(2)10至10000g。
[0096]
上述反应中的反应温度优选为-78至180℃,更优选为-60至160℃,并且甚至更优选为-40至140℃。
[0097]
上述反应中的反应时间可以任意设定。考虑到收率,期望用气相色谱法(gc)或硅胶薄层色谱法(tlc)监测反应以确认反应完成。反应时间通常为约0.5至24小时。
[0098]
[iii]制备具有二甲基环丁烷环的二醇化合物(4)的方法
[0099]
接下来,将在下文中解释根据监测化学反应式制备具有二甲基环丁烷环的二醇化合物(4)的方法。该方法包括使具有二甲基环丁烷环的二酯化合物(1)进行还原反应,以制备具有二甲基环丁烷环的二醇化合物(4)(参见下面的实施例2)。
[0100][0101]
还原剂的实例包括氢;硼烷;脂族烃基硼烷化合物,例如双(3-甲基-2-丁基)硼烷;脂族烃基硅烷化合物,例如三乙基硅烷;金属氢化物,例如氢化铝;脂族烃基金属氢化物,例如二异丁基氢化铝;复合氢化物,例如硼氢化钠、硼氢化锂、硼氢化钾、硼氢化钙、三甲氧基硼氢化钠、三乙基硼氢化锂、氢化铝钠、氢化铝锂、三甲氧基氢化铝锂、二乙氧基氢化铝锂、叔丁氧基乙氧基氢化铝锂、双(2-甲氧基乙氧基)氢化铝钠;和脂族烃氧基或其脂族烃基衍生物。
[0102]
还原剂可以单独使用或组合使用。还原剂可以是商购的。
[0103]
就氢化物而言,相对于每摩尔具有二甲基环丁烷环的二酯化合物(1),还原剂的用量优选为3.5至100.0mol,更优选为3.6至20.0mol,并且甚至更优选为3.7至15.0mol。
[0104]
还原反应中使用的溶剂的实例包括醚,例如乙醚、丁醚、四氢呋喃和1,4-二恶烷;烃,例如己烷、庚烷、苯、甲苯、二甲苯和枯烯;氯化物溶剂,例如二氯甲烷、氯仿和三氯乙烯;非质子极性溶剂,例如n,n-二甲基甲酰胺、1,3-二甲基-2-咪唑啉酮、二甲基亚砜和六甲基磷酸三酰胺;腈,例如乙腈和丙腈;酯,例如乙酸乙酯和乙酸正丁酯;醇,例如甲醇、乙醇和叔丁醇;和水。
[0105]
溶剂可以单独使用或组合使用。溶剂可以是商购的。
[0106]
相对于每摩尔具有二甲基环丁烷环的二酯化合物(1),溶剂的用量优选为10至20000g。
[0107]
反应温度优选为-78至180℃,更优选为-78至160℃,并且甚至更优选为-78至140℃。
[0108]
上述反应中的反应时间可以任意设定。考虑到收率,期望用气相色谱法(gc)或硅胶薄层色谱法(tlc)监测反应以确认反应完成。反应时间通常为约0.5至24小时。
[0109]
具有二甲基环丁烷环的二醇化合物(4)的实例包括下式(4-1)的(s,z)-2-(3-羟甲基-2,2-二甲基环亚丁基)丙-1-醇、下式(4-2)的(r,z)-2-(3-羟甲基-2,2-二甲基环亚丁基)丙-1-醇、下式(4-3)的(s,e)-2-(3-羟甲基-2,2-二甲基环亚丁基)丙-1-醇、下式(4-4)的(r,e)-2-(3-羟甲基-2,2-二甲基环亚丁基)丙-1-醇,以及它们的外消旋体、非对映体混合物和对映体混合物。
[0110][0111]
[iv]制备二甲基环丁烷化合物(5)的方法
[0112]
接下来,以下将说明根据以下化学反应式的制备二甲基环丁烷化合物(5)的方法。该方法包括将具有二甲基环丁烷环的二醇化合物(4)中的hoch
2-(ch
3
)c=部分中的羟基和任选地-ch
2
oh部分中的羟基改变为另一基团。
[0113][0114]
x
1
的实例包括具有包括羰基的碳原子在内的1至10个碳原子的酰氧基、具有包括羰基的碳原子在内的2至10个碳原子的脂族烃氧基羰氧基、具有1至10个碳原子的脂族烃磺酰氧基、具有6至20个碳原子的芳烃磺酰氧基、具有1至12个碳原子的脂族烃氧基、具有6至12个碳原子的芳氧基、具有3至20个碳原子的硅氧基、具有3至30个碳原子的三脂族烃基膦基、具有12至30个碳原子的三芳基膦基和卤素原子。卤素原子的实例包括氯原子、溴原子和碘原子。
[0115]
x
2
的实例包括羟基、具有包括羰基的碳原子在内的1至10个碳原子的酰氧基、具有包括羰基的碳原子在内的2至10个碳原子的脂族烃氧基羰氧基、具有1至10个碳原子的脂族烃磺酰氧基、具有6至20个碳原子的芳烃磺酰氧基、具有1至12个碳原子的脂族烃氧基、具有6至12个碳原子的芳氧基、具有3至20个碳原子的硅氧基和卤素原子。卤素原子的实例包括氯原子、溴原子和碘原子。
[0116]
具有包括羰基的碳原子在内的1至10个碳原子的酰氧基的实例包括直链脂族酰氧基,例如甲酰氧基、乙酰氧基、丙酰氧基、丁酰氧基、戊酰氧基、己酰氧基、庚酰氧基、辛酰氧基、壬酰氧基、癸酰氧基和巴豆酰氧基(crotonyloxy group);支链脂族酰氧基,例如2-甲基丙酰氧基、新戊酰氧基、2-甲基丁酰氧基、3-甲基-2-丁烯酰氧基和3-甲基-3-丁烯酰氧基;卤代酰氧基,例如三氯乙酰氧基和三氟乙酰氧基;和芳族酰氧基,例如苯甲酰氧基;并且还可以包括与上述基团具有异构关系的酰氧基。这些酰氧基的一部分氢原子可以被甲基、乙基或卤素原子取代。卤素原子的实例包括氯原子、溴原子和碘原子。
[0117]
考虑到可用性,具有包括羰基的碳原子之内的1至10个碳原子的酰氧基的特别优选的实例包括甲酰氧基、乙酰氧基、丙酰氧基、新戊酰氧基、2-甲基丁酰氧基和苯甲酰氧基。
[0118]
具有包括羰基的碳原子在内的2至10个碳原子的脂族烃氧基羰氧基的实例包括直链饱和脂族烃氧基羰氧基,例如甲氧基羰氧基、乙氧基羰氧基、正丙氧基羰氧基、正丁氧基羰氧基、正戊氧基羰氧基、正己氧基羰基氧基、正庚氧基羰氧基、正辛氧基羰氧基、正壬氧基羰氧基和正癸氧基羰氧基;支链饱和脂族烃氧基羰氧基,例如异丙氧基羰氧基和叔丁氧基羰氧基;直链不饱和脂族烃氧基羰氧基,例如2-丙烯氧基羰氧基和2-丙炔氧基羰氧基;支链不饱和脂族烃氧基羰氧基,例如2-甲基-2-丙烯氧基羰氧基;环脂族烃氧基羰氧基,例如环丙氧基羰氧基、2-甲基环丙氧基羰氧基、环丁氧基羰氧基和环戊氧基羰氧基;具有芳环的脂族烃氧基羰氧基,例如苄氧基羰氧基和对甲氧基苄氧基羰氧基;氧基脂族烃氧基羰氧基,例
如甲氧基甲氧基羰氧基、苄氧基甲氧基羰氧基、和对甲氧基苄氧基甲氧基羰氧基;和卤代脂族烃氧基羰氧基,例如2,2,2-三氯乙氧基羰氧基;并且还可以包括与上述基团具有异构关系的脂族烃氧基羰氧基。这些脂族烃氧基羰氧基的一部分氢原子可以被甲基、乙基或卤素原子取代。卤素原子的实例包括氯原子、溴原子和碘原子。
[0119]
考虑到可获得性,具有包括羰基的碳原子在内的2至10个碳原子的脂族烃氧基羰氧基的特别优选实例包括甲氧基羰氧基、乙氧基羰氧基和正丙氧基羰氧基。
[0120]
具有1至10个碳原子的脂族烃磺酰氧基的实例包括甲磺酰氧基、乙磺酰氧基、1-丁磺酰氧基、1-戊磺酰氧基、1-己磺酰氧基、1-庚磺酰氧基、1-辛磺酰氧基、1-壬磺酰氧基、1-癸磺酰氧基、烯丙基磺酰氧基、10-樟脑磺酰氧基、三氟甲磺酰氧基和α-苄磺酰氧基;并且还可以包括与上述基团具有异构关系的脂族烃磺酰氧基。这些脂族烃磺酰氧基的一部分氢原子可以被甲基、乙基或卤素原子取代。卤素原子的实例包括氯原子、溴原子和碘原子。
[0121]
考虑到可获得性,具有1至10个碳原子的脂族烃磺酰氧基的特别优选的实例包括甲磺酰氧基和乙磺酰氧基。
[0122]
具有6至20个碳原子的芳烃磺酰氧基的实例包括苯磺酰氧基、4-氯苯磺酰氧基、4-甲氧基苯磺酰氧基、2-硝基苯磺酰氧基、2,4,6-三甲基苯磺酰氧基、对甲苯磺酰氧基、1-萘磺酰氧基和2-萘磺酰氧基;并且还可以包括与上述基团具有异构关系的芳烃磺酰氧基。这些芳烃磺酰氧基的一部分氢原子可以被甲基、乙基或卤素原子取代。卤素原子的实例包括氯原子、溴原子和碘原子。
[0123]
考虑到可获得性,具有6至20个碳原子的芳烃磺酰氧基的特别优选实例包括苯磺酰氧基和对甲苯磺酰氧基。
[0124]
具有1至12个碳原子的脂族烃氧基的实例包括直链饱和脂族烃氧基,例如甲氧基、乙氧基、正丙氧基、正丁氧基、正戊氧基、正己氧基、正庚氧基、正辛氧基、正壬氧基、正癸氧基、正十一烷氧基和正十二烷氧基;支链饱和脂族烃氧基,例如异丙氧基、异丁氧基和叔丁氧基;直链不饱和脂族烃氧基,例如2-丙烯氧基和2-丙炔氧基;支链不饱和脂族烃氧基,例如2-甲基-2-丙烯氧基;环脂族烃氧基,例如环丙氧基、2-甲基环丙氧基、环丁氧基和环戊氧基;具有芳环的脂族烃氧基,例如苄氧基和对甲氧基苄氧基;氧基脂族烃氧基,例如甲氧基甲氧基、2-甲氧基乙氧基甲氧基、苄氧基甲氧基、对甲氧基苄氧基甲氧基、1-乙氧基乙氧基、1-烯丙氧基乙氧基和四氢吡喃-2-氧基;和卤代脂族烃氧基,例如2,2,2-三氯乙氧基和五氟乙氧基;并且还可以包括与上述基团具有异构关系的脂族烃氧基。这些脂族烃氧基的一部分氢原子可以被甲基、乙基或卤素原子取代。卤素原子的实例包括氯原子、溴原子和碘原子。
[0125]
考虑到制备的容易性,具有1至12个碳原子的脂族烃氧基的特别优选的实例包括甲氧基、乙氧基、2-丙烯氧基、甲氧基甲氧基、1-乙氧基乙氧基、1-烯丙氧基乙氧基和四氢吡喃-2-氧基。
[0126]
具有6至12个碳原子的芳氧基的实例包括苯氧基、4-氯苯氧基、4-甲氧基苯氧基、萘氧基和4-联苯氧基;并且还可以包括与上述基团具有异构关系的芳氧基。这些芳氧基的一部分氢原子可以被甲基、乙基或卤素原子取代。卤素原子的实例包括氯原子、溴原子和碘原子。
[0127]
考虑到可获得性,具有6至12个碳原子的芳氧基的特别优选的实例包括苯氧基和
萘氧基。
[0128]
具有3至20个碳原子的硅氧基的实例包括三脂族烃基硅氧基,例如三甲基硅氧基、三乙基硅氧基、三异丙基硅氧基和叔丁基二甲基硅氧基;单脂族烃基二芳基硅氧基,例如叔丁基二苯基硅氧基;并且还可以包括与上述基团具有异构关系的硅氧基。这些具有3至20个碳原子的硅氧基的一部分氢原子可以被甲基、乙基或卤素原子取代。卤素原子的实例包括氯原子、溴原子和碘原子。
[0129]
考虑到可获得性,具有3至20个碳原子的硅氧基的特别优选的实例包括三甲基硅氧基、三乙基硅氧基、三异丙基硅氧基和叔丁基二甲基硅氧基。
[0130]
具有3至30个碳原子的三脂族烃基膦基的实例包括三甲基膦基、三乙基膦基、三丙基膦基、三丁基膦基、三戊基膦基、三己基膦基、三庚基膦基、三辛基膦基、三壬基膦基、和三环己基膦基。
[0131]
考虑到可获得性,具有3至30个碳原子的三脂族烃基膦基的特别优选的实例包括三丁基膦基、三环己基膦基和三辛基膦基。
[0132]
具有12至30个碳原子的三芳基膦基的实例包括三苯基膦基、三(2-甲基苯基)膦基、三糠基膦基和三(1-萘基)膦基。
[0133]
考虑到可获得性,具有12至30个碳原子的三芳基膦基的特别优选的实例包括三苯基膦基和三(2-甲基苯基)膦基。
[0134]
卤素原子的实例包括氯原子、溴原子和碘原子。考虑到可获得性,卤素原子的特别优选实例包括氯原子和溴原子。
[0135]
二甲基环丁烷化合物(5)的实例包括具有两个酰氧基的二甲基环丁烷化合物、具有两个卤素原子的二甲基环丁烷化合物、具有膦基和羟基的二甲基环丁烷化合物以及具有卤素原子和酰氧基的二甲基环丁烷化合物。
[0136]
具有两个酰氧基的二甲基环丁烷化合物的实例包括[3-(2-酰氧基-1-甲基亚乙基)-2,2-二甲基环丁基]甲基酰化物,例如[3-(2-乙酰氧基-1-甲基亚乙基)-2,2-二甲基环丁基]甲基乙酸酯和[3-[2-(2-甲基丁酰氧基)-1-甲基亚乙基]-2,2-二甲基环丁基]甲基2-甲基丁酸酯。
[0137]
具有两个卤素原子的二甲基环丁烷化合物的实例包括1-卤甲基-3-(2-卤-1-甲基亚乙基)-2,2-二甲基环丁烷化合物,例如1-氯甲基-3-(2-氯-1-甲基亚乙基)-2,2-二甲基环丁烷。
[0138]
具有膦基和羟基的二甲基环丁烷化合物的实例包括[2-(3-羟甲基-2,2-二甲基环亚丁基)丙基]三苯基膦(phosphonium)化合物,例如[2-(3-羟甲基-2,2-二甲基环亚丁基)丙基]三苯基膦。
[0139]
具有卤素原子和酰氧基的二甲基环丁烷化合物的实例包括[2,2-二甲基-3-(2-卤-1-甲基亚乙基)环丁基]甲基酰化物,例如[2,2-二甲基-3-(2-溴-1-甲基亚乙基)环丁基]甲基乙酸酯。
[0140]
用于将羟基改变为另一基团的上述反应可以通过已知方法进行。
[0141]
例如,具有两个酰氧基的如下通式(5a)的二甲基环丁烷化合物,可以通过使具有二甲基环丁烷环的二醇化合物(4)与酰化剂进行酰化反应来制备,如下化学反应式所示(参见下面的实施例3和4)。
[0142][0143]
x
4
代表具有包括羰基的碳原子在内的1至10个碳原子的酰氧基。x
4
的实例是由上述针对x
1
和x
2
限定的具有1至10个碳原子的酰氧基。
[0144]
酰化剂的实例包括酸酐,例如乙酸酐、丙酸酐、丁酸酐和2-甲基丁酸酐;以及酰氯,例如乙酰氯、丙酰氯、丁酰氯和2-甲基丁酰氯。
[0145]
酰化剂可以单独使用或组合使用。酰化剂可以是可商购的。
[0146]
相对于每摩尔具有二甲基环丁烷环的二醇化合物(4),酰化剂的用量优选为1.4至100摩尔,更优选为1.6至50摩尔,并且甚至更优选为1.8至20摩尔。
[0147]
酰化反应中使用的碱的实例包括醇盐,例如甲醇钠、乙醇钠、叔丁醇钠、叔戊醇钠、甲醇锂、乙醇锂、叔丁醇锂、叔戊醇锂、甲醇钾、乙醇钾、叔丁醇钾和叔戊醇钾;有机金属化合物,例如甲基锂、乙基锂、正丁基锂、甲基氯化镁和二甲亚砜钠;金属酰胺,例如酰胺钠、酰胺锂、二异丙基酰胺锂、六甲基二硅叠氮化锂、六甲基二硅叠氮化钠、六甲基二硅叠氮化钾和二环己基酰胺锂;金属氢化物,例如氢化钠、氢化钾和氢化钙;和有机碱化合物,例如三乙胺、二异丙基乙胺、三丁胺、n,n-二甲基苯胺、n,n-二乙基苯胺、吡啶、4-二甲基氨基吡啶、咪唑、喹啉、吡咯烷、哌啶、可力丁、二甲基吡啶、吗啉和1,8-二氮杂双环[5.4.0]-7-十一烯。
[0148]
该碱可以单独使用或组合使用。该碱可以是商购的。
[0149]
相对于每摩尔具有二甲基环丁烷环的二醇化合物(4),碱的使用量优选为1.5至110摩尔,更优选为1.7至60摩尔,并且甚至更优选为1.9至30摩尔。
[0150]
酰化反应中使用的溶剂的实例包括醚,例如乙醚、丁醚、四氢呋喃和1,4-二恶烷;烃,例如己烷、庚烷、苯、甲苯、二甲苯和枯烯;氯化物溶剂,例如二氯甲烷、氯仿和三氯乙烯;非质子极性溶剂,例如n,n-二甲基甲酰胺、1,3-二甲基-2-咪唑啉酮、二甲基亚砜和六甲基磷酸三酰胺;腈,例如乙腈和丙腈;酯,例如乙酸乙酯和乙酸正丁酯;醇,例如甲醇、乙醇和叔丁醇;和水。
[0151]
溶剂可以单独使用或组合使用。溶剂可以是商购的。
[0152]
相对于每摩尔具有二甲基环丁烷环的二醇化合物(4),溶剂的使用量优选为10至10,000g。
[0153]
酰化反应中的反应温度优选为-78至180℃,更优选为-60至160℃,而且甚至更优选为-40至140℃。
[0154]
上述反应中的反应时间可以任意设定。考虑到收率,期望用气相色谱法(gc)或硅胶薄层色谱法(tlc)监测反应以确认反应完成。反应时间通常为约0.5至24小时。
[0155]
具有两个卤素原子的如下通式(5b)的二甲基环丁烷化合物可以通过使具有二甲基环丁烷环的二醇化合物(4)与卤素源和膦化合物进行卤化反应来制备,如以下化学反应式所示(参见下面的实施例5)。
[0156][0157]
x
5
代表卤素原子。卤素原子的实例包括氯原子、溴原子和碘原子。x
5
衍生自在卤化反应中使用的卤素源。
[0158]
卤素源的实例包括四卤化碳化合物,例如四氯化碳和四溴化碳;和卤素分子,如溴和碘。
[0159]
卤素源可以单独使用或组合使用。卤素源可以是商购的。
[0160]
相对于每摩尔具有二甲基环丁烷环的二醇化合物(4),卤素源的用量优选为1.4至1,000摩尔,更优选为1.6至500摩尔,并且甚至更优选为1.8至200摩尔。
[0161]
膦化合物的实例包括三芳基膦化合物,例如三苯基膦;三脂族烃基膦化合物,例如三辛基膦。
[0162]
膦化合物可以单独使用或组合使用。该膦化合物可以是可商购的。
[0163]
相对于每摩尔具有二甲基环丁烷环的二醇化合物(4),膦化合物的用量优选为1.4至20.0摩尔,更优选为1.6至16摩尔,并且甚至更优选为1.8至14摩尔。
[0164]
卤化反应可以在碱的存在下进行。
[0165]
碱的实例包括有机碱化合物,例如三乙胺、二异丙基乙胺、三丁胺、n,n-二甲基苯胺、n,n-二乙基苯胺、吡啶、4-二甲基氨基吡啶、咪唑、喹啉、吡咯烷、哌啶、可力丁、二甲基吡啶、吗啉和1,8-二氮杂双环[5.4.0]-7-十一烯。
[0166]
该碱可以单独使用或组合使用。该碱可以是商购的。
[0167]
相对于每摩尔具有二甲基环丁烷环的二醇化合物(4),碱的使用量优选为0至1000摩尔,更优选0至500摩尔,并且甚至更优选0至200摩尔。
[0168]
卤化反应中使用的溶剂的实例包括醚,例如乙醚、丁醚、四氢呋喃、1,4-二恶烷;烃,例如己烷、庚烷、苯、甲苯、二甲苯和枯烯;氯化物溶剂,例如二氯甲烷、氯仿、四氯化碳和三氯乙烯;非质子极性溶剂,例如n,n-二甲基甲酰胺、1,3-二甲基-2-咪唑啉酮、二甲基亚砜和六甲基磷酸三酰胺;腈,例如乙腈和丙腈;和酯,例如乙酸乙酯和乙酸正丁酯。
[0169]
溶剂可以单独使用或组合使用。溶剂可以是商购的。
[0170]
相对于每摩尔具有二甲基环丁烷环的二醇化合物(4),溶剂的使用量优选为0至20,000g。
[0171]
卤化反应中的反应温度优选为-78至180℃,更优选为-60至160℃,而且甚至更优选为-40至140℃。
[0172]
卤化反应中的反应时间可以任意设定。考虑到收率,期望用气相色谱法(gc)或硅胶薄层色谱法(tlc)监测反应以确认反应完成。反应时间通常为约0.5至24小时。
[0173]
具有膦基和羟基的如下通式(5c)的二甲基环丁烷化合物可以通过使具有二甲基环丁烷环的二醇化合物(4)与膦氢卤化物(phosphine hydrohalide)进行膦化(phosphonation)反应来制备,如以下化学反应式所示(参见下面的实施例6)。
[0174][0175]
x
6
代表具有3至30个碳原子的三脂族烃基膦基或具有12至30个碳原子的三芳基膦基。
[0176]
具有3至30个碳原子的三脂族烃基膦基的实例如针对x
1
所述。
[0177]
具有12至30个碳原子的三芳基膦基的实例包括在x
1
是具有12至30个碳原子的三芳基膦基的情况下的上述基团。x
6
衍生自在膦化反应中使用的膦氢卤化物。
[0178]
膦氢卤化物的实例包括三苯基膦氢氯化物、三苯基膦氢溴化物和三苯基膦氢碘化物。
[0179]
膦氢卤化物可以单独使用或组合使用。膦氢卤化物可以是可商购的。
[0180]
相对于每摩尔具有二甲基环丁烷环的二醇化合物(4),膦氢卤化物的用量优选为0.7至10.0摩尔,更优选为0.8至8.0摩尔,并且甚至更优选为0.9至6.0摩尔
[0181]
在膦化反应中使用的溶剂的实例包括醚,例如乙醚、丁醚、四氢呋喃和1,4-二恶烷;烃,例如己烷、庚烷、苯、甲苯、二甲苯和枯烯;氯化物溶剂,例如二氯甲烷、氯仿和三氯乙烯;非质子极性溶剂,例如n,n-二甲基甲酰胺、1,3-二甲基-2-咪唑啉酮、二甲基亚砜和六甲基磷酸三酰胺;腈,例如乙腈和丙腈;酯,例如乙酸乙酯和乙酸正丁酯;醇,例如甲醇、乙醇和叔丁醇;和水。
[0182]
溶剂可以单独使用或组合使用。溶剂可以是商购的。
[0183]
相对于每摩尔具有二甲基环丁烷环的二醇化合物(4),溶剂的使用量优选为10至10,000g。
[0184]
膦化反应中的反应温度优选为-78至180℃,更优选为-60至160℃,并且甚至更优选为-40至140℃。
[0185]
膦化反应中的反应时间可以任意设定。考虑到收率,期望用气相色谱法(gc)或硅胶薄层色谱法(tlc)监测反应以确认反应完成。反应时间通常为约0.5至24小时。
[0186]
具有二甲基环丁烷环的二醇化合物(4)中的羟基可以分多个步骤改变。
[0187]
例如,具有卤素原子和酰氧基的如下通式(5d)的二甲基环丁烷化合物可以通过将上述具有两个酰氧基的二甲基环丁烷化合物(5a)与卤化氢化合物卤化来制备,如以下化学反应式所示(参见下面的实施例7)。
[0188][0189]
具有卤原子和酰氧基的二甲基环丁烷化合物(5d)中的x
4
和x
5
如上限定。
[0190]
卤化氢化合物的实例包括氯化氢、溴化氢和碘化氢。
[0191]
卤化氢化合物可以单独使用或组合使用。卤化氢可以是商购的。
[0192]
相对于每摩尔具有两个酰氧基的二甲基环丁烷化合物(5a),卤化氢化合物的用量优选为0.7至10摩尔,更优选为0.8至8摩尔,并且甚至更优选为0.9至6摩尔。
[0193]
卤化反应中使用的溶剂的实例包括醚,例如乙醚、丁醚、四氢呋喃和1,4-二恶烷;烃,例如己烷、庚烷、苯、甲苯、二甲苯和枯烯;氯化物溶剂,例如二氯甲烷、氯仿、四氯甲烷和三氯乙烯;非质子极性溶剂,例如n,n-二甲基甲酰胺、1,3-二甲基-2-咪唑啉酮、二甲基亚砜和六甲基磷酸三酰胺;腈,例如乙腈和丙腈;酯,例如乙酸乙酯和乙酸正丁酯;羧酸,例如甲酸、乙酸和丙酸;和水。
[0194]
溶剂可以单独使用或组合使用。溶剂可以是商购的。
[0195]
相对于每摩尔具有两个酰氧基的二甲基环丁烷化合物(5a),溶剂的使用量优选为10至10,000g。
[0196]
卤化反应中的反应温度优选为-78至180℃,更优选为-60至160℃,并且甚至更优选为-40至140℃。
[0197]
卤化反应中的反应时间可以任意设定。考虑到收率,期望用气相色谱法(gc)或硅胶薄层色谱法(tlc)监测反应以确认反应完成。反应时间通常为约0.5至24小时。
[0198]
二甲基环丁烷化合物(5)的实例包括如下通式(5-1)的(s,z)形式的二甲基环丁烷化合物、如下通式(5-2)的(r,z)形式的二甲基环丁烷化合物、如下通式(5-3)的(s,e)形式的二甲基环丁烷化合物、和如下通式(5-4)的(r,e)形式的二甲基环丁烷化合物,及其外消旋体、非对映体混合物和对映体混合物。
[0199][0200]
[v]异丙烯基二甲基环丁烷化合物(6)和异亚丙基二甲基环丁烷化合物(7)的制备方法。
[0201]
接着,以下将说明如下通式(6)的异丙烯基二甲基环丁烷化合物和如下通式(7)的异亚丙基二甲基环丁烷化合物的制备方法。该方法包括使二甲基环丁烷化合物(5)进行还原反应以制备异丙烯基二甲基环丁烷化合物(6)和/或异亚丙基二甲基环丁烷化合物(7)。必要时,还原反应在金属催化剂和配体的存在下使用还原剂进行。
[0202][0203]
x
3
代表羟基、具有包括羰基的碳原子在内的1至10个碳原子的酰氧基、具有包括羰基的碳原子在内的2至10个碳原子的脂族烃氧基羰氧基、具有1至10个碳原子的脂族烃磺酰氧基、具有6至20个碳原子的芳烃磺酰氧基、具有1至12个碳原子的脂族烃氧基、具有6至12个碳原子的芳氧基、具有3至20个碳原子的硅氧基或卤素原子。x
3
中的每个可以与x
1
和x
2
相同。在上述还原反应中,在维持(maintain)二甲基环丁烷化合物(5)中的x
2
的情况下,x
2
与x
3
在反应后相同。而在不维持x
2
的情况下,x
2
与x
3
在反应后不同。
[0204]
还原剂的实例包括氢;甲酸和甲酸盐/酯,例如甲酸钠、甲酸铵和三乙基甲酸铵;硼烷,脂族烃基硼烷化合物,例如双(3-甲基-2-丁基)硼烷;脂族烃基硅烷化合物,例如三乙基硅烷;金属氢化物,例如氢化铝;脂族烃基金属氢化物,例如二异丁基氢化铝;复合氢化物,例如硼氢化钠、硼氢化锂、硼氢化钾、硼氢化钙、三甲氧基硼氢化钠、三乙基硼氢化锂、氢化铝钠、氢化铝锂、三甲氧基氢化铝锂、二乙氧基氢化铝锂、三叔丁氧基氢化铝锂、双(2-甲氧
基乙氧基)氢化铝钠;及其脂族烃氧基或脂族烃基衍生物。
[0205]
还原剂可以单独使用或组合使用。还原剂可以是可商购的。
[0206]
就氢化物而言,相对于每摩尔二甲基环丁烷化合物(5),还原剂的用量优选为0.7至100.0摩尔,更优选为0.8至80.0摩尔,并且甚至更优选为0.9至60.0摩尔。
[0207]
还原反应可以在金属催化剂的存在下进行。
[0208]
金属催化剂的实例包括钯催化剂、镍催化剂、铁催化剂、钴催化剂、钼催化剂、钨催化剂、铑催化剂、铱催化剂,考虑到收率和选择性,钯催化剂是优选的。
[0209]
钯催化剂的实例包括零价钯催化剂,例如四(三苯基膦)钯和双(二苯亚甲基丙酮)钯催化剂;以及二价钯催化剂,例如乙酸钯、双(三苯基膦)双乙酸钯、三氟乙酸钯、氯化钯、双(三苯基膦)二氯化钯、烯丙基氯化钯和双(2,4-戊二酮合)钯。
[0210]
金属催化剂可以单独使用或组合使用。金属催化剂可以是商购的。
[0211]
相对于每摩尔二甲基环丁烷化合物(5),金属催化剂的用量优选为0.0001至1摩尔,更优选为0.0002至0.9摩尔,并且甚至更优选为0.0003至0.8摩尔。
[0212]
如果需要,可以将配体与金属催化剂一起使用。
[0213]
配体的实例包括亚磷酸酯化合物,例如亚磷酸三乙酯和亚磷酸三苯酯;膦化合物,例如三丁基膦、三环己基膦、三辛基膦、三苯基膦、2,2'-双(二苯基膦基)-1,1'-联萘(binap)和2-(二叔丁基膦基)联苯(即2-(联苯基)-二叔丁基膦);丙酮衍生物,例如乙酰丙酮和二苯亚甲基丙酮;腈化合物,例如乙腈和苄腈;含氮化合物,例如二甲基咪唑啉酮、乙二胺和六甲基磷酸三酰胺;和二烯化合物,例如1,5-环辛二烯和2,5-降冰片二烯。
[0214]
配体可以单独使用或组合使用。配体可以是商购的。
[0215]
相对于每摩尔金属催化剂,配体的使用量优选为0.001至10,000摩尔,更优选为0.01至1,000摩尔,并且甚至更优选为0.1至100摩尔。
[0216]
还原反应中使用的溶剂的实例包括醚,例如乙醚、丁醚、四氢呋喃和1,4-二恶烷;烃,例如己烷、庚烷、苯、甲苯、二甲苯和枯烯;氯化物溶剂,例如二氯甲烷、氯仿和三氯乙烯;非质子极性溶剂,例如n,n-二甲基甲酰胺、1,3-二甲基-2-咪唑啉酮、二甲基亚砜和六甲基磷酸三酰胺;腈,例如乙腈和丙腈;酯,例如乙酸乙酯和乙酸正丁酯;醇,例如甲醇、乙醇和叔丁醇;酮,例如丙酮和2-丁酮;和水。
[0217]
溶剂可以单独使用或组合使用。溶剂可以是商购的。
[0218]
相对于每摩尔二甲基环丁烷化合物(5),溶剂的用量优选为10至150,000g。
[0219]
还原反应中的反应温度优选为-78至180℃,更优选为-60至160℃,并且甚至更优选为-40至140℃。
[0220]
还原反应中的反应时间可以任意设定。考虑到收率,期望用气相色谱法(gc)或硅胶薄层色谱法(tlc)监测反应以确认反应完成。反应时间通常为约0.5至30小时。
[0221]
异丙烯基二甲基环丁烷化合物(6)的实例包括如下通式(6-1)的(1r,3r)-3-异丙烯基-2,2-二甲基环丁烷化合物、如下通式(6-2)的(1s,3s)-3-异丙烯基-2,2-二甲基环丁烷化合物、如下通式(6-3)的(1r,3s)-3-异丙烯基-2,2-二甲基环丁烷化合物和如下通式(6-4)的(1s,3r)-3-异丙烯基-2,2-二甲基环丁烷化合物及其外消旋体、非对映体混合物和对映体混合物。
[0222][0223]
异丙烯基二甲基环丁烷化合物(6)的实例包括具有酰氧基甲基的异丙烯基二甲基环丁烷化合物、具有卤甲基的异丙烯基二甲基环丁烷化合物、具有羟甲基的异丙烯基二甲基环丁烷化合物和具有脂族烃磺酰氧基甲基的异丙烯基二甲基环丁烷化合物。
[0224]
具有酰氧基甲基的异丙烯基二甲基环丁烷化合物的实例包括(3-异丙烯基-2,2-二甲基环丁基)甲基丙烯酸酯化合物,例如(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸酯、(3-异丙烯基-2,2-二甲基环丁基)甲基2-甲基丁酸酯和(3-异丙烯基-2,2-二甲基环丁基)甲基3-甲基-3-丁烯酸酯。
[0225]
具有卤甲基的异丙烯基二甲基环丁烷化合物的实例包括1-卤甲基-3-异丙烯基-2,2-二甲基环丁烷化合物,例如1-氯甲基-3-异丙烯基-2,2-二甲基环丁烷。
[0226]
具有羟甲基的异丙烯基二甲基环丁烷化合物的实例包括(3-异丙烯基-2,2-二甲基环丁基)甲醇。
[0227]
具有脂族烃磺酰氧基甲基的异丙烯基二甲基环丁烷化合物的实例包括(3-异丙烯基-2,2-二甲基环丁基)甲基脂族烃磺酸酯化合物,例如(3-异丙烯基-2,2-二甲基环丁基)甲基甲磺酸酯。
[0228]
异亚丙基二甲基环丁烷化合物(7)的实例包括如下通式(7-1)的(1r)-3-异亚丙基-2,2-二甲基环丁烷化合物、如下通式(7-2)的(1s)-3-异亚丙基-2,2-二甲基环丁烷化合物及其外消旋体和对映体的混合物。
[0229][0230]
异亚丙基二甲基环丁烷化合物(7)的实例包括具有酰氧基甲基的异亚丙基二甲基环丁烷化合物、具有卤甲基的异亚丙基二甲基环丁烷化合物、具有羟甲基的异亚丙基二甲基环丁烷化合物和具有脂族烃磺酰氧基甲基的异亚丙基二甲基环丁烷化合物。
[0231]
具有酰氧基甲基的异亚丙基二甲基环丁烷化合物的实例包括(3-异亚丙基-2,2-二甲基环丁基)甲基丙烯酸酯化合物,例如(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯、(3-异亚丙基-2,2-二甲基环丁基)甲基2-甲基丁酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基3-甲基-2-丁烯酸酯。
[0232]
具有卤甲基的异亚丙基二甲基环丁烷化合物的实例包括1-卤甲基-3-异亚丙基-2,2-二甲基环丁烷化合物,例如1-氯甲基-3-异亚丙基-2,2-二甲基环丁烷。
[0233]
具有羟甲基的异亚丙基二甲基环丁烷化合物的实例包括(3-异亚丙基-2,2-二甲基环丁基)甲醇。
[0234]
具有脂族烃磺酰氧基甲基的异亚丙基二甲基环丁烷化合物的实例包括(3-异亚丙基-2,2-二甲基环丁基)甲基脂族烃磺酸酯化合物,例如(3-异亚丙基-2,2-二甲基环丁基)
甲基甲磺酸酯。
[0235]
如下通式(6a)的具有酰氧基甲基的异丙烯基二甲基环丁烷化合物和如下通式(7a)的异亚丙基二甲基环丁烷化合物可以通过使具有两个酰氧基的二甲基环丁烷化合物(5a)进行还原反应来制备,如以下化学反应式所示(参见下面的实施例8、9、10、11和12)。如果需要,可以在金属催化剂和配体的存在下使用还原剂进行还原反应。
[0236][0237]
具有酰氧基甲基的异丙烯基二甲基环丁烷化合物(6a)中的x
4
和异亚丙基二甲基环丁烷化合物(7a)中的x
4
如上所限定。
[0238]
具有卤代甲基的如下通式(6b)的异丙烯基二甲基环丁烷化合物和如下通式(7b)的异亚丙基二甲基环丁烷化合物可以通过将具有两个卤素原子的二甲基环丁烷化合物(5b)进行还原反应来制备,如以下化学反应式所示(参见下面的实施例13)。如果需要,可以在金属催化剂和配体的存在下使用还原剂进行还原反应。
[0239][0240]
具有卤甲基的异丙烯基二甲基环丁烷化合物(6b)和异亚丙基二甲基环丁烷化合物(7b)中的x
5
如上所限定。
[0241]
例如,具有羟基甲基的下式(6c)的异丙烯基二甲基环丁烷化合物和下式(7c)的异亚丙基二甲基环丁烷化合物可以通过使具有膦基和羟基的二甲基环丁烷化合物(5c)进行还原反应来制备,如以下化学反应式所示(参见下面的实施例14)。如果需要,可以在金属催化剂和配体的存在下使用还原剂进行还原反应。
[0242][0243]
如图7所示,具有羟甲基的异丙烯基二甲基环丁烷化合物(6c)和异亚丙基二甲基环丁烷化合物(7c)可以通过使具有卤素原子和酰氧基的二甲基环丁烷化合物(5d)进行还原反应来制备,如以下化学反应式所示(参见下面的实施例15)。如果需要,可以在金属催化剂和配体的存在下使用还原剂进行还原反应。
[0244][0245]
如果需要,具有特定基团x
3
的异丙烯基二甲基环丁烷化合物(6')和/或具有特定基团x
3
的异亚丙基二甲基环丁烷化合物(7')可以通过改变异丙烯基二甲基环丁烷化合物(6)和/或异亚丙基二甲基环丁烷化合物(7)中的x
3
为某些基团x
3
来获得,其中x
3
的选项如上所限定(参见下面的实施例21)。可以通过已知方法进行基团的改变。
[0246]
具有酰氧基甲基的异丙烯基二甲基环丁烷化合物(6a)和异亚丙基二甲基环丁烷
化合物(7a)可以通过使具有卤代甲基的异丙烯基二甲基环丁烷化合物(6b)和/或异亚丙基二甲基环丁烷化合物(7b)与羧酸盐进行酰氧基化反应来制备,如以下化学反应式所示(参见下面的实施例16)。
[0247][0248]
化学反应式显示从化合物(6b)和(7b)的混合物制备化合物(6a)和(7a)的混合物,从化合物(6b)制备化合物(6a),以及从化合物(7b)制备化合物(7a)。
[0249]
羧酸盐的实例包括金属羧酸盐,例如乙酸锂、乙酸钠、乙酸钾、乙酸铯、乙酸镁和乙酸钙;和羧酸铵,例如乙酸铵和乙酸四丁铵。
[0250]
羧酸盐可以单独使用或组合使用。羧酸盐可以是商购的。
[0251]
羧酸盐可以在反应体系中通过使羧酸与碱例如氢氧化钠、碳酸钾和氢氧化四丁铵反应来制备。
[0252]
相对于每摩尔具有卤代甲基的异丙烯基二甲基环丁烷化合物(6b)和异亚丙基二甲基环丁烷化合物(7b)总体(a total),羧酸盐的用量优选为0.7至10摩尔,更优选为0.8至8摩尔,并且甚至更优选为0.9至6摩尔。
[0253]
酰氧基化反应可以在卤化物的存在下进行。
[0254]
卤化物的实例包括金属卤化物,例如碘化锂、碘化钠、碘化钾、碘化铯、碘化镁、碘化钙、溴化锂、溴化钠、溴化钾、溴化铯、溴化镁和溴化钙;卤化铵化合物,例如碘化铵、溴化铵、碘化四丁铵、溴化四丁铵和氯化四丁铵。
[0255]
卤化物可以单独使用或组合使用。卤化物可以是商购的。
[0256]
相对于每摩尔具有卤代甲基的异丙烯基二甲基环丁烷化合物(6b)和异亚丙基二甲基环丁烷化合物(7b)总体,卤化物的用量优选为0.0001至10摩尔,更优选为0.0002至8摩尔,并且甚至更优选为0.0003至6摩尔。
[0257]
酰氧基化反应中使用的溶剂的实例包括醚,例如乙醚、丁醚、四氢呋喃和1,4-二恶烷;烃,例如己烷、庚烷、苯、甲苯、二甲苯和枯烯;氯化物溶剂,例如二氯甲烷、氯仿和三氯乙烯;非质子极性溶剂,例如n,n-二甲基乙酰胺、n,n-二甲基甲酰胺、1,3-二甲基-2-咪唑啉酮、二甲基亚砜和六甲基磷酸三酰胺;腈,例如乙腈和丙腈;酯,例如乙酸乙酯和乙酸正丁酯;醇,例如甲醇、乙醇和叔丁醇;酮,例如丙酮和2-丁酮;和水。
[0258]
溶剂可以单独使用或组合使用。溶剂可以是商购的。
[0259]
相对于每摩尔具有卤代甲基的异丙烯基二甲基环丁烷化合物(6b)和异亚丙基二甲基环丁烷化合物(7b)总体,溶剂的用量优选为10至10,000g。
[0260]
酰氧基化反应中的反应温度优选为-78至200℃,更优选为-60至180℃,并且甚至更优选为-40至160℃。
[0261]
酰氧基化反应中的反应时间可以任意设定。考虑到收率,期望用气相色谱法(gc)或硅胶薄层色谱法(tlc)监测反应以确认反应完成。反应时间通常为约0.5至24小时。
[0262]
具有酰氧基甲基的如下通式(6a)的异丙烯基二甲基环丁烷化合物和异亚丙基二甲基环丁烷化合物(7a)可以通过使具有羟甲基的异丙烯基二甲基环丁烷化合物(6c)和/或异亚丙基二甲基环丁烷化合物(7c)与酰化剂进行酰化反应来制备,如以下化学反应式所示(参见以下实施例17、18和22)。
[0263][0264]
化学反应式显示从化合物(6c)和(7c)的混合物制备化合物(6a)和(7a)的混合物,从化合物(6c)制备化合物(6a),以及从化合物(7a)制备化合物(7c)。
[0265]
酰化剂的实例包括酸酐,例如乙酸酐;以及酰氯,例如乙酰氯。
[0266]
酰化剂可以单独使用或组合使用。酰化剂可以是可商购的。
[0267]
相对于每摩尔具有羟甲基的异丙烯基二甲基环丁烷化合物(6c)和异亚丙基二甲基环丁烷化合物(7c)总体,酰化剂的用量优选为0.7至100摩尔,更优选为0.8至50摩尔,并且甚至更优选为0.9至20摩尔。
[0268]
酰化反应中使用的碱的实例包括醇盐,例如甲醇钠、乙醇钠、叔丁醇钠、叔戊醇钠、甲醇锂、乙醇锂、叔丁醇锂、叔戊醇锂、甲醇钾、乙醇钾、叔丁醇钾和叔戊醇钾;有机金属化合物,例如甲基锂、乙基锂、正丁基锂、甲基氯化镁和二甲亚砜钠;金属酰胺,例如酰胺钠、酰胺锂、二异丙基酰胺锂、六甲基二硅叠氮化锂、六甲基二硅叠氮化钠、六甲基二硅叠氮化钾和二环己基酰胺锂;金属氢化物,例如氢化钠、氢化钾和氢化钙;有机碱化合物,例如三乙胺、二异丙基乙胺、三丁胺、n,n-二甲基苯胺、n,n-二乙基苯胺、吡啶、4-二甲基氨基吡啶、咪唑、喹啉、吡咯烷、哌啶、可力丁、二甲基吡啶、吗啉和1,8-二氮杂双环[5.4.0]-7-十一烯。
[0269]
该碱可以单独使用或组合使用。该碱可以是商购的。
[0270]
相对于每摩尔具有羟甲基的异丙烯基二甲基环丁烷化合物(6c)和异亚丙基二甲基环丁烷化合物(7c)总体,碱的使用量优选为0.7至100摩尔,更优选为0.8至50摩尔,并且甚至更优选为0.9至20摩尔。
[0271]
酰化反应中使用的溶剂的实例包括醚,例如乙醚、丁醚、四氢呋喃和1,4-二恶烷;烃,例如己烷、庚烷、苯、甲苯、二甲苯和枯烯;氯化物溶剂,例如二氯甲烷、氯仿和三氯乙烯;非质子极性溶剂,例如n,n-二甲基甲酰胺、1,3-二甲基-2-咪唑啉酮、二甲基亚砜和六甲基磷酸三酰胺;腈,例如乙腈和丙腈;酯,例如乙酸乙酯和乙酸正丁酯;和水。
[0272]
溶剂可以单独使用或组合使用。溶剂可以是商购的。
[0273]
相对于每摩尔具有羟甲基的异丙烯基二甲基环丁烷化合物(6c)和异亚丙基二甲基环丁烷化合物(7c)总体,溶剂的使用量优选为10至15,000g。
二恶烷;和烃,例如己烷、庚烷、苯、甲苯、二甲苯和枯烯;氯化物溶剂,例如二氯甲烷、氯仿和三氯乙烯;非质子极性溶剂,例如n,n-二甲基甲酰胺、1,3-二甲基-2-咪唑啉酮、二甲基亚砜和六甲基磷酸三酰胺;腈,例如乙腈和丙腈;酯,例如乙酸乙酯和乙酸正丁酯;和水。
[0287]
溶剂可以单独使用或组合使用。溶剂可以是商购的。
[0288]
相对于每摩尔具有羟甲基的异丙烯基二甲基环丁烷化合物(6c)和异亚丙基二甲基环丁烷化合物(7c)总体,溶剂的使用量优选为10至10,000g。
[0289]
脂族烃磺酰化反应中的反应温度优选为-78至180℃,更优选为-60至160℃,并且甚至更优选为-40至140℃。
[0290]
脂族烃磺酰基化反应中的反应时间可以任意设定。考虑到收率,期望用气相色谱法(gc)或硅胶薄层色谱法(tlc)监测反应以确认反应完成。反应时间通常为约0.5至24小时。
[0291]
具有酰氧基甲基的异丙烯基二甲基环丁烷化合物(6a)和异亚丙基二甲基环丁烷化合物(7a)可以通过使具有脂族烃磺酰氧基甲基的异丙烯基二甲基环丁烷化合物(6d)和/或异亚丙基二甲基环丁烷化合物(7d)与羧酸盐进行酰氧基化反应来制备,如以下化学反应式所示(参见以下实施例20)。
[0292][0293]
化学反应式显示从化合物(6d)和(7d)的混合物制备化合物(6a)和(7a)的混合物,从化合物(6d)制备化合物(6a),以及从化合物(7d)制备化合物(7a)。
[0294]
羧酸盐的实例包括3-甲基-2-丁烯酸的碱金属盐,例如3-甲基-2-丁烯酸锂、3-甲基-2-丁烯酸钠、3-甲基-2-丁烯酸钾和3-甲基-2-丁烯酸铯;3-甲基-2-丁烯酸的碱土金属盐,例如3-甲基-2-丁烯酸镁和3-甲基-2-丁烯酸钙;和羧酸铵,例如3-甲基-2-丁烯酸铵和3-甲基-2-丁烯酸四丁铵。
[0295]
羧酸盐可以单独使用或组合使用。羧酸盐可以是商购的。
[0296]
羧酸盐可以在反应体系中通过使羧酸与碱例如氢氧化钠、碳酸钾和氢氧化四丁铵反应来制备。
[0297]
相对于每摩尔具有脂族烃磺酰氧基甲基的异丙烯基二甲基环丁烷化合物(6d)和异亚丙基二甲基环丁烷化合物(7d)总体,羧酸盐的用量为0.7至10摩尔,更优选0.8至8摩尔,并且甚至更优选0.9至6摩尔。
[0298]
酰氧基化反应可以在卤化物的存在下进行。
[0299]
卤化物的实例包括金属卤化物,例如碘化锂、碘化钠、碘化钾、碘化铯、碘化镁、碘化钙、溴化锂、溴化钠、溴化钾、溴化铯、溴化镁和溴化钙;卤化铵化合物,例如碘化铵、溴化铵、碘化四丁铵、溴化四丁铵和氯化四丁铵。
4.21(4h,m)ppm.
[0317]
13
c-nmr(150mhz,cdcl
3
):δ=13.16,14.31,14.42,21.11,26.88,30.86,45.64,48.25,60.02,60.27,120.12,160.91,168 0.09,172.82ppm.
[0318]
以下是由此制备的(z)-3-(1-乙氧基羰基亚乙基)-2,2-二甲基环丁烷羧酸乙酯(无色或浅黄色油状液体)的光谱数据。
[0319]
ir(d-atr):νmax=2981,2961,2930,2870,1732,1715,1671,1449,1371,1342,1301,1280,1247,1185,1156,1114,1095,1077,1049,860,772cm-1
.
[0320]
1
h-nmr(500mhz cdcl
3
):δ=1.23(3h,s),1.26(3h,t,j=7.3hz),1.28(3h,t,j=7.3hz),1.42(3h,s),1.69(3h,t,j=1.5hz),2.64-2.71(1h,m),2.81(1h,dd,j=7.6,8.8hz),3.01-3.08(1h,m),4.09-4.22(4h,m)ppm.
[0321]
13
c-nmr(150mhz,cdcl
3
):δ=14.19,14.31,14.41,20.73,26.59,27.84,44.85,49.80,59.99,60.29,120.38,159.90,166.68,172.93ppm.
[0322]
实施例2
[0323]
2-(3-羟甲基-2,2-二甲基环亚丁基)丙-1-醇的制备
[0324][0325]
将1.01m二异丁基氢化铝(dibal)的甲苯溶液(1l,1.01mol)置于氮气气氛中的反应器中,并在-60℃搅拌。将如实施例1中获得的3-(1-乙氧基羰基亚乙基)-2,2-二甲基环丁烷羧酸乙酯(36.6g,0.144mol)的e:z=57:43的几何异构体混合物在四氢呋喃(thf)(80g)中的溶液,在-50℃以下的反应器内部温度滴加到该溶液中。滴加完成后,将混合物的温度逐渐升高至10℃,然后将混合物搅拌5小时。随后,将罗谢尔盐的饱和水溶液加入该混合物中,分离有机层,并通过常规洗涤、干燥和浓缩进行后处理,以获得目标粗化合物2-(3-羟甲基-2,2-二甲基环亚丁基)丙-1-醇,为e:z=57:43的几何异构体混合物(24.5g,0.144mol),粗收率为100%。
[0326]
以下是由此制备的(e)-2-(3-羟甲基-2,2-二甲基环亚丁基)丙-1-醇(无色或浅黄色油状液体)的光谱数据。
[0327]
ir(d-atr):νmax=3322,2955,2922,2864,1703,1459,1382,1361,1311,1276,1224,1167,1101,1053,1031,1005,942,886cm-1
.
[0328]
1
h-nmr(500mhz cdcl
3
):δ=1.18(3h,s),1.28(3h,s),1.66(3h,t,j=1.9hz),1.76(2h,brs),2.06-2.13(1h,m),2.19-2.26(1h,m),2.66-2.72(1h,m),3.61(1h,dd,j=7.2,10.7hz),3.75(1h,dd,j=7.6,10.7hz),3.89(2h,brs)ppm.
[0329]
13
c-nmr(150mhz,cdcl
3
):δ=14.19,20.51,27.54,28.24,42.71,44.40,63.78,63.88,125.64,142.47ppm.
[0330]
以下是由此制备的(z)-2-(3-羟甲基-2,2-二甲基环亚丁基)丙-1-醇(无色或浅黄色油状液体)的光谱数据。
[0331]
ir(d-atr):νmax=3329,2954,2925,2865,1702,1445,1374,1362,1312,1272,1249,1166,1121,1066,1026,1003,888cm-1
.
[0332]
1
h-nmr(500mhz cdcl
3
):δ=1.18(3h,s),1.28(3h,s),1.56(3h,t,j=1.3hz),1.57
(2h,brs),2.07-2.23(2h,m),2.59-2.65(1h,m),3.62(1h,dd,j=6.8,10.7hz),3.76(1h,dd,j=7.6,10.7hz),3.98-4.05(2h,m)ppm.
[0333]
13
c-nmr(150mhz,cdcl
3
):δ=15.07,21.90,27.63,29.56,42.49,44.58,62.51,63.97,126.32,143.79ppm.
[0334]
实施例3
[0335]
[3-(2-乙酰氧基-1-甲基亚乙基)-2,2-二甲基环丁基]甲基乙酸酯的制备
[0336][0337]
将实施例2中得到的2-(3-羟甲基-2,2-二甲基环亚丁基)丙-1-醇(24.5g,0.144mol)的e:z=57:43的几何异构体混合物、甲苯(202g)、和吡啶(114g,1.44mol)置于氮气气氛中的反应器中并在10℃搅拌。在20℃以下的反应器内部温度,将乙酸酐(73.6g,0.721mol)滴加到溶液中。滴加完成后,将混合物在15℃搅拌6小时。随后,将水加入混合物中,分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液进行减压蒸馏,得到目标化合物[3-(2-乙酰氧基-1-甲基亚乙基)-2,2-二甲基环丁基]甲基乙酸酯,为e:z=57:43的几何异构体混合物(30.0g,0.118mol),收率为82%。
[0338]
以下是由此制备的[(e)-3-(2-乙酰氧基-1-甲基亚乙基)-2,2-二甲基环丁基]甲基乙酸酯(无色或浅黄色油状液体)的光谱数据。
[0339]
ir(d-atr):νmax=2958,1740,1459,1380,1365,1235,1171,1023,974,893,830,605cm-1
.
[0340]
1
h-nmr(500mhz cdcl
3
):δ=1.16(3h,s),1.27(3h,s),1.61(3h,t,j=1.9hz),2.02(3h,s),2.04(3h,s)),2.20-2.29(2h,m),2.68-2.75(1h,m),4.06-4.14(2h,m),4.32(1h,d,j=11.8hz),4.35(1h,d,j=11.8hz)ppm.
[0341]
13
c-nmr(150mhz,cdcl
3
):δ=14.51,20.54,20.92,20.95,27.72,27.85,39.05,44.62,65.25,65.31,121.57,144.58,171.06,171.11ppm.
[0342]
以下是由此制备的[(z)-3-(2-乙酰氧基-1-甲基亚乙基)-2,2-二甲基环丁基]甲基乙酸酯(无色或浅黄色油状液体)的光谱数据。
[0343]
ir(d-atr):νmax=2957,1741,1462,1366,1236,1024,975,891,631,606cm-1
.
[0344]
1
h-nmr(500mhz cdcl
3
):δ=1.15(3h,s),1.26(3h,s),1.51-1.52(3h,m),2.02(3h,s),2.04(3h,s),2.17-2.27(2h,m),2.61-2.69(1h,m),4.09(1h,d,j=5.4hz),4.12(1h,d,j=5.4hz),4.47(2h,brs)ppm.
[0345]
13
c-nmr(150mhz,cdcl
3
):δ=15.46,20.91,29.94,21.65,27.80,28.82,38.88,44.79,64.06,65.23,121.91,145.70,171 0.05,171.14ppm.
[0346]
实施例4
[0347]
[3-[2-(2-甲基丁酰氧基)-1-甲基亚乙基]-2,2-二甲基环丁基]甲基2-甲基丁酸酯的制备
[0348][0349]
将如实施例2中所获得的2-(3-羟甲基-2,2-二甲基环亚丁基)丙-1-醇(1.72g,10.1mmol)的e:z=57:43的几何异构体混合物、四氢呋喃(thf)(36g)和吡啶(16g,0.202mol)置于氮气气氛的反应器中,并在0℃搅拌1小时。在20℃以下的反应器内部温度,将2-甲基丁酰氯(4.85g,40.2mmol)滴加到溶液中。滴加完成后,将混合物在20℃搅拌3小时。随后,将水加入混合物中,分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液通过硅胶柱色谱法(己烷:乙酸乙酯=30:1)纯化,得到目标化合物[3-[2-(2-甲基丁酰氧基)-1-甲基亚乙基]-2,2-二甲基环丁基]甲基2-甲基丁酸酯,为e:z=57:43的几何异构体混合物(1.88g,5.56mmol),收率为55%。
[0350]
以下是由此制备的(3-[2-(2-甲基丁酰氧基)-1-甲基亚乙基]-2,2-二甲基环丁基)甲基2-甲基丁酸酯(无色或浅黄色油状液体)的光谱数据。
[0351]
1
h-nmr(500mhz cdcl
3
):δ=0.87-0.91(6h,m),1.12(3h,d,j=4.2hz),1.13(3h,d,j=4.6hz),1.14,1.16(3h,s,s),1.26,1.27(3h,s,s),1.40-1.52,1.61-1.72(7h,m),2.19-2.41(4h,m),2.62-2.76(1h,m),4.08-4.27(2h,m),4.32-4.40,4.44-4.50(2h,m)ppm.
[0352]
实施例5
[0353]
1-氯甲基-3-(2-氯-1-甲基亚乙基)-2,2-二甲基环丁烷的制备
[0354][0355]
将如实施例2中获得的2-(3-羟甲基-2,2-二甲基环亚丁基)丙-1-醇的e:z=57:43的几何异构体混合物(1.64g,9.61mmol)和四氯化碳(48g,0.31mol)置于氮气气氛的反应器中,并在0℃搅拌。随后,加入三苯膦(7.56g,28.8mmol),将混合物搅拌24小时,同时逐渐加热至20℃的温度。随后,在环境温度下向反应混合物中加入甲醇(5g),并搅拌1小时。浓缩反应混合物,然后加入己烷并通过过滤除去沉淀物。浓缩滤液,并将浓缩物通过硅胶柱色谱法(己烷)纯化,得到目标化合物1-氯甲基-3-(2-氯-1-甲基亚乙基)-2,2-二甲基环丁烷,为e:z=57:43的几何异构体的混合物(1.06g,5.13mmol),收率为53%。
[0356]
以下是由此制备的1-氯甲基-3-(2-氯-1-甲基亚乙基)-2,2-二甲基环丁烷(无色或浅黄色油状液体)的光谱数据。
[0357]
1
h-nmr(500mhz cdcl
3
):δ=1.20,1.23(3h,s),1.31,1.35(3h,s),1.59,1.71(3h,m),2.21-2.37(2h,m),2.70-2.85(1h,m),3.50-3.54(1h,m),3.61-3.66(1h,m),3.89,4.02(2h,m)ppm.
[0358]
实施例6
[0359]
[2-(3-羟甲基-2,2-二甲基环亚丁基)丙基]三苯基鏻溴化物的制备
[0360]
将如实施例2中所获得的2-(3-羟甲基-2,2-二甲基环亚丁基)丙-1-醇(300mg,1.76mmol)的e:z=57:43的几何异构体混合物、乙腈(12g)、和三苯基膦氢溴化物(670mg,1.95mmol)置于氮气气氛的反应器中,并回流搅拌5小时。将吡啶(1g)加入到所获得的[2-(3-羟甲基-2,2-二甲基环亚丁基)丙基]三苯基鏻溴化物的溶液中,并将混合物减压浓缩。接着,向浓缩液中加入甲苯(12g),并进行减压浓缩两次,来得到目标粗化合物[2-(3-羟甲基-2,2-二甲基环亚丁基)丙基]三苯基鏻溴化物(872mg,1.76mmol),粗收率为100%。
[0361]
以下是由此制备的[2-(3-羟甲基-2,2-二甲基环亚丁基)丙基]三苯基鏻溴化物(无色或浅黄色油状液体)的光谱数据。
[0362]
1
h-nmr(500mhz cd
3
cn):δ=0.72,1.06(3h,s),0.85,1.17(3h,s),1.28-1.32,1.43-1.47(3h,m),1.47-2.70(3h,m),3.18-3.22,3.32-3.46(2h,m),3.83,3.91(2h,d,j=14.6hz,d,j=14.6hz),7.26-7.92(15h,m)ppm.
[0363]
实施例7
[0364]
[2,2-二甲基-3-(2-溴-1-甲基亚乙基)环丁基]甲基乙酸酯的制备
[0365]
将实施例3中得到的[3-(2-乙酰氧基-1-甲基亚乙基)-2,2-二甲基环丁基]甲基乙酸酯(1.78g,6.99mmol)的e:z=57:43的几何异构体混合物、二氯甲烷(30g)和30%溴化氢的乙酸溶液(2.83g,10.5mmol)置于氮气气氛的反应器中,并在20℃搅拌6小时。随后,将饱和碳酸氢钠水溶液添加至反应混合物,分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液通过硅胶柱色谱法(己烷:乙酸乙酯=30:1)纯化,得到目标化合物[2,2-二甲基-3-(2-溴-1-甲基亚乙基)环丁基]甲基乙酸酯,为e:z=57:43的几何异构体混合物(1.70g,6.18mmol),收率为88%。
[0366]
以下是由此制备的[2,2-二甲基-3-(2-溴-1-甲基亚乙基)环丁基]甲基乙酸酯(无色或浅黄色油状液体)的光谱数据。
[0367]
1
h-nmr(500mhz cdcl
3
):δ=1.15,1.20(3h,s,s),1.26,1.31(3h,s,s),1.59-1.60,1.70-171(3h,m),2.03(3h,s),2.15-2.29(2h,m),2.60-2.75(1h,m),3.82,3.94,3.97(2h,s,d,j=9.6hz,d,j=9.6hz),4.08-4.15(2h,m)ppm.
[0368]
实施例8
[0369]
(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯的制备
[0370]
[0371]
将实施例3中得到的[3-(2-乙酰氧基-1-甲基亚乙基)-2,2-二甲基环丁基]甲基乙酸酯(483mg,1.90mmol)的e:z=57:43的几何异构体混合物、乙腈(12g)、2-(二叔丁基膦基)联苯(230mg,0.771mmol)和乙酸钯(40mg,0.18mmol)置于氮气气氛的反应器中,并在20℃搅拌。然后,在反应体系中加入三乙胺(770mg,7.61mmol)和甲酸(260mg,5.65mmol)以形成甲酸三乙铵,并在30℃搅拌19小时。随后,将水加入反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液用硅胶柱色谱法(己烷:乙酸乙酯=50:1)纯化,得到目标化合物(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯,为78:18:4的顺式、反式和在双键处的区域异构体(即(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯)的混合物,(328mg,1.67mmol),收率为88%。
[0372]
以下是由此制备的顺式-(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯(无色或浅黄色油状液体)的光谱数据。
[0373]
ir(d-atr):νmax=3080,2957,2870,1743,1647,1460,1385,1368,1240,1162,1031,972,886,641,607,556cm-1
.
[0374]
1
h-nmr(500mhz cdcl
3
):δ=0.81(3h,s),1.19(3h,s),1.59(1h,q,j=10.7hz)1.64(3h,t,j=0.8hz),1.89(1h,dt,j=7.6,10.7hz),2.02(3h,s),2.13-2.22(1h,m),2.37-2.41(1h,m)3.94(1h,dd,j=8.6,11.3hz);4.04(1h,dd,j=6.3,11.3hz);4.56(1h,brs);4.79-4.82(1h,m)ppm.
[0375]
13
c-nmr(150mhz,cdcl
3
):δ=16.07,21.02,22.92,22.96,30.92,39.74,41.05,48.83,64.95,109.42,144.93,171.05ppm.
[0376]
实施例9
[0377]
(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯的制备
[0378][0379]
将实施例3中得到的[3-(2-乙酰氧基-1-甲基亚乙基)-2,2-二甲基环丁基]甲基乙酸酯(483mg,1.90mmol)的e:z=57:43的几何异构体混合物、乙腈(12g)将三苯基膦(200mg,0.763mmol)和乙酸钯(40mg,0.18mmol)置于氮气气氛的反应器中并在20℃搅拌。然后,在反应体系中加入三乙胺(770mg,7.61mmol)和甲酸(260mg,5.65mmol)以形成甲酸三乙铵,并回流搅拌24小时。随后,将水加入反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液用硅胶柱色谱法(己烷:乙酸乙酯=50:1)纯化,得到目标化合物(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯,为68:30:2的顺式、反式和在双键处的区域异构体(即(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯)的混合物,(321mg,1.63mmol),收率为86%。
[0380]
实施例10
[0381]
(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸酯和(3-异亚丙基-2,2-二甲基环丁
基)甲基乙酸酯的制备
[0382][0383]
将实施例3中得到的[3-(2-乙酰氧基-1-甲基亚乙基)-2,2-二甲基环丁基]甲基乙酸酯(1.86g,7.33mmol)的e:z=57:43的几何异构体混合物、四氢呋喃(thf)(19g)、三辛基膦(220mg,0.594mmol)和乙酸钯(33mg,0.15mmol)置于氮气气氛的反应器中并在20℃搅拌。然后,在反应体系中加入三乙胺(2.97g,29.3mmol)和甲酸(1.01g,22.0mmol)形成甲酸三乙铵,并在35℃搅拌5小时。随后,将水加入反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液用硅胶柱色谱法(己烷:乙酸乙酯=50:1)纯化,得到目标化合物(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯,为65:34:1的顺式、反式和在双键处的区域异构体(即(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯)的混合物,(1.27g,6.45mmol),收率为88%。
[0384]
实施例11
[0385]
(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯的制备
[0386][0387]
将乙酸钯(1.86g,8.27mmol)、四氢呋喃(thf)(1602g)、三辛基膦(12.3g,33.1mmol)和[3-(2-乙酰氧基-1-甲基亚乙基)-2,2-二甲基环丁基]甲基乙酸酯为e:z=70:30的几何异构体混合物(420g,1.65mol)放置在氮气气氛的反应器中并在45℃搅拌。随后,在内部温度为50℃以下的反应器中滴加三乙胺(335g,3.31mol)和甲酸(114g,2.48mol)的乙腈(mecn)(335g)溶液。滴加完成后,将混合物在45℃搅拌4小时。然后,向反应混合物中加入乙酸和盐水,并且分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将所得浓缩液减压蒸馏,得到目标化合物(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯,为68:31:1的顺式、反式和在双键处的区域异构体(即(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯)的混合物,(310g,1.58mmol),收率为96%。由此获得的顺式-(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸酯(无色或浅黄色油状液体)的光谱数据具有与实施例8相同的光谱。
[0388]
实施例12
[0389]
(3-异丙烯基-2,2-二甲基环丁基)甲基-2-甲基丁酸酯和(3-异亚丙基-2,2-二甲
基环丁基)甲基2-甲基丁酸酯
[0390][0391]
将实施例4中获得的[3-[2-(2-甲基丁酰氧基)-1-甲基亚乙基]-2,2-二甲基环丁基]甲基2-甲基丁酸酯的e:z=57:43的几何异构体混合物(1.84g,5.43mmol)、四氢呋喃(thf)(40g)、三辛基膦(160mg,0.436mmol)和乙酸钯(24mg,0.11mmol)置于氮气气氛的反应器中,并在20℃搅拌1小时。然后,在反应体系中加入三乙胺(2.19g,21.7mmol)和甲酸(750mg,16.3mmol)以形成甲酸三乙铵,并在35℃搅拌24小时。随后,将水加入反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液用硅胶柱色谱法(己烷:乙酸乙酯=80:1)纯化,得到目标化合物(3-异丙烯基-2,2-二甲基环丁基)甲基2-甲基丁酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基2-甲基丁酸酯,为64:32:4的顺式、反式和在双键处的区域异构体(即(3-异亚丙基-2,2-二甲基环丁基)甲基2-甲基丁酸酯)的混合物(1.15g,4.84mmol),收率为89%。
[0392]
以下是由此制备的顺式-(3-异丙烯基-2,2-二甲基环丁基)甲基2-甲基丁酸酯(无色或浅黄色油状液体)的光谱数据。
[0393]
1
h-nmr(500mhz cdcl
3
):δ=0.81(3h,s),0.89(3h,t,j=7.5hz),1.11(3h,q,j=7.0hz),1.20(3h,s),1.40-1.51(1h,m),1.56-1.72(5h,m),1.87(1h,dt,j=7.6,10.7hz),2.13-2.22(1h,m),2.29-2.41(2h,m),3.92,3.94(1h,dd,j=6.1,11.1hz,dd,j=6.1,11.1hz,4.04,4.05(1h,dd,j=6.1,11.1hz,dd,j=6.1,11.1hz),4.55(1h,brs),4.78-4.81(1h,m)ppm.
[0394]
实施例13
[0395]
1-氯甲基-3-异丙烯基-2,2-二甲基环丁烷和1-氯甲基-3-异亚丙基-2,2-二甲基环丁烷的制备
[0396][0397]
将实施例5中得到的1-氯甲基-3-(2-氯-1-甲基亚乙基)-2,2-二甲基环丁烷(988mg,4.77mmol)的e:z=57:43的几何异构体混合物、四氢呋喃(thf)(20g)、三辛基膦(280mg,0.763mmol)和乙酸钯(40mg,0.18mmol)置于氮气气氛的反应器中,并在20℃搅拌1小时。然后,在反应体系中加入三乙胺(1.93g,19.1mmol)和甲酸(660mg,14.3mmol)以形成
甲酸三乙铵,并在55℃搅拌24小时。随后,将水加入反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液通过硅胶柱色谱法(己烷)纯化,得到目标化合物1-氯甲基-3-异丙烯基-2,2-二甲基环丁烷和1-氯甲基-3-异亚丙基-2,2-二甲基环丁烷,为53:46:1的顺式、反式和在双键处的区域异构体(即1-氯甲基-3-异亚丙基-2,2-二甲基环丁烷)的混合物,(553mg,3.20mmol),收率为67%。
[0398]
由此制备的1-氯甲基-3-异丙烯基-2,2-二甲基环丁烷(无色或浅黄色油状液体)的光谱数据如下。
[0399]
1
h-nmr(500mhz cdcl
3
):δ=0.85,0.98(3h,s),1.14,1.26(3h,s),1.57,1.72(1h,q,j=10.7hz,m),1.66-1.67(3h,m),1.98,2.04-2.10(1h,dt,j=7.7,10.7hz,m),2.15-2.30(1h,m),2.35-2.39,2.52-2.57(1h,m),3.40-3.49,3.60,3.72(2h,m,dd,j=8.8,10.7hz,dd,j=6.8,10.7hz),4.56,4.66(1h,brs,brs),4.80-4.83,4.85-4.87(1h,m)ppm.
[0400]
实施例14
[0401]
(3-异丙烯基-2,2-二甲基环丁基)甲醇的制备
[0402][0403]
将实施例6中获得的目标粗产物[2-(3-羟甲基-2,2-二甲基环亚丁基)丙基]三苯基鏻溴化物(872mg,1.76mmol)和四氢呋喃(thf)(70g)置于氮气气氛的反应器中并在0℃搅拌。随后,在10℃以下的反应器内部温度滴加3.60m的双(2-甲氧基乙氧基)氢化钠铝(2.00ml,7.20mmol)的甲苯溶液。滴加完成后,将混合物逐渐加热搅拌至20℃达1小时。随后,将10重量%的氢氧化钠水溶液加入到反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液用硅胶柱色谱法(己烷:乙酸乙酯=10:1)纯化,得到目标化合物(3-异丙烯基-2,2-二甲基环丁基)甲醇,为77:23的顺式和反式形式的几何异构体混合物(195mg,1.27mmol),收率为72%。
[0404]
在gc中未检测到双键区域异构体(3-异亚丙基-2,2-二甲基环丁基)甲醇。
[0405]
以下是由此制备的顺式-(3-异丙烯基-2,2-二甲基环丁基)甲醇(无色或浅黄色油状液体)的光谱数据。
[0406]
1
h-nmr(500mhz cdcl
3
):δ=0.82(3h,s),1.22(3h,s),1.55(1h,q,j=10.7hz),1.65(3h,s),1.85-1.91(1h,m),2.03-2.10(1h,m),2.34-2.39(1h,m),3.52(1h,dd,j=6.5,10.7hz),3.59(1h,dd,j=8.3,10.7hz),4.55(1h,brs),4.78-4.81(1h,m)ppm.
[0407]
以下是由此制备的反式-(3-异丙烯基-2,2-二甲基环丁基)甲醇(无色或浅黄色油状液体)的光谱数据。
[0408]
1
h-nmr(500mhz cdcl
3
):δ=0.95(3h,s),1.12(3h,s),1.51(1h,brs),1.58-1.63(1h,m),1.65(3h,s),1.76-1.90(1h,m),2.03-2.14(1h,m),2.53-2.59(1h,m),3.69(1h,dd,j=7.6,10.7hz),3.85(1h,dd,j=7.3,10.7hz),4.62(1h,brs),4.81-4.84(1h,m)ppm.
[0409]
实施例15
[0410]
(3-异亚丙基-2,2-二甲基环丁基)甲醇的制备
[0411][0412]
将氢化铝锂(570mg,15.0mmol)和四氢呋喃(thf)(60g)置于氮气气氛的反应器中,并在0℃搅拌1小时。在5℃以下的反应器内部温度,将[2,2-二甲基-3-(2-溴-1-甲基亚乙基)环丁基]甲基乙酸酯的e:z=57:43的几何异构体混合物(1.62g,5.89mmol)滴加到此溶液中。滴加完成后,将混合物逐渐加热搅拌至20℃达6小时。随后,添加水(570mg)和15重量%的氢氧化钠溶液(570mg),随后进一步添加水(1.71g),并过滤。将获得的滤液减压浓缩,并通过硅胶柱色谱法(己烷:乙酸乙酯=10:1)纯化,得到目标化合物(3-异亚丙基-2,2-二甲基环丁基)甲醇(909mg,5.89mmol),收率为100%。
[0413]
在gc中未检测到双键区域异构体(3-异亚丙基-2,2-二甲基环丁基)甲醇。
[0414]
以下是由此制备的(3-异亚丙基-2,2-二甲基环丁基)甲醇(无色或浅黄色油状液体)的光谱数据。
[0415]
1
h-nmr(500mhz cdcl
3
):δ=1.15(3h,s),1.26(3h,s),1.45(3h,s),1.56-1.58(3h,m),1.63(1h,brs),2.03-2.14(2h,m),2.54-2.62(1h,m),3.61(1h,dd,j=6.9,10.7hz),3.76(1h,dd,j=7.7,10.7hz)ppm.
[0416]
13
c-nmr(150mhz,cdcl
3
):δ=18.48,19.53,20.90,27.70,28.67,42.65,44.05,64.30,122.42,137.39ppm.
[0417]
实施例16
[0418]
(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯的制备
[0419][0420]
将如实施例13中获得的1-氯甲基-3-异丙烯基-2,2-二甲基环丁烷和1-氯甲基-3-异亚丙基-2,2-二甲基环丁烷的混合物(535mg,3.10mmol)、乙酸钠(580mg,7.07mmol)、碘化钠(100mg,0.667mmol)和n,n-二甲基乙酰胺(20g)放置在氮气气氛的反应器中并在150℃搅拌24小时。随后,将水加入反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液用硅胶柱色谱法(己烷:乙酸乙酯=50:1)纯化,得到目标化合物(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯,为57:42:1的顺式、反式和在双键处的区域异构体(即(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯)的混合物,(255mg,1.30mmol),收率为42%。
[0421]
实施例17
[0422]
(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸酯的制备
[0423][0424]
将如实施例14中所获得的(3-异丙烯基-2,2-二甲基环丁基)甲醇的77:23的顺式和反式的几何异构体混合物(154mg,1.00mmol)、吡啶(316mg)和甲苯(10g)置于氮气气氛的反应器中,并在0℃搅拌。随后,在10℃以下的反应器内部温度中滴加乙酸酐(204mg,2.00mmol)。滴加完成后,将混合物逐渐加热搅拌至20℃达6小时。随后,将水加入反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液通过硅胶柱色谱法(己烷:乙酸乙酯=50:1)纯化,得到目标化合物(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸酯,为77:23的顺式和反式形式的几何异构体混合物(183mg,0.930mmol),收率为93%。
[0425]
实施例18
[0426]
(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯的制备
[0427][0428]
将如实施例15中获得的(3-异亚丙基-2,2-二甲基环丁基)甲醇(818mg,5.30mmol)、甲苯(10g)、吡啶(1.68g,21.2mmol)和乙酸酐(1.09g,10.7mmol)置于氮气气氛的反应器中,并在20℃搅拌24小时。随后,将水加入反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液通过硅胶柱色谱法(己烷:乙酸乙酯=50:1)纯化,得到目标化合物(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯(911mg,4.64mmol),收率为88%。
[0429]
以下是由此制备的(3-异亚丙基-2,2-二甲基环丁基)甲基乙酸酯(无色或浅黄色油状液体)的光谱数据。
[0430]
1
h-nmr(500mhz cdcl
3
):δ=1.13(3h,s),1.24(3h,s),1.45(3h,s),1.57(3h,t,j=1.9hz),2.03(3h,s),2.10-2.22(2h,m),2.56-2.63(1h,m),4.07-4.15(2h,m)ppm.
[0431]
13
c-nmr(150mhz,cdcl
3
):δ=18.49,19.53,20.98,21.00,27.72,28.37,38.99,44.20,65.73,122.67,136.93,171.20ppm.
[0432]
实施例19
[0433]
(3-异亚丙基-2,2-二甲基环丁基)甲基甲磺酸酯的制备
[0434][0435]
将根据实施例15获得的(3-异亚丙基-2,2-二甲基环丁基)甲醇(858mg,5.56mmol)、四氢呋喃(thf)(20g)和三乙胺(1.71g,16.9mmol)放入氮气气氛的反应器中,在0℃搅拌1小时。在10℃以下的反应器内部温度中,向该溶液中滴加甲磺酰氯(1.09g,10.7mmol)。滴加完成后,将混合物在20℃搅拌1小时。随后,将水加入反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液通过硅胶柱色谱法(己烷:乙酸乙酯=10:1)纯化,得到目标化合物(3-异亚丙基-2,2-二甲基环丁基)甲磺酸
甲酯(1.29g,5.56mmol),收率为100%。
[0436]
以下是由此制备的(3-异亚丙基-2,2-二甲基环丁基)甲基甲磺酸酯(无色或浅黄色油状液体)的光谱数据。
[0437]
1
h-nmr(500mhz cdcl
3
):δ=1.17(3h,s),1.27(3h,s),1.45(3h,brs),1.58(3h,t,j=1.9hz),2.15-2.22(1h,m),2.25-2.33(1h,m),2.61-2.67(1h,m),3.00(3h,s),4.23(1h,dd,j=7.3,9.9hz),4.31(1h,dd,j=8.0,10.0hz)ppm.
[0438]
实施例20
[0439]
(3-异亚丙基-2,2-二甲基环丁基)甲基3-甲基-2-丁烯酸酯的制备
[0440][0441]
将如实施例19中获得的(3-异亚丙基-2,2-二甲基环丁基)甲磺酸甲酯(1.29g,5.56mmol)、甲苯(40g)、水(430mg)、异戊烯酸(3-甲基-2-丁烯酸)(690mg,6.92mmol)、碳酸钾(610mg,4.39mmol)和四丁基氯化铵(60mg,0.23mmol)置于氮气气氛的反应器中,并在100℃搅拌24小时。随后,将水加入反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液用硅胶柱色谱法(己烷:乙酸乙酯=50:1)纯化,得到目标化合物(3-异亚丙基-2,2-二甲基环丁基)甲基3-甲基-2-丁烯酸酯,(1.20g,5.06mmol),收率为91%。
[0442]
以下是由此制备的(3-异亚丙基-2,2-二甲基环丁基)甲基3-甲基-2-丁烯酸酯(无色或浅黄色油状液体)的光谱数据。
[0443]
ir(d-atr):νmax=2956,2917,2864,1719,1659,1449,1376,1361,1349,1272,1227,1146,1076,993,851cm-1
.
[0444]
1
h-nmr(500mhz cdcl
3
):δ=1.14(3h,s),1.25(3h,s),1.45(3h,brs),1.56-1.58(3h,m),1.88(3h,d,j=1.5hz),2.12-2.30(5h,m),2.56-2.64(1h,m),4.11(1h,dd,j=6.8,11.4hz),4.15(1h,dd,j=8.0,11.5hz),5.64-5.66(1h,m)ppm.
[0445]
13
c-nmr(150mhz,cdcl
3
):δ=18.50,19.54,20.15,20.99,27.34,27.78,28.39,39.14,44.21,64.75,116.15,122.53,137.18,156.25,166.82ppm.
[0446]
实施例21
[0447]
(3-异丙烯基-2,2-二甲基环丁基)甲醇和(3-异亚丙基-2,2-二甲基环丁基)甲醇的制备
[0448]
[0449]
将如实施例11中获得的(3-异丙烯基-2,2-二甲基环丁基)甲基乙酸酯(60.3g,307mmol)的几何异构体混合物、甲醇(94g)、和25%的氢氧化钠水溶液(94g)置于氮气气氛的反应器中,并在20℃搅拌12小时。随后,将盐水加入到反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液减压蒸馏,得到目标化合物(3-异丙烯基-2,2-二甲基环丁基)甲醇和(3-异亚丙基-2,2-二甲基环丁基)甲醇,为67:32:1的顺式、反式和在双键上的区域异构体(即(3-异亚丙基-2,2-二甲基环丁基)甲醇)的混合物(46.0g,298mmol),收率为97%。由此获得的顺式-(3-异丙烯基-2,2-二甲基环丁基)甲醇(无色或淡黄色油状液体)和由此获得的反式-(3-异丙烯基-2,2-二甲基环丁基)甲醇(无色或浅黄色油性液体)的光谱数据具有与实施例14相同的光谱。
[0450]
实施例22
[0451]
(3-异丙烯基-2,2-二甲基环丁基)甲基2-甲基丁酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基2-甲基丁酸酯的制备
[0452][0453]
将如实施例21中获得的(3-异丙烯基-2,2-二甲基环丁基)甲醇的几何异构体混合物(12.6g,82.0mmol)、四氢呋喃(thf)(100g)和吡啶(16.9g,213mmol)放置在氮气气氛的反应器中,并在0℃搅拌。随后,在15℃以下的反应器内部温度,将2-甲基丁酰氯(12.9g,107mmol)滴加到溶液中。滴加完成后,将混合物逐渐加热搅拌至20℃达6小时。随后,将盐水加入到反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液进行减压蒸馏,从而获得目标化合物(3-异丙烯基-2,2-二甲基环丁基)甲基2-甲基丁酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基2-甲基丁酸酯,为68:31:1的顺式、反式和在双键处的区域异构体(即(3-异亚丙基-2,2-二甲基环丁基)2-甲基丁酸甲酯)的混合物(19.5g,81.6mmol),收率为100%。如此获得的顺式-(3-异丙烯基-2,2-二甲基环丁基)甲基2-甲基丁酸酯的光谱数据具有与实施例14相同的光谱。
[0454]
实施例23
[0455]
(3-异丙烯基-2,2-二甲基环丁基)甲基3-甲基-3-丁烯酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基3-甲基-3-丁烯酸酯的制备
[0456][0457]
将按实施例21获得的(3-异丙烯基-2,2-二甲基环丁基)甲醇的几何异构体混合物(13.4g,86.6mmol)、二氯甲烷(665g)、3-甲基-3-丁烯酸(12.5g,125mmol)、和4-二甲基氨基吡啶(dmap)(1.06g,8.66mmol)放在氮气气氛的反应器中,并在0℃搅拌。加入n,n
′-
二环己基碳二亚胺(dcc)(24.8g,120mmol)。将混合物逐渐加热搅拌至20℃达2小时。随后,将醚和盐水加入到反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液用硅胶柱色谱法(己烷:乙酸乙酯=40:1)纯化,得到目标化合物(3-异丙烯基-2,2-二甲基环丁基)甲基3-甲基-3-丁烯酸酯和(3-异亚丙基-2,2-二甲基环丁基)甲基3-甲基-3-丁烯酸酯,为67:32:1的顺式、反式和在双键处的区域异构体(即(3-异亚丙基-2,2-二甲基环丁基)甲基3-甲基-3-丁烯酸酯(20.2g,85.6mmol),收率为99%。
[0458]
以下是由此制备的顺式-(3-异丙烯基-2,2-二甲基环丁基)甲基3-甲基-3-丁烯酸酯(无色或浅黄色油状液体)的光谱数据。
[0459]
ir(d-atr):νmax=3080,2956,2870,1738,1648,1454,1385,1370,1337,1284,1241,1153,1075,1030,994,889cm-1
.
[0460]
1
h-nmr(500mhz cdcl
3
):δ=0.80(3h,s),1.19(3h,s),1.61(1h,q,j=10.7hz),1.64-1.65(3h,m),1.79-1.81(3h,m),1.88(1h,dt,j=10.7,7.5hz),2.15-2.22(1h,m),2.39(1h,dd,j=10.7,7.5hz),3.00-3.01(2h,m),3.96(1h,dd,j=8.8,11.1hz),4.07(1h,dd),j=6.5,11.1hz),4.56(1h,s),4.79-4.81(1h,m),4.83-4.84(1h,m),4.89-4.91(1h,m)ppm.
[0461]
13
c-nmr(150mhz,cdcl
3
):δ=16.09,22.46,22.86,22.94,30.91,39.78,41.07,43.57,48.81,65.12,109.44,114.61,138.52,144.94,171.32,ppm.
[0462]
实施例24
[0463]
(3-异亚丙基-2,2-二甲基环丁基)甲基2-甲基丁酸酯的制备
[0464][0465]
将根据实施例15获得的(3-异亚丙基-2,2-二甲基环丁基)甲醇(9.16g,59.4mmol)、四氢呋喃(thf)(100g)和吡啶(14.1g)置于氮气气氛的反应器中,并在0℃搅拌。
在15℃以下的反应器的内部温度滴加2-甲基丁酰氯(10.8g,89.2mmol)。滴加完成后,将混合物逐渐加热搅拌至20℃达3小时。随后,将盐水加入到反应混合物中,并分离有机层,并通过常规洗涤、干燥和浓缩进行后处理。然后,将得到的浓缩液进行减压蒸馏,获得目标化合物(3-异亚丙基-2,2-二甲基环丁基)甲基2-甲基丁酸酯(14.2g,59.4mmol),收率为100%。
[0466]
以下是由此制备的(3-异亚丙基-2,2-二甲基环丁基)甲基2-甲基丁酸酯(无色或浅黄色油状液体)的光谱数据。
[0467]
ir(d-atr):νmax=2964,2935,2878,1735,1461,1383,1361,1264,1240,1186,1152,1081,1013,973,889,755cm-1
.
[0468]
1
h-nmr(500mhz cdcl
3
):δ=0.89(3h,t,j=7.5hz),1.13(3h,d,j=8.0hz),1.13(3h,s),1.24(3h,s),1.42-1.50(4h,m),1.57(3h,t,j=1.7hz),1.60-1.77(1h,m),2.09-2.23(2h,m),2.30-2.39(1h,m),2.55-2.61(1h,m),4.08-4.15(2h,m)ppm.
[0469]
13
c-nmr(150mhz,cdcl
3
):δ=11.64,16.58,16.63,18.50,19.54,21.02,21.04,26.72,26.75,27.50,27.52,28.40,39.12,39.15,41.17,44.20,65.33,122.60,136.99,176.73ppm。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
相关标签:
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



