一种新型黄连素衍生物及其合成方法和应用与流程
 2021-02-02 12:02:36|
2021-02-02 12:02:36| 372|
372| 起点商标网
起点商标网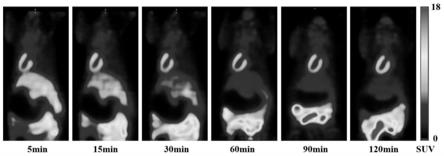
[0001]
本发明属于显像剂领域,具体涉及一种新型黄连素衍生物及其合成方法和应用。
背景技术:
[0002]
虽然冠心病的诊断和治疗方案在近年来取得较大发展,但在世界范围内(尤其是欧美国家),冠心病任然是严重威胁人类健康的重大疾病之一。在我国,冠心病及心脏相关疾病的发生率和死亡率也呈上升趋势。据世界卫生组织(who)最新数据显示,未来5年左右我国将会迎来心血管疾病的高峰,因此,冠心病等心脏相关疾病的早期诊断、早期干预和预后评价显得尤为重要。
[0003]
心肌灌注显像作为一种无创的诊断技术,在心脏相关疾病中的诊断尤为重要。与临床广泛使用的单光子核素计算机断层扫描(spect)心肌灌注显像相比,正电子核素计算机断层扫描(pet)具有更高的空间和时间分辨率,灵敏度更高,且兼具心肌灌注定量等优点。遗憾的是,目前临床可用的正电子核素心肌显像剂的半衰期均较短,如13n-nh3
·
h2o,h
215
o,82rb等,极大限制了临床应用。
[0004]
现有技术通过对天然产物盐酸小檗碱(黄连素)的功能和结构进行解析,发现了黄连素10位侧链衍生的一系列产物具有较好的心肌靶向性,并成功制备了正电子核素
18
f标记的产物,通过体内外实验验证了其靶向性和在疾病诊断中的应用价值。然而黄连素10位侧链衍生物的制备非常困难,难以实现进一步的研究和临床转化。
[0005]
目前为止还没有
18
f正电子核素标记的心肌显像剂应用于临床,处于研究阶段的心肌灌注显像剂要么不太稳定,进入体内容易分解,要么pet影像质量较差,具有较高的本底噪声,难以形成比较清晰的影像,或者肝脏摄取太高,造成心脏成像质量差。
[0006]
因此,研发新型正电子核素心肌灌注显像剂,是近年来核素探针研发的热点。
18
f作为一个广泛存在于药物结构中的卤素元素f的正电子同位素,不仅可方便的与小分子心肌靶向分子兼容,其物理半衰期达到109.8分钟,同时其发射的正电子湮灭后产生的511kev的伽马光子,也适宜于临床显像,因此
18
f是开发新型pet正电子药物的首选核素。本课题组也开展了基于
18
f核素标记的心肌灌注显像剂的研究,并成功开发了一系列
18
f标记的黄连素母环10位侧链取代的衍生物作为心肌灌注显像剂。然而,该系列化合物的原料合成难度较大,产率很低,难以实现临床转化。
[0007]
综上,一种心肌摄取更高,同时原料易得,降低了分子探针合成的成本,有利于临床转化的新型黄连素衍生物及其合成方法有待研究。
技术实现要素:
[0008]
针对上述问题,本发明旨在提供一种新型黄连素衍生物及其合成方法和应用,本发明的
18
f标记的新型黄连素衍生物心肌摄取更高,同时原料易得,降低了分子探针合成的成本,有利于临床转化。
[0009]
为了达到上述的目的,本发明所采用的技术方案是:
[0010]
新型黄连素衍生物,其结构式为:
[0011][0012]
其中,n=1,2,3
…
,r为卤素离子或其他阴离子。优选的,侧链为聚乙二醇侧链或烷基侧链。
[0013]
进一步的,侧链为乙二醇,一缩二乙二醇,二缩三乙二醇,三缩四乙二醇和其他聚乙二醇中的任意一种。
[0014]
进一步的,r为cl离子,br离子和对甲苯磺酸阴离子中的任一种。
[0015]
进一步的,新型黄连素衍生物的正电子核素探针的结构式为:
[0016][0017]
进一步的,所述正电子核素探针的化学合成前体,其结构式为:
[0018][0019]
其中,lg为离去基团,作为亲核试剂进攻的位点,lg为-ots或-otf。
[0020]
进一步的,新型黄连素衍生物的正电子核素探针的制备方法,包括以下步骤:
[0021]
1)取式i化合物在真空条件下加热生成式ii化合物;
[0022][0023]
2)将式ii化合物与lg-(ch
2
)n-lg或lg-(ch
2-ch
2-o)n-(ch
2
)
2-lg在碱性条件下反应生成式iii前体化合物;
[0024][0025]
3)将式iii前体化合物与
18
f离子发生亲核取代反应,生成
18
f标记的正电子核素探针;
[0026][0027]
进一步的,使用亲核取代反应的正电子核素标记方法,即以氮杂冠醚k2.2.2为相转移催化剂,乙腈为溶剂的条件下,前体化合物经密闭加热反应10-20分钟即可制得
18
f标记的正电子核素探针,该探针经分离纯化后即可用于进一步的体内外研究。
[0028]
进一步的,
18
f离子在kryptofix(k-222)与k
2
co
3
催化下,与含有2-5mg前体化合物的1ml乙腈溶液在90度下反应20分钟即可制备
18
f标记的正电子核素探针。
[0029]
进一步的,所述新型黄连素衍生物在心肌显像剂上的应用。
[0030]
进一步的,所述新型黄连素衍生物的正电子核素探针在心肌显像剂上的应用。
[0031]
进一步的,所述新型黄连素衍生物在制备诊断冠心病的试剂中的应用。
[0032]
进一步的,所述新型黄连素衍生物的正电子核素探针在制备诊断冠心病的试剂中的应用。
[0033]
本发明对异喹啉类生物碱黄连素的结构进行衍生,在前期的基础上优化了衍生的位点,引入了含f的侧链,制备了一系列具有心肌靶向性的探针,并通过正电子核素
18
f的标记实验,成功的制备了该系列化合物的
18
f标记物。通过对正常动物的研究了该系列化合物在体内的吸收、分布、代谢与排泄等药理和药物代谢性质,并通过显像实验验证了该系列化合物的心肌显像特性。
[0034]
据该系列分子结构推测,该系列化合物是通过心肌线粒体内外膜差通过主动转运进入心肌细胞线粒体内,从而实现选择性浓聚于心肌线粒体内部。通过该机制实现心肌选择性浓聚核素探针而显像探针,包括了临床上广泛使用的99mtc-mibi。
[0035]
本发明以黄连素9位选择性脱甲基的产物为起始物,合成了一系列黄连素母环9位含f侧链取代的衍生物,9位取代的衍生物与10位取代的衍生物相比,心肌摄取更高,同时原料易得,降低了分子探针合成的成本,有利于临床转化。
[0036]
本发明的有益效果:
[0037]
本发明
18
f标记的新型黄连素衍生物(黄连素9位取代的衍生物)具有较好的心肌靶向性,可作为心肌显像剂,其机制是通过心肌存在的大量线粒体内外膜电位差主动转运实现选择性浓聚于心肌细胞线粒体内。同时,与10位取代衍生物相比,本发明涉及的9位取代的衍生物具有更高的
‘
心脏-肝脏
’
摄取比值,拥有更好的心肌显像图像,能更好的反映心脏的功能。因此,本发明涉及到的正电子核素标记物可作为心肌显像探针,应用于临床,可反映心肌线粒体代谢功能,间接反映心肌存活状态,进行心脏功能评价。9位取代的衍生物与10位取代的衍生物相比,心肌摄取更高,同时原料易得,降低了分子探针合成的成本,有利于临床转化。
附图说明
[0038]
图1为实施例化合物在正常动物(wistar大鼠)中的pet显像;
[0039]
图2为实施例化合物在正常动物(wistar大鼠)中心脏、血液、肝脏及肺部中标准摄取值随时间变化曲线;
[0040]
图3为黄连素10位脱甲基产物结构式和黄连素9位脱甲基产物结构式及其对应的
18
f丙基取代放射性探针(化合物10为10位取代,化合物5为9位取代);
[0041]
图4为化合物5和化合物10分别在原代心肌细胞和心肌成纤维细胞中的摄取速率;
[0042]
图5为化合物5与化合物10在正常大鼠中的pet显像。
具体实施方式
[0043]
为了进一步说明本发明的技术效果,下面通过实施例对本发明进行具体描述。
[0044]
18
f标记的新型黄连素衍生物的具体制备方法如下:
[0045][0046]
将化合物1,(1g,2.69mmol)放置于圆底烧瓶中,并使用真空接头与水泵连接。开启水泵抽真空,待真空稳定在0.1mpa时,油浴加热170度。在此温度下加热1h,取出真空瓶,冷至室温,移除水泵。使用柱层析分离粗产物,得到9位选择性脱甲基的产物化合物2 0.85g,产率88.3%。1h nmr()10.20(s,1h),8.66(s,1h),7.95(s,1h),7.14(s,1h),7.02(d,1h),6.82(d,1h),6.07(s,2h),5.35(s,1h),4.45(dd,2h),3.83(s,3h),3.12(dd,2h).
[0047][0048]
将化合物2(300mg,0.83mmol)溶于10ml乙腈中,加入碳酸钾(150mg,1.09mmol)和化合物3(354mg,0.922mmol),完毕后于70度加热反应过夜,反应完全后冷却至室温,过滤,旋干溶剂,硅胶柱层析纯化分离,得到350mg化合物4,收率73.2%。1h nmr(400mhz,dmso-d6)δ9.80(s,1h),8.94(s,1h),8.20(d,j=9.1hz,1h),8.00(d,j=9.1hz,1h),7.79(s,1h),7.47(d,j=7.9hz,2h),7.12
–
7.08(m,3h),6.17(s,2h),4.95(t,j=6.3hz,2h),4.42(t,j=6.1hz,2h),4.06(s,3h),3.94(t,j=6.5hz,2h),3.21(t,j=6.3hz,2h),2.34(m,2h),2.28(s,3h).13c nmr(101mhz,dmso-d6)δ150.73,150.31,148.16,146.26,145.73,142.96,138.00(2c),133.51,131.17,128.47(2c),127.16,125.94(2c),124.01,121.95,120.91,120.70,108.88,105.92,102.56,71.69,57.58,55.75,42.63,33.09,26.80,21.24.hrms esi-ms-q-tof for c29h28no7s+[m]+found,534.1580m/z;calcd mass,534.1581.
[0049][0050]
加速器生产的
18
f-hf溶液通过液体管路传输到屏蔽热室,并被强阳离子交换柱qma
柱捕获,使用冠醚(k222-k
2
co
3
)淋洗液将吸附在qma柱上的
18
f离子洗脱到玻璃反应管中,加热除去h
2
o,并再次加入乙腈再次加热吹干除残留水分。将化合物4(2mg)溶于2ml乙腈中,并通入反应管中,加热90度反应20分钟。反应完毕后使用5ml 30%mecn和70%含0.1%三氟乙酸的去离子水混合液稀释,并使用半制备hplc进行分离,采用的色谱系统为:安捷伦1100hplc系统,waters sunfire prep c185um(250*10mm)column,30%mecn-70%h2o(0.1%tfa),5ml/min。约20分钟左右出现一放射性峰,收集该放射性峰并进行溶剂置换,洗去mecn,用含5%乙醇的无菌蒸馏水混合液溶解最终产品,即可用于后续的显像实验。
[0051][0052]
将化合物2(300mg,0.83mmol)溶于10ml乙腈中,加入碳酸钾(186mg,1.35mmol)和化合物3(425mg,1.03mmol),完毕后于70度加热反应过夜,反应完全后冷却至室温,过滤,旋干溶剂,硅胶柱层析纯化分离,得到386mg化合物7,收率63.0%。
1
hnmr(400mhz,dmso-d
6
)δ9.71(s,1h),8.94(s,1h),8.20(d,j=9.1hz,1h),8.01(d,j=9.1hz,1h),7.80(s,1h),7.71
–
7.64(m,2h),7.48(d,j=8.1hz,2h),7.41(d,j=8.1hz,2h),7.15
–
7.07(m,3h),6.18(s,2h),4.92(t,j=6.3hz,2h),4.42
–
4.33(m,2h),4.16
–
4.10(m,2h),4.06(s,3h),3.83
–
3.75(m,2h),3.69
–
3.61(m,2h),3.21(t,j=6.3hz,2h),2.39(s,3h),2.28(s,3h).
13
c nmr(101mhz,dmso-d
6
)δ150.80,150.30,148.17,146.31,145.69,145.40,142.99,137.98(2c),133.46,132.73,131.04,130.55(2c),128.47(2c),127.94(2c),127.06,125.94(2c),124.03,122.24,120.95,120.73,108.90,105.91,102.57,73.37,70.55,69.91,68.30,57.50,55.95,26.82,21.54,21.23.hrms esi-ms-q-tof for c
30
h
30
no
8
s
+
[m]
+
found,564.1685m/z;calcdmass,564.1687.
[0053][0054]
加速器生产的
18
f-hf溶液通过液体管路传输到屏蔽热室,并被强阳离子交换柱qma柱捕获,使用冠醚(k222-k
2
co
3
)淋洗液将吸附在qma柱上的
18
f离子洗脱到玻璃反应管中,加热除去h
2
o,并再次加入乙腈再次加热吹干除残留水分。将化合物8(2mg)溶于2ml乙腈中,并通入反应管中,加热90度反应20分钟。反应完毕后使用5ml 30%mecn和70%含0.1%三氟乙酸的去离子水混合液稀释,并使用半制备hplc进行分离,采用的色谱系统为:安捷伦1100hplc系统,waters sunfire prep c18 5um(250*10mm)column,30%mecn-70%h2o(0.1%tfa),5ml/min。约20分钟左右出现一放射性峰,收集该放射性峰并进行溶剂置换,洗去mecn,用含5%乙醇的无菌蒸馏水混合液溶解最终产品,即可用于后续的显像实验。
[0055]
以下通过试验例具体说明本发明的有益效果:
[0056]
正常大鼠pet显像实验:通过正电子核素标记实验得到放射性标记物之后,并通过
在线的制备hplc纯化、溶剂置换、制剂等步骤后,即得到可用于动物显像的核素探针无菌注射液。选择正常wistar大鼠,使用小动物麻醉机经异氟烷-氧气混合气体麻醉后,按照0.16mci/kg的剂量进行尾静脉注射(最大注射体积不超过1ml),并进行micro pet/ct(iris micro-pet/ct,inviscan)静态扫描,在注射后30,60,90及120分钟时采集pet信号并重建pet图像。
[0057]
正常大鼠pet显像如图1所示,尾静脉注射5分钟后放射性药物开始在心脏浓聚,同时大部分药物浓聚在肝脏。30分钟后,肝脏浓聚的药物逐渐代谢,并逐渐向下消化道分布。60分钟以后,药物在肝脏中的分布逐渐到本底水平,心脏中一直保持较高的摄取。120分钟时,心脏的放射性一直保持,肝脏中几乎无放射性浓聚,肠道中有较高的放射性分布,应该为药物代谢后的生理分布。在所有时间点,其他主要内脏或组织器官均未见异常摄取。
[0058]
为量化放射性药物在体内摄取,我们采取suv(标准摄取值,standard uptake value)来评价药物的摄取。suv=病灶的放射性浓度(kbq/ml)/注射剂量(mbq)/体重(kg),该值越高说明该部位放射性探针浓聚越高。本实验中,勾画肺部、心脏心肌层、血池及肝脏为感兴趣区,通过软件计算suv,并按照suv-注射时间作图(图2)。图二展示了主要脏器suv随时间变化的曲线,由该图可知,肝脏在15分钟时摄取达到峰值,之后逐渐下降;心肌在30分钟时摄取达到峰值,但是该时间点肝脏摄取较高,无法获得较高的
‘
心-肝
’
比;心-肝
’
比在120分钟时达到最大值,同时120分钟时获得最清晰的心脏图像。
[0059]
与此同时,我们比较了9位取代的放射性标记探针与10位取代的放射性标记探针的体内外性质。本研究中,使用18f-氟丙基在小檗红碱9位取代的探针(图3,化合物5)与18f-氟丙基在小檗红碱10位取代的探针(图3,化合物10)进行了细胞摄取实验和体内显像实验数据进行对比。在体外细胞实验中(图4),化合物5与化合物10显示了相似的心肌细胞摄取率。然而,在原代心肌细胞(nrvms:primary neonatal rat ventricular myocytes)中,化合物5显示了更高的摄取率(2.87%:2.44%);在心肌成纤维细胞(nih/3t3:mouse embryo fibroblast cell line)中,二者的摄取率相似(0.97%:0.91%)。同时,在正常大鼠的心肌显像中(图5),二者的结果也显示了一定的差异。与放射性探针5相比,放射性探针10显示了更高的脂溶性,肝脏摄取较高;同时,放射性探针5显示了更高的心脏摄取及
‘
心-肝
’
比值,心脏显示更清晰。
[0060]
综上所述,本发明涉及的小檗红碱9位取代的探针比10位取代的探针具有更优异的体内外靶向性质。
[0061]
最后需要说明的是,以上实施例仅用于说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明的技术方案进行了详细说明,本领域技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明的宗旨和范围,其均应涵盖在本发明的保护范围当中。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



