磺酰基防己诺林碱类化合物及其制备方法和应用与流程
 2021-02-02 11:02:22|
2021-02-02 11:02:22| 227|
227| 起点商标网
起点商标网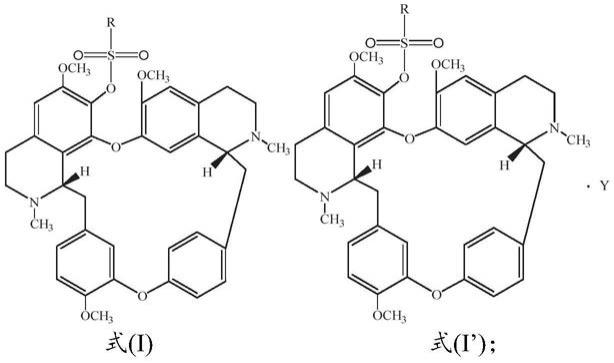
[0001]
本发明涉及医药领域,具体涉及磺酰基防己诺林碱类化合物及其制备方法和应用。
背景技术:
[0002]
公开该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
[0003]
尿酸是嘌呤经xod代谢的最终产物,人体内尿酸的生成、吸收、分解以及排泄之间处于一种稳态平衡,一旦上述过程中的某一处发生紊乱,就会导致体内尿酸的稳态平衡发生异常,进而就会引起高尿酸血症。
[0004]
xod在尿酸合成中起到了关键性作用,抑制xod的活性,能够减少体内尿酸的生成进而使得血清中尿酸的浓度降低,因此抑制xod的活性已成为研发治疗高尿酸血症药物的一个重要策略。随着研究的进展,多种xod抑制剂在临床上得到了广泛应用,并且在一定程度上起到了较好的效果。1966年经美国fda批准上市的别嘌醇作为临床上应用最早、使用最为广泛的xod抑制剂,在相当长的时间内受到了广泛的应用。别嘌醇是次黄嘌呤的异构体,能与次黄嘌呤竞争性结合xod的活性位点泪蝶呤中心,从而阻止次黄嘌呤最终代谢成为尿酸。但是,临床数据报告显示,别嘌醇容易引起较为严重的皮肤不良反应,如过敏性皮疹、重症多形性红斑、剥脱性和紫癜性病变等,同时长期大量的服用别嘌醇也会引起白细胞以及血小板的减少、粒细胞缺乏症等血液系统疾病,严重时可引起继发性感染或内脏器官功能衰竭而危及生命。鉴于别嘌醇一系类的副作用以及较高的有效使用剂量,限制了其在临床上的应用。非布索坦与托匹司他分别是2009年和2013年经美国fda批准上市的新型的非嘌呤类xod抑制剂,与别嘌醇相比,此类抑制剂对xod的选择性和活性有所提高,主要适用于对别嘌醇敏感或肾功能受损的高尿酸血症患者。但是,非布索坦与托匹司他常见的不良反应主要有肝功能异常、头痛、腹泻、呕吐和关节疼痛等,同时此类xod抑制剂主要通过肝脏代谢,禁止肝功能不全者使用,因此其使用范围很小。
[0005]
因此,开发活性高的xod抑制剂非常有必要。
技术实现要素:
[0006]
本发明的目的是克服上述不足而提供一种磺酰基防己诺林碱类化合物及其制备方法。本发明的另一目的是提供该磺酰基防己诺林碱类化合物在xod抑制剂药物中的应用。
[0007]
具体地,本发明的技术方案如下:
[0008]
在本发明的第一方面,本发明提供了一种磺酰基防己诺林碱类化合物,其具有式(i)或式(i
’
)所示结构:
[0009][0010]
其中,r选自烃基、芳烃基、苄基、杂环基、取代烃基、取代芳烃基、取代苄基、取代杂环基;其中,取代烃基的取代基团为卤素或硝基,取代芳烃基的取代基团、取代苄基的取代基团、取代杂环基的取代基团为卤素、烷基、硝基中的一种或多种;y选自1分子的无机酸、有机酸或2分子的无机酸、有机酸。
[0011]
本发明所述取代烃基可以为一取代烃基,也可以为二取代烃基、三取代烃基等多取代烃基。本发明所述取代芳烃基可以为一取代芳烃基,也可以为二取代芳烃基、三取代芳烃基等多取代芳烃基。本发明所述取代苄基可以为一取代苄基,也可以为二取代苄基、三取代苄基等多取代苄基。本发明所述取代杂环基可以为一取代杂环基,也可以为二取代杂环基、三取代杂环基等多取代杂环基。
[0012]
优选地,所述烃基为c
1-8
烷基;取代烃基为卤素取代的c
1-8
烷基。
[0013]
优选地,所述烃基为甲基、乙基、正丙基、异丙基、环丙烷基、正丁基、异正丁基、正己烷基或正辛烷基。
[0014]
优选地,所述取代烃基为氯甲基、溴甲基、三氯甲基、2-氯乙烷基或2-溴乙烷基。
[0015]
优选地,所述芳烃为苯基或萘基。
[0016]
优选地,所述取代芳烃基为邻氯苯基、间氯苯基、对氯苯基、3,4-二氯苯基、邻溴苯基、间溴苯基、对溴苯基、3,4-二溴苯基、邻氟苯基、间氟苯基、对氟苯基、3,4-二氟苯基、对甲基苯基或对硝基苯基。
[0017]
优选地,所述取代苄基为邻氯苄基、间氯苄基、对氯苄基、3,4-二氯苄基、邻溴苄基、间溴苄基、对溴苄基、3,4-二溴苄基、邻氟苄基、间氟苄基、对氟苄基或3,4-二氟苄基。
[0018]
优选地,所述杂环基为噻吩基或吡啶基。
[0019]
优选地,所述取代杂环基为5-氯噻吩基、5-溴噻吩基或1,2-二甲基-1h-咪唑基。
[0020]
优选地,无机酸为盐酸、氢溴酸或氢碘酸。
[0021]
优选地,有机酸为甲酸、乙酸、丙酸、丙二酸、1,4-丁二酸、苯甲酸、烟酸、富马酸、苹果酸、马来酸、葡萄糖酸或柠檬酸。
[0022]
优选地,y为1分子乙酸、2分子盐酸或2分子氢溴酸。
[0023]
优选地,本发明的式(i)或式(i
’
)化合物具有下表1中所示结构:
[0024]
表1
[0025]
[0026]
[0027]
naoh-k、γ-al
2
o
3-koh-na、γ-al
2
o
3-koh-k、甲醇钠、乙醇钠、丙醇钠、丁醇钠、氨基钠、金属钠、氢化钠、氢氧化钠、氢氧化钾、氢氧化钙、氧化钠、氧化钾、氧化钙、碳酸钾、碳酸钠、氨水、乙胺、二乙胺、三乙胺、甲胺、二甲胺、三甲胺、吡啶和哌啶中的一种或多种。
[0037]
优选地,所述防己诺林碱、rso
2
x、碱性物质的摩尔比为1:0.1~10:0.01~10,优选为1︰1.0~1.2︰0.6~3.0。
[0038]
优选地,所述分离纯化方法选自过滤、树脂处理、水洗、蒸馏、结晶、萃取、活性炭处理、分子筛处理和层析中的一种或多种的结合。
[0039]
本发明所述的分离纯化的方法可以为:比如,在tlc检测防己诺林碱全部反应,升温至室温后,加水,用二氯甲烷、三氯甲烷、丙酮或乙酸乙酯萃取1至多次{如3次比如[(50~300)ml
×
3]},tlc追踪反应与产物的分离纯化过程,萃取液回收,得固体物在干燥比如在50~60℃下干燥4~6h,得到目标产物。
[0040]
比如,在tlc检测防己诺林碱全部反应,将反应液浓缩,进行层析(如中性氧化铝柱提纯),洗脱剂为二氯甲烷:甲醇(120:1~50:1)。
[0041]
比如,在tlc检测防己诺林碱全部反应,将反应液浓缩,在0℃的冷井中结晶,快速过滤,干燥。
[0042]
在本发明的第三方面,本发明提供了一种药物组合物,包括上述磺酰基防己诺林碱类化合物。
[0043]
在本发明的第四方面,本发明提供了一种药物制剂,包括上述磺酰基防己诺林碱类化合物及药学上可接受的辅料和/或载体。
[0044]
本发明所述药物制剂的给药剂型可以是液体剂型、固体剂型。液体剂型可以是真溶液类、胶体类、微粒剂型、乳剂剂型、混旋剂型等。固体剂型可以是片剂、胶囊、丸剂、粉剂、颗粒剂、栓剂、冻干粉等。
[0045]
本发明所述的辅料包括但不局限于:粘合剂(如糖浆、山梨醇等)、填充剂(玉米淀粉、乳糖等)、润滑剂(如硬脂酸镁、聚乙二醇等)、崩解剂(马铃薯淀粉等)等。
[0046]
本发明所述的载体包括但不局限于:离子交换剂、氧化铝、硬脂酸铝、卵磷脂、人血清蛋白、磷酸盐、甘油、山梨酯、山梨酸钾、水、聚乙烯吡咯烷酮、纤维素物质、聚乙二醇、羧甲基纤维素钠、聚丙烯酸酯、蜂蜡、羊毛酯等。载体在药物组合物中的含量可以是1重量%-98重量%,通常大约占到80重量%。
[0047]
在本发明第五方面,本发明提供了一种上述磺酰基防己诺林碱类化合物、上述药物组合物或上述药物制剂在为xod抑制剂中的应用。
[0048]
在本发明第六方面,本发明提供了一种上述磺酰基防己诺林碱类化合物、上述药物组合物或上述药物制剂在制备治疗高尿酸血症药物中的应用。
[0049]
本发明的有益效果是:
[0050]
本发明磺酰基防己诺林碱类化合物因具有双苄基异喹啉母核结构同时具有含磺酰基团特征,对xod具有较好的抑制活性,本发明化合物在1.56~6.25μm对xod抑制率普遍都高于80%,其活性远高于临床用药别嘌醇,约为别嘌醇的2~6倍。
具体实施方式
[0051]
应该指出,以下详细说明都是示例性的,旨在对本发明提供进一步的说明。除非另
有指明,本文使用的所有技术和科学术语具有与本发明所属技术领域的普通技术人员通常理解的相同含义。
[0052]
需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本发明的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作、器件、组件和/或它们的组合。
[0053]
为了使得本领域技术人员能够更加清楚地了解本发明的技术方案,以下将结合具体的实施例详细说明本发明的技术方案。
[0054]
实施例1
[0055]
将100.0mg防己诺林碱(约0.18mmol)溶于3ml的二氯甲烷中,加入充满氩气的两颈烧瓶中,并置于控温至0℃的冷井中,磁力搅拌下加入溶于2ml的二氯甲烷的三乙胺66.5mg(约0.72mmol),混合1h后,加入31.0mg(约0.27mmol)的甲基磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用120:1,80:1洗脱),分离纯化,制得白色粉末状产物117.5mg(约0.17mmol),熔点:208.1-209.9℃,收率94.4%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ7.40(dd,j=8.2,1.9hz,1h),7.15(dd,j=8.2,2.5hz,1h),6.85(d,j=7.7hz,2h),6.81(dd,j=8.3,2.5hz,1h),6.56(s,1h),6.46(s,1h),6.40(s,1h),6.33(dd,j=8.3,2.0hz,1h),6.04(s,1h),3.92(s,3h),3.78(s,3h),3.70(dd,j=22.5,12.4hz,2h),3.52(dd,j=16.1,12.9hz,2h),3.43
–
3.36(m,3h),2.99(tdd,j=18.0,13.2,6.7hz,6h),2.87(d,j=8.4hz,3h),2.81(dd,j=13.8,6.1hz,2h),2.69(d,j=9.0hz,3h),2.60
–
2.45(m,2h),2.30(s,3h);
13
c nmr(101mhz,cdcl
3
)δ154.05,150.13,149.26,148.93,148.67,147.04,142.47,134.36,133.63,132.65,130.52,127.64,127.09,125.34,123.40,122.98,122.30,122.05,121.91,115.88,112.33,111.54,106.14,64.38,61.37,56.10,56.01,55.80,45.84,44.89,43.77,42.29,41.83,41.37,39.53,39.12,23.39,22.12;hrms(esi):calcd for c
38
h
42
n
2
o
8
s m/z:686.2662,found:687.2711[m+h]
+
。即表1中的化合物1。
[0056]
实施例2
[0057]
将100.0mg防己诺林碱(约0.18mmol)溶于3ml的三氯甲烷中,加入充满氩气的两颈烧瓶中,并置于控温至-20℃的冷井中,磁力搅拌下,加入溶于2ml的三氯甲烷的nah 5.0mg(约0.20mmol),混合1h后,加入23.2mg(约0.18mmol)的乙基磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用120:1,80:1洗脱),分离纯化,制得白色粉末状产物113.6mg(约0.162mmol),熔点:205.5-207.2℃,收率90.0%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ7.36(dd,j=8.2,1.9hz,1h),7.14(dd,j=8.2,2.4hz,1h),6.82(dt,j=8.3,5.3hz,3h),6.51(d,j=16.7hz,2h),6.42
–
6.30(m,2h),6.04(s,1h),3.92(s,3h),3.88
–
3.81(m,1h),3.81
–
3.73(m,3h),3.69(s,1h),3.62
–
3.41(m,3h),3.37(d,j=11.3hz,3h),3.31
–
3.11(m,2h),3.08
–
2.64(m,10h),2.59(s,3h),2.47(ddd,j=36.1,25.3,16.1hz,2h),2.35
–
2.23(m,3h),1.26(t,j=7.4hz,3h);
13
c nmr(101mhz,cdcl
3
)δ153.58,150.32,149.36,148.89,148.10,146.92,142.25,135.08,134.46,132.51,132.40,130.42,128.47,128.30,127.70,123.67,122.78,122.12,121.94,121.41,115.79,112.60,111.39,106.14,63.94,61.37,56.08,56.06,55.86,46.42,46.02,
45.14,43.71,42.46,42.30,41.47,38.94,24.77,22.14;hrms(esi):calcd for c
39
h
44
n
2
o
8
s m/z:700.2818,found:701.2892[m+h]
+
。即表1中的化合物2。
[0058]
实施例3
[0059]
将100.0mg防己诺林碱(约0.18mmol)溶于10ml的二氯甲烷中,加入充满氩气的两颈烧瓶中,并置于控温至0℃的冷井中,在搅拌下加入溶于2ml的二氯甲烷的哌啶62.0mg(约0.72mmol),混合1h后,加入25.6mg(约0.20mmol)的正丙基磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩至原液体积的1/3,0℃的冷井中结晶4h以上,快速过滤,低于50℃下真空干燥,制得白色粉末状产物115.9mg(约0.162mmol),熔点:204.9-206.5℃,收率90.0%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ7.29(dd,j=8.2,1.9hz,1h),7.06(dd,j=8.1,2.4hz,1h),6.74(dt,j=8.3,5.4hz,3h),6.43(d,j=14.0hz,2h),6.36
–
6.19(m,2h),5.96(s,1h),3.84(s,3h),3.76(dd,j=11.1,5.3hz,0h),3.73
–
3.65(m,3h),3.62(d,j=9.7hz,0h),3.40(ddd,j=11.9,9.6,5.7hz,1h),3.26(d,j=14.9hz,3h),2.93
–
2.74(m,2h),2.70
–
2.59(m,1h),2.57
–
2.45(m,1h),2.23(d,j=16.7hz,1h),1.76
–
1.57(m,1h),0.89(t,j=7.5hz,1h);
13
c nmr(101mhz,cdcl
3
)δ153.60,150.38,149.37,148.97,148.10,146.92,142.25,135.16,134.52,132.46,130.42,128.42,127.63,123.67,122.78,122.15,121.95,121.55,115.84,112.60,111.38,106.14,64.04,61.39,56.09,56.08 55.87,53.46,45.19,43.74,42.41,41.52,39.23,29.72,24.73,22.11,17.16,12.91;hrms(esi):calcd for c
40
h
46
n
2
o
8
s m/z:714.2975,found:715.3008[m+h]
+
。即表1中的化合物3。
[0060]
实施例4
[0061]
将100.0mg防己诺林碱(约0.18mmol)溶于10ml的dmf溶剂中,加入充满氩气的两颈烧瓶中,并置于控温至10℃的冷井中,磁力搅拌下,加入溶于3ml的dmf溶剂的三乙胺66.5mg(约0.72mmol),混合1h后,加入31.2mg(约0.20mmol)的正丁基磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用120:1,80:1洗脱),分离纯化,制得白色粉末状产物120.8mg(约0.166mmol),熔点:203.3-205.1℃,收率92.2%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ7.29(d,j=8.0hz,1h),7.06(d,j=7.8hz,1h),6.82
–
6.71(m,3h),6.43(d,j=16.6hz,2h),6.34
–
6.22(m,2h),5.95(s,1h),3.84(s,3h),3.78(dd,j=11.0,4.8hz,1h),3.67(d,j=11.1hz,3h),3.62(d,j=9.8hz,1h),3.46
–
3.36(m,2h),3.28(s,3h),2.95
–
2.78(m,6h),2.7
–
2.60(m,2h),2.53(s,3h),2.49
–
2.30(m,2h),2.21(s,3h),1.62(dt,j=30.1,15.2hz,2h),1.36
–
1.12(m,4h),0.81(t,j=7.2hz,3h);
13
c nmr(101mhz,cdcl
3
)δ153.64,150.37,149.36,148.97,148.12,146.93,142.26,135.11,134.54,132.55,130.40,128.44,128.20,127.70,123.67,122.81,122.13,121.93,121.57,115.87,112.60,111.41,106.14,64.06,61.39,56.07,56.07,55.87,51.63,45.17,43.75,42.48,42.31,41.55,39.19,25.28,24.67,22.09,21.50,13.58;hrms(esi):calcd for c
41
h
48
n
2
o
8
s m/z:728.3131,found:729.3204[m+h]
+
。即表1中的化合物6。
[0062]
实施例5
[0063]
将100.0mg防己诺林碱(约0.18mmol)溶于5ml的四氢呋喃溶剂中,加入充满氩气的两颈烧瓶中,并置于控温至5℃的冷井中,磁力搅拌下,加入溶于2ml的四氢呋喃的三乙胺66.5mg(约0.72mmol),混合1h后,加入35.1mg(约0.20mmol)的苯磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩至原液体积的1/3,0℃的冷井中结晶4h以上,快速过滤,低于50
℃下真空干燥,制得白色粉末状产物117.3mg(约0.157mmol),熔点:202.2-204.1℃,收率87.2%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ7.66(dd,j=15.5,7.8hz,4h),7.47(t,j=7.4hz,2h),7.33(d,j=8.1hz,1h),7.16(dd,j=8.1,1.4hz,1h),6.88(s,2h),6.78
–
6.72(m,1h),6.51
–
6.44(m,2h),6.32
–
6.20(m,2h),3.93(s,3h),3.69(dd,j=15.9,7.6hz,2h),3.52(dd,j=19.7,9.0hz,2h),3.44(s,3h),3.27(d,j=12.0hz,3h),3.26
–
3.12(m,2h),2.97
–
2.87(m,4h),2.74(dd,j=16.4,7.2hz,2h),2.63(d,j=6.5hz,4h),2.47(dd,j=17.6,12.5hz,2h),2.29(s,3h);
13
c nmr(101mhz,cdcl
3
)δ153.75,150.99,149.31,148.87,147.75,147.12,142.39,137.39,135.25,135.03,134.60,133.56,132.52,130.25,128.58,128.36,128.19,128.11,123.77,122.85,121.69,121.03,116.08,112.70,111.52,106.00,63.87,61.37,56.13,55.78,55.69,45.08,43.85,42.39,42.03,39.77,24.30,22.04;hrms(esi):calcd for c
43
h
44
n
2
o
8
s m/z:748.2852,found:749.2864[m+h]
+
。即表1中的化合物15。
[0064]
实施例6
[0065]
将100.0mg防己诺林碱(约0.18mmol)溶于5ml的dmso溶剂中,加入充满氩气的两颈烧瓶中,并置于控温至25℃的冷井中,磁力搅拌下,加入溶于2ml的dmso溶剂的三甲胺42.5mg(约0.72mmol),混合1h后,加入38.0mg(约0.20mmol)的对甲苯磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用120:1,80:1洗脱),分离纯化,制得白色粉末状产物119.5mg(约0.157mmol),熔点:201.7-203.6℃,收率87.2%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ7.53(d,j=8.1hz,2h),7.36
–
7.20(m,4h),7.15(dd,j=8.0,1.9hz,1h),6.87(s,2h),6.75(dd,j=8.2,1.9hz,1h),6.46(d,j=8.7hz,2h),6.32
–
6.22(m,2h),3.92(s,3h),3.77
–
3.51(m,4h),3.47(s,3h),3.28(s,3h),2.97
–
2.69(m,8h),2.64(s,3h),2.54(d,j=13.7hz,2h),2.47(s,3h),2.28(s,3h);
13
c nmr(101mhz,cdcl
3
)δ153.73,151.10,149.25,148.83,147.78,147.10,144.42,142.40,135.23,134.99,134.58,134.37,132.61,132.35,130.08,129.13,128.65,128.21,127.64,123.62,122.88,121.65,121.58,120.98,116.15,115.94,112.74,111.50,106.09,64.06,61.40,56.11,55.78,55.72,45.08,43.84,42.48,42.29,41.91,39.62,24.32,22.06,21.83;hrms(esi):calcd for c
44
h
46
n
2
o
8
s m/z:762.2975,found:763.3008[m+h]
+
。即表1中的化合物16。
[0066]
实施例7
[0067]
将100.0mg防己诺林碱(约0.18mmol)溶于10ml的甲苯溶剂中,加入充满氩气的两颈烧瓶中,并置于控温至0℃的冷井中,磁力搅拌下,加入溶于5ml的甲苯溶剂的金属钠5.5mg(约0.21mmol),混合1h后,加入44.2mg(约0.20mmol)的4-硝基苯磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用120:1,80:1洗脱),分离纯化,制得淡黄色粉末状产物117.2mg(约0.148mmol),熔点:202.6-204.4℃,收率82.2%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ8.22(d,j=8.8hz,3h),7.76(d,j=8.8hz,2h),7.20
–
7.15(m,1h),7.04(dd,j=8.1,2.5hz,1h),6.78(s,2h),6.68(dd,j=8.3,2.5hz,1h),6.38(d,j=20.5hz,2h),6.25
–
6.17(m,2h),3.85(s,3h),3.61
–
3.54(m,2h),3.38(s,3h),3.23(s,3h),3.16
–
2.61(m,10h),2.57(s,3h),2.48
–
2.36(m,2h),2.19(s,3h);
13
c nmr(101mhz,cdcl
3
)δ153.65,150.49,150.43,149.38,148.54,
147.73,147.11,142.84,141.92,135.11,134.24,133.11,132.54,130.09,129.77,128.64,128.40,127.80,123.87,123.69,122.80,122.01,121.81,120.30,115.80,112.78,111.52,106.16,64.04,61.33,56.12,55.76,45.07,43.76,42.57,42.35,41.95,38.15,25.08,22.15;hrms(esi):calcd for c
43
h
43
n
3
o
10
s m/z:793.2669,found:794.2656[m+h]
+
。即表1中的化合物17。
[0068]
实施例8
[0069]
将100.0mg防己诺林碱(约0.18mmol)溶于10ml的乙醇中,加入充满氩气的两颈烧瓶中,并置于控温至-5℃的冷井中,磁力搅拌下,加入溶于5ml的乙醇的乙醇钠24.5mg(约0.36mmol),混合1h后,加入42.0mg(约0.20mmol)的4-氯苯磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用120:1,80:1洗脱),分离纯化,制得淡黄色粉末状产物114.2mg(约0.146mmol),熔点:215.3-217.1℃,收率81.1%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ7.52(d,j=8.6hz,2h),7.47
–
7.27(m,4h),7.11(dd,j=8.1,2.4hz,1h),6.79(s,2h),6.68(dd,j=8.2,2.4hz,1h),6.37(d,j=12.4hz,2h),6.26
–
6.18(m,2h),3.86(s,3h),3.62
–
3.54(m,2h),3.45(s,3h),3.33(ddd,j=23.1,12.3,8.9hz,2h),3.21(s,3h),2.92
–
2.62(m,8h),2.57(s,3h),2.49
–
2.37(m,2h),2.20(s,3h);
13
c nmr(101mhz,cdcl
3
)δ153.64,150.93,149.42,148.61,147.68,147.10,142.23,140.15,135.93,135.10,134.40,132.60,130.30,130.05,129.34,128.92,128.50,128.37,128.21,128.02,123.80,122.77,121.87,120.41,115.80,112.79,111.49,106.13,63.96,61.37,56.07,55.79,53.54,45.08,43.84,42.54,42.34,42.04,39.15,24.58,22.12;hrms(esi):calcd for c
43
h
43
cln
2
o
8
s m/z:782.2829,found:783.2862[m+h]
+
。即表1中的化合物20。
[0070]
实施例9
[0071]
将100.0mg防己诺林碱(约0.18mmol)溶于10ml的叔丁醇溶剂中,加入充满氩气的两颈烧瓶中,并置于控温至-5℃的冷井中,磁力搅拌下,加入溶于5ml的叔丁醇的叔丁醇钠35.0mg(约0.36mmol),混合1h后,加入50.7mg(约0.20mmol)的2-溴苯磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用120:1,80:1洗脱),分离纯化,制得白色粉末状产物123.6mg(约0.149mmol),熔点:216.3-218.5℃,收率82.8%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ7.79(t,j=1.6hz,1h),7.70(d,j=8.0hz,1h),7.51(d,j=8.0hz,1h),7.38
–
7.16(m,3h),7.10(dd,j=8.1,2.5hz,1h),6.83
–
6.77(m,2h),6.66(dd,j=8.3,2.5hz,1h),6.38(d,j=7.2hz,2h),6.25(s,1h),6.17(dd,j=8.3,2.0hz,1h),3.83(d,j=9.4hz,3h),3.65(dd,j=11.1,5.4hz,1h),3.57(d,j=9.9hz,1h),3.45(s,3h),3.43
–
3.31(m,2h),3.20(s,3h),2.96
–
2.59(m,8h),2.55(s,3h),2.43(dd,j=30.0,9.4hz,2h),2.20(s,3h);
13
c nmr(101mhz,cdcl
3
)δ153.77,150.96,149.26,148.70,147.61,147.12,142.29,139.25,136.62,135.06,134.51,132.69,131.39,130.17,128.53,128.32,127.98,127.22,123.98,122.85,122.46,121.77,120.61,116.26,112.81,111.47,106.22,63.74,61.38,56.11,55.80,46.14,45.02,43.80,42.37,39.64,24.33,22.00;hrms(esi):calcd for c
43
h
43
brn
2
o
8
s m/z:826.1923,found:827.1965[m+h]
+
。即表1中的化合物22。
[0072]
实施例10
[0073]
将100.0mg防己诺林碱(约0.18mmol)溶于3ml的二氯甲烷中,加入充满氩气的两颈烧瓶中,并置于控温至-5℃的冷井中,磁力搅拌下,加入γ-al
2
o
3-na 20.0mg,混合1h后,加入50.7mg(约0.20mmol)的3-溴苯磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用100:1,60:1洗脱),分离纯化,制得白色粉末状产物128.0mg(约0.155mmol),熔点:215.8-217.7℃,收率86.1%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ7.79(t,j=1.6hz,1h),7.70(d,j=8.0hz,1h),7.51(d,j=8.0hz,1h),7.38
–
7.16(m,3h),7.10(dd,j=8.1,2.5hz,1h),6.83
–
6.77(m,2h),6.66(dd,j=8.3,2.5hz,1h),6.38(d,j=7.2hz,2h),6.25(s,1h),6.17(dd,j=8.3,2.0hz,1h),3.83(d,j=9.4hz,3h),3.65(dd,j=11.1,5.4hz,1h),3.57(d,j=9.9hz,1h),3.45(s,3h),3.43
–
3.31(m,2h),3.20(s,3h),2.96
–
2.59(m,8h),2.55(s,3h),2.43(dd,j=30.0,9.4hz,2h),2.20(s,3h);
13
c nmr(101mhz,cdcl
3
)δ153.77,150.96,149.26,148.70,147.61,147.12,142.29,139.25,136.62,135.06,134.51,132.69,131.39,130.17,128.53,128.32,127.98,127.22,123.98,122.85,122.46,121.77,120.61,116.26,112.81,111.47,106.22,63.74,61.38,56.11,55.80,46.14,45.02,43.80,42.37,39.64,24.33,22.00;hrms(esi):calcd for c
43
h
43
brn
2
o
8
s m/z:826.1923found:827.1844[m+h]
+
。即表1中的化合物23。
[0074]
实施例11
[0075]
将100.0mg防己诺林碱(约0.18mmol)溶于3ml的二氯甲烷中,加入充满氩气的两颈烧瓶中,并置于控温至-5℃的冷井中,磁力搅拌下,加入γ-al
2
o
3-k 20.0mg,混合1h后,加入38.8mg(约0.20mmol)的2-氟苯磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用100:1,60:1洗脱),分离纯化,制得白色粉末状产物117.4mg(约0.153mmol),熔点:205.1-207.2℃,收率85.0%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ7.66
–
7.43(m,2h),7.15(ddd,j=27.5,17.5,8.3hz,4h),6.77(d,j=7.8hz,2h),6.67(dd,j=8.2,2.0hz,1h),6.41(d,j=3.2hz,2h),6.18(d,j=12.3hz,2h),5.27(s,1h),3.83(s,3h),3.65
–
3.53(m,2h),3.42(dd,j=19.0,9.5hz,2h),3.35
–
3.28(m,3h),3.22(s,3h),3.17
–
2.55(m,8h),2.52(s,3h),2.38(dd,j=35.6,30.4hz,2h),2.22(d,j=16.2hz,3h);
13
c nmr(101mhz,cdcl
3
)δ160.96,158.37,153.80,150.52,149.29,148.93,147.91,147.10,142.35,135.91,135.00,134.68,132.65,132.53,131.06,130.26,128.46,128.22,127.69,125.95,123.71,122.9,121.71,120.96,117.15,116.94,116.14,112.77,111.52,105.83,63.91,61.34,56.12,55.79,55.56,45.03,43.76,42.39,42.29,41.72,39.88,24.14,22.00;hrms(esi):calcd for c
43
h
43
fn
2
o
8
s m/z:766.2724,found:767.2717[m+h]
+
。即表1中的化合物26。
[0076]
实施例12
[0077]
将100.0mg防己诺林碱(约0.18mmol)溶于3ml的哌啶溶剂中,加入充满氩气的两颈烧瓶中,并置于控温至-5℃的冷井中,磁力搅拌下,加入γ-al
2
o
3-naoh-na 20.0mg,混合1h后,加入38.8mg(约0.20mmol)的4-氟苯磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用100:1,60:1洗脱),分离纯化,制得白色粉末状产物122.9mg(约0.16mmol),熔点:206.0-207.7℃,收率88.9%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ7.63(d,j=6.8hz,2h),7.40
–
7.07(m,5h),6.86(s,2h),6.75(d,j=7.8hz,1h),6.49(s,2h),6.26(d,j=13.2hz,2h),3.91(s,3h),3.67(t,j=10.0hz,
2h),3.48(d,j=10.5hz,2h),3.38(s,3h),3.30(s,3h),2.79(ddd,j=33.4,22.7,13.2hz,8h),2.60(s,3h),2.57
–
2.34(m,2h),2.28(s,3h);
13
c nmr(101mhz,cdcl
3
)δ166.95,153.77,150.89,149.39,148.74,147.81,147.14,142.32,134.98,134.45,133.49,132.61,131.43,130.22,128.31,128.11,127.74,123.84,122.82,121.85,120.72,116.02,115.96,115.79,112.73,111.52,106.04,63.98,61.35,56.13,55.77,45.05,43.85,42.39,42.09,39.20,24.49,22.08;
[0078]
hrms(esi):calcd for c
43
h
43
fn
2
o
8
s m/z:766.2724,found:767.2717[m+h]
+
。即表1中的化合物28。
[0079]
实施例13
[0080]
将100.0mg防己诺林碱(约0.18mmol)溶于3ml的二氯甲烷中,加入充满氩气的两颈烧瓶中,并置于控温至0℃的冷井中,磁力搅拌下,加入γ-al
2
o
3-naoh-k 22.0mg,混合1h后,加入36.4mg(约0.20mmol)的2-噻吩磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用100:1,50:1洗脱),分离纯化,制得白色粉末状产物111.5mg(0.148mmol),熔点:202.5-204.2℃,收率82.2%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ7.56(d,j=4.9hz,1h),7.38(d,j=3.8hz,1h),7.26(dd,j=8.1,1.7hz,1h),7.07(dd,j=8.1,2.4hz,1h),7.01
–
6.96(m,1h),6.78(d,j=8.0hz,2h),6.68(dd,j=8.2,2.4hz,1h),6.42(t,j=9.4hz,2h),6.28
–
6.16(m,2h),5.37(s,1h),3.83(d,j=9.1hz,3h),3.70
–
3.59(m,2h),3.43(d,j=11.3hz,3h),3.36(dd,j=27.5,17.6hz,2h),3.22(s,3h),2.75(ddd,5.8hz,8h),2.54(d,j=9.2hz,3h),2.49
–
2.30(m,2h),2.26
–
2.18(m,3h);
13
c nmr(101mhz,cdcl
3
)δ153.74,150.97,149.34,149.15,148.97,147.83,147.09,142.37,137.00,135.16,134.63,133.66,132.65,130.27,128.55,127.96,127.91,127.05,123.79,122.83,121.79,121.24,116.06,112.64,111.49,105.85,64.06,61.37,56.13,55.81,55.79,45.16,43.82,42.56,42.31,41.94,40.33,24.16,22.06;hrms(esi):calcd for c
41
h
42
n
2
o
8
s
2
m/z:754.2383,found:755.2459[m+h]
+
。即表1中的化合物43。
[0081]
实施例14
[0082]
将100.0mg防己诺林碱(约0.18mmol)溶于3ml的二氯甲烷中,加入充满氩气的两颈烧瓶中,并置于控温至0℃的冷井中,磁力搅拌下,加入溶于2ml的二氯甲烷的三乙胺66.5mg(约0.72mmol),混合1h后,加入35.4mg(约0.20mmol)的3-吡啶磺酰氯进行反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用100:1,50:1洗脱),分离纯化,制得白色粉末状产物108.0mg(约0.144mmol),熔点:207.2-208.9℃,收率80.0%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ8.77(dd,j=10.1,3.3hz,2h),7.84(d,j=8.1hz,1h),7.31(dd,j=8.0,3.5hz,2h),7.19(s,1h),7.10(dd,j=8.1,2.3hz,1h),6.79(s,2h),6.69(dd,j=8.2,2.3hz,1h),6.41(d,j=16.1hz,2h),6.27
–
6.17(m,2h),3.86(s,3h),3.75
–
3.60(m,2h),3.40(s,3h),3.34(s,3h),2.96
–
2.76(m,6h),2.68(d,j=12.2hz,2h),2.59(s,3h),2.49
–
2.35(m,2h),2.21(s,3h);
13
c nmr(101mhz,cdcl
3
)δ153.77,150.36,149.28,148.84,147.83,147.11,142.15,136.06,135.09,134.42,134.03,132.95,132.60,130.37,128.62,127.93,127.71,123.84,123.28,122.81,121.87,121.08,115.94,112.68,111.47,105.92,63.80,61.33,56.12,55.81,55.56,53.49,50.82,43.68,42.30,41.87,39.89,24.21,22.09;hrms(esi):calcd for c
42
h
43
n
3
o
8
s m/z:749.2804,
found:750.2824[m+h]
+
。即表1中的化合物47。
[0083]
实施例15
[0084]
将100.0mg防己诺林碱(约0.18mmol)溶于3ml的二氯甲烷中,加入充满氩气的两颈烧瓶中,并置于控温至0℃的冷井中,磁力搅拌下加入溶于2ml的二氯甲烷的三乙胺66.5mg(约0.72mmol),混合1h后,加入31.0mg(约0.27mmol)的甲基磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用120:1,60:1洗脱),分离纯化,制得白色粉末状产物110.0mg(约0.16mmol),熔点:208.0-209.7℃。该产物在搅拌、温度控制60℃以下缓慢添加36%hcl,至溶液ph值为7.0后停止添加盐酸并继续搅拌反应2h,在60℃下真空干燥6h,即得白色粉末状产物113.9mg(约0.15mmol),收率83.3%,目的产物熔点:253.2-255.1℃,产物分析表征:
1
h nmr(400mhz,cd
3
od)δ8.17(br,1h),8.01(br,1h),7.39(dd,j=8.2,1.9hz,1h),7.14(dd,j=8.2,2.5hz,1h),6.84(d,j=7.7hz,2h),6.80(dd,j=8.3,2.5hz,1h),6.55(s,1h),6.45(s,1h),6.39(s,1h),6.32(dd,j=8.3,2.0hz,1h),6.03(s,1h),3.91(s,3h),3.77(s,3h),3.61(dd,j=22.5,12.4hz,2h),3.49(dd,j=16.1,12.9hz,2h),3.42
–
3.36(m,3h),2.98(tdd,j=18.0,13.2,6.7hz,6h),2.86(d,j=8.4hz,3h),2.65(dd,j=13.8,6.1hz,2h),2.71(d,j=9.0hz,3h),2.40
–
2.55(m,2h),2.31(s,3h);
13
c nmr(101mhz,cd
3
od)δ155.25,151.34,150.45,150.12,149.87,148.24,143.67,135.55,134.82,133.84,131.71,128.83,128.28,124.45,124.59,124.17,123.49,123.24,123.09,116.07,113.52,112.73,107.33,72.20,73.57,69.56,67.01,57.29,49.76,48.47,46.03,45.97,43.02,42.56,40.72,40.31,22.58,21.31;hrms(esi):calcd for c
38
h
42
n
2
o
8
s[m-2hcl]m/z:686.2662,found:687.2732[m-2hcl+h]
+
。即表1中的化合物48。
[0085]
实施例16
[0086]
将100.0mg防己诺林碱(约0.18mmol)溶于3ml的三氯甲烷中,加入充满氩气的两颈烧瓶中,并置于控温至-20℃的冷井中,磁力搅拌下,加入溶于2ml的三氯甲烷的nah 5.0mg(约0.20mmol),混合1h后,加入23.2mg(约0.18mmol)的乙基磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用120:1,60:1洗脱),分离纯化,制得白色粉末状产物116.2mg(约0.166mmol),熔点:205.7-207.6℃。该产物在搅拌、温度控制60℃以下缓慢添加36%hcl,至溶液ph值为7.0后停止添加盐酸并继续搅拌反应2h,在60℃下真空干燥6h,即得白色粉末状产物123.8mg(约0.16mmol),收率88.8%,目的产物熔点:252.7-254.4℃,产物分析表征:
1
h nmr(400mhz,cd
3
od)δ8.15(br,1h),7.99(br,1h),7.35(dd,j=8.2,1.9hz,1h),7.13(dd,j=8.2,2.4hz,1h),6.81(dt,j=8.3,5.3hz,3h),6.50(d,j=16.7hz,2h),6.41
–
6.29(m,2h),6.03(s,1h),3.91(s,3h),3.87
–
3.80(m,1h),3.80
–
3.72(m,3h),3.68(s,1h),3.61
–
3.40(m,3h),3.36(d,j=11.3hz,3h),2.99
–
2.89(m,2h),2.87
–
2.63(m,8h),2.59(s,3h),2.46(ddd,j=36.1,25.3,16.1hz,2h),2.34
–
2.22(m,3h),1.25(t,j=7.4hz,3h);
13
c nmr(101mhz,cd
3
od)δ155.12,151.52,150.77,150.17,149.54,148.47,143.69,136.56,135.96,133.97,133.94,131.90,129.79,129.77,129.31,125.14,124.25,123.62,122.47,122.91,116.24,114.10,112.79,107.62,70.85,57.27,49.31,48.77,47.90,47.52,46.60,43.81,42.95,40.33,24.24,21.62;hrms(esi):calcd for c
39
h
44
n
2
o
8
s[m-2hcl]m/z:700.2818,found:701.2876[m-2hcl+h]
+
。目的
产物即表1中的化合物49。
[0087]
实施例17
[0088]
将100.0mg防己诺林碱(约0.18mmol)溶于5ml的四氢呋喃溶剂中,加入充满氩气的两颈烧瓶中,并置于控温至5℃的冷井中,磁力搅拌下,加入溶于2ml的四氢呋喃的三乙胺66.5mg(约0.72mmol),混合1h后,加入35.1mg(约0.20mmol)的苯磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩至原液体积的1/3,0℃的冷井中结晶4h以上,快速过滤,低于50℃下真空干燥,制得白色粉末状产物116.0mg(约0.155mmol),熔点:202.3-204.2℃。该产物在搅拌、温度控制50℃以下缓慢添加36%hcl,至溶液ph值为7.0后停止添加盐酸并继续搅拌反应2h,在50℃下真空干燥6h,即得白色粉末状产物123.2mg(约0.15mmol),收率83.2%,目的产物熔点:255.3-257.1℃。产物分析表征:
1
h nmr(400mhz,cd
3
od)δ8.11(br,1h),7.94(br,1h),7.65(dd,j=15.5,7.8hz,4h),7.46(t,j=7.4hz,2h),7.32(d,j=8.1hz,1h),7.15(dd,j=8.1,1.4hz,1h),6.87(s,2h),6.77
–
6.72(m,1h),6.50
–
6.45(m,2h),6.31
–
6.20(m,2h),3.92(s,3h),3.68(dd,j=15.9,7.6hz,2h),3.51(dd,j=19.7,9.0hz,2h),3.43(s,3h),3.26(d,j=12.0hz,3h),3.25
–
3.12(m,2h),3.12
–
2.97(m,4h),2.73(dd,j=16.4,7.2hz,2h),2.69(d,j=6.5hz,4h),2.45(dd,j=17.6,12.5hz,2h),2.28(s,3h);
13
c nmr(101mhz,cd
3
od)δ154.80,152.04,150.36,149.92,148.90,148.17,143.44,138.43,136.30,136.08,135.65,134.61,133.57,131.30,129.563,129.41,129.24,129.16,124.82,123.90,122.74,122.05,117.13,113.75,112.57,107.05,74.92,72.42,67.18,66.82,56.74,49.45,48.57,46.13,43.08,40.82,23.35,21.09;hrms(esi):calcd for c
43
h
44
n
2
o
8
s[m-2hcl]m/z:748.2852,found:749.2897[m-2hcl+h]
+
。即表1中的化合物62。
[0089]
实施例18
[0090]
将100.0mg防己诺林碱(约0.18mmol)溶于10ml的叔丁醇溶剂中,加入充满氩气的两颈烧瓶中,并置于控温至-10℃的冷井中,磁力搅拌下,加入溶于5ml的叔丁醇的叔丁醇钠35.0mg(约0.36mmol),混合1h后,加入50.7mg(约0.20mmol)的3-溴苯磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用120:1,60:1洗脱),分离纯化,制得白色粉末状产物134.6mg(约0.16mmol),熔点:216.5-218.2℃,该产物在搅拌、温度控制50℃以下缓慢添加36%hcl,至溶液ph值为7.0后停止添加盐酸并继续搅拌反应2h,在50℃下真空干燥6h,即得白色粉末状产物144.1mg(约0.16mmol),收率88.8%。产物分析表征:
1
h nmr(400mhz,cd
3
od)δ8.97(br,1h),8.78(br,1h),7.78(t,j=1.6hz,1h),7.69(d,j=8.0hz,1h),7.50(d,j=8.0hz,1h),7.37
–
7.15(m,3h),7.09(dd,j=8.1,2.5hz,1h),6.82
–
6.77(m,2h),6.65(dd,j=8.3,2.5hz,1h),6.37(d,j=7.2hz,2h),6.24(s,1h),6.16(dd,j=8.3,2.0hz,1h),3.82(d,j=9.4hz,3h),3.64(dd,j=11.1,5.4hz,1h),3.56(d,j=9.9hz,1h),3.44(s,3h),3.42
–
3.31(m,2h),3.19(s,3h),2.75
–
2.59(m,8h),2.57(s,3h),2.42(dd,j=30.0,9.4hz,2h),2.21(s,3h);
13
c nmr(101mhz,cd
3
od)δ154.79,151.98,150.28,149.72,148.63,148.14,143.31,140.27,137.64,136.08,135.53,133.71,132.41,131.19,129.55,129.35,129.00,128.24,125.01,123.87,123.48,122.79,121.63,117.28,113.83,112.49,107.24,72.13,71.82,69.16,67.70,49.85,48.59,47.16,46.04,40.66,23.35,21.02;hrms(esi):calcd for c
43
h
43
brn
2
o
8
s[m-2hcl]m/z:826.1923,found:827.1957[m-2hcl+h]
+
。即表1中的化合物70。
[0091]
实施例19
[0092]
将100.0mg防己诺林碱(约0.18mmol)溶于3ml的三氯甲烷中,加入充满氩气的两颈烧瓶中,并置于控温至0℃的冷井中,磁力搅拌下,加入γ-al
2
o
3-naoh-k 22.0mg,混合1h后,加入36.4mg(约0.20mmol)的2-噻吩磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用100:1,50:1洗脱),分离纯化,制得白色粉末状产物113.2mg(0.15mmol),熔点:202.7-204.5℃。该产物在搅拌、温度控制50℃以下缓慢添加36%hcl,至溶液ph值为7.0后停止添加盐酸并继续搅拌反应2h,在50℃下真空干燥6h,即得白色粉末状产物124.2mg(约0.15mmol),收率83.3%,目的产物熔点:244.5-247.4℃。产物分析表征:
1
h nmr(400mhz,cd
3
od)δ8.23(br,1h),7.93(br,1h),7.55(d,j=4.9hz,1h),7.37(d,j=3.8hz,1h),7.25(dd,j=8.1,1.7hz,1h),7.06(dd,j=8.1,2.4hz,1h),7.00
–
6.96(m,1h),6.77(d,j=8.0hz,2h),6.67(dd,j=8.2,2.4hz,1h),6.41(t,j=9.4hz,2h),6.27
–
6.16(m,2h),5.36(s,1h),3.82(d,j=9.1hz,3h),3.69
–
3.59(m,2h),3.42(d,j=11.3hz,3h),3.35(dd,j=27.5,17.6hz,2h),3.21(s,3h),2.67(ddd,5.8hz,8h),2.53(d,j=9.2hz,3h),2.48
–
2.30(m,2h),2.29
–
2.21(m,3h);
13
c nmr(101mhz,cd
3
od)δ154.75,151.98,150.35,150.16,149.98,148.84,148.11,143.38,138.01,136.17,135.64,134.67,133.66,131.28,129.56,128.97,128.92,128.06,124.80,123.84,122.80,122.25,117.07,113.65,112.50,106.86,75.54,74.02,72.80,71.17,65.07,62.38,50.23,49.57,43.32,42.95,41.34,23.17,21.07;hrms(esi):calcd for c
41
h
42
n
2
o
8
s
2
[m-2hcl]m/z:754.2383,found:755.2447[m-2hcl+h]
+
。即表1中的化合物90。
[0093]
实施例20
[0094]
将100.0mg防己诺林碱(约0.18mmol)溶于3ml的dmf溶剂中,加入充满氩气的两颈烧瓶中,并置于控温至5℃的冷井中,磁力搅拌下加入溶于2ml的dmf溶剂的三乙胺66.5mg(约0.72mmol),混合1h后,加入31.0mg(约0.27mmol)的甲基磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用120:1,60:1洗脱),分离纯化,制得白色粉末状产物109.9mg(约0.16mmol),熔点:208.3-209.9℃,该产物在搅拌、温度控制50℃以下缓慢添加60%丙酸,至溶液ph值为7.0后停止添加丙酸并继续搅拌反应2h,在50℃下真空干燥6h,即得白色粉末状产物121.7mg(约0.16mmol),收率88.9%,目的产物熔点:245.5-247.3℃。产物分析表征:
1
h nmr(400mhz,cd
3
od)δ8.27(br,1h),7.41(dd,j=8.2,1.9hz,1h),7.16(dd,j=8.2,2.5hz,1h),6.86(d,j=7.7hz,2h),6.82(dd,j=8.3,2.5hz,1h),6.57(s,1h),6.47(s,1h),6.41(s,1h),6.34(dd,j=8.3,2.0hz,1h),6.05(s,1h),3.93(s,3h),3.79(s,3h),3.71(dd,j=22.5,12.4hz,2h),3.42(dd,j=16.1,12.9hz,2h),3.42
–
3.36(m,3h),2.73(m,2h),2.30(tdd,j=18.0,13.2,6.7hz,6h),2.88(d,j=8.4hz,3h),2.82(dd,j=13.8,6.1hz,2h),2.70(d,j=9.0hz,3h),2.61
–
2.45(m,2h),2.31(s,3h),2.05(s,3h);
13
c nmr(101mhz,cd
3
od)δ173.35,153.06,149.14,148.27,147.94,147.68,146.05,141.48,133.37,132.64,131.66,129.53,126.65,126.10,124.35,122.41,121.99,121.31,121.06,120.92,114.89,111.34,110.55,105.15,69.39,65.38,62.02,61.81,55.11,52.85,51.90,42.78,41.30,40.84,40.38,38.54,38.13,34.27,22.40,21.30,21.13;hrms(esi):calcd for c
38
h
42
n
2
o
8
s[m-c
3
h
6
o
2
]m/z:686.2685,found:687.2735[m-c
3
h
6
o
2
+h]
+
。即表1中的化合物95。
[0095]
实施例21
[0096]
将100.0mg防己诺林碱(约0.18mmol)溶于3ml的dmso溶剂中,加入充满氩气的两颈烧瓶中,并置于控温至-5℃的冷井中,磁力搅拌下,加入γ-al
2
o
3-na 20.0mg,混合1h后,加入50.7mg(约0.20mmol)的3-溴苯磺酰氯反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用100:1,60:1洗脱),分离纯化,制得白色粉末状产物132.4mg(约0.16mmol),熔点:215.5-217.2℃,该产物在搅拌、温度控制60℃以下缓慢添加50%富马酸(提前用dmso溶剂溶解),至溶液ph值为7.0后停止添加富马酸并继续搅拌反应2h,在50℃下真空干燥6h,即得白色粉末状产物141.6mg(约0.15mmol),收率83.3%,目的产物熔点:244.5-247.4℃。产物分析表征:
1
h nmr(400mhz,cd
3
od)δ10.76(br,1h),8.01(br,1h),7.78(t,j=1.6hz,1h),7.69(d,j=8.0hz,1h),7.50(d,j=8.0hz,1h),7.37
–
7.16(m,3h),7.09(dd,j=8.1,2.5hz,1h),6.82
–
6.77(m,2h),6.65(dd,j=8.3,2.5hz,1h),6.37(d,j=7.2hz,2h),6.24(s,1h),6.16(dd,j=8.3,2.0hz,1h),5.91(d,j=8.77,1h),5.54(d,j=8.77,1h),3.82(d,j=9.4hz,3h),3.64(dd,j=11.1,5.4hz,1h),3.56(d,j=9.9hz,1h),3.44(s,3h),3.42
–
3.31(m,2h),3.19(s,3h),2.75
–
2.59(m,8h),2.57(s,3h),2.42(dd,j=30.0,9.4hz,2h),2.22(s,3h);
13
c nmr(101mhz,cd
3
od)δ179.05,172.87,154.90,151.99,150.29,149.73,148.64,148.15,143.42,140.28,137.65,136.09,135.54,133.82,132.52,131.20,129.58,129.35,129.01,128.25,125.01,123.88,123.49,122.90,121.64,117.29,113.84,112.60,107.25,67.37,66.65,64.77,62.51,61.14,60.83,57.17,56.05,53.83,52.50,40.67,23.37,22.03;hrms(esi):calcd for c
43
h
43
n
2
o
8
sbr[m-c
4
h
4
o
4
]m/z:826.1923found:827.1857[m-c
4
h
4
o
4
+h]
+
。即表1中的化合物117。
[0097]
实施例22
[0098]
将100.0mg防己诺林碱(约0.18mmol)溶于3ml的二氯甲烷中,加入充满氩气的两颈烧瓶中,并置于控温至0℃的冷井中,磁力搅拌下,加入溶于2ml的二氯甲烷的三乙胺66.5mg(约0.72mmol),混合1h后,加入35.4mg(约0.20mmol)的3-吡啶磺酰氯进行反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用100:1,50:1洗脱),分离纯化,制得白色粉末状产物112.3mg(约0.15mmol),熔点:207.1-208.7℃,该产物在搅拌、温度控制50℃以下缓慢添加60%醋酸,至溶液ph值为7.0后停止添加醋酸并继续搅拌反应2h,在50℃下真空干燥6h,即得白色粉末状产物1303.5mg(约0.15mmol),收率83.4%,目的产物熔点:247.7-249.3℃。产物分析表征:
1
h nmr(400mhz,cd
3
od)δ8.75(dd,j=10.1,3.3hz,2h),8.02(br,1h),7.82(d,j=8.1hz,1h),7.29(dd,j=8.0,3.5hz,2h),7.17(s,1h),7.08(dd,j=8.1,2.3hz,1h),6.77(s,2h),6.68(dd,j=8.2,2.3hz,1h),6.39(d,j=16.1hz,2h),6.25
–
6.17(m,2h),3.84(s,3h),3.73
–
3.60(m,2h),3.38(s,3h),3.35(s,3h),2.74
–
2.66(m,6h),2.62(d,j=12.2hz,2h),2.57(s,3h),2.47
–
2.35(m,2h),2.29(s,3h),2.23(s,3h);
13
c nmr(101mhz,cd
3
od)δ171.91,152.79,149.38,148.30,147.86,146.85,146.13,141.17,135.08,134.11,133.44,133.05,131.97,131.62,129.39,127.64,126.95,126.73,122.86,122.30,121.83,120.89,120.10,114.96,111.70,110.49,104.94,62.82,61.83,60.58,60.35,59.51,58.84,55.14,52.70,51.32,40.89,38.91,25.31,23.73,22.11;hrms(esi):calcd for c
42
h
43
n
3
o
8
s[m-2c
2
h
4
o
2
]m/z:749.2804,found:750.2852[m-2c
2
h
4
o
2
+h]
+
。即表1中的化合物137。
[0099]
实施例23
[0100]
将100.0mg防己诺林碱(约0.18mmol)溶于3ml的二氯甲烷中,加入充满氩气的两颈烧瓶中,并置于控温至10℃的冷井中,磁力搅拌下,加入溶于2ml的二氯甲烷的三乙胺66.5mg(约0.72mmol),混合1h后,加入45.2mg(约0.20mmol)的2-萘磺酰氯反应2h,之后加热至60℃反应,tlc追踪反应。反应结束后,将反应液浓缩,过中性氧化铝柱提纯,洗脱剂为二氯甲烷:甲醇(分别采用120:1,80:1洗脱),分离纯化,制得淡黄色粉末状产物118.0mg(约0.148mmol),收率82.2%。产物分析表征:
1
h nmr(400mhz,cdcl
3
)δ8.20(s,1h),8.02
–
7.75(m,4h),7.69(t,j=7.5hz,1h),7.56(dd,j=15.4,8.1hz,2h),6.85
–
6.73(m,3h),6.61(d,j=7.4hz,1h),6.54(dd,j=8.2,2.1hz,1h),6.30(d,j=23.5hz,2h),6.21(s,1h),6.03(d,j=8.2hz,1h),4.40(s,1h),3.84(s,3h),3.53(d,j=10.0hz,1h),3.45(d,j=10.1hz,3h),3.33(ddd,j=21.6,20.7,10.6hz,2h),3.19(d,j=14.4hz,3h),2.94
–
2.68(m,6h),2.53(s,3h),2.51
–
2.31(m,4h),2.20(d,j=12.1hz,3h);
13
c nmr(101mhz,cdcl
3
)δ153.47,151.48,149.29,148.57,147.57,147.12,142.42,135.28,134.63,134.59,134.47,132.42,131.87,129.97,129.52,128.73,128.08,127.79,127.59,123.85,122.83,121.50,120.04,115.89,112.84,111.47,106.42,63.42,61.42,56.12,56.59,55.77,44.96,43.91,42.41,42.32,42.23,39.05,24.34,22.05;hrms(esi):calcd for c
47
h
46
n
2
o
8
s m/z:798.2975,found:799.3029[m+h]
+
。即表1中的化合物138。
[0101]
其他化合物可以通过与以上实施例类似的制备方法(包括提纯方法)获得。
[0102]
实施例24体外抑制xod活性实验
[0103]
首先制备磷酸盐缓冲液(pbs,10mm,ph=7.4),xod(92u/l)和黄嘌呤(0.5mm),然后在4℃下保存以备后用。接下来,准确称取化合物1~140,并且将母液浓度配制为200μm,进一步将待测试化合物用pbs稀释至不同浓度(50、25、12.5、6.25、3.125、1.5625μm)。同时设置空白对照和阳性对照,分别用pbs和别嘌醇(广州康和药业有限公司)代替测试化合物。反应在每孔包含200μl反应混合物的96孔微孔板中进行,每个浓度设置3次重复。首先,将100μl不同浓度的测试化合物与50μl xod(上海源叶生物科技有限公司)混合,并在37℃恒温箱平衡5min,然后加入50μl的黄嘌呤(上海源叶生物科技有限公司)引发反应,并将反应在37℃恒温箱温育30min。反应结束后,通过酶标仪测量每个孔的od值,并使用microsoft excel 2013分析数据,根据抑制率(%)计算空白组和试验化合物组的od值变化,并且使用graphpad prism 7.0计算ic
50
值,以评估测试化合物的xod抑制活性。
[0104]
计算公式:抑制率(%)=(od
blank-od
compound
)/od
blank
×
100%
[0105]
od
blank
表示空白组的od值,od
compound
表示待测化合物组的od值。
[0106]
体外抑制xod活性实验结果汇总与表2。
[0107]
表2磺酰基防己诺林碱类化合物抑制xod活性ic
50
值
[0108]
[0109][0110]
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修
改、等同替换、改进等,均应包含在本发明的保护范围之内。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 


