一种用于病原微生物检测体液标本的保存剂及其应用的制作方法
 2021-02-02 11:02:56|
2021-02-02 11:02:56| 293|
293| 起点商标网
起点商标网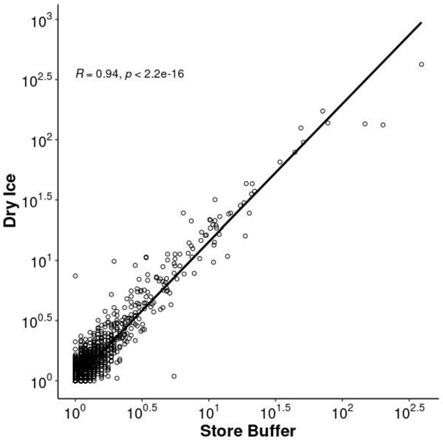
[0001]
本申请涉及病原微生物检测领域,特别是涉及一种用于病原微生物检测体液标本的保存剂及其应用。
背景技术:
[0002]
在病原微生物检测中,标本包含脑脊液、血液、痰液、肺泡灌洗液、尿液、脓液等其它体液,即病原微生物检测体液标本。一般来说,标本距离检测实验室或者检测中心通常有一定的距离,尤其是外送检测类标本,通常因为标本运输、实验安排等原因都需要经过一段时间之后才能开始后续的检测。待检的标本在常温条件下所含微生物或继续生长,或死亡,遗传物质核酸发生降解,多种方式均可导致标本中的微生物发生变化;从而影响检测结果的准确性和有效性。病原微生物检测需要的是能尽可能真实的反应原始标本中的微生物组成;因此,为了避免标本中的微生物发生变化,原则上标本不能长时间简单置于常温条件下,最好不超过30分钟。
[0003]
然而,实际操作中,病原微生物检测标本采集后,需要不同距离的运输等各种原因,不能立刻进行后续试验。因此,目前比较常规的作法是,第一,将标本保存于干冰环境中进行运输,以保证微生物组成的稳定性;第二,对标本进行预处理,例如预先对标本进行核酸提取,然后采用可反复使用的冰袋进行低温运输。
[0004]
其中,基于干冰保存和运输的方法,虽然可以较好的保障微生物的稳定性;但是,标本运输成本较高。单一份的病原微生物待检测标本原本重量≤20g,体积≤50ml;干冰运输的操作方式一般是将标本放置在装有干冰的泡沫盒中,干冰在常温下属于易挥发物质,通常按照运输所需时间长短来预备干冰数量,一般是3公斤左右/天。受地理位置和交通的影响,通常至少准备24~48小时干冰的量来寄送标本,这极大的增加了标本运输的综合成本。
[0005]
基于标本预处理的方法,其运输虽然只需要采用冰袋进行低温运输即可;但是,标本预处理对标本取样和处理环境以及操作人员的要求都很高。病原微生物检测标本取出后需要立刻进行核酸的提取,需要在无污染的分子实验室进行,操作人员必须掌握相应的分子实验知识和技术才能有效的对标本进行核酸提取。尤其待检标本中可能包含rna病毒等需要经过复杂的前处理才能变成稳定的核酸。相对于在中心实验室或者检测中心统一进行核酸提取而言,分散在不同地方的预处理能会对检测标本造成更多的人为偏差,最终影响病原微生物检测结果的准确性。
技术实现要素:
[0006]
本申请的目的是针对干冰保存和运输病原微生物检测体液标本综合成本高的问题,提供一种新的用于病原微生物检测体液标本的保存剂及其应用。
[0007]
本申请采用了以下技术方案:
[0008]
本申请的一方面公开了一种用于病原微生物检测体液标本的保存剂,其包括重量
百分比60~80%的超纯无菌水、0.5~3%的核酸酶抑制剂、1~5%的代谢抑制剂、10~25%的防腐剂和5~8%的抗凝剂。
[0009]
需要说明的是,本申请的保存剂可以在常温下较长时间的保障病原微生物检测体液标本中的微生物细胞和核酸的稳定性;本申请的一种实现方案中,微生物组成常温条件下维持稳定的时间可达7天,最多可至12天;能够很好的满足长途运输的使用需求。实践证实,添加本申请的保存剂后,病原微生物检测标本常温运输72小时,甚至96小时,其中的微生物组成不发生明显变化。采用本申请的保存剂对病原微生物检测体液标本进行保存,只需要将采集的标本与保存剂在采样管中混合即可,使用简单方便;这种方法不需要复杂的标本预处理,降低了对标本取样地点及操作人员的要求;也不需要添加相对昂贵且沉重的干冰来运输,极大的降低了标本运输的综合成本;并且,更为重要的是,本申请的保存液能够很好的保障微生物细胞和核酸的稳定性,从而确保了最终的病原微生物检测结果的准确性和可信度。
[0010]
优选的,抗凝剂为edta钾盐、edta钠盐、柠檬酸钠、肝素和枸杞酸钠中的至少一种。
[0011]
优选的,防腐剂为二唑烷基脲、咪唑烷基脲、1,3-二氯-5,5-二甲基乙内酰脲(以下简称“二氯海因”)、钠羟甲基甘氨酸、二羟甲基脲、2-溴-2-硝基-1,3-二醇(以下简称“溴硝醇”)、恶唑烷、钠羟甲基甘氨酸和金刚烷季铵中的至少一种。
[0012]
优选的,代谢抑制剂为ata、甘油醛、磷酸二羟丙酮、甘油醛-3-磷酸、3-磷酸-2-磷酸甘油酸、磷酸、丙酮酸、氟化钠和钾代谢抑制剂中的至少一种。
[0013]
优选的,核酸酶抑制剂为硫酸铵、二硫苏糖醇、β-巯基乙醇、半胱氨酸、二硫赤藓醇和二价阳离子中的至少一种。
[0014]
优选的,二价阳离子为mg
2+
、mn
2+
、zn
2+
、fe
2+
、ca
2+
和cu
2+
中的至少一种。
[0015]
本申请的另一面公开了本申请的保存剂在制备标本采样装置中的应用。
[0016]
本申请的再一面公开了一种体液标本采样管,该体液标本采样管内具有本申请的保存剂。
[0017]
需要说明的是,本申请的体液标本采样管在使用之前,都是采用密封盖封存,保存液可以在体液标本采样管中长时间常温放置,或者也可以将体液标本采样管保存于-4℃的低温环境。使用时,直接开启密封盖,将标本放入采样管中,简单的颠倒摇晃混匀标本和保存剂即可。
[0018]
优选的,体液标本采样管还具有密封盖,在首次开启之前,密封盖将本申请的保存剂密封保存在体液标本采样管内。
[0019]
优选的,保存剂在真空环境或者无菌的保护气氛环境下封存于体液标本采样管内。
[0020]
本发明的有益效果在于:
[0021]
本发明提供的保存剂及其在制备标本采样装置中的应用,可以保证病原微生物标本中的微生物细胞和核酸在常温下长期保持稳定,从而使得病原微生物检测标本无需进行核酸提取等预处理即可在常温运输,无需采用干冰,大大降低了病原微生物检测标本的运输成本,而且为病原微生物检测能够尽可能真实的反应原始标本中的微生物组成奠定了基础,提高了病原微生物检测结果的准确性。
附图说明
[0022]
图1是本申请实施例中肺泡灌洗液标本干冰运输和保存剂检测出微生物组成的对比结果,其中,纵坐标“dry ice”即干冰运输的标本的检测结果,横坐标“store buffer”即保存剂运输的标本的检测结果;
[0023]
图2是本申请实施例中脑脊液标本干冰运输和保存剂检测出微生物组成的对比结果,其中,纵坐标“dry ice”即干冰运输的标本的检测结果,横坐标“store buffer”即保存剂运输的标本的检测结果。
具体实施方式
[0024]
下面通过具体实施例结合附图对本申请进行详细说明。以下实施例仅用于对本申请进行说明,不应理解为对本申请的限制。
[0025]
实施例
[0026]
本例用于病原微生物检测体液标本的保存剂,由重量百分比60~80%的超纯无菌水、0.5~3%的核酸酶抑制剂、1~5%的代谢抑制剂、10~25%的防腐剂和5~8%的抗凝剂组成。其中,抗凝剂为edta钾盐、edta钠盐、柠檬酸钠、肝素或枸杞酸钠;防腐剂为二唑烷基脲、咪唑烷基脲、1,3-二氯-5,5-二甲基乙内酰脲、钠羟甲基甘氨酸、二羟甲基脲、2-溴-2-硝基-1,3-二醇、恶唑烷、钠羟甲基甘氨酸或金刚烷季铵;代谢抑制剂为ata、甘油醛、磷酸二羟丙酮、甘油醛-3-磷酸、3-磷酸-2-磷酸甘油酸、磷酸、丙酮酸、氟化钠或钾代谢抑制剂;核酸酶抑制剂为硫酸铵、二硫苏糖醇、β-巯基乙醇、半胱氨酸、二硫赤藓醇或二价阳离子。
[0027]
保存剂的制备方法,主要包括,在无菌操作台上,按照以上配比称取各组分,然后,将各组分溶于超纯无菌水中即可。
[0028]
本例按照以上配比具体制备了不同核酸酶抑制剂、不同代谢抑制剂、不同防腐剂和不同抗凝剂的保存剂,详细配方如表1所示。
[0029]
表1保存剂配方
[0030]
编号核酸酶抑制剂代谢抑制剂防腐剂抗凝剂试验1硫酸铵1%甘油醛1%二唑烷基脲15%edta钾盐5%试验2硫酸铵2%甘油醛3%二唑烷基脲20%edta钾盐6%试验3硫酸铵0.5%甘油醛5%二唑烷基脲10%edta钾盐7%试验4硫酸铵3%甘油醛4%二唑烷基脲25%edta钾盐8%试验5二硫苏糖醇2%甘油醛3%二唑烷基脲20%edta钾盐6%试验6β-巯基乙醇2%ata 3%咪唑烷基脲20%edta钠盐6%试验7半胱氨酸2%磷酸二羟丙酮3%二氯海因20%柠檬酸钠6%试验8二硫赤藓醇2%甘油醛-3-磷酸3%钠羟甲基甘氨酸20%肝素6%试验9二价阳离子mgcl
2 2%3-磷酸-2-磷酸甘油酸3%二羟甲基脲20%枸杞酸钠6%试验10硫酸铵1%磷酸3%溴硝醇20%edta钾盐5%试验11硫酸铵1%丙酮酸3%恶唑烷20%edta钾盐5%试验12硫酸铵1%氟化钠3%钠羟甲基甘氨酸20%edta钾盐5%试验13硫酸铵1%钾代谢抑制剂3%金刚烷季铵20%edta钾盐5%
[0031]
表1中,各组分的百分比均为重量百分比,余量为超纯无菌水。
[0032]
本例按照表1的配方配制了十三种保存剂,在无菌操作台上,将十三种保存剂各取100μl,分别放入不同的标本采样管内。然后将新鲜采集的肺泡灌洗液各500μl放入装有保
存剂的标本采样管内;其中,肺泡灌洗液是利用支气管镜向人支气管肺泡内注人生理盐水并随即吸出,收集肺泡表面有效液体,即肺泡灌洗液,后续试验使用的脑脊液由腰椎穿刺采集得到;密封后上下颠倒15次,混匀标本和保存剂,然后室温(空调室内温度约25℃)放置保存,每间隔1天取10μl标本和保存剂的混合液进行微生物检测,本例采用的是高通量测序检测微生物。具体的,核酸提取采用凯杰微生物dna提取试剂盒(qiaamp dna micro kit),按试剂盒说明书提取步骤进行核酸取核酸后,利用bgiseq-50进行高通量测序。
[0033]
对高通量测序得到的测序数据,按照如下步骤处理后得到微生物组成:1、低质量数据过滤;2、去除宿主dna数据;3、利用bwa比对微生物参考基因组库,包括jgi下的img数据库,ncbi的genbank等微生物基因组构建的参考数据库;4、计算比对结果中,每种微生物的组成,综合考虑微生物相对组成。
[0034]
结果显示,十三种保存液都能够在室温下长期保存标本中的微生物,微生物组成在7天内保持稳定,没有显著变化,这种稳定性最多可以持续至12天。特别是edta钾盐5~6%、防腐剂15~20%、代谢抑制剂1~3%、核酸酶抑制剂1~2%,余量为超纯无菌水的保存剂,可以持续12天保持标本中的微生物稳定。以上结果说明,本例的保存液能够在25℃室温下长期保障液体标本中的微生物稳定性,为后续微生物检测奠定了基础。
[0035]
另外,对于二价阳离子型的核酸酶抑制剂,除表1采用的mgcl
2
以外,其它类似的mn
2+
、zn
2+
、fe
2+
、ca
2+
和cu
2+
二价阳离子都可以用于本例,其效果与mg
2+
相当。
[0036]
在以上试验的基础上,本例进一步对干冰保存和运输相同的标本进行了对比试验,具体如下:
[0037]
将本例试验2的保存剂分别装入两个标本采样管内,每管装入保存剂200μl;另外去两个空的标本采样管;分别取相同的肺泡灌洗液1ml装入含有保存剂的标本采样管和空标本采样管中;分别取相同的脑脊液1ml装入含有保存剂的标本采样管和空标本采样管中;其中,空标本采样管放置的标本密封后放在盛有5公斤干冰的紧密泡沫箱内运输;考虑到运输车厢内的温度可能较高,本例将与保存液混合的标本放置于添加冰袋的泡沫箱中运输,其温度约为4℃~20℃。四个标本在运输36小时后抵达检测中心,经由相同的标准高通量测序技术检测其中的微生物组成。
[0038]
根据高通量测序结果,按照其对应物种的丰都进行标准化处理后,分别计算同一份标本在常温保存剂与干冰保存下物种组成一致性,利用pearson相关系数来评估两种条件下结果是否一致,其中pearson相关系数越接近1,说明两种方法差异越小,同时检验结果中计算出p值,p值越小,说明两个样品之间的线性相关性越好,一般p值<0.05才说明检验结果可信。
[0039]
结果如表2和图1、图2所示,表2为采用保存剂的标本与干冰运输的标本的一致性对比结果,图1为肺泡灌洗液标本干冰运输(dry ice)和保存剂(store buffer)检测出微生物组成的对比结果,图2为脑脊液标本干冰运输(dry ice)和保存剂(store buffer)检测出微生物组成的对比结果。
[0040]
表2保存剂运输标本与干冰运输标本的一致性比对结果
[0041][0042]
表2、图1和图2的结果显示,不论是脑脊液标本还是肺泡灌洗液标本,将标本放入预置本例保存剂的标本管中置于常温或者将标本放入标本管置于干冰中,36小时结果一致性极好。说明保存剂的运输方案可以替代干冰环境的运输方案,这可以极大的降低运输成本。
[0043]
以上内容是结合具体实施方式对本申请所作的详细说明,不能认定本申请的实现方式只局限于这些说明。对于本申请技术领域的普通技术人员来说,在不脱离本申请基本发明构思的前提下,还可以进行若干简单推演或替换。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



