一种两步法制备大麻素的方法与流程
 2021-02-02 04:02:35|
2021-02-02 04:02:35| 411|
411| 起点商标网
起点商标网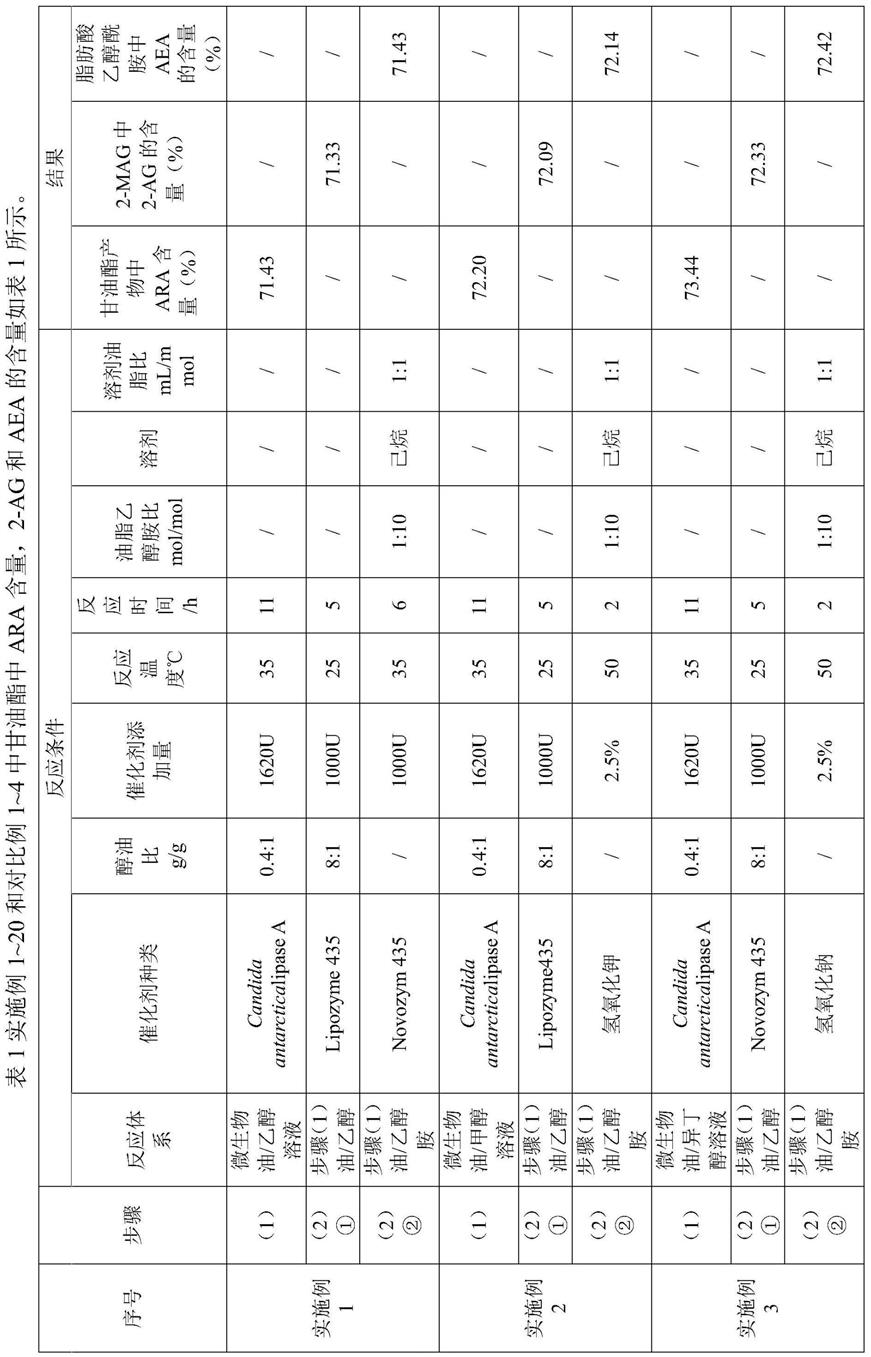
[0001]
本发明涉及一种两步法制备大麻素的方法,属于油脂深加工领域。
背景技术:
[0002]
内源性大麻素系统(ecs)在调节许多基本生物学功能中扮演着重要的角色,其中包括:睡眠与清醒的周期、食欲、情绪、记忆、生育力、孕后幼胎发育等。在人类和其他脊椎动物中,ecs由两个主要的大麻素受体组成,此外还有许多修饰主要受体作用的次要受体。大麻素受体依赖于人体产生的化学信号,称为内源性大麻素。两种最重要的内源性大麻素是花生四烯酸乙醇酰胺(anandamide,aea)和2-花生四烯酸单甘酯(2-arachidonoylglycerol,2-ag)。这些内源性大麻素在中枢神经系统的神经元(神经)细胞的突触中产生,并响应各种生物信号而释放。
[0003]
花生四烯乙醇胺和2-花生四烯酸单甘酯作为两种重要的内源性脂质信号调节分子,在动物组织中的含量较低、结构不稳定,并且难于实现大量提取获得。化学法虽然易于操作和控制,但多使用有毒的催化剂且催化剂选择性低,反应温度高,产品后处理复杂,食品级优势并不明显。采用酶法制备aea和2-ag,可克服传统化学法催化剂选择性低、反应温度高、产品后处理复杂等缺陷。
[0004]
反应底物花生四烯酸(ara)或其衍生物的纯度是影响产品aea和2-ag品质的关键,目前酶法合成内源性大麻素多为一步法,存在的问题是如果使用ara含量低的原料,虽然成本低,但是合成目标物的得率低,产物中内源性大麻素的含量低,后期纯化困难,难以得到高纯度的2-ag和aea,影响产品的使用效果和商业价值;如果使用市售高纯度的ara或其衍生物标品,其原料价格比较昂贵,成本高。
[0005]
因此,本领域亟需一种目标产物纯度高且成本低的大麻素制备方法。
技术实现要素:
[0006]
鉴于上述和/或现有酶法制备大麻素的方法中存在的问题提出了本发明。
[0007]
为解决上述技术问题,本发明提供了如下技术方案:一种两步法制备大麻素的方法,包括:
[0008]
(1)取含有花生四烯酸(ara)的油脂、脂肪酶和醇于反应器中,反应一段时间,脱除脂肪酸酯和/或游离脂肪酸,得到富含花生四烯酸的甘油酯;其中,所述脂肪酶包括来源于南极假丝酵母(candida antarctica)的candida antarcticalipase a和曲霉(aspergilus sp.)的novozymet2.0一种或多种;
[0009]
(2)取步骤(1)制备得到的富含花生四烯酸的甘油酯,
[0010]
①
与乙醇按质量比1:1~10混合,加入脂肪酶,在一定温度下进行醇解反应,得到大麻素2-花生四烯酸单甘酯;其中,所述脂肪酶包括来源于南极假丝酵母candida antarctica的novozym 435和lipozyme 435
[0011]
②
与乙醇胺按摩尔比按一定摩尔比在溶剂体系或无溶剂体系下混合充分后,加入
催化剂,在一定的温度下反应后,得到大麻素花生四烯酸乙醇酰胺。
[0012]
作为本发明所述两步法制备大麻素的方法的一种优选方案,其中:所述含有花生四烯酸(ara)的油脂,包括含有花生四烯酸(ara)的藻油、植物油、鱼油和微生物油脂中一种或多种。
[0013]
作为本发明所述两步法制备大麻素的方法的一种优选方案,其中:步骤(2)
②
中所述催化剂包括来源于南极假丝酵母candida antarctica的novozym 435和lipozyme 435、甲醇钠、甲醇钾、氢氧化钠、氢氧化钾中的一种或者多种。
[0014]
作为本发明所述两步法制备大麻素的方法的一种优选方案,其中:步骤(1)中所述反应的体系中还包含水。
[0015]
作为本发明所述两步法制备大麻素的方法的一种优选方案,其中:步骤(1)中所述醇为甲醇、乙醇和异丁醇中的一种或几种;所述醇的浓度为10%~90%,溶剂为水。
[0016]
作为本发明所述两步法制备大麻素的方法的一种优选方案,其中:步骤(1)中所述醇和含有花生四烯酸的油脂的质量比为(0.1~7):1,优选(0.1~2):1。
[0017]
作为本发明所述两步法制备大麻素的方法的一种优选方案,其中:步骤(1)中所述时间为1~48h,优选4~48h,反应温度为20~60℃。
[0018]
作为本发明所述两步法制备大麻素的方法的一种优选方案,其中:步骤(1)中所述脂肪酶的添加量为每克含有花生四烯酸的油脂添加10~10000u脂肪酶,优选每克含有花生四烯酸的油脂添加20~2000u脂肪酶。
[0019]
作为本发明所述两步法制备大麻素的方法的一种优选方案,其中:步骤(2)
①
中所述反应时间为0.5~15h,反应温度为10~50℃;所述脂肪酶的添加量为每克富含花生四烯酸的单甘酯添加10~10000u脂肪酶,优选每克富含花生四烯酸的甘油酯添加20~2000u脂肪酶。
[0020]
作为本发明所述两步法制备大麻素的方法的一种优选方案,其中:步骤(2)
②
中,所述富含花生四烯酸的甘油酯与乙醇胺按摩尔比为1:(1~30),所述溶剂包括己烷、醚类溶剂和乙醇中的一种或几种。
[0021]
作为本发明所述两步法制备大麻素的方法的一种优选方案,其中步骤(2)
②
中所述有机溶剂体积和富含花生四烯酸的甘油酯的比例以ml:mmol计为(0~5):1。
[0022]
作为本发明所述两步法制备大麻素的方法的一种优选方案,其中:步骤(2)
②
中所述反应时间为0.5~12h,反应温度为20~70℃。
[0023]
作为本发明所述两步法制备大麻素的方法的一种优选方案,其中:步骤(2)
②
中所述脂肪酶的添加量为每克富含花生四烯酸的甘油酯添加10~10000u脂肪酶,所述化学催化剂的添加量为油脂质量的0.5~5.0%。
[0024]
本发明有益效果:
[0025]
(1)本发明提供一种制备大麻素的方法,即两步法制备2-ag和aea,第一步采用酶法醇解富集油脂中的ara,得到富含ara的油脂,第二步直接将富含ara的油脂作为原料,分别催化合成制备2-ag和aea,与一步法相比,两步法制备产物中2-ag和aea的含量更高。
[0026]
(2)本发明选用的candida antarctica lipase a和novozymet2.0脂肪酶在醇解体系中具有较强的活性,对pufas也具有较强的“歧视性”,利用此特性实现在醇体系中富集ara,这样高浓度ara的原料直接通过醇解法富集获取,价格低廉,成本低。
具体实施方式
[0027]
(1)ara含量的测定方法
[0028]
取50mg样品于10ml刻度管,加入2ml 0.5mol/l的氢氧化钾-甲醇溶液,65℃皂化30min,冷却后加入2ml 25%体积分数的三氟化硼-甲醇溶液,70℃水浴5min;加入2ml正己烷振荡3-4min提取脂肪酸甲酯,加入4ml饱和nacl溶液,取上层溶液加入无水硫酸钠振荡(10000rpm离心5min),注射器吸取过膜,利用气相色谱进行检测,其中,气相色谱检测的操作参数为:选用7890气相色谱仪,火焰离子化检测器(fid);气相色谱柱为60m
×
0.32mm
×
2.5μm;氮气流速设定为1.0ml/min,进样器和检测器的温度设置为250℃。初始柱温保持在80℃下0.5min,然后以40℃/min的速率从80℃增加到165℃。以4℃/min的速率将柱温升高至230℃,并在230℃下保持4min。利用峰面积归一法计算ara含量。
[0029]
(2)醇解反应的产物的分析方法
[0030]
采用waters 1525高效液相色谱仪分析(hplc)样品中的脂质组成,得到反应产物中的sn-2-mag含量。取醇解后的混合产物20mg,加入1ml流动相(正己烷:异丙醇:甲酸=15:1:0.003)溶解,过膜,液相色谱检测,液相色谱操作参数为:hplc,sepax hp硅胶柱(孔径5μm,4.6mm
×
250mm)示差检测器;以1.0ml/min的速率用己烷、异丙醇和甲酸(15:1:0.003,v/v/v)洗脱。
[0031]
(3)花生四烯酸乙醇酰胺的分析方法
[0032]
采用trace isq气相色谱-质谱联用仪分析反应产物中aea的含量。样品衍生化处理操作如下:将约5mg脱水反应产物加入到2ml的玻璃样品瓶内,用600μl的吡啶溶解后加入200μl的硅烷化试剂(hmds+tmcs+pyridine,3:1:9),将混合溶液旋涡振荡30s后于室温下反应30min,过0.22μm有机滤膜后用于gc-ms待测。
[0033]
gc检测条件为:色谱柱:db-5柱(30m
×
0.25mm
×
0.25μm);检测器:fid;进样口和检测器的温度分别为250℃和300℃,进样量为1μl。分流比为20:1。
[0034]
升温程序为:初始温度180℃保持0.5min,以3℃/min升温至250℃并保持11min,总分析时间约为34.8min。采用面积归一法进行定量分析。
[0035]
ms检测条件为:离子源温度设为220℃,传输线温度设为250℃,离子化方式设为ei,电子能量为70ev,扫描时间2.0~35.50min,质谱定性采用扫描方式,分子离子碎片扫描范围为m/z 50~550。
[0036]
为使本发明的上述目的、特征和优点能够更加明显易懂,下面结合说明书实施例对本发明的具体实施方式做详细的说明。
[0037]
在下面的描述中阐述了很多具体细节以便于充分理解本发明,但是本发明还可以采用其他不同于在此描述的其它方式来实施,本领域技术人员可以在不违背本发明内涵的情况下做类似推广,因此本发明不受下面公开的具体实施例的限制。
[0038]
其次,此处所称的“一个实施例”或“实施例”是指可包含于本发明至少一个实现方式中的特定特征、结构或特性。在本说明书中不同地方出现的“在一个实施例中”并非均指同一个实施例,也不是单独的或选择性的与其他实施例互相排斥的实施例。
[0039]
本发明中脂肪酶candida antarctica lipase a(6000u/g)、novozymet2.0(1000u/g)、lipozyme 435(10000u/g)、novozym 435(10000u/g)购自诺维信生物技术有限公司。
[0040]
本发明中所用油脂均为市售,其中富含ara的m.alpina微生物油脂中ara含量是43.12%;富含ara藻油中ara含量为48.72%。其他试剂无特殊说明,均为市售。
[0041]
实施例1
[0042]
(1)准确称取ara微生物油脂(ara含量为43.12%)3.0g、无水乙醇1.2g(醇油质量比0.4:1)、4.8g水和candida antarctica lipase a脂肪酶1620u,加入到反应釜中,放入磁力转子,封口。将反应釜放在磁力搅拌器上,反应釜接入循环水,水温为恒温35℃,保持11h。反应结束后,除去混合物中的脂肪酸酯和游离脂肪酸,得到富含ara的甘油酯。甘油酯产品的脂肪酸组成中,ara含量如表1所示。
[0043]
(2)取得到的富含花生四烯酸的甘油酯,分别:
[0044]
①
取上述第一步得到的富含ara微生物油脂(ara含量为71.43%)1.0g,加入无水乙醇8g(醇油质量比8:1)和lipozyme 435脂肪酶1000u加入到反应釜中,放入磁力转子,封口。将反应釜放在磁力搅拌器上,反应釜接入循环水,水温为恒温25℃,保持5h。反应结束后,纯化得到富含2-ag的2-mag产物,经hplc和gc分析,2-mag中2-ag的含量如表1所示。
[0045]
②
取上述第一步得到的富含ara微生物油脂(ara含量为71.43%)1.0mmol,加入乙醇胺10mmol(油脂和乙醇胺摩尔比为1:10)、己烷1ml(溶剂和油脂比(ml/mmol)1:1)和novozym 435脂肪酶1000u加入到反应釜中,放入磁力转子,封口。将反应釜放在磁力搅拌器上,反应釜接入循环水,水温为恒温35℃,保持6h。反应结束后,纯化得到富含aea的脂肪酸乙醇胺,经气相色谱-质谱联用仪分析,脂肪酸乙醇酰胺中aea的含量如表1所示。
[0046]
实施例2
[0047]
同实施例1,但是改变第(1)步反应体系中醇种类为甲醇;改变第(2)
②
步反应体系中催化剂种类为氢氧化钾,添加量为油脂质量的2.5%,温度改为50℃,反应时间为2h,其余操作相同,所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0048]
实施例3
[0049]
同实施例1,但是改变第(1)步反应体系中醇种类为异丁醇,改变第(2)
①
步反应体系中脂肪酶种类为novozym 435,添加量为1000u;改变第(2)
②
步反应体系中催化剂种类为氢氧化钠,添加量为油脂质量的2.5%,温度改为50℃,反应时间为2h,其余操作相同,所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0050]
实施例4
[0051]
同实施例1,但是改变第(1)步反应体系中脂肪酶种类为novozymet2.0,添加量为1620u,改变第(2)
②
步反应体系中催化剂种类为甲醇钠,添加量为油脂质量的2.5%,温度改为50℃,反应时间为2h,其余操作相同,所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0052]
实施例5
[0053]
同实施例4,但是改变第(1)步反应体系中醇种类为甲醇,改变第(2)
②
步反应体系中催化剂添加量为油脂质量的4%,其余操作相同,所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0054]
实施例6
[0055]
同实施例1,但是改变第(1)步反应体系中的醇添加质量为12g,其余操作相同,所
得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0056]
实施例7
[0057]
同实施例1,但是改变第(1)步反应体系中的醇添加质量为0.3g其余操作相同,所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0058]
实施例8
[0059]
同实施例1,但是改变第(1)步反应体系中油脂种类为藻油,其余操作相同,所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0060]
实施例9
[0061]
同实施例1,但是改变第(1)步反应体系中脂肪酶添加量为60u,改变第(2)
①
步反应体系中脂肪酶种类为novozym 435,添加量为1000u,改变第(2)
②
步反应体系中催化剂种类为甲醇钠,添加量为油脂质量的2.5%,反应时间为2h,其余操作相同,所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0062]
实施例10
[0063]
同实施例9,但是改变第(1)步反应体系中脂肪酶添加量为3600u,改变第(2)
①
步反应体系中脂肪酶种类为lipozyme 435,添加量为1000u,改变第(2)
②
步反应体系中溶剂为乙醚,其余操作相同,所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0064]
实施例11
[0065]
同实施例9,但是改变第(1)步反应体系中反应温度为20℃,改变第(2)
②
步反应体系中溶剂为己烷和乙醇混合物(二者体积比为1:1),其余操作相同,所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0066]
实施例12
[0067]
同实施例9,但是改变第(1)步反应体系中反应温度为50℃,改变第(2)
②
步反应体系中溶剂油比(ml/mol)为0:1(减少溶剂),改变反应体系中油脂和乙醇胺摩尔比为1:3(减少乙醇胺用量)其余操作相同,所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0068]
实施例13
[0069]
同实施例9,但是改变第(1)步反应体系中反应时间为4h,改变第(2)
②
步反应体系中溶剂油比(ml/mol)为0.5:1(减少溶剂),所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0070]
实施例14
[0071]
同实施例9,但是改变第(1)步反应体系中反应时间为48h,改变第(2)
②
步反应体系中溶剂油比(ml/mol)为4:1(增加溶剂),所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0072]
实施例15
[0073]
同实施例1,改变第(2)
②
步反应体系中催化剂种类为lipozyme 435,添加量为1000u,其余操作相同,所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0074]
实施例16
lipase脂肪酶1620u,加入到反应釜中,放入磁力转子,封口。将反应釜放在磁力搅拌器上,反应釜接入循环水,水温为恒温35℃,保持11h。反应结束后,用koh-乙醇水溶液脱去水解掉的游离脂肪酸,之后3次水洗,取上层澄清油相,蒸去溶剂得到富含ara的微生物油甘油酯。甘油酯产品的脂肪酸组成中,ara含量如表1所示。
[0091]
(2)取得到的富含花生四烯酸的甘油酯,分别:
[0092]
①
取上述第一步得到的ara微生物油脂1.0g,加入无水乙醇8g(醇油质量比8:1)和lipozyme 435脂肪酶1000u,加入到反应釜中,放入磁力转子,封口。将反应釜放在磁力搅拌器上,反应釜接入循环水,水温为恒温25℃,保持5h。反应结束后,纯化得到富含2-ag的2-mag产物,经hplc和gc分析,2-mag中2-ag的含量如表1所示。
[0093]
②
取上述第一步得到的ara微生物油脂1.0mmol,加入乙醇胺10mmol(油脂和乙醇胺摩尔比为1:10)、己烷1ml(溶剂油比(ml/mmol)1:1)和novozym 435脂肪酶1000u,加入到反应釜中,放入磁力转子,封口。将反应釜放在磁力搅拌器上,反应釜接入循环水,水温为恒温35℃,保持6h。反应结束后,纯化得到富含aea的脂肪酸乙醇酰胺,经气相色谱-质谱联用仪分析,脂肪酸乙醇酰胺中aea的含量如表1所示。
[0094]
对比例3
[0095]
同对比例2,但是改变第反应体系中脂肪酶种类为novozymet2.0,添加量为1620u,其余操作相同,其余操作相同,所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0096]
对比例4
[0097]
同对比例1,但是改变第反应体系中油脂种类为为藻油,其余操作相同,所得甘油酯中ara含量,2-mag中2-ag的含量和脂肪酸乙醇酰胺中aea的含量如表1所示。
[0098]
[0099]
[0100]
[0101]
[0102]
[0103][0104]
由表1可知,通过实施例1~3和对比例2相比,当脂肪酶为candida antarctica lipase a时,本发明的醇解体系使得藻油甘油酯产物ara含量由43.12%可以提高到70%以
上,优于水解体系的60.20%,富集效果更优。通过实施例4~5和对比例3相比,当脂肪酶为novozymet2.0时,本发明的醇解体系使得藻油甘油酯产物ara含量由43.12%可以提高到65%以上,明显优于水解体系的53.41%。
[0105]
通过实施例1和对比例1,实施例8和对比例4相比较说明lipozyme 435在甲醇体系下不能产生富集效果。实施例1中ara含量富集到70%以上,对比例1中ara含量没有增加,结果是2-ag和aea的含量分别为42.63%和41.40%,合成效果不如本发明产生的技术效果。说明反应底物ara含量高的情况下产物中2-ag和aea的含量更高。
[0106]
虽然本发明已以较佳实施例公开如上,但其并非用以限定本发明,任何熟悉此技术的人,在不脱离本发明的精神和范围内,都可做各种的改动与修饰,因此本发明的保护范围应该以权利要求书所界定的为准。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



