一株分泌安眠酮单克隆抗体的杂交瘤细胞株及其应用的制作方法
 2021-02-02 00:02:16|
2021-02-02 00:02:16| 343|
343| 起点商标网
起点商标网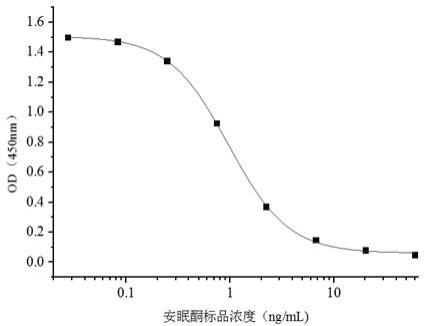
[0001]
本发明涉及一株分泌安眠酮单克隆抗体的杂交瘤细胞株及其应用,属于免疫检测技术领域。
背景技术:
[0002]
安眠酮(methaqualone)又名海米那,甲奎酮或眠可欣,属于非巴比妥类中枢神经镇定药,在临床上用于神经衰弱、失眠、麻醉前给药,常做为镇静和催眠药物。长期使用安眠酮会形成依赖性,造成毒物癖;大剂量服用会引起中毒,已属国家管制类的精神药品。2007年,农业部明确规定安眠酮在动物性食品中的残留为零。但由于安眠酮生产工艺简单,随着畜牧养殖业的迅速发展,安眠酮仍被非法用于畜禽养殖,造成了动物性食品的不安全。
[0003]
对于安眠酮兽药残留的检测,常采用高效液相色谱法、气相色谱法、气相或液相色谱质谱联用法。但这些方法存在样品前处理复杂和检测时间长等不足,不适用于大量样品的快速检测,为了维护广大消费者的利益,有必要建立一种针对安眠酮的高效、快速的检测方法。
[0004]
酶联免疫法(elisa)是一种极为高效、敏感、快速的检测方法,检测时对样本的前处理简单、纯化步骤少、分析容量大、检测成本低而且操作简便,适用于大量样本的现场快速检测,因此在兽药残留分析中得到了广泛应用。而使用酶联免疫法检测安眠酮的前提是得到对安眠酮具有高特异性和高灵敏度的单克隆抗体,因此,找到一种制备对安眠酮具有高特异性和高灵敏度的单克隆抗体的方法十分关键。
技术实现要素:
[0005]
本发明的目的是克服上述不足之处,提供一株分泌安眠酮单克隆抗体的杂交瘤细胞株及其应用。此杂交瘤细胞株分泌的安眠酮单克隆抗体对安眠酮具有较好的特异性和检测灵敏度(ic
50
值为0.96ng/ml),可以用于建立安眠酮的免疫学检测方法,检测食品中安眠酮的残留。
[0006]
本发明的技术方案,一株分泌安眠酮单克隆抗体的杂交瘤细胞株tz1b1,已保藏于中国微生物菌种保藏管理委员会普通微生物中心cgmcc,地址北京市朝阳区北辰西路1号院3号中国科学院微生物研究所,分类命名为单克隆细胞株,保藏日期2019年11月28日,保藏编号cgmcc no.19173。
[0007]
本发明提供了上述一种分泌安眠酮单克隆抗体的杂交瘤细胞株tz1b1的制备方法,包含如下步骤:(1)使用安眠酮半抗原制备安眠酮完全抗原,将获得的安眠酮完全抗原制备成含抗原弗氏佐剂与含抗原不完全弗氏佐剂;(2)将得到的含抗原弗氏佐剂通过背部皮下注射,注射进入balb/c小鼠体内进行多次免疫,首次免疫采用含抗原完全弗氏佐剂,加强免疫采用含抗原不完全弗氏佐剂;(3)将经过上述免疫过程的小鼠进行采血,通过间接elisa检测小鼠血清免疫效价和免
疫抑制能力,筛选出血清中安眠酮抗体含量高的获得免疫的小鼠;(4)将筛选出的小鼠用含抗原不完全弗氏佐剂再进行最后一次加强免疫,然后通过腹腔注射进行冲刺免疫,冲刺免疫采用不含弗氏佐剂的安眠酮完全抗原进行;(5)将进行冲刺免疫后的balb/c小鼠的脾细胞和骨髓瘤细胞融合,将融合的细胞通过培养基培养,利用间接elisa检测阳性细胞孔,并进一步利用间接竞争elisa法测定阳性细胞孔的抑制效果,通过有限稀释法对有最好抑制的阳性细胞孔进行亚克隆,最终筛选出获得能分泌安眠酮单克隆抗体的杂交瘤细胞株tz1b1。
[0008]
在本发明的一种实施方式中,所述步骤(2)、(4)首次免疫与加强免疫之间间隔一个月,加强免疫之间间隔21天,加强免疫与冲刺免疫之间间隔18~21天。
[0009]
在本发明的一种实施方式中,所述步骤(2)、(4)首次免疫剂量为100μg/只,加强免疫剂量为50μg/只,冲刺免疫剂量为25μg/只。
[0010]
在本发明的一种实施方式中,所述步骤(2)、(4)的免疫过程,包含1次首次免疫、4次加强免疫和1次冲刺免疫。
[0011]
在本发明的一种实施方式中,所述步骤(3)中的采血为第3次免疫过程结束后第7天进行采血。
[0012]
在本发明的一种实施方式中,所述步骤(5)中的细胞融合是在冲刺免疫结束3天后进行。
[0013]
在本发明的一种实施方式中,所述步骤(5)中的细胞融合是通过聚乙二醇(peg 4000)法进行的。
[0014]
在本发明的一种实施方式中,所述步骤(5)中的培养基为rpmi-1640培养基。
[0015]
在本发明的一种实施方式中,所述步骤(5)中的亚克隆次数为3次。
[0016]
安眠酮单克隆抗体,它由所述保藏编号为cgmcc no. 19173的杂交瘤细胞株tz1b1分泌产生。
[0017]
本发明提供了上述安眠酮单克隆抗体的制备方法,所述方法为取balb/c小鼠,腹腔注射石蜡油,再腹腔注射保藏编号为cgmcc no. 19173的杂交瘤细胞株tz1b1,注射后收集腹水,将腹水纯化,将获得的单抗低温保存。
[0018]
在本发明的一种实施方式中,所述方法为取8-10周龄balb/c小鼠,每只小鼠腹腔注射石蜡油1ml,7天后每只小鼠腹腔注射1
×
106保藏编号为cgmcc no. 19173的杂交瘤细胞株,从第7天开始收集腹水,将腹水通过辛酸-硫酸铵法纯化,获得的单抗置于-20℃保存。
[0019]
一种安眠酮半抗原,其简称为mtq-cooh,分子式如下:
。
[0020]
一种安眠酮完全抗原,筒称为mtq-cooh-klh,分子式如下:。
[0021]
本发明还提供了上述安眠酮单克隆抗体的应用,将其应用于食品安全检测中安眠酮残留的分析检测。
[0022]
本发明的有益效果:本发明获得的安眠酮单克隆抗体可以用于免疫分析检测,其对安眠酮有较好的检测灵敏度和特异性(ic
50
值为0.96ng/ml)、对安眠酮类似物交叉率小于10%,交叉率=(安眠酮的ic
50
/类似物的ic
50
)
×
100%。
[0023]
生物材料样品保藏:一株分泌安眠酮单克隆抗体的杂交瘤细胞株tz1b1,已保藏于中国微生物菌种保藏管理委员会普通微生物中心cgmcc,地址北京市朝阳区北辰西路1号院3号中国科学院微生物研究所,分类命名为单克隆细胞株,保藏日期2019年11月28日,保藏编号cgmcc no.19173。
附图说明
[0024]
图1本发明安眠酮单克隆抗体对安眠酮的抑制标准曲线。
具体实施方式
[0025]
本发明下面的实施例仅作为本发明内容的进一步说明,不能作为本发明的限定内容或范围。下面通过实施例对本发明作进一步说明。
[0026]
下述实施例中涉及的培养基如下:rpmi-1640培养基(mg/l):l-精氨酸290、l-门冬酰胺50、l-门冬氨酸20、l-胱氨酸二盐
酸盐65.15、l-谷氨酸20、甘氨酸10、l-组氨酸15、l-羟脯氨酸20、l-异亮氨酸50、l-亮氨酸50、l-赖氨酸盐酸盐40、l-甲硫氨酸15、l-苯丙氨酸15、l-脯氨酸20、l-丝氨酸30、l-苏氨酸20、l-色氨酸5、l-酪氨酸23.19、l-缬氨酸20、对氨基苯甲酸1、硝酸钙100、无水硫酸镁48.84、无水磷酸二氢钠676.13、氯化钾400、氯化钠6000、葡萄糖2000、还原谷胱甘肽1、酚红5、l-谷氨酰胺300、生物素0.2、d-泛酸钙0.25、叶酸1、i-肌醇35、烟酰胺1、氯化胆碱3、盐酸吡哆醇1、核黄素0.2、盐酸硫胺素1、维生素b12 0.005、碳酸氢钠2000。
[0027]
下述实施例中涉及的试剂如下:碳酸盐缓冲液(cbs):称取na2co
3 1.59 g,nahco
3 2.93 g,分别溶于少量双蒸水后混合,加双蒸水至约800ml混匀,调ph值至9.6,加双蒸水定容至1000ml,4℃贮存备用;磷酸盐缓冲液(pbs):8.00g nacl,0.2g kcl,0.2g kh2po4,2.9g na2hpo4·
12 h2o,溶于800ml纯水中,用naoh或hcl调ph到7.2~7.4,定容至1000ml;pbst:含0.05 %吐温20的pbs;抗体稀释液:pbs 加入 0.1%明胶。
[0028]
tmb显色液:a液:na2hpo
4.
12h2o 18.43g,柠檬酸 9.33g,纯水定容至1000ml;b液:60mg tmb 溶于100ml乙二醇中。a、b液按体积比5:1混合即为tmb显色液,现用现混。
[0029]
下述实施例中涉及的检测方法如下:安眠酮抑制率检测方法:通过棋盘试验选择ic-elisa中最合适的抗原和抗体浓度。用碳酸盐缓冲液(cbs)将抗原稀释至0.03,0.1,0.3和1μg/ ml,并用抗体稀释液将抗体稀释至0.03,0.1,0.3和1μg/ ml。选择最佳工作点后,将安眠酮标准品稀释0,0.027,0.082,0.25,0.74,2.22,6.67,20和60ng/ml等浓度,按照ic-elisa操作步骤,最后用originpro 8.5做图(结果如图1所示),获得安眠酮标准抑制曲线,计算ic
50
。
[0030]
实施例1:安眠酮半抗原的合成由于安眠酮小分子不具有免疫原性,不能刺激小鼠产生免疫应答,进而产生抗体,因此需通过蛋白连接技术将安眠酮偶联到蛋白上,使其获得免疫原性;蛋白偶联技术中常用的活泼基团有氨基,羧基,羟基,巯基等,鉴于安眠酮分子结构中不含有氨基,羧基,羟基,因此需要在其结构上衍生出羧基。
[0031]
本发明衍生后的安眠酮半抗原结构如下:;衍生过程包括如下四个反应:
1.在反应容器中加入1b(1.2 eq.)、pd(oac)2(0.04 eq.)、p(o-tol)3(0.06 eq.)和1a,加入net3(0.3m),通过冷冻-泵循环法置换3次气体,在ar氛围下60℃搅拌2h,升温至80℃搅拌24h得到中间产物2a。
[0032]
2.在反应容器中加入2a,再加入5-10mol的pd/c,加适量乙醇溶解,用氢气置换气体3次,氢气氛围下室温搅拌4h,滤去pd/c,收集滤液旋干,过柱分离得到中间产物3a。
[0033]
3.在反应容器中加入3a,加入3 eq.naoh水溶液,适量乙醇,50℃下反应3h,冷却后用盐酸酸化至ph=2-4,用乙酸乙酯进行萃取,无水硫酸钠干燥,旋干,过柱分离得到中间产物4a。
[0034]
4.在反应容器中加入4a,4b(1.2 eq.),加入醋酸(0.3m),回流3天,冷却后用乙酸乙酯进行萃取,无水硫酸钠干燥,旋干,过柱分离得到安眠酮半抗原。
[0035]
实施例2:安眠酮完全抗原的合成称取9.45mg 安眠酮半抗原(mtq-cooh),6.21mg n-羟基琥珀酰亚胺(nhs),溶解于300μl n,n-二甲基甲酰胺(dmf)中,室温搅拌反应10min;再称取10.35mg 1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc),用100μl dmf充分溶解后,加入到mtq-cooh溶液中,室温搅拌反应4-6h(称为a液)。取6mg klh,用0.01m碳酸盐缓冲液(cbs)稀释至3mg/ml(称为b液),再逐滴将a液缓慢加入到b液中,室温反应过夜;然后用0.01m pbs溶液透析,除去未反应的小分子半抗原,得到完全抗原mtq-cooh-klh,并通过紫外吸收扫描方法进行鉴定。
[0036]
实施例3:安眠酮包被原的合成将4.2mg安眠酮半抗原(mtq-cooh)、2.8mgn-羟基琥珀酰亚胺(nhs)溶解于300μl无水n,n-二甲基甲酰胺(dmf)中,室温搅拌反应10min,得到安眠酮半抗原(mtq-cooh)溶液;将4.6mg 1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)溶解于100μl无水dmf后,加入到mtq-cooh溶液中,室温搅拌进行反应4-6h,得到a液;将6mg鸡卵白蛋白(ova)用1ml浓度为0.01mmol/l的碳酸盐缓冲液(cbs)稀释,得到b液;逐滴将a液缓慢加入到b液中进行反应,得到反应液;用pbs溶液透析反应液,除去未反应的小分子半抗原,得到包被原(mtq-cooh-ova)。
[0037]
实施例4:分泌安眠酮单克隆抗体的杂交瘤细胞株的制备1、动物免疫的获得:将安眠酮完全抗原与等量弗氏佐剂混合乳化后,对balb/c小鼠进行颈背部皮下多点注射免疫(冲刺免疫除外);首次免疫用完全弗氏佐剂,剂量为100μg/只;多次加强免疫用不完全弗氏佐剂且剂量减半即为50μg/只;冲刺免疫不用佐剂,直接用生理盐水稀释后腹腔注射,剂量再减半即为25μg/只;首次免疫与第二次加强免疫之间间隔一个月,多次加强免疫之间间隔21天,冲刺免疫与最后一次加强免疫之间间隔18-21天;通过间接竞争酶联免疫法(ic-elisa)观测小鼠免疫效果即检测小鼠血清的效价和抑制;2、细胞融合:在冲刺免疫三天后,按照常规peg(聚乙二醇,分子量为4000)方法进行细胞融合,具体步骤如下:a、断尾取血,颈椎脱臼法处死小鼠后,立即放入75%酒精中消毒,浸泡5min左右,无菌操作取出小鼠的脾脏,用注射器的胶头适度研磨并通过200目细胞筛网得到脾细胞悬液,收集,离心(1200rpm,8min),用rpmi-1640培养基洗涤脾细胞三次,最后一次离心后,将脾细胞稀释到一定体积,计数,备用;b、收集sp2/0细胞:融合前7-10天,将sp2/0瘤细胞用含10% fbs(胎牛血清)rpmi-1640 培养基在5% co2培养箱中培养,融合前要求sp2/0瘤细胞数量达到(1~4)
×
107,保证融合前sp2/0瘤细胞处于对数生长期,融合时,收集瘤细胞,悬浮于rpmi-1640基础培养液中,进行细胞计数;c、融合过程7min:第1min,将1ml的peg 4000由慢到快滴加到细胞中;第2min,静置;第3min和第4min,在1min内滴加1ml rpmi-1640培养基;第5min和第6min,在1min内滴加2ml rpmi-1640培养基;第7min,每10s滴加1ml的rpmi-1640培养基;然后37℃温浴5min;离心(800rpm,8min),弃上清,重悬入含20%胎牛血清、2%的50
×
hat的rpmi-1640筛选培养液中,按照200μl/孔加到96孔细胞板,置于37℃、5% co2培养箱中培养;3、细胞筛选与细胞株建立:在细胞融合的第3天对融合细胞进行rpmi-1640筛选培养液半换液,第5天进行用含20% 胎牛血清,1%的100
×
ht的rpmi-1640过渡培养液进行全换液,在第7天取细胞上清进行筛选;筛选分两步:第一步先用ic-elisa法筛选出阳性细胞孔,第二步选用安眠酮为标准品,用ic-elisa法对阳性细胞进行抑制效果测定;选择对安眠酮标准品有较好抑制的细胞孔,采用有限稀释法进行亚克隆,七天后用同样的方法进行检测;按上述方法进行三次亚克隆,最终获得分泌安眠酮单克隆抗体杂交瘤细胞株tz1b1。
[0038]
实施例5:安眠酮单克隆抗体的制备与鉴定取8-10周龄balb/c小鼠,每只小鼠腹腔注射无菌石蜡油1ml;7天后每只小鼠腹腔注射1
×
106安眠酮杂交瘤细胞,从第七天开始收集腹水,将腹水通过辛酸-饱和硫酸铵法进行抗体纯化;在偏酸条件下,正辛酸可以沉淀腹水中除igg免疫球蛋白外的其他杂蛋白,然后离心,弃沉淀;再用等量饱和度的硫酸铵溶液沉淀igg型的单克隆抗体,离心,弃上清,用0.01m的pbs溶液(ph7.4)溶解后,透析脱盐,最终得到纯化后的单克隆抗体置于-20℃保存。
[0039]
使用间接竞争elisa,测得安眠酮单克隆抗体的ic
50
值为0.96ng/ml、对安眠酮类似物交叉率小于10%,说明对安眠酮有很好的灵敏度,可用于安眠酮免疫分析检测。(交叉率=
(安眠酮的ic
50
/类似物的ic
50
)
×
100%)。
[0040]
实施例6:安眠酮单克隆抗体的应用将杂交瘤细胞株tz1b1通过体内腹水制备的单克隆抗体应用于安眠酮的elisa添加回收试验,具体步骤如下:(1)将用碳酸盐缓冲液(cbs)稀释好的浓度为0.3μg/ml的包被原包被96孔酶标板,每孔100μl,37℃包被2h后,用pbst洗液洗板三次,每次每孔200μl,每次3min,拍干;(2)用含0.2%明胶的cbs进行封闭,每孔200μl,37℃封闭2h,用pbst洗液洗板三次,每次每孔200μl,每次3min,拍干;(3)用磷酸盐缓冲液(pbs)分别配置0,0.027,0.082,0.25,0.74,2.22, 6.67,20和60ng/ml的安眠酮标准溶液,将标准溶液以及待检测样品提取液,分别加入到已经封闭好的酶标板中,每孔50μl,每个样品重复3个孔,再每孔加入50μl以1:32000稀释的抗安眠酮单克隆抗体,37℃反应0.5h后,洗板拍干;(4)每孔加入100μl用含0.1%明胶的pbs以1:3000稀释的hrp标记的羊抗鼠igg二抗,37℃反应0.5h后,洗板拍干;(5)每孔加入100μl的tmb显色液,37℃显色15min后,每孔加入50μl 2m的h2so4终止液,450nm测吸光值;安眠酮单克隆抗体对安眠酮的抑制标准曲线如图1所示,用ic-elisa测定安眠酮单克隆抗体的ic
50
值为0.96ng/ml,说明该抗体对安眠酮有较好的灵敏度,可用于安眠酮的免疫分析检测。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



