一种利用微通道反应器连续制备瑞德西韦中间体的方法与流程
 2021-02-01 23:02:25|
2021-02-01 23:02:25| 244|
244| 起点商标网
起点商标网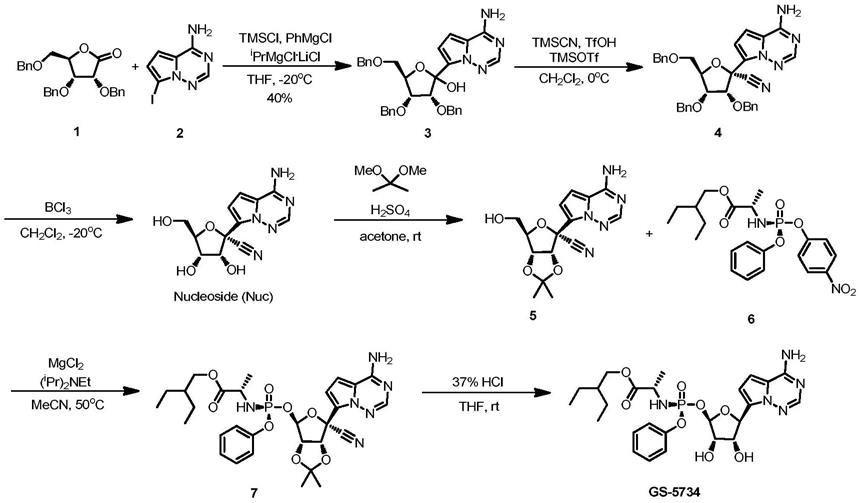
[0001]
本发明属于化学合成领域,具体涉及一种利用微通道反应器连续制备抗病毒药物瑞德西韦中间体(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4
-ꢀ
双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈的方法。
背景技术:
[0002]
瑞德西韦(remdesivir),化学名:(2s)-2-ethylbutyl2-(((s)-(((2r,3s,4r,5r)
ꢀ-
5-(4-aminopyrrolo[2,1f][1,2,4]triazin-7-yl)-5-cyano-3,4-dihydroxytetrahydrofuran-2
-ꢀ
yl)methoxy)(phenoxy)phosphoryl)amino)propanoate,cas号:1809249-37-3。是一种腺苷类似的氨基酸磷脂前体广谱抗病毒药物,其对rna病毒具有的广谱抗病毒活性,可以抑制包括非典型肺炎(sars冠状病毒)、埃博拉冠状病毒和其它多种冠状病毒。2020年1月31日,《新英格兰医学杂志》报道了世界首例使用瑞德西韦治愈新冠肺炎确诊患者的病例(new england journal of medicine,2020)。
[0003][0004]
传统的瑞德西韦制备工艺主要有两种:1);第一代合成方法共五步反应,收率分别为60%,58%,74%,21%,23%,总收率不到2%,并且反应过程需要进行sfc拆分反应,很难达到工业放大的要求(j.med.chem.2017,60,1648-1661); 2)nature报道了瑞德西韦的第二代合成方法,该方法避免了手性拆分,可在实验室放大至百克级合成规模(nature,2016,531(7594):381-385)。共6步反应(合成路线如下图所示),收率分别为40%,85%,86%,90%,70%,69%,总收率只有12.7%,其中中间体6的合成需分两步进行,收率分别为80%、39%。
[0005][0006]
虽然第二代合成方法可放大至百克规模,但随着新冠肺炎疫情的持续蔓延,瑞德
西韦的需求量大大增加,传统的釜式间歇合成方法完全无法满足患者的需求,因此,开发一种连续化、规模化的瑞德西韦制备工艺成为了急需解决的问题。
[0007]
其中,中间体4(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4
-ꢀ
双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈的合成是由中间体3通过苄位氰基化反应生成,该反应过程需要在-78℃条件下将三氟甲烷磺酸(tfoh)、三氟甲磺酸三甲基硅脂(tmsotf)和三甲基氰硅烷(tmscn)依次滴加入反应体系,操作过程繁琐。而且三氟甲烷磺酸(tfoh)、三氟甲磺酸三甲基硅脂(tmsotf) 和三甲基氰硅烷(tmscn)具有很大的毒性和腐蚀性,对操作人员健康危害较大且对设备要求较高。
技术实现要素:
[0008]
技术问题:本发明要解决的技术问题是提供一种利用微通道反应器连续制备瑞德西韦中间体(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈的方法,以解决现有技术存在的反应条件苛刻、操作过程繁琐、环境污染、工业放大困难等问题。
[0009]
技术方案:为解决上述问题,本发明采用的技术方案如下:本发明提供了一种利用微通道反应器制备瑞德西韦中间体(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f] [1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈的方法,所述微通道反应器由混合器和反应模块组成,其中,混合器和反应模块通过连接管路或其它连接设备实现串联:
[0010]
(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈,化学式如式i所示,合成方法包括以下步骤:
[0011][0012]
(1)将(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇加入到有机溶剂中,作为物料ⅰ;
[0013]
(2)将三氟甲烷磺酸(tfoh)和三氟甲磺酸三甲基硅酯(tmsotf)依次加入到有机溶剂中充分混合,作为物料ⅱ;
[0014]
(3)三甲基氰硅烷(tmscn),作为物料ⅲ;
[0015]
(4)同时将物料ⅰ和物料ⅱ泵入混合器中进行混合,再泵入物料ⅲ进行混合;混合后输送至反应模块中进行反应,再将有机碱泵入反应模块中与反应液混合,出样口收集流出液,后处理得到(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4] 三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈。
[0016]
作为改进,所述微通道反应器的尺寸为:内径0.5~5mm,长度0.5~40m;所述微通道反应器为孔道结构,孔道数量根据需要增加或减少,孔道材质为耐腐蚀的材料,如碳纤维材料、氧化铜材料或聚四氟乙烯材料。
[0017]
优选地,步骤(1)和步骤(2)所述的有机溶剂分别独立地为二氯甲烷、四氢呋喃、丙酮、乙腈、二甲基亚砜、n,n-二甲基亚胺中的一种或几种。
[0018]
优选地,步骤(1),物料ⅰ中,(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇的浓度为0.5~2.0mol/l;
[0019]
优选地,步骤(2),物料ⅱ中,三氟甲烷磺酸(tfoh)的浓度为1.0~5.0mol/l,三氟甲磺酸三甲基硅酯(tmsotf)的溶度为1.0~5.0mol/l。
[0020]
优选地,步骤(4),反应体系中,
[0021]
(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇与三氟甲烷磺酸(tfoh)的摩尔比为1:1.0~3.0;
[0022]
(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇与三氟甲磺酸三甲基硅酯(tmsotf)的摩尔比为1:1.0~3.0;
[0023]
(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇与三甲基氰硅烷(tmscn)的摩尔比为1:2.0~6.0。
[0024]
优选地,
[0025]
步骤(4)所述的物料ⅰ进料流速为0.5~10.0ml/min;
[0026]
步骤(4)所述的物料ⅱ进料流速为0.5~10.0ml/min;
[0027]
步骤(4)所述的物料ⅲ进料流速为0.2~5.0ml/min。
[0028]
优选地,步骤(4)中,有机碱为三乙胺(et3n)。
[0029]
优选地,微通道反应模块的温度为-78~(-40)℃。
[0030]
优选地,反应液在反应模块中的停留时间为30s~30min。
[0031]
有益效果:与现有技术相比,本发明涉及的微通道反应器具有价格便宜、便于运输、清洗方便、传质传热效率高、更易于工业放大等特点。本发明涉及的反应克服了传统合成方法所需的严苛条件,减少了繁琐了加料步骤,降低了污染物的排放,符合绿色可持续化学发展理念,具有良好的工业应用前景,适用于瑞德西韦中间体(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈的制备。
[0032]
本发明提供的利用微通道反应器合成瑞德西韦中间体的方法相对于现有技术,具有以下突出的优势:
[0033]
(1)微通道反应器采用连续流的方式,物料混合效果好、返混极低,可有效提升反应效率与产品质量。
[0034]
(2)设备占地面积小,操作简单,可以减少人工操作步骤,降低生产成本,生产经济性得到保障。
[0035]
(3)微通道反应器传质传热效率高,提高了反应的安全系数。
[0036]
(4)实时在线反应体积只有几至几十毫升,大大降低反应的安全隐患。
[0037]
(5)微通道反应器具有较好的去除反应热的能力,可克服极低反应温度的限制,反应温度可以由零下78℃提高至零下40℃,降低了能耗。
[0038]
(6)将传统合成方法所需的数小时的反应时间缩短至几分钟。
[0039]
(7)原料转化率可达86~98%,产物收率高达82~94%。
附图说明
[0040]
图1为本发明方法合成路线图。
具体实施方式
[0041]
下面结合具体实施例对本发明做进一步说明,但本发明不受实施例的限制。
[0042]
实施例1
[0043]
本实施例提供了一种利用微通道反应器连续制备瑞德西韦中间体 (2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基) 甲基)四氢呋喃-2-腈的方法,如图1所示,具体合成方法包括以下步骤:
[0044]
称取(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇27.60g(50mmol,1.0equiv),充分溶解在二氯甲烷中,配制成50ml溶液,作为物料ⅰ;量取8.8ml tfoh(100mmol,2.0equiv),用适量的二氯甲烷溶解,加入18.0ml tmsotf(100mmol,2.0equiv),配制成50.0 ml溶液,作为物料ⅱ;量取25.0ml tmscn(200mmol,4.0equiv),作为物料ⅲ。通过注射泵将物料ⅰ和物料ⅱ泵入反应体系内,充分混合后泵入物料ⅲ,其中,物料ⅰ进料流速为5.0ml/min,物料ⅱ进料流速为5.0ml/min,物料ⅲ进料流速为2.5ml/min。混合后输送至反应模块中反应,其中,反应模块的管道内径为1.0mm,长度20m,体积15.7ml,停留时间1.3min,反应器温度-78℃。最后利用注射泵将25ml有机碱三乙胺泵入体系与流出的反应液混合,tlc监测反应,待反应结束后收集流出的反应液,向反应液中缓慢加入40gnahco3和150 ml水,充分搅拌后分离,水层用二氯甲烷萃取并收集有机相,减压蒸馏除去溶剂并回收,重结晶得(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4
-ꢀ
双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈19.09g,收率68%。
[0045]
实施例2
[0046]
本实施例提供了一种利用微通道反应器连续制备瑞德西韦中间体 (2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基) 甲基)四氢呋喃-2-腈的方法,如图1所示,具体合成方法包括以下步骤:
[0047]
称取(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇27.60g(50mmol,1.0equiv),充分溶解在二氯甲烷中,配制成50ml溶液,作为物料ⅰ;量取8.8ml tfoh(100mmol,2.0equiv),用适量的二氯甲烷溶解,加入18.0ml tmsotf(100mmol,2.0equiv),配制成50.0 ml溶液,作为物料ⅱ;量取25.0ml tmscn(200mmol,4.0equiv),作为物料ⅲ。通过注射泵将物料ⅰ和物料ⅱ泵入反应体系内,充分混合后泵入物料ⅲ,其中,物料ⅰ进料流速为5.0ml/min,物料ⅱ进料流速为5.0ml/min,物料ⅲ进料流速为2.5ml/min。混合后输送至反应模块中反应,其中,反应模块的管道内径为1.5mm,长度9m,体积15.9ml,停留时间1.3min,反应器温度-78℃。最后利用注射泵将25ml有机碱三乙胺泵入体系与流出的反应液混合,tlc监测反应,待反应结束后收集流出的反应液,向反应液中缓慢加入40gnahco3和150 ml水,充分搅拌后分离,水层用二氯甲烷萃取并收集有机相,减压蒸馏除去溶剂并回收,重结晶得(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4
-ꢀ
双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈17.39g,收率62%。
[0048]
实施例3
[0049]
本实施例提供了一种利用微通道反应器连续制备瑞德西韦中间体 (2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基) 甲基)四氢呋喃-2-腈的方法,如图1所示,具体合成方法包括以下步骤:
[0050]
称取(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇27.60g(50mmol,1.0equiv),充分溶解在二氯甲烷中,配制成50ml溶液,作为物料ⅰ;量取8.8ml tfoh(100mmol,2.0equiv),用适量的二氯甲烷溶解,加入18.0ml tmsotf(100mmol,2.0equiv),配制成50.0 ml溶液,作为物料ⅱ;量取25.0ml tmscn(200mmol,4.0equiv),作为物料ⅲ。通过注射泵将物料ⅰ和物料ⅱ泵入反应体系内,充分混合后泵入物料ⅲ,其中,物料ⅰ进料流速为5.0ml/min,物料ⅱ进料流速为5.0ml/min,物料ⅲ进料流速为2.5ml/min。混合后输送至反应模块中反应,其中,反应模块的管道内径为0.8mm,长度30m,体积15.1ml,停留时间1.2min,反应器温度-78℃。最后利用注射泵将25ml有机碱三乙胺泵入体系与流出的反应液混合,tlc监测反应,待反应结束后收集流出的反应液,向反应液中缓慢加入40gnahco3和150 ml水,充分搅拌后分离,水层用二氯甲烷萃取并收集有机相,减压蒸馏除去溶剂并回收,重结晶得(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4
-ꢀ
双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈20.19g,收率72%。
[0051]
实施例4
[0052]
本实施例提供了一种利用微通道反应器连续制备瑞德西韦中间体 (2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基) 甲基)四氢呋喃-2-腈的方法,如图1所示,具体合成方法包括以下步骤:
[0053]
称取(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇27.60g(50mmol,1.0equiv),充分溶解在二氯甲烷中,配制成50ml溶液,作为物料ⅰ;量取8.8ml tfoh(100mmol,2.0equiv),用适量的二氯甲烷溶解,加入18.0ml tmsotf(100mmol,2.0equiv),配制成50.0 ml溶液,作为物料ⅱ;量取25.0ml tmscn(200mmol,4.0equiv),作为物料ⅲ。通过注射泵将物料ⅰ和物料ⅱ泵入反应体系内,充分混合后泵入物料ⅲ,其中,物料ⅰ进料流速为4.0ml/min,物料ⅱ进料流速为4.0ml/min,物料ⅲ进料流速为2.0ml/min。混合后输送至反应模块中反应,其中,反应模块的管道内径为0.8mm,长度30m,体积15.1ml,停留时间1.5min,反应器温度-78℃。最后利用注射泵将25ml有机碱三乙胺泵入体系与流出的反应液混合,tlc监测反应,待反应结束后收集流出的反应液,向反应液中缓慢加入40gnahco3和150 ml水,充分搅拌后分离,水层用二氯甲烷萃取并收集有机相,减压蒸馏除去溶剂并回收,重结晶得(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7
-ꢀ
基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈21.32g,收率76%。
[0054]
实施例5
[0055]
本实施例提供了一种利用微通道反应器连续制备瑞德西韦中间体 (2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基) 甲基)四氢呋喃-2-腈的方法,如图1所示,具体合成方法包括以下步骤:
[0056]
称取(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧
基)-5-((苄氧基)甲基)四氢呋喃-2-醇27.60g(50mmol,1.0equiv),充分溶解在二氯甲烷中,配制成50ml溶液,作为物料ⅰ;量取8.8ml tfoh(100mmol,2.0equiv),用适量的二氯甲烷溶解,加入18.0ml tmsotf(100mmol,2.0equiv),配制成50.0 ml溶液,作为物料ⅱ;量取25.0ml tmscn(200mmol,4.0equiv),作为物料ⅲ。通过注射泵将物料ⅰ和物料ⅱ泵入反应体系内,充分混合后泵入物料ⅲ,其中,物料ⅰ进料流速为2.5ml/min,物料ⅱ进料流速为2.5ml/min,物料ⅲ进料流速为1.25ml/min。混合后输送至反应模块中反应,其中,反应模块的管道内径为0.8mm,长度30m,体积15.1ml,停留时间2.4min,反应器温度-78℃。最后利用注射泵将25ml有机碱三乙胺泵入体系与流出的反应液混合,tlc监测反应,待反应结束后收集流出的反应液,向反应液中缓慢加入40gnahco3和 150ml水,充分搅拌后分离,水层用二氯甲烷萃取并收集有机相,减压蒸馏除去溶剂并回收,重结晶得(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7
-ꢀ
基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈23.29g,收率83%。
[0057]
实施例6
[0058]
本实施例提供了一种利用微通道反应器连续制备瑞德西韦中间体 (2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基) 甲基)四氢呋喃-2-腈的方法,如图1所示,具体合成方法包括以下步骤:
[0059]
称取(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇27.60g(50mmol,1.0equiv),充分溶解在二氯甲烷中,配制成50ml溶液,作为物料ⅰ;量取8.8ml tfoh(100mmol,2.0equiv),用适量的二氯甲烷溶解,加入18.0ml tmsotf(100mmol,2.0equiv),配制成50.0 ml溶液,作为物料ⅱ;量取25.0ml tmscn(200mmol,4.0equiv),作为物料ⅲ。通过注射泵将物料ⅰ和物料ⅱ泵入反应体系内,充分混合后泵入物料ⅲ,其中,物料ⅰ进料流速为2.0ml/min,物料ⅱ进料流速为2.0ml/min,物料ⅲ进料流速为1.0ml/min。混合后输送至反应模块中反应,其中,反应模块的管道内径为0.8mm,长度30m,体积15.1ml,停留时间3.0min,反应器温度-78℃。最后利用注射泵将25ml有机碱三乙胺泵入体系与流出的反应液混合,tlc监测反应,待反应结束后收集流出的反应液,向反应液中缓慢加入40gnahco3和150 ml水,充分搅拌后分离,水层用二氯甲烷萃取并收集有机相,减压蒸馏除去溶剂并回收,重结晶得(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4
-ꢀ
双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈24.13g,收率86%。
[0060]
实施例7
[0061]
本实施例提供了一种利用微通道反应器连续制备瑞德西韦中间体 (2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基) 甲基)四氢呋喃-2-腈的方法,如图1所示,具体合成方法包括以下步骤:
[0062]
称取(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇27.60g(50mmol,1.0equiv),充分溶解在二氯甲烷中,配制成50ml溶液,作为物料ⅰ;量取8.8ml tfoh(100mmol,2.0equiv),用适量的二氯甲烷溶解,加入18.0ml tmsotf(100mmol,2.0equiv),配制成50.0 ml溶液,作为物料ⅱ;量取25.0ml tmscn(200mmol,4.0equiv),作为物料ⅲ。通过注射泵将物料ⅰ和物料ⅱ泵入反应体系内,充分混合后泵入物料ⅲ,其中,物料ⅰ进料流速为1.0ml/min,物料ⅱ进料流速为
1.0ml/min,物料ⅲ进料流速为0.5ml/min。混合后输送至反应模块中反应,其中,反应模块的管道内径为0.8mm,长度30m,体积15.1ml,停留时间6.0min,反应器温度-78℃。最后利用注射泵将25ml有机碱三乙胺泵入体系与流出的反应液混合,tlc监测反应,待反应结束后收集流出的反应液,向反应液中缓慢加入40gnahco3和150 ml水,充分搅拌后分离,水层用二氯甲烷萃取并收集有机相,减压蒸馏除去溶剂并回收,重结晶得(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4
-ꢀ
双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈24.68g,收率88%。
[0063]
实施例8
[0064]
本实施例提供了一种利用微通道反应器连续制备瑞德西韦中间体 (2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基) 甲基)四氢呋喃-2-腈的方法,如图1所示,具体合成方法包括以下步骤:
[0065]
称取(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇27.60g(50mmol,1.0equiv),充分溶解在二氯甲烷中,配制成50ml溶液,作为物料ⅰ;量取8.8ml tfoh(100mmol,2.0equiv),用适量的二氯甲烷溶解,加入18.0ml tmsotf(100mmol,2.0equiv),配制成 50.0ml溶液,作为物料ⅱ;量取25.0ml tmscn(200mmol,4.0equiv),作为物料ⅲ。通过注射泵将物料ⅰ和物料ⅱ泵入反应体系内,充分混合后泵入物料ⅲ,其中,物料ⅰ进料流速为2.0ml/min,物料ⅱ进料流速为2.0ml/min,物料ⅲ进料流速为1.0ml/min。混合后输送至反应模块中反应,其中,反应模块的管道内径为0.8mm,长度30m,体积15.1ml,停留时间3.0min,反应器温度-60℃。最后利用注射泵将25ml有机碱三乙胺泵入体系与流出的反应液混合,tlc监测反应,待反应结束后收集流出的反应液,向反应液中缓慢加入40gnahco3和 150ml水,充分搅拌后分离,水层用二氯甲烷萃取并收集有机相,减压蒸馏除去溶剂并回收,重结晶得(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7
-ꢀ
基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈25.24g,收率90%。
[0066]
实施例9
[0067]
本实施例提供了一种利用微通道反应器连续制备瑞德西韦中间体 (2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基) 甲基)四氢呋喃-2-腈的方法,如图1所示,具体合成方法包括以下步骤:
[0068]
称取(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇27.60g(50mmol,1.0equiv),充分溶解在二氯甲烷中,配制成50ml溶液,作为物料ⅰ;量取8.8ml tfoh(100mmol,2.0equiv),用适量的二氯甲烷溶解,加入18.0ml tmsotf(100mmol,2.0equiv),配制成50.0 ml溶液,作为物料ⅱ;量取25.0ml tmscn(200mmol,4.0equiv),作为物料ⅲ。通过注射泵将物料ⅰ和物料ⅱ泵入反应体系内,充分混合后泵入物料ⅲ,其中,物料ⅰ进料流速为2.0ml/min,物料ⅱ进料流速为2.0ml/min,物料ⅲ进料流速为1.0ml/min。混合后输送至反应模块中反应,其中,反应模块的管道内径为0.8mm,长度30m,体积15.1ml,停留时间3.0min,反应器温度-40℃。最后利用注射泵将25ml有机碱三乙胺泵入体系与流出的反应液混合,tlc监测反应,待反应结束后收集流出的反应液,向反应液中缓慢加入40gnahco3和150 ml水,充分搅拌后分离,水层用二氯甲烷萃取并收集有机相,减压蒸馏除去溶剂并回收,重结晶得(2r,3r,4r,5r)-2-(4-氨基
吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4
-ꢀ
双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈26.37g,收率94%。
[0069]
实施例10
[0070]
(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈,合成方法包括以下步骤:
[0071]
(1)将(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇加入到有机溶剂中,作为物料ⅰ,其中, (3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇的浓度为0.5mol/l;
[0072]
(2)将三氟甲烷磺酸(tfoh)和三氟甲磺酸三甲基硅酯(tmsotf)依次加入到有机溶剂中充分混合,作为物料ⅱ;其中,三氟甲烷磺酸(tfoh)的浓度为1.0mol/l,三氟甲磺酸三甲基硅酯(tmsotf)的溶度为1.0mol/l;
[0073]
(3)三甲基氰硅烷(tmscn),作为物料ⅲ;
[0074]
(4)同时将物料ⅰ和物料ⅱ泵入混合器中进行混合,再泵入物料ⅲ进行混合;混合后输送至反应模块中进行反应,再将有机碱三乙胺(et3n)泵入反应模块中与反应液混合,出样口收集流出液,后处理得到(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈,收率为86%;微通道反应模块的温度为-40℃;反应液在反应模块中的停留时间为30s;
[0075]
其中,通过控制流速,使:
[0076]
(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇与三氟甲烷磺酸(tfoh)的摩尔比为1:1.0;
[0077]
(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇与三氟甲磺酸三甲基硅酯(tmsotf)的摩尔比为1:1.0;
[0078]
(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇与三甲基氰硅烷(tmscn)的摩尔比为1:2.0;
[0079]
步骤(1)和步骤(2)所述的有机溶剂均为乙腈,采用二氯甲烷、四氢呋喃、丙酮、乙腈、二甲基亚砜、n,n-二甲基亚胺作为溶剂也可以实现本发明的目的。
[0080]
实施例11
[0081]
(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈,合成方法包括以下步骤:
[0082]
(1)将(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇加入到有机溶剂中,作为物料ⅰ,其中, (3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇的浓度为2.0mol/l;
[0083]
(2)将三氟甲烷磺酸(tfoh)和三氟甲磺酸三甲基硅酯(tmsotf)依次加入到有机溶剂中充分混合,作为物料ⅱ;其中,三氟甲烷磺酸(tfoh)的浓度为5.0mol/l,三氟甲磺酸三甲基硅酯(tmsotf)的溶度为5.0mol/l;
[0084]
(3)三甲基氰硅烷(tmscn),作为物料ⅲ;
[0085]
(4)同时将物料ⅰ和物料ⅱ泵入混合器中进行混合,再泵入物料ⅲ进行混合;混合
后输送至反应模块中进行反应,再将有机碱三乙胺(et3n)泵入反应模块中与反应液混合,出样口收集流出液,后处理得到(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈,收率为90%;微通道反应模块的温度为-78℃;反应液在反应模块中的停留时间为 30min;
[0086]
其中,通过控制流速,使:
[0087]
(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇与三氟甲烷磺酸(tfoh)的摩尔比为1:3.0;
[0088]
(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇与三氟甲磺酸三甲基硅酯(tmsotf)的摩尔比为1:3.0;
[0089]
(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇与三甲基氰硅烷(tmscn)的摩尔比为1:6.0;
[0090]
步骤(1)和步骤(2)所述的有机溶剂均为乙腈,采用二氯甲烷、四氢呋喃、丙酮、乙腈、二甲基亚砜、n,n-二甲基亚胺作为溶剂也可以实现本发明的目的。
[0091]
通过如下实验说明本发明方法优势:
[0092]
1、为了考察微通道反应器尺寸对反应收率的影响,在实施例1(即:微通道反应器内径1.0mm,长度20m,体积15.7ml,物料ⅰ进料流速为5.0ml/min,物料ⅱ进料流速为5.0ml/min,物料ⅲ进料流速为2.5ml/min,停留时间1.3min)。在此基础上采用不同的微通道反应尺寸,进而考察微通道反应尺寸对反应收率的影响,具体设置如下:实施例2采用微通道反应尺寸内径1.5mm,长度9m,体积15.9ml;实施例3采用微通道反应尺寸内径0.8mm,长度30m,体积15.1ml。比较结果如表1所示。
[0093]
表1微通道反应器尺寸对反应收率的影响
[0094]
实验组内径(mm)长度(m)体积(ml)收率(%)实施例11.02015.768实施例21.5915.962实施例30.83015.172
[0095]
由表1可知,微通道反应器尺寸对反应收率影响较大,反应器内径减小时物料混合效果较好,反应收率提高,而内径过小可能会引起管道堵塞,因此微通道反应器内径是反应的关键工业参数,反应器内径为0.8mm最合适。
[0096]
2、为了考察停留时间对反应收率的影响,在实施例3(即:微通道反应器内径0.8mm,长度30m,体积15.1ml,物料ⅰ进料流速为5.0ml/min,物料ⅱ进料流速为5.0ml/min,物料ⅲ进料流速为2.5ml/min,停留时间1.2min)。在此基础上采用不同的停留时间,进而考察停留时间对反应收率的影响,具体设置如下:实施例4停留时间采用1.5min;实施例5停留时间采用2.4min;实施例5停留时间采用3.0min;实施例5停留时间采用6.0min。比较结果如表2所示。
[0097]
表2停留时间对反应收率的影响
[0098]
实验组停留时间(min)收率(%)实施例31.272实施例41.576实施例52.483
实施例63.086实施例76.088
[0099]
由表2可知,反应的停留时间对反应收率的影响很大,在时间过短的情况下,反应有原料剩余,而时间过长对反应收率提高不明显,因此反应的停留时间是反应的关键工艺参数,停留时间为3.0min最合适。
[0100]
3、为了考察反应温度对反应收率的影响,在实施例7(即:微通道反应器内径0.8mm,长度30m,体积15.1ml,物料ⅰ进料流速为2.0ml/min,物料ⅱ进料流速为2.0ml/min,物料ⅲ进料流速为1.0ml/min,停留时间3.0min,反应温度为-78℃)。在此基础是采用不同的反应温度,进而考察反应温度对反应收率的影响,具体设置如下:实施例8采用反应温度为-60℃;实施例9采用反应温度为-40℃。比较结果如表3所示。
[0101]
表3反应温度对反应收率的影响
[0102]
实验组反应温度(℃)收率(%)实施例7-7888实施例8-6090实施例9-4094
[0103]
由表3可知,反应温度对反应收率影响很大,反应收率随着温度的升高而提高,反应温度可由-78℃提升至-40℃,收率可达94%。
[0104]
对比例(反应瓶)
[0105]
将27.60g(3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4-双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-醇(50mmol,1.0equiv)加入到250ml茄形瓶中,加入50ml二氯甲烷溶解,反应瓶至于-78℃,缓慢加入8.8ml tfoh(100mmol, 2.0equiv),搅拌10min后缓慢加入18.0ml tmsotf(100mmol,2.0equiv),搅拌30min后滴加25.0ml tmscn(200mmol,4.0equiv)。反应液在-78℃下反应 2h后加入25ml et3n并升温至室温,缓慢加入40g nahco3和150ml水搅拌10min。反应液用二氯甲烷萃取,收集有机相,用无水na2so4干燥,减压蒸馏除去溶剂,重结晶得(2r,3r,4r,5r)-2-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-3,4
-ꢀ
双(苄氧基)-5-((苄氧基)甲基)四氢呋喃-2-腈21.32g,收率76%。
[0106]
通过将本发明实施例与对比例进行比较可知:微通道反应器可将传统方法所需的数小时的反应时间缩短至几分钟;反应瓶合成过程中加料步骤繁琐且会损害操作人员健康,而利用微通道反应器合成目标产物由进料泵自动进料,减少了认为操作;反应瓶合成过程持液量大,加料过程存在危险性高,而微通道反应器由于持液量小(不到20ml),大大降低了危险系数;同时,微通道反应器将原来所需的-78℃反应温度提升至-40℃,降低了能耗。因此,微通道反应器与常规反应瓶相比具有反应速度快、持液量小、安全环保等优点,同时还提高了反应的收率。
[0107]
虽然本发明已以较佳的实施例公开如上,但其并非用以限定本发明,任何熟悉此技术的人,在不脱离本发明的精神和范围内,都可以做各种改动和修饰,因此本发明的保护范围应该以权利要求书所界定的为准。
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询

tips


 商标分类
商标分类  商标转让
商标转让 



