用于生产二氧化氯的方法和装置与流程
 2021-01-31 02:01:53|
2021-01-31 02:01:53| 346|
346| 起点商标网
起点商标网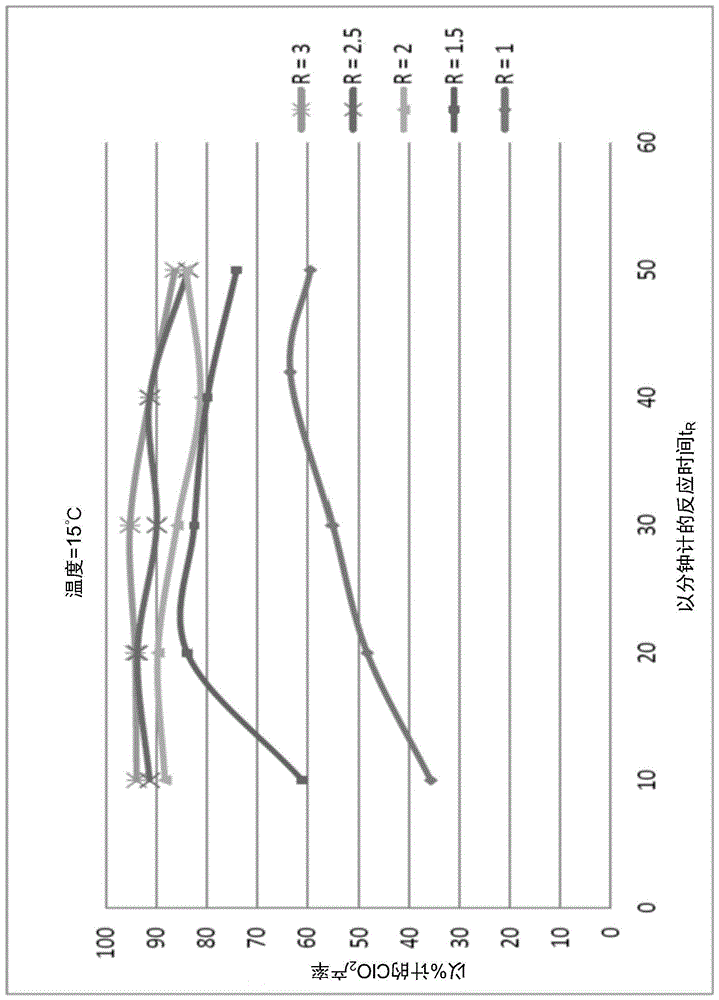
本发明涉及一种用于生产二氧化氯水溶液的方法,该方法将酸、亚氯酸盐和任选的水引入反应器中,其中,将引入到反应器中的酸相对于引入到反应器中的亚氯酸盐摩尔过量地引入反应器中。
此外,本发明涉及一种用于生产二氧化氯水溶液的装置,该装置具有反应器、用于将酸引入反应器的第一管线、用于将亚氯酸盐引入反应器的第二管线和任选的用于将水引入反应器的第三管线,该装置适于实施根据本发明的方法。
背景技术:
在室温和大气压下,二氧化氯(clo2)是黄红色的气体,具有消毒性并在水中具有良好的溶解性和稳定性。但是,气态二氧化氯在空气中在300g/m3的浓度下会爆炸性分解。取决于压力和温度,在浓度为30g/l的水溶液中,液态二氧化氯可能沉淀,并爆炸性分解。
二氧化氯的消毒作用比氯的消毒作用强,并且不依赖于水的ph。在使用过程中不产生不希望的氯化的消毒副产物,并且消毒后的水的味道和气味不受到不良影响。尤其由于这些优点,它正在越来越多的应用中替代原本常用的氯。
二氧化氯用于公共饮用水和废水处理领域中,用于工业设施、饮料制造商、餐饮和医院以及住宅中,以实现饮用水、自来水和生产用水的可靠消毒和灭菌。二氧化氯主要根据亚氯酸盐-酸法或根据亚氯酸盐-氯法,通过相应设计的二氧化氯系统当场生产。
本发明涉及亚氯酸盐-酸法,其中亚氯酸盐水溶液与酸反应生成二氧化氯(clo2)和氯化物。
亚氯酸钠-盐酸法中,亚氯酸钠(naclo2)与盐酸(hcl)根据下述反应方程式反应:
5naclo2+4hcl→4clo2+5nacl+2h2o
以生成二氧化氯(clo2)和氯化钠(nacl),该法被广泛使用。或者,亚氯酸盐-酸法也可以用其它酸来进行,例如硫酸,也可以用其它亚氯酸盐来进行,例如亚氯酸钾。
通过二氧化氯系统可以实现通过二氧化氯进行的消毒,在例如来自dvgw(德国燃气与水科学技术协会,germantechnicalandscientificassociationforgasandwater)的法规(dvgw工作表w224和w624)中规定了该二氧化氯系统的运行模式。根据这些法规中的指南,为了使亚氯酸钠溶液与盐酸反应,规定盐酸与亚氯酸盐相比至少过量三倍,以确保二氧化氯的化学计量产率为可靠的消毒所必需的至少85%。更准确地,根据dvgw工作表w224,规定添加的酸化学计量过量至少三倍,即每摩尔亚氯酸盐至少使用2.4摩尔酸。为使在所有运行条件(例如系统的温度和已利用生产能力)下也能获得高产率,实践中已经确立了三倍摩尔过量,即实践中每摩尔亚氯酸盐通常使用三摩尔酸(r=3)。根据上述反应方程式,这相当于化学计量过量375%。例如,以1:1的体积比使用dvgw工作表中所述的化学品浓度,其通常通过9%盐酸和7.5%亚氯酸钠溶液的方式预先配制,可以实现三倍摩尔过量。
在公共饮用水和废水的处理中,以及在工业应用中,必须对大量的水进行消毒或灭菌,而用于该目的所必需的化学品代表着相当大的成本因素。因此,对能够以较低成本实施或运行的方法和装置存在需求。
技术实现要素:
在这种背景下,本发明的目的尤其是提供一种方法,利用该方法可以显著降低根据亚氯酸盐-酸法生产二氧化氯的常规方法中所产生的成本。同时,本发明将提供一种可以实施这种方法的设备。
根据本发明,该目的通过一种生产二氧化氯水溶液的方法来实现,该方法将酸、亚氯酸盐和任选的水引入反应器中,其中,在该方法中确定反应器中的反应温度,并且选定引入到反应器中的酸、亚氯酸盐和/或水的量,使得引入到反应器中的酸相对于引入到反应器的亚氯酸盐摩尔过量地引入反应器中,其中摩尔过量的程度随着所确定的反应温度高低而变化。
附图说明
为了展示与本发明相关的优点,参考附图。其中:
图1:在15℃的反应温度以及不同的反应时间下,当使用摩尔过量为r=1至3的酸时,二氧化氯的化学计量产率,
图2:在25℃的反应温度以及不同的反应时间下,当使用摩尔过量为r=1至3的酸时,二氧化氯的化学计量产率,
图3:在35℃的反应温度以及不同的反应时间下,当使用摩尔过量为r=1至3的酸时,二氧化氯的化学计量产率,以及
图4:根据本发明的用于生产二氧化氯水溶液的装置的一个具体实施方式的示意图。
具体实施方式
实践中,4kg/h的二氧化氯生产能力并不罕见,例如,在用于工业生产用水和冷却水的处理以对生产用水和冷却水进行灭菌的情况下。根据发明人的计算,在具有这种生产能力的二氧化氯系统的运行中,每年所使用的化学品(在计算例中为亚氯酸钠和盐酸)的成本可减少约40000欧元/年,并且在该工艺中将酸的量从r=3(每摩尔亚氯酸盐3摩尔酸)减少到r=2(每摩尔亚氯酸盐2摩尔酸)也不会导致二氧化氯的产率低于目标产率(≥85%)。
根据本发明,其通过以下方式实现:确定反应器(酸与亚氯酸盐在其中反应)中的反应温度,并且选定反应器中的酸相对于亚氯酸盐的摩尔过量,使得摩尔过量的程度随着所确定的反应温度高低而变化。其依据是,发明人发现在较低的反应温度下,需要与dvgw工作表中规定的三倍摩尔过量相比更小的酸的摩尔过量。但是,如果反应器中有较高的反应温度,则为了实现至少85%的二氧化氯产率,事实上dvgw规定的三倍摩尔过量是必须的。
原则上,根据本发明的方法可以不连续地或连续地进行。本发明所使用的“亚氯酸盐”是亚氯酸的盐,优选选自亚氯酸钠(naclo2)和亚氯酸钾(kclo2)。
在本发明的含义内,术语“酸”特别地包括无机酸,例如,盐酸(hcl)和硫酸(h2so4)。本发明还包括实施方式,其中将酸以其一种盐的形式加入,例如以硫酸氢钠(nahso4)的形式加入。
根据本发明的方法在“反应器”中实施。该反应器为具有反应器容器的化学反应器,由酸、亚氯酸盐和任选的水形成的反应混合物可以在其中反应。反应器容器具有被反应器容器壁包围的反应器内部,并且在运行期间反应混合物存在于该反应器内部中。
通过将离析物酸和亚氯酸盐引入反应器内部,形成“反应混合物”。混合优选通过涡旋混合来实现,并且在特定的实施方式中可以加速,例如通过以陡峭的计量行程将离析物和任选的水引入反应器。
在本发明的含义内,术语“反应温度”表示反应器中的温度,或者更准确地,表示反应器内部中的温度,或者进一步更准确地,表示反应混合物中的温度。通常,根据本发明的方法中的反应温度在5至50℃的范围内。在具体的实施方式中,反应温度在5至45℃的范围内,在10至50℃的范围内或在10至40℃的范围内。
本发明中术语“摩尔过量”是指引入到反应器中的酸与引入到反应器中的亚氯酸盐的比率。即,1摩尔酸与1摩尔亚氯酸盐的比率下,没有摩尔过量(r=1)。但是,如果每摩尔亚氯酸盐添加例如1.5摩尔酸,2摩尔酸或甚至3摩尔酸,则引入到反应器中并与亚氯酸盐混合的酸相对于引入到反应器中的亚氯酸盐,以1.5倍的摩尔过量(r=1.5),以两倍的摩尔过量(r=2),甚至以三倍的摩尔过量(r=3)存在。
这里值得牢记的是,术语“摩尔过量”与术语“化学计量过量”不同义。从上述亚氯酸钠与盐酸反应生成二氧化氯、亚氯酸钠和水的反应方程式出发,三倍摩尔酸过量对应于375%的化学计量过量。
根据本发明,酸相对于亚氯酸盐的摩尔过量可以在r=1.5至4.0的范围内。在具体的实施方式中,该摩尔过量在r=2.0至4.0的范围内,在r=2.5至4.0的范围内,在r=2.5至3.0的范围内,在r=2.5至3.5的范围内或在r=2.5至3.0的范围内。
在本发明的一个具体实施方式中,将引入到反应器中的酸在10至40℃的范围内确定的反应温度下并以相对于引入到反应器中的亚氯酸盐在r=2.0至3.5的范围内的摩尔过量引入反应器中。
在本发明的一个优选实施方式中,引入到反应器中的酸相对于引入到反应器中的亚氯酸盐的摩尔过量的程度随着反应温度的升高而增加。在具体的实施方式中,该增加连续地发生。在本发明的其它实施方式中,该增加递增地发生。在本发明的具体实施方式中,该增加部分连续地且部分递增地发生。
在本发明的实施方式中,摩尔过量的程度随反应温度的升高部分或完全连续地增加,在特定反应温度(t)下存在的摩尔过量(r)优选根据下式确定:
r=2.0+0.05x(t-10)+/-0.5
在根据本发明的方法的实施方式中,摩尔过量的程度随反应温度的升高部分或完全递增地增加,可以提供以下增量中的一个或多个:
-在10至<25℃的反应温度下,摩尔过量在r=2.0至2.5的范围内。
-在25至30℃的反应温度下,摩尔过量在r=2.5至3.0的范围内。
-在>30至40℃的反应温度下,摩尔过量在r=3.0至3.5的范围内。
在本发明的具体实施方式中,增量的分布使得在<30℃、<29℃、<28℃、<27℃或<25℃的反应温度下,摩尔过量为r=2.5,任选地,公差范围为+/-0.2。在>30℃、>29℃、>28℃、>27℃、>26℃或>25℃的反应温度下,摩尔过量为r=3.0,任选地,公差范围为+/-0.2。
根据本发明,可以通过多种方式确定反应温度。使用在反应器内部或反应混合物中测定的温度直接确定反应温度,例如通过温度传感器测定,该温度传感器设置在反应器容器中并具有腐蚀保护,并由例如钛套筒保护而免受反应混合物的影响。
在另一实施方式中,使用在反应器容器外壁上测定的温度确定反应温度。在其它实施方式中,在进行引入的管线上、或容器(离析物从其中取出)中、或其容器壁上,测定引入到反应器中的离析物酸、亚氯酸盐和/或水的温度。由于根据亚氯酸盐-酸法生产二氧化氯时的反应热相对较低,并且若由该反应热加热反应混合物,则与所用离析物的温度的差别在1至2℃的范围内,因此通过这种方式也可以非常准确地确定反应混合物中的反应温度。
在一个具体实施方式中,确定本发明方法实施的环境中的空气温度,如果容器(反应的离析物从其中取出)处在该相同环境中。在此假定在该环境中存储在容器中的离析物具有与环境本身基本相同的温度,其结果是可以直接从中确定反应器中的反应温度。
在本发明的具体实施方式中,酸相对于亚氯酸盐的摩尔过量根据反应时间的持续以及反应温度高低而变化。
“反应时间”在此对应于由离析物产生的反应混合物在反应器中的停留时间。反应时间可以在1至100分钟的范围内。在具体实施方式中,反应时间在1至40分钟的范围内或在4至40分钟的范围内。在其它实施方式中,反应时间在1至30分钟的范围内或在4至30分钟的范围内。
在本发明的一个具体实施方式中,将相对于亚氯酸盐的摩尔过量为2.0至3.5的酸引入反应器中,其中摩尔过量的值随着反应时间的持续而从20分钟的反应时间、30分钟的反应时间或40分钟的反应时间增加。
在本发明的其它具体实施方式中,摩尔过量(r)的程度在以下范围中的一个或多个内:
-在1至<4分钟的反应时间范围内,摩尔过量的程度在r=2.0至2.5的范围内。
-在4至30分钟的反应时间范围内,摩尔过量的程度在r=2.5至3.0的范围内。
-在>30至40分钟的反应时间范围内,摩尔过量的程度在r=3.0至3.5的范围内。
在本发明的具体实施方式中,酸使用盐酸或硫酸。在使用盐酸的实施方式中,可以使用浓度为25至36重量%的浓盐酸或浓度为3至6重量%的稀盐酸。
在本发明的具体实施方式中,所用亚氯酸盐是亚氯酸钠或亚氯酸钾的水溶液。在本发明的具体实施方式中,水溶液中亚氯酸钠或亚氯酸钾的浓度为20至30重量%。
根据dvgw的指南,必须确保二氧化氯的最小化学计量产率为85%。在根据本发明的方法中,其实现方式为,酸的摩尔过量根据反应温度和/或反应时间而变化。在本发明的具体实施方式中,通过这种控制,实现了87%的最小化学计量产率或甚至90%的最小产率。在本发明的优选实施方式中,通过该方法实现的产率为90至95%。通过这种方式,可以确保始终安全地、可靠地满足dvgw所要求的85%的最低产率。
本发明还包括一个“二氧化氯系统”,即一种用于生产二氧化氯水溶液的装置,其中,该装置具有反应器、用于将酸引入反应器的第一管线,用于将亚氯酸盐引入反应器的第二管线和任选的用于将水引入反应器的第三管线,其中,该装置的特征尤其在于,它具有用于确定反应器中反应温度的设备和用于控制通过第一、第二和/或第三管线进入反应器的酸、亚氯酸盐和/或水的流量的控制单元。设置控制单元,以将引入到反应器中的酸相对于引入到反应器中的亚氯酸盐摩尔过量地引入反应器中,其中该摩尔过量随着反应温度高低而变化。
本发明所使用的“反应器”为具有反应器容器的化学反应器,由酸、亚氯酸盐和任选的水形成的反应混合物可以在其中反应。反应器容器具有包围反应器内部的反应器容器壁,并且在运行期间反应混合物存在于该反应器内部中。在反应器容器壁中设置至少一个入口,通过该入口可将亚氯酸盐-酸反应的离析物和任选的水引入反应器内部。
设置根据本发明的二氧化氯系统,使得可以通过该系统实施根据本发明的方法。在不连续地进行根据本发明的方法的实施方式中,反应器优选用于间歇操作的混合容器。但是,在绝大多数情况下,根据本发明的方法是连续地进行的,在这种情况下的二氧化氯系统的实施方式中,反应器优选流动反应器。
离析物和任选的水通过管线进料到反应器中。该管线是与离析物和任选的水的源头连接的管道。
在具体实施方式中,在至少一条管线上设置计量泵,通过该计量泵可以对至少一种离析物和任选的水进行计量。优选地,为酸设置一个计量泵,为亚氯酸盐设置一个计量泵,并且任选地为水设置一个计量泵。
在具体实施方式中,在至少一条管线上和/或在反应器上设置阀,通过该阀可以改变至少一种离析物和任选的水的流量。优选地,为酸设置一个阀,为亚氯酸盐设置一个阀,并且任选地为水设置一个阀。
在具体实施方式中,在至少一条管线上和/或在反应器上设置流量控制器,通过该流量控制器可以监测至少一种离析物和任选的水的流量。
通过根据本发明所提供的对引入到反应器中的酸的量的控制,可以直接在反应器中设定酸的过量程度。或者,也可以通过控制引入的亚氯酸盐的量设定酸的过量程度。
或者或此外,该方法还可以通过向反应器中添加水进行控制。由此,可以设定反应混合物的有效反应体积。此外,引入额外的水可以确保二氧化氯不超过30g/l的最大浓度。最后,通过这种方式甚至可以非常精确地设定所需的二氧化氯浓度,例如,20g/l的目标浓度。此外,也可以通过供应大量的水进行稀释来终止反应。特别是在低系统输出的情况下,由此减少了在反应器中高浓度下的停留时间,并由此提高了所获得的二氧化氯溶液的稳定性。
根据本发明,该控制通过二氧化氯系统中的控制单元实现。该控制单元是电子单元,其中存储有电子数据,该电子数据定义要在多少温度和多少反应时间下设置多少摩尔过量(r),以实现所需的二氧化氯产率。为此,控制单元具有至少一个信号输入端和至少一个信号输出端,通过其可以经有线或无线方式接收和发送信号。
特别地,控制单元具有信号输入端,其用于接收来自设备的信号,该信号用于确定反应温度。任选地,控制单元还具有另一信号输入端,其用于接收来自一个或多个流量控制器的信号。
此外,控制单元特别地具有信号输出端,其用于发送信号,该信号用于控制引入到反应器中的酸和/或亚氯酸盐和任选的水的量。例如可以将用于控制酸和/或亚氯酸盐和任选的水的量的该信号发送到相应的阀,通过该阀可以改变至少一种离析物和任选的水的流量,或者发送到相应的计量泵。
根据本发明的二氧化氯系统中所提供的用于确定反应温度的设备是用于确定温度的测量装置,特别是温度计,该温度计的温度传感器布置在反应器内部中、或反应器容器外壁上、或管线(通过其引入一种离析物或水)上、或容器(离析物或水从其中取出)中、或容器壁(离析物或水从其中取出)上、或系统所在的空间中。
出于原始公开的目的,需要指出的是,如从本说明书、附图和权利要求书中向本领域技术人员所揭示的,所有特征即使仅仅结合特定的其他特征进行了描述,也可以与这里公开的其他特征或特征组合以单独的或任何组合的方式进行组合,除非这被明确排除或者技术条件使得这种组合不可能或毫无意义。在此省略所有可设想的特征组合的全面清楚的描述仅仅是为了说明书的简洁和可读性。
此外,需要指出的是,对于本领域技术人员来说不言而喻的是,以下实施例仅用于举例说明以实施例形式再现的本发明的可能实施例。因此,本领域技术人员将立即理解,具有权利要求中所述的根据本发明的特征或特征组合的所有其他实施方式也落入本发明的保护范围内。在此省略所有可设想的实施例的全面清楚的描述仅仅是为了说明书的简洁和可读性。
实施例
为了研究亚氯酸盐和酸的量以及反应温度和反应时间对二氧化氯产率的影响,进行了实验室测试。为此,使用了体积为25ml的气密玻璃注射器,其在实验室方法中充当反应器。使用ptfe塞子密封注射器,结果可以将注射器及其内容物在水浴中孵育。气密玻璃注射器应被视为间歇式反应器,其中可以在特定时间点(反应时间)取出5毫升的二氧化氯样品。
在实验室测试中,酸使用浓度为9重量%的盐酸。亚氯酸盐以浓度为7.5重量%的亚氯酸钠水溶液的形式提供。选定这些浓度,使得当其以相同体积混合在一起时,盐酸相对于亚氯酸盐以三倍摩尔过量存在。为了获得较小的摩尔过量或甚至等摩尔比(r=1),必须相应地稀释所用盐酸溶液。
通过碘量法定量测定所产生的二氧化氯。
图1中的曲线显示,在15℃的反应温度下,随着相对于所用的亚氯酸盐的酸摩尔比率越高,二氧化氯的产率增加。随着酸比率的增加,反应速率也增加,这可以从摩尔过量为r=1.5的峰位移中观察到。摩尔过量为r=1至2时,在较宽的反应时间范围内达不到要求的至少85%(化学计量)的二氧化氯产率。这只有在摩尔过量为r=2.5时才能被确保。
图2所示的曲线显示在25℃的反应温度下的结果,从该曲线中可以看出,在10至30分钟的反应时间下,原则上r=2的酸摩尔比率足以获得85%或更高的产率。当摩尔过量为r=2.5时,最长至40分钟的反应时间也是可能的。
图3的曲线反映了反应温度为35℃时的比率,从该曲线中可以看出,仅当摩尔过量为r=3时,才能在最长至40分钟的反应时间下可靠地实现至少85%的产率。
从目前的结果可以看出,在15℃和25℃的温度下并在10至30分钟的反应时间下,可以使用r=2的酸摩尔比率,以达到如dvgw工作表所要求的至少85%的产率。但是,如果反应时间超过30分钟,则在15℃和25℃的反应温度下,必须使用至少为r=2.5的酸比率,以稳定所需的85%的产率而不使其由于二氧化氯的分解而降低,该分解在这些温度下剧烈地开始。在35℃的反应温度下并在10至20分钟的反应时间下,r=2的酸摩尔比率可足以达到所需的产率。但是,如果反应时间大于20分钟,则需要酸比率为r=3以补偿二氧化氯的分解。
图4显示根据本发明的用于生产二氧化氯的二氧化氯系统1的一个具体实施方式的示意图。在该二氧化氯系统1中,设置有用于容纳酸的容器2、用于容纳亚氯酸盐的容器3和用于容纳水的容器4。在本发明的另一实施方式中,该装置不具有用于容纳水的容器4。
用于容纳酸、亚氯酸盐和水的容器2、3和4通过管线5、6和7与反应器11连接,为了能够将相应的流体引入反应器容器中。在不具有水容器4的实施方式中,也不设置用于引入水的管线7。
在此处所示的实施例中,在管线5、6和7上设置有阀8、9和10,通过其可以改变通过管线5、6和7的流体流量。通过控制单元12进行阀8、9和10的控制,并且由此进行流量控制,其通过信号线15、16和17与相应的阀8、9或10连接。在本发明的另一实施方式中,使用其他计量装置代替所示的阀,例如计量泵。
在反应器11上设置有温度计13,在此处所示的实施例中,该温度计13测定反应器容器外壁上的温度,并将所测定的温度经由信号线14传输至控制单元12。
在控制单元12中,使用温度计13所测定的反应温度来确定二氧化氯的必要最小产率85%所必需的酸的摩尔过量(r),相应地,通过阀8、9和/或10控制对酸和/或亚氯酸盐和/或水(如果存在水容器4)的计量。在此还考虑了反应时间,该反应时间取决于在给定时间点运行二氧化氯系统1时的生产能力。
由反应器11中的二氧化氯系统1所生产的二氧化氯溶液经由出口18被引导到要使用二氧化氯溶液的地方。
附图标记列表
1用于生产二氧化氯的装置(二氧化氯系统)
2酸的容器
3亚氯酸盐的容器
4水的容器
5酸的管线
6亚氯酸盐的管线
7水的管线
8酸的阀
9亚氯酸盐的阀
10水的阀
11反应器
12控制单元
13温度计
14温度的信号线
15酸流量的信号线
16亚氯酸盐流量的信号线
17水流量的信号线
18二氧化氯溶液的出口
起点商标作为专业知识产权交易平台,可以帮助大家解决很多问题,如果大家想要了解更多知产交易信息请点击 【在线咨询】或添加微信 【19522093243】 与客服一对一沟通,为大家解决相关问题。
与客服一对一沟通,为大家解决相关问题。
此文章来源于网络,如有侵权,请联系删除
 热门咨询
热门咨询



 商标分类
商标分类  商标转让
商标转让 



